医薬品情報
| 総称名 | タリビッド |
|---|---|
| 一般名 | オフロキサシン |
| 欧文一般名 | Ofloxacin |
| 製剤名 | オフロキサシン耳科用液 |
| 薬効分類名 | ニューキノロン系抗菌耳科用製剤 |
| 薬効分類番号 | 1329 |
| ATCコード | S02AA16 |
| KEGG DRUG |
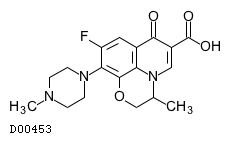
D00453
オフロキサシン
|
| KEGG DGROUP |
DG01549
ニューキノロン系抗生物質
|
| JAPIC | 添付文書(PDF) |
添付文書情報2021年7月 改訂(第1版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| タリビッド耳科用液0.3% | TARIVID Otic Solution 0.3% | アルフレッサファーマ | 1329706Q1039 | 111.2円/mL | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
本剤の成分又はレボフロキサシン水和物に対し過敏症の既往歴のある患者[9.1.1参照]
4. 効能または効果
5. 効能または効果に関連する注意
<中耳炎>
5.1 「抗微生物薬適正使用の手引き」1)を参照し、抗菌薬投与の必要性を判断した上で、本剤の投与が適切と判断される場合に投与すること。
5.2 炎症が中耳粘膜に限局している場合に本剤による局所的治療が適用となる。しかし、炎症が鼓室周辺にまで及ぶような場合には、本剤による局所的治療以外、経口剤などによる全身的治療を検討することが望ましい。
6. 用法及び用量
通常、成人に対して、1回6〜10滴を1日2回点耳する。点耳後は約10分間の耳浴を行う。なお、症状により適宜回数を増減する。小児に対しては、適宜滴数を減ずる。
7. 用法及び用量に関連する注意
4週間の投与を目安とし、その後の継続投与については、長期投与に伴う真菌の発現や菌の耐性化等に留意し、漫然と投与しないよう慎重に行うこと。
8. 重要な基本的注意
本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 キノロン系抗菌薬に対し過敏症の既往歴のある患者(ただし、本剤又はレボフロキサシンに対し過敏症の既往歴のある患者には投与しないこと)[2.参照]
9.5 妊婦
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有効性を考慮し、授乳の継続又は中止を検討すること。
11. 副作用
11.2 その他の副作用
| 1%未満 | 頻度不明 | |
| 過敏症 | − | 過敏症状 |
| 耳 | 耳痛 | 外耳道発赤 |
| その他 | − | 頭痛、菌交代症 |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 使用する際の薬液の温度が低いと、めまいを起こすおそれがあるので、使用時には、できるだけ体温に近い状態で使用すること。
14.1.2 点耳の際、容器の先端が直接耳に触れないように注意すること。
15. その他の注意
15.2 非臨床試験に基づく情報
オフロキサシンの経口投与により、動物実験(幼若犬、幼若ラット)で関節異常が認められている。
16. 薬物動態
16.1 血中濃度
16.3 分布
成人患者1例の中耳腔内に0.3%オフロキサシン水溶液を1回10滴、1日2回、計19回点耳・耳浴した場合、90分後の中耳粘膜中濃度は19.5μg/g、また、成人患者3例に0.1%オフロキサシン水溶液10滴を単回点耳・耳浴した場合、30分後の耳漏中濃度は107〜610μg/mLと高値を示した4)。
16.4 代謝
モルモットに0.3%14C-オフロキサシン水溶液を中耳腔内に単回投与し、投与後0〜24時間での尿中代謝物を検討した結果、未変化体が大部分(87%)であり、脱メチル体、N-オキサイド、グルクロン酸抱合体が僅かに認められた5)。
16.5 排泄
モルモットに0.3%14C-オフロキサシン水溶液を中耳腔内に単回投与し、尿及び糞中への放射能排泄を検討した結果、投与後72時間までに投与量の約90%が尿中に排泄され、糞中への排泄は僅かであった5)。
16.8 その他
16.8.1 オフロキサシンの経口投与は、フェニル酢酸系又はプロピオン酸系非ステロイド性消炎鎮痛剤との併用で痙攣を起こすおそれがある。しかし、本剤の点耳・耳浴による局所投与の場合には、最高血清中濃度が経口投与の場合に比較して1/100程度と低値であり、これら消炎鎮痛剤との併用で痙攣が誘発される可能性はほとんどないと推定された。
16.8.2 小児に対するオフロキサシンの経口投与は、幼若動物で関節異常が認められており、安全性が確立していないので禁忌である。しかし、本剤の点耳・耳浴による局所投与の場合には、最高血清中濃度が経口投与の場合に比較して1/100程度と低値であり、小児を対象とした臨床試験においても安全性が認められた。
注)本剤の承認用量は、1回6〜10滴を1日2回(成人)である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<外耳炎>
17.1.1 国内臨床試験
1日2回点耳・耳浴治療による一般臨床試験の概要は次のとおりである。
| 疾患名 | 有効率(%)〔有効症例/総症例〕 | |
| 外耳炎 | 81.7〔49/60〕 | |
| 外耳道炎 | 80.4〔37/46〕 | |
| 鼓膜炎 | 85.7〔12/14〕 | |
<中耳炎>
17.1.2 国内臨床試験
1日2回点耳・耳浴治療による一般臨床試験及び二重盲検比較試験の概要は次のとおりである。
| 疾患名 | 有効率(%)〔有効症例/総症例〕 | |
| 中耳炎 | 88.1〔141/160〕 | |
| 急性化膿性中耳炎 | 91.3〔42/46〕 | |
| 慢性化膿性中耳炎急性増悪症 | 86.0〔74/86〕 | |
| 慢性化膿性中耳炎 | 89.3〔25/28〕 | |
また、中耳炎を対象とし、セファレキシンの経口投与を基礎治療にプラセボを対照とした二重盲検比較試験において、有効性が確認されている。
<効能共通>
17.1.3 国内臨床試験(除菌効果)
外耳炎、中耳炎に対する一般臨床試験において、1日1〜2回点耳・耳浴治療による起炎菌の除菌率は、黄色ブドウ球菌(91株)で97.8%(89株)、コアグラーゼ陰性ブドウ球菌(68株)で92.6%(63株)であった。化膿レンサ球菌(3株)を含むレンサ球菌属(14株)及び肺炎球菌(4株)は全株消失した。プロテウス・ブルガリス(2株)はともに消失、プロテウス・ミラビリス(6株)の消失率は83.3%(5株)であった。インフルエンザ菌(6株)は全株消失、緑膿菌(32株)も全株消失した。
18. 薬効薬理
18.1 作用機序
18.2 抗菌作用
19. 有効成分に関する理化学的知見
19.1. オフロキサシン
22. 包装
5mL×5、5mL×10[プラスチック瓶]
23. 主要文献
- 厚生労働省健康局結核感染症課編:抗微生物薬適正使用の手引き
- 石井正則 他, 耳鼻咽喉科展望, 33 (補4), 595-605, (1990)
- 馬場駿吉 他, 耳鼻と臨床, 36 (補3), 590-604, (1990)
- 馬場駿吉 他, 耳鼻咽喉科展望, 35 (6), 497-502, (1992)
- 岡崎 治 他, 耳鼻と臨床, 36 (1), 47-55, (1990) »DOI
- Fujimoto,T.et al., Chemotherapy., 36 (4), 268-276, (1990) »PubMed
- Imamura,M.et al., Antimicrob Agents Chemother., 31 (2), 325-327, (1987) »PubMed
- Hoshino,K.et al., Antimicrob Agents Chemother., 35 (2), 309-312, (1991) »PubMed
- Tanaka,M.et al., Antimicrob Agents Chemother., 35 (7), 1489-1491, (1991) »PubMed
- Tanaka,M.et al., Antimicrob Agents Chemother., 41 (11), 2362-2366, (1997) »PubMed
- 佐藤謙一 他, Chemotherapy., 32 (S-1), 1-12, (1984) »DOI
- 五島瑳智子 他, Chemotherapy., 32 (S-1), 22-46, (1984) »DOI
- 西野武志 他, Chemotherapy., 32 (S-1), 62-83, (1984) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
アルフレッサファーマ株式会社
製品情報部
〒540-8575
大阪市中央区石町二丁目2番9号
電話:06-6941-0306
FAX:06-6943-8212
製品情報問い合わせ先
アルフレッサファーマ株式会社
製品情報部
〒540-8575
大阪市中央区石町二丁目2番9号
電話:06-6941-0306
FAX:06-6943-8212
26. 製造販売業者等
26.1 製造販売元
アルフレッサファーマ株式会社
大阪市中央区石町二丁目2番9号