医薬品情報
| 総称名 | スガマデクス |
|---|---|
| 一般名 | スガマデクスナトリウム |
| 欧文一般名 | Sugammadex Sodium |
| 製剤名 | スガマデクスナトリウム注射液 |
| 薬効分類名 | 筋弛緩回復剤 |
| 薬効分類番号 | 3929 |
| ATCコード | V03AB35 |
| KEGG DRUG |
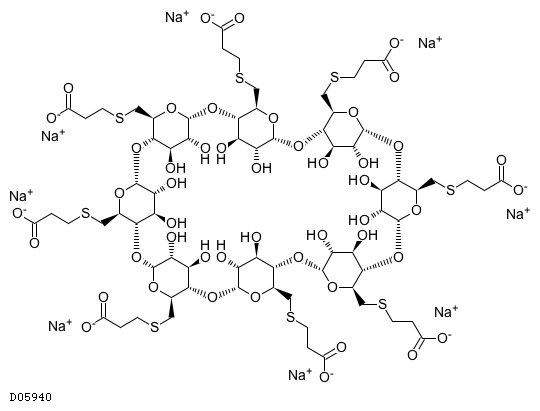
D05940
スガマデクスナトリウム
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年2月 作成(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| スガマデクス静注液200mgシリンジ「サワイ」 | SUGAMMADEX Intravenous Injection Syringes[SAWAI] | 沢井製薬 | 39294A2G1028 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
ロクロニウム臭化物又はベクロニウム臭化物による筋弛緩状態からの回復
5. 効能または効果に関連する注意
本剤はロクロニウム臭化物又はベクロニウム臭化物以外の筋弛緩剤による筋弛緩状態からの回復に対しては使用しないこと。
6. 用法及び用量
通常、成人にはスガマデクスとして、浅い筋弛緩状態(筋弛緩モニターにおいて四連(TOF)刺激による2回目の収縮反応(T2)の再出現を確認した後)では1回2mg/kgを、深い筋弛緩状態(筋弛緩モニターにおいてポスト・テタニック・カウント(PTC)刺激による1〜2回の単収縮反応(1-2PTC)の出現を確認した後)では1回4mg/kgを静脈内投与する。また、ロクロニウム臭化物の挿管用量投与直後に緊急に筋弛緩状態からの回復を必要とする場合、通常、成人にはスガマデクスとして、ロクロニウム臭化物投与3分後を目安に1回16mg/kgを静脈内投与する。
7. 用法及び用量に関連する注意
7.1 筋弛緩モニターによる確認ができない場合は、十分な自発呼吸の発現を確認した後はスガマデクスとして2mg/kgを投与すること。十分な自発呼吸の発現を確認する前のロクロニウム臭化物による筋弛緩に対してはスガマデクスとして4mg/kgを投与するが、筋弛緩状態からの回復が遅延することがあるため、患者の状態を十分に観察すること。なお、筋弛緩モニターによる確認ができない場合の自発呼吸の発現を確認する前のベクロニウム臭化物による筋弛緩に対する本剤の有効性及び安全性は確立されていない。
7.2 ベクロニウム臭化物の挿管用量投与直後に緊急に筋弛緩状態からの回復を必要とする場合の本剤の有効性及び安全性は確立していない。
8. 重要な基本的注意
8.1 筋弛緩及び筋弛緩の回復の程度を客観的に評価し、本剤を安全かつ適切に使用するために、筋弛緩モニターを可能な限り行うこと。
8.2 挿管困難が予測される患者に対しては、気道確保の方法について予め十分に検討を行い、緊急に筋弛緩状態からの回復を必要とする場合の本剤16mg/kgの投与は、必要最小限の使用に留めること。
8.3 自発呼吸が回復するまで必ず調節呼吸を行うこと(ガス麻酔器又は人工呼吸器を使用すること)。
8.4 筋弛緩作用の残存による呼吸抑制、誤嚥等の合併症を防止するため、患者の筋弛緩が十分に回復したことを確認した後に抜管すること。また、抜管後も筋弛緩作用の再発が起きるおそれがあるので患者の観察を十分に行うこと。
8.5 維持麻酔中に本剤を投与すると、浅麻酔となっている場合には、四肢や体幹の動き、バッキングなどが起こることがあるので、必要に応じて麻酔薬又はオピオイドを追加投与すること。
8.6 手術後にロクロニウム臭化物及びベクロニウム臭化物の筋弛緩作用を増強する薬剤を併用する際は筋弛緩の再発に注意し、筋弛緩の再発が発現した場合は、人工呼吸など適切な処置を行うこと。
8.8 本剤投与後数分以内に心室細動、心室頻拍、心停止、高度徐脈があらわれることがあるので、循環動態の観察を十分に行うこと。[11.1.2参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心拍出量の低下のある患者
筋弛緩からの回復が遅延するおそれがある。
9.1.2 浮腫性疾患の患者
筋弛緩からの回復が遅延するおそれがある。
9.1.3 アレルギー素因のある患者
9.1.4 呼吸器疾患の既往歴のある患者
気管支痙攣を起こすおそれがある。[11.1.4参照]
9.1.5 血液凝固障害を伴う患者
健康成人を対象とした海外試験において活性化部分トロンボプラスチン時間又はプロトロンビン時間の一過性の延長が認められている3)。
9.2 腎機能障害患者
本剤は腎排泄されるため、排泄が遅延するおそれがある。[16.6.1参照]
9.3 肝機能障害患者
肝機能障害患者を対象とした臨床試験は実施していない。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中に移行することが報告されている4)。
9.7 小児等
国内において、小児等を対象とした臨床試験は実施していない5)。
9.8 高齢者
筋弛緩からの回復が遅延するおそれがある。外国の臨床試験において、高齢者で回復時間がわずかに遅延する傾向が認められた。[17.1.3参照]
10. 相互作用
10.2 併用注意
| トレミフェン | 筋弛緩状態からの回復の遅延又は筋弛緩の再発が生じるおそれがあるので、本剤投与後6時間以降に投与すること。 | 本剤に包接されたロクロニウム臭化物又はベクロニウム臭化物と置換し、ロクロニウム臭化物又はベクロニウム臭化物の血中濃度が上昇することがある。 |
| 経口避妊剤 ノルエチステロン・エチニルエストラジオール等 | 経口避妊剤の作用が減弱することがある。経口避妊剤服用当日に本剤が投与された場合は飲み忘れた場合と同様の措置を講じること。 | 本剤と包接体を形成し、経口避妊剤の血中濃度が低下することがある。 |
| 抗凝固剤 ワルファリン等 | 本剤との併用により、抗凝固作用が増強されるおそれがあるので、患者の状態を観察するとともに血液凝固に関する検査値に注意すること。 | 作用機序は不明であるが、海外試験において、本剤4mg/kgと抗凝固剤の併用中に活性化部分トロンボプラスチン時間(APTT)又はプロトロンビン時間(PT)の軽度で一過性の延長が認められている。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
潮紅、蕁麻疹、紅斑性皮疹、喘鳴、血圧低下、頻脈、舌腫脹、咽頭浮腫等を起こすことがある。
注)外国人健康成人に本剤を非麻酔下で投与したとき、アナフィラキシーを含む過敏反応は16mg/kg投与群で14/148例(9.5%)、4mg/kg投与群で10/151例(6.6%)認められた。
11.1.2 心室細動、心室頻拍、心停止、高度徐脈(いずれも頻度不明)[8.8参照]
11.1.3 冠動脈攣縮(頻度不明)
11.1.4 気管支痙攣(0.3%未満)[9.1.4参照]
11.2 その他の副作用
| 1〜5%未満 | 1%未満 | 頻度不明 | |
| 消化器 | 悪心、嘔吐 | ||
| 精神神経系 | 浮動性めまい、味覚異常 | ||
| 循環器 | 頻脈、徐脈、高血圧、低血圧 | ||
| 呼吸器 | 咳嗽 | ||
| 泌尿器 | β-N-アセチル-D-グルコサミニダーゼ増加、尿中アルブミン陽性、尿中β2-ミクログロブリン増加 | ||
| 骨格筋・結合組織 | 筋力低下 | ||
| 過敏症 | 潮紅、そう痒、発疹 | ||
| その他 | 悪寒、体動 |
12. 臨床検査結果に及ぼす影響
血清中プロゲステロンの測定値が見かけ上低値を示すことがあるので注意すること6)。
14. 適用上の注意
14.1 薬剤投与時の注意
他の薬剤と併用する場合には、別々の投与経路で使用するか、又は同一点滴回路を使用する場合は回路内を生理食塩水等の中性溶液を用いて洗浄するなど混合しないようにすること。なお、オンダンセトロン塩酸塩水和物、ベラパミル塩酸塩及びラニチジン塩酸塩との混合において、配合変化が報告されている。
14.2 薬剤投与後の注意
開封後の使用は1回限りとし、使用後の残液はシリンジとともに速やかに廃棄すること。
16. 薬物動態
16.1 血中濃度
16.3 分布
16.4 代謝
16.5 排泄
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
重度腎機能障害患者(クレアチニンクリアランス30mL/min未満、透析患者を含む)又は腎機能正常患者(クレアチニンクリアランス80mL/min以上)に麻酔下でスガマデクスナトリウム(スガマデクスとして2mg/kg)を単回静脈内投与したときの薬物動態パラメータは表2のとおりであった12)13)。別の試験において、重度腎機能障害患者(クレアチニンクリアランス30mL/min未満)、中等度腎機能障害患者(クレアチニンクリアランス30〜50mL/min)又は腎機能正常患者(クレアチニンクリアランス80mL/min以上)に非麻酔下でスガマデクスナトリウム(スガマデクスとして4mg/kg)を単回静脈内投与したときの薬物動態パラメータは表2のとおりであった14)(外国人データ)。[9.2参照]
| 投与量※(mg/kg) | 腎機能障害の程度 | 症例数 | AUC0-∞(μg・min/mL) | CL(mL/min) | Vss(mL) | t1/2(min) |
| 2 | 腎機能正常患者 | 13 | 1,728[34.8] | 95.2[22.1] | 13,800[20.5] | 139[44.4] |
| 重度腎機能障害患者注) | 13 | 27,463[114] | 5.53[108] | 15,986[35.5] | 2,139[121] | |
| 4 | 腎機能正常患者 | 6 | 3,750 | 95.0[16.0] | - | 148[13.5] |
| 中等度腎機能障害患者 | 6 | 9,060 | 37.8[39.6] | - | 344[29.8] | |
| 重度腎機能障害患者 | 6 | 20,340 | 16.0[26.8] | - | 794[35.5] |
臨床試験において、スガマデクスナトリウムの血漿中濃度はhigh-flux膜による平均6時間の透析により約70%減少した。low-flux膜ではスガマデクスナトリウムは除去されなかった15)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内外第II相試験
各科領域手術患者(ASA分類Class1〜3)に、非盲検下でロクロニウム臭化物0.9mg/kg又はベクロニウム臭化物0.1mg/kgを静脈内投与した後、筋弛緩モニターにおける四連(TOF)刺激による2回目の収縮反応(T2)の再出現時にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を、またポスト・テタニック・カウント(PTC)刺激による1〜2回の単収縮反応(1-2PTC)の出現時にスガマデクスナトリウム(スガマデクスとして4.0mg/kg)を単回静脈内投与したとき、スガマデクスナトリウム投与開始からTOF比(T4/T1の比)0.9に回復するまでの時間は表1のとおりであり、ロクロニウム臭化物投与後のスガマデクスナトリウムによる筋弛緩状態からの回復時間は、ベクロニウム臭化物投与後と比較して早い傾向が認められた16)17)18)19)20)。
| スガマデクスナトリウム投与時の筋弛緩状態 | 筋弛緩剤の種類 | スガマデクスナトリウム投与量(スガマデクスとして) | 人種 | 投与開始からTOF比(T4/T1の比)0.9に回復するまでの時間(平均値±標準偏差、PPS) |
| 浅い筋弛緩(T2再出現時) | ロクロニウム臭化物 | 2.0mg/kg | 日本人 | 2.2±1.2分(n=7) |
| 白人 | 1.4±0.5分(n=9) | |||
| ベクロニウム臭化物 | 2.0mg/kg | 日本人 | 2.8±0.8分(n=6) | |
| 白人 | 3.4±1.9分(n=7) | |||
| 深い筋弛緩(1-2PTC出現時) | ロクロニウム臭化物 | 4.0mg/kg | 日本人 | 1.6±0.9分(n=11) |
| 白人 | 1.6±0.7分(n=10) | |||
| ベクロニウム臭化物 | 4.0mg/kg | 日本人 | 3.0±2.4分(n=10) | |
| 白人 | 3.3±3.5分(n=8) |
浅い筋弛緩(T2再出現時)にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した群(日本人n=19)で報告された副作用は尿中アルブミン陽性、β2ミクログロブリン増加、血中ビリルビン増加(各n=1)だった。
深い筋弛緩(1-2PTC出現時)にスガマデクスナトリウム(スガマデクスとして4.0mg/kg)を投与した群(日本人n=21)で報告された副作用は口渇(n=2)、味覚異常(n=1)だった。
深い筋弛緩(1-2PTC出現時)にスガマデクスナトリウム(スガマデクスとして4.0mg/kg)を投与した群(日本人n=21)で報告された副作用は口渇(n=2)、味覚異常(n=1)だった。
17.1.2 海外第III相試験
(1)
各科領域手術患者(ASA分類Class1〜4)に、非盲検下でロクロニウム臭化物0.6mg/kg又はベクロニウム臭化物0.1mg/kgを静脈内投与した後、筋弛緩モニターにおける四連(TOF)刺激による2回目の収縮反応(T2)の再出現時にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)又はネオスチグミンメチル硫酸塩50μg/kgを、またポスト・テタニック・カウント(PTC)刺激による1〜2回の単収縮反応(1-2PTC)の出現時にスガマデクスナトリウム(スガマデクスとして4.0mg/kg)又はネオスチグミンメチル硫酸塩70μg/kgを単回静脈内投与したとき、スガマデクスナトリウム又はネオスチグミンメチル硫酸塩投与開始からTOF比(T4/T1の比)0.9に回復するまでの時間は表2のとおりであり、スガマデクスナトリウムによる回復時間はネオスチグミンメチル硫酸塩と比較して有意に早かった(p<0.0001、回復時間の対数変換値を用いて治療群及び施設を因子とした二元配置分散分析)21)22)。
| スガマデクスナトリウム投与時の筋弛緩状態 | 筋弛緩剤の種類 | 投与群 | 投与開始からTOF比(T4/T1の比)0.9に回復するまでの時間(幾何平均値注1)、ITT) |
| 浅い筋弛緩(T2再出現時) | ロクロニウム臭化物 | スガマデクスナトリウム | 1.5分(n=48) |
| ネオスチグミンメチル硫酸塩 | 18.5分(n=48) | ||
| ベクロニウム臭化物 | スガマデクスナトリウム | 2.8分(n=48) | |
| ネオスチグミンメチル硫酸塩 | 16.8分(n=45) | ||
| 深い筋弛緩(1-2PTC出現時) | ロクロニウム臭化物 | スガマデクスナトリウム | 2.9分(n=37) |
| ネオスチグミンメチル硫酸塩 | 50.4分(n=37) | ||
| ベクロニウム臭化物 | スガマデクスナトリウム | 4.5分(n=47) | |
| ネオスチグミンメチル硫酸塩 | 66.2分(n=36) |
浅い筋弛緩(T2再出現時)にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した群(n=96)で報告された主な副作用は悪心、嘔吐、処置による高血圧(各n=4)だった。
深い筋弛緩(1-2PTC出現時)にスガマデクスナトリウム(スガマデクスとして4.0mg/kg)を投与した群(n=83)で報告された主な副作用は悪心(n=5)だった。
深い筋弛緩(1-2PTC出現時)にスガマデクスナトリウム(スガマデクスとして4.0mg/kg)を投与した群(n=83)で報告された主な副作用は悪心(n=5)だった。
(2)各科領域手術患者(ASA分類Class1〜2)に、非盲検下でロクロニウム臭化物1.2mg/kgを静脈内投与した3分後にスガマデクスナトリウム(スガマデクスとして16.0mg/kg)を静脈内投与したときのロクロニウム臭化物投与後からT1が10%に回復するまでの時間(平均値±標準偏差)は4.4±0.7分(n=55)であり、スキサメトニウム塩化物水和物1.0mg/kgを静脈内投与後からT1が10%に回復するまでの時間(平均値±標準偏差)7.1±1.6分(n=55)と比較して有意に早かった(p<0.0001、治療群及び施設を因子とした二元配置分散分析)23)24)。
スガマデクスナトリウム(スガマデクスとして16.0mg/kg)を投与した群(n=56)で報告された主な副作用は処置合併症(n=4)だった。
スガマデクスナトリウム(スガマデクスとして16.0mg/kg)を投与した群(n=56)で報告された主な副作用は処置合併症(n=4)だった。
17.1.3 海外第III相試験(高齢者)
各科領域手術を受ける高齢患者及び非高齢患者(ASA分類Class1〜3)に、非盲検下でロクロニウム臭化物0.6mg/kgを静脈内投与した後、筋弛緩モニターにおける四連(TOF)刺激によるT2再出現時にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を単回静脈内投与したとき、スガマデクスナトリウム投与開始からTOF比(T4/T1の比)0.9に回復するまでの時間(平均値±標準偏差)は、非高齢者群(18〜64歳)で2.5±1.3分(n=48)、65〜74歳群で2.9±1.6分(n=62)、75歳以上群で3.9±1.7分(n=40)であった20)25)26)。[9.8参照]
スガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した65〜74歳群(n=62)で報告された副作用は頻脈、発熱、処置による低血圧、浮動性めまい、乏尿(各n=1)だった。スガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した75歳以上群は副作用の報告がなかった。
スガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した65〜74歳群(n=62)で報告された副作用は頻脈、発熱、処置による低血圧、浮動性めまい、乏尿(各n=1)だった。スガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した75歳以上群は副作用の報告がなかった。
17.1.4 海外第III相試験(腎機能障害患者)
各科領域手術を受ける重度腎機能障害患者(クレアチニンクリアランス30mL/min未満)又は腎機能正常患者(クレアチニンクリアランス80mL/min以上)に、非盲検下でロクロニウム臭化物0.6mg/kgを静脈内投与した後、筋弛緩モニターにおける四連(TOF)刺激によるT2再出現時にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を、またポスト・テタニック・カウント(PTC)刺激による1〜2回の単収縮反応(1-2PTC)の出現時にスガマデクスナトリウム(スガマデクスとして4.0mg/kg)を単回静脈内投与したとき、スガマデクスナトリウム投与開始からTOF比(T4/T1の比)0.9に回復するまでの時間は表3のとおりであった27)28)29)30)。
| スガマデクスナトリウム投与時の筋弛緩状態 | スガマデクスナトリウム投与量(スガマデクスとして) | 投与開始からTOF比(T4/T1の比)0.9に回復するまでの時間 | |
| 浅い筋弛緩(T2再出現時) | 2.0mg/kg | 腎機能正常患者(ASA分類Class1〜2) | 1.7±0.6分注2)(n=14、PP) |
| 重度腎機能障害患者(ASA分類Class2〜3) | 2.0±0.7分注2)(n=15、PP) | ||
| 深い筋弛緩(1-2PTC出現時) | 4.0mg/kg | 腎機能正常患者(ASA分類Class1〜3) | 1.9分注3)(n=32、ITT) |
| 重度腎機能障害患者(ASA分類Class2〜3) | 3.4分注3)(n=35、ITT) | ||
浅い筋弛緩(T2再出現時)にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した腎機能正常患者群(n=15)で報告された副作用は下痢、悪心、麻酔合併症、酸素飽和度低下(各n=1)だった。
浅い筋弛緩(T2再出現時)にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した重度腎機能障害患者群(n=15)で報告された副作用は下痢、麻酔合併症、頭痛(各n=1)だった。
浅い筋弛緩(T2再出現時)にスガマデクスナトリウム(スガマデクスとして2.0mg/kg)を投与した重度腎機能障害患者群(n=15)で報告された副作用は下痢、麻酔合併症、頭痛(各n=1)だった。
18. 薬効薬理
18.1 作用機序
スガマデクスナトリウムは、γ-シクロデキストリンを修飾した選択的筋弛緩剤結合剤である。血漿中で筋弛緩剤のロクロニウム臭化物又はベクロニウム臭化物と包接体を形成し、神経筋接合部のニコチン受容体と結合可能な筋弛緩剤の濃度を減少させる。この結果、ロクロニウム臭化物又はベクロニウム臭化物による筋弛緩作用が阻害される31)。
18.2 筋弛緩剤との親和性
スガマデクスナトリウムは、ステロイド系筋弛緩剤であるロクロニウム臭化物及びベクロニウム臭化物に対して非常に高い親和性を示した(結合定数はそれぞれ15.1及び8.8×106M-1)が、スキサメトニウム塩化物水和物に対する親和性は認められなかった32)。
18.3 筋弛緩回復作用
18.3.1 ロクロニウム臭化物又はベクロニウム臭化物がスガマデクスナトリウムに包接されることにより、筋弛緩剤の作用が阻害され、筋弛緩状態からの回復が得られる。In vitro試験において、スガマデクスナトリウムは、ロクロニウム臭化物及びベクロニウム臭化物による筋弛緩を回復させた33)34)。
18.3.2 ロクロニウム臭化物又はベクロニウム臭化物の持続注入により、サル拇指内転筋のTOF反応の最初の反応T1が90%抑制される筋弛緩状態に維持し、持続注入の停止後に自然回復させた場合と、460nmol/kgのスガマデクスナトリウムを投与した場合の、TOF比(T4/T1の比)0.9に回復するまでの時間を比較した。TOF比(T4/T1の比)0.9に回復するまでの時間は、ロクロニウム臭化物による筋弛緩に対して、自然回復で14.5±1.1分、スガマデクスナトリウム投与後1.9±0.5分(平均値±標準誤差、n=4)であった。また、ベクロニウム臭化物による筋弛緩に対して、自然回復で23.1±1.8分、スガマデクスナトリウム投与後4.4±0.6分(n=4)であった35)36)。
18.3.3 サルにED90(単収縮高を90%抑制する用量)の5倍用量のロクロニウム臭化物(800nmol/kg)又はベクロニウム臭化物(70nmol/kg)を投与し、拇指内転筋に深い筋弛緩を引き起こした後、生理食塩水又は1,150nmol/kg(ロクロニウム臭化物の約1.4倍、ベクロニウム臭化物の約16.4倍の濃度)のスガマデクスナトリウムを投与した(n=4)。ロクロニウム臭化物による筋弛緩に対し、TOF比(T4/T1の比)0.9に回復するまでの時間は、生理食塩水投与後28.2±3.4分(平均値±標準誤差)であったのに対し、スガマデクスナトリウム投与後7.9±1.8分と有意に短縮した。一方、ベクロニウム臭化物による筋弛緩に対し、TOF比(T4/T1の比)0.9に回復するまでの時間は、生理食塩水投与後49.0±4.7分であったのに対し、スガマデクスナトリウム投与後48.6±8.3分であった37)。
19. 有効成分に関する理化学的知見
19.1. スガマデクスナトリウム
20. 取扱い上の注意
20.1 製品の安定性を保持するため脱酸素剤を封入しているので、ピロー包装は使用直前まで開封しないこと。また、開封後は速やかに使用すること。
20.2 ピロー包装開封前に、酸素検知剤(ピンクのライン)が青紫〜青色に変色している場合は使用しないこと。
22. 包装
10シリンジ(2mL/シリンジ[脱酸素剤入り])
23. 主要文献
- 筋弛緩剤(ロクロニウム臭化物)再投与時に関する検討(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.8)
- スガマデクスナトリウム投与後のスキサメトニウム塩化物水和物の作用(ブリディオン静注:2010年1月20日承認、申請資料概要2.6.2.2)
- 血液凝固パラメータへの影響(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.9)
- ラット乳汁排泄試験(ブリディオン静注:2010年1月20日承認、申請資料概要2.6.4.6)
- Plaud, B.et al., Anesthesiology, 110, 284-294, (2009) »PubMed
- 臨床化学検査に及ぼす影響(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.2.2)
- 日本人単回投与試験(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.11)
- ヒトにおける薬物動態(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.2.3)
- 血漿タンパクへの結合(ブリディオン静注:2010年1月20日承認、申請資料概要2.6.4.4)
- 赤血球への結合(ブリディオン静注:2010年1月20日承認、申請資料概要2.6.4.4)
- Peeters,P.et al., Biopharm.Drug Dispos., 32, 159-167, (2011) »PubMed
- Staals,L.M.et al., Br.J.Anaesth., 104, 31-39, (2010) »PubMed
- 腎機能障害患者(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.28)
- Min,K.C.et al., Int.J.Clin.Pharmacol.Ther., 55, 746-752, (2017) »PubMed
- Cammu,G.et al., Br.J.Anaesth., 109, 382-390, (2012) »PubMed
- 日本人を対象としたT2再出現時投与におけるブリッジング試験(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.19)
- Puhringer,F.K.et al., Br.J.Anaesth., 105, 610-619, (2010) »PubMed
- 日本人を対象とした1-2PTC時投与におけるブリッジング試験(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.20)
- Duvaldestin,P.et al., Anesth.Analg., 110, 74-82, (2010) »PubMed
- 個々の試験結果の要約(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.3.2)
- Jones,R.K.et al., Anesthesiology, 109, 816-824, (2008) »PubMed
- 海外第III相試験[1](ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.24,2.7.6.26)
- Lee,C.et al., Anesthesiology, 110, 1020-1025, (2009) »PubMed
- 海外第III相試験[2](ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.27)
- McDonagh,D.L.et al., Anesthesiology, 114, 318-329, (2011) »PubMed
- 海外第III相試験(高齢者)(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.29)
- Staals,L.M.et al., Br.J.Anaesth., 101, 492-497, (2008) »PubMed
- Panhuizen,I.F.et al., Br.J.Anaesth., 114, 777-784, (2015) »PubMed
- 海外第III相試験(腎機能障害患者)(ブリディオン静注:2010年1月20日承認、申請資料概要2.7.6.28)
- FDA Center for Drug Evaluation and Research:Application No.022225Orig1s000:Clinical Pharmacology Review
- 作用機序(ブリディオン静注:2010年1月20日承認、申請資料概要2.6.1)
- 等温マイクロカロリメトリー法による結合親和性(ブリディオン静注:2010年1月20日承認、申請資料概要2.6.2.2)
- Zhang,M.Q., Drugs Fut., 28, 347-354, (2003)
- 筋弛緩回復作用[1](ブリディオン静注:2010年1月20日承認、申請資料概要2.5.1.1)
- Egmond,J.et al., Eur.J.Anaesthesiol., 18, 100, (2001)
- 筋弛緩回復作用[2](ブリディオン静注:2010年1月20日承認、申請資料概要2.6.2.2)
- ロクロニウム臭化物及びベクロニウム臭化物による深い筋弛緩からの回復(ブリディオン静注:2010年1月20日承認、申請資料概要2.6.2.2)
24. 文献請求先及び問い合わせ先
文献請求先
沢井製薬株式会社
医薬品情報センター
〒532-0003
大阪市淀川区宮原5丁目2-30
電話:0120-381-999
FAX:06-7708-8966
製品情報問い合わせ先
沢井製薬株式会社
医薬品情報センター
〒532-0003
大阪市淀川区宮原5丁目2-30
電話:0120-381-999
FAX:06-7708-8966
26. 製造販売業者等
26.1 製造販売元
沢井製薬株式会社
大阪市淀川区宮原5丁目2-30