医薬品情報
| 総称名 | ゾニサミド |
|---|---|
| 一般名 | ゾニサミド |
| 欧文一般名 | Zonisamide |
| 製剤名 | ゾニサミド口腔内崩壊錠 |
| 薬効分類名 | パーキンソン病治療薬(レボドパ賦活剤) レビー小体型認知症に伴うパーキンソニズム治療薬(レボドパ賦活剤) |
| 薬効分類番号 | 1169 |
| KEGG DRUG |
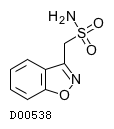
D00538
ゾニサミド
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年2月 作成(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ゾニサミドOD錠25mgTRE「フェルゼン」 | Zonisamide OD Tablets TRE「FELDSENF」 | フェルゼンファーマ | 11690A5F2154 | 劇薬, 処方箋医薬品注) | |
| ゾニサミドOD錠50mgTRE「フェルゼン」 | Zonisamide OD Tablets TRE「FELDSENF」 | フェルゼンファーマ | 11690A5F1166 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 妊婦又は妊娠している可能性のある女性[9.5参照]
2.2 本剤の成分に対して過敏症の既往歴のある患者
4. 効能または効果
<OD錠25mg>
○パーキンソン病(レボドパ含有製剤に他の抗パーキンソン病薬を使用しても十分に効果が得られなかった場合)
○レビー小体型認知症に伴うパーキンソニズム(レボドパ含有製剤を使用してもパーキンソニズムが残存する場合)
<OD錠50mg>
パーキンソン病(レボドパ含有製剤に他の抗パーキンソン病薬を使用しても十分に効果が得られなかった場合)
6. 用法及び用量
<OD錠25mg>
本剤は、レボドパ含有製剤と併用する。
パーキンソン病
通常、成人にゾニサミドとして、1日1回25mgを経口投与する。
なお、パーキンソン病における症状の日内変動(wearing-off現象)の改善には、1日1回50mgを経口投与する。
なお、パーキンソン病における症状の日内変動(wearing-off現象)の改善には、1日1回50mgを経口投与する。
レビー小体型認知症に伴うパーキンソニズム
通常、成人にゾニサミドとして、1日1回25mgを経口投与する。
<OD錠50mg>
パーキンソン病
本剤は、レボドパ含有製剤と併用する。
通常、成人にゾニサミドとして、1日1回25mgを経口投与する。
なお、パーキンソン病における症状の日内変動(wearing-off現象)の改善には、1日1回50mgを経口投与する。
なお、パーキンソン病における症状の日内変動(wearing-off現象)の改善には、1日1回50mgを経口投与する。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
8.1 連用中は定期的に肝・腎機能、血液検査を行うことが望ましい。[11.1.4参照]
8.2 眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械の操作に従事させないよう注意すること。
8.3 発汗減少があらわれることがあり、特に夏季に体温が上昇することがあるので、本剤投与中は体温上昇に留意し、このような場合には高温環境下をできるだけ避け、適切な処置を行うこと。[11.1.10参照]
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
9.3.1 重篤な肝機能障害又はその既往歴のある患者
血中濃度が上昇するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。妊娠中にゾニサミド製剤を投与された患者が心室中隔欠損、心房中隔欠損等を有する児を出産したとの報告があり、動物実験(マウス、ラット、イヌ、サル)で流産、催奇形作用(口蓋裂、心室中隔欠損等)が報告されている。また、妊娠中にゾニサミド製剤を投与された患者の児に呼吸障害があらわれたとの報告がある。[2.1参照]
9.6 授乳婦
授乳しないことが望ましい。ヒト母乳中への移行が報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能(腎機能、肝機能等)が低下している。
10. 相互作用
相互作用序文
本剤は、主として薬物代謝酵素CYP3Aで代謝される。[16.4.2参照]
薬物代謝酵素用語
CYP3A
10.2 併用注意
| 抗てんかん剤 フェニトイン カルバマゼピン フェノバルビタール バルプロ酸 等 | 本剤と抗てんかん剤の併用時、これらの薬剤を減量又は中止した場合に、本剤の血中濃度が上昇することがある。 | フェニトイン、カルバマゼピン、フェノバルビタールではCYPが誘導され、本剤の血中濃度が低下することが示唆されている。 |
| フェニトイン | 眼振、構音障害、運動失調等のフェニトインの中毒症状があらわれることがあるので、できるだけ血中濃度を測定し、減量するなど適切な処置を行うこと。 | 本剤によりフェニトインの代謝が抑制され、血中濃度が上昇することが示唆されている。 |
| 三環系抗うつ剤 アミトリプチリン等 四環系抗うつ剤 マプロチリン等 | MAO-B阻害作用を有するセレギリンにおいて、三環系抗うつ剤との併用により、高血圧、失神、不全収縮、発汗、てんかん、動作・精神障害の変化及び筋強剛といった副作用があらわれ、更に死亡例も報告されている。 | 相加・相乗作用によると考えられる。 |
| レセルピン誘導体 レセルピン等 | 本剤の作用が減弱される可能性がある。 | 脳内ドパミンを減少させる。 |
| フェノチアジン系薬剤 クロルプロマジン等 ブチロフェノン系薬剤 ハロペリドール等 スルピリド メトクロプラミド | 本剤の作用が減弱される可能性がある。 | 脳内ドパミン受容体を遮断する。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 悪性症候群(1%未満)
本剤投与中又は投与中止後に悪性症候群があらわれることがある。発熱、意識障害、無動無言、高度の筋硬直、不随意運動、嚥下困難、頻脈、血圧の変動、発汗、血清CKの上昇等があらわれた場合には、体冷却、水分補給等の全身管理、及び再投与後に漸減するなど適切な処置を行うこと。なお、本症発症時には、ミオグロビン尿を伴う腎機能の低下がみられることがある。
11.1.2 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、紅皮症(剥脱性皮膚炎)(いずれも頻度不明)
発熱、紅斑、水疱・びらん、そう痒感、咽頭痛、眼充血、口内炎等の異常が認められた場合には、投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.3 過敏症症候群(頻度不明)
初期症状として発疹、発熱がみられ、さらにリンパ節腫脹、肝機能障害等の臓器障害、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがある。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること。
11.1.4 再生不良性貧血、無顆粒球症、赤芽球癆(いずれも頻度不明)、血小板減少(1%未満)[8.1参照]
11.1.5 急性腎障害(頻度不明)
11.1.6 間質性肺炎(頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常、好酸球増多等を伴う間質性肺炎があらわれることがあるので、このような症状があらわれた場合には、投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.7 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、γ-GTPの上昇等を伴う重篤な肝機能障害、黄疸があらわれることがある。
11.1.8 横紋筋融解症(1%未満)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇等があらわれた場合には、投与を中止し、適切な処置を行うこと。また、横紋筋融解症による急性腎障害の発症に注意すること。
11.1.9 腎・尿路結石(1%未満)
腎疝痛、排尿痛、血尿、結晶尿、頻尿、残尿感、乏尿等があらわれた場合には、投与を中止するなど適切な処置を行うこと。
11.1.10 発汗減少に伴う熱中症(頻度不明)
発汗減少があらわれ、体温が上昇し、熱中症をきたすことがある。発汗減少、体温上昇、顔面潮紅、意識障害等がみられた場合には、投与を中止し、体冷却等の適切な処置を行うこと。[8.3参照]
11.1.11 幻覚(1%以上)、妄想、錯乱、せん妄(いずれも1%未満)等の精神症状
11.2 その他の副作用
| 1%以上 | 1%未満 | 頻度不明 | |
| 過敏症 | 発疹、湿疹、そう痒感 | ||
| 精神神経系 | 眠気(6.7%)、ジスキネジア、気力低下、抑うつ、めまい・ふらつき、睡眠障害、頭痛・頭重、幻視・幻聴 | 精神活動緩慢化、不安・不穏、精神症状の悪化、感覚異常、無気力・自発性低下、異常感、激越、行動異常、興奮、認知症の悪化、意識消失、異常な夢、自殺企図注)、ジストニア、しびれ感、認知障害 | 運動失調 |
| 循環器 | 血圧低下、動悸、起立性低血圧、血圧上昇、上室性期外収縮、心室性期外収縮 | ||
| 消化器 | 食欲不振(5.2%)、悪心、口渇、胃不快感、便秘 | 嘔吐、下痢、味覚異常、胸やけ、腹部膨満感、流涎、胃炎、嚥下障害、胃痛、歯周炎、腹部不快感、胃潰瘍、口内炎、歯肉炎 | |
| 血液 | 白血球減少、赤血球減少、ヘモグロビン減少、白血球増加、ヘマトクリット減少、貧血、顆粒球減少、血小板減少、好酸球増多 | ||
| 肝臓 | ALT、ALP、AST、LDH上昇 | γ-GTP上昇、肝機能異常 | |
| 腎・泌尿器 | BUN上昇 | 排尿障害、頻尿、クレアチニン上昇、尿失禁、尿中蛋白陽性、膀胱炎 | |
| その他 | 体重減少、CK上昇、立ちくらみ、浮腫、倦怠感 | 脱力感、転倒、発熱、血中カリウム減少、トリグリセリド上昇、腰痛、視覚障害、四肢痛、脱水、気管支炎、筋肉痛、血中尿酸上昇、血糖上昇、呼吸困難、前立腺癌、打撲、汗疹、関節痛、顔面潮紅、血中コレステロール上昇、骨折、体重増加、脱毛、白内障、副鼻腔炎 | 発汗減少 |
13. 過量投与
13.1 症状
昏睡状態、ミオクローヌス、眼振等の症状があらわれる。
13.2 処置
特異的な解毒剤は知られていない。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.2 本剤は舌の上にのせて唾液を浸潤させると崩壊するため、水なしで服用可能である。また、水で服用することもできる。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 本剤による治療中、原因不明の突然死が報告されている。
15.1.2 血清免疫グロブリン(IgA、IgG等)の異常があらわれることがある。
15.1.3 パーキンソン病患者を対象とした国内臨床試験において、トレリーフ錠を投与された患者での自殺又は自殺関連行為の副作用発現割合は0.24%(2/842例)であった。また、パーキンソニズムを伴うレビー小体型認知症患者を対象とした国内臨床試験では、自殺又は自殺関連行為の副作用は発現していない。[8.4、11.2、15.1.4参照]
15.1.4 海外で実施されたゾニサミド製剤(承認外効能・効果、用法・用量)を含む複数の抗てんかん薬における、てんかん、精神疾患等を対象とした199のプラセボ対照臨床試験の検討結果において、自殺念慮及び自殺企図の発現のリスクが、抗てんかん薬の服用群でプラセボ群と比較して約2倍高く(抗てんかん薬服用群:0.43%、プラセボ群:0.24%)、抗てんかん薬の服用群では、プラセボ群と比べ1,000人あたり1.9人多いと計算された(95%信頼区間:0.6〜3.9)。また、てんかん患者のサブグループでは、プラセボ群と比べ1,000人あたり2.4人多いと計算されている。なお、海外臨床試験におけるゾニサミド製剤の自殺念慮及び自殺企図の発現率は0.45%であり、プラセボ群では0.23%であった。[8.4、11.2、15.1.3参照]
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
| 剤形 | Tmax(h)a) | Cmax(μg/mL)b) | t1/2(h)b) | AUC0-96(μg・h/mL)b) |
| ゾニサミドOD錠25mg | 8.0(1.0-12.0) | 0.100±0.015 | 96.6±32.5 | 7.16±0.93 |
| ゾニサミド錠25mg | 4.0(1.0-24.0) | 0.099±0.015 | 99.1±24.2 | 7.00±0.87 |
| 剤形 | Tmax(h)a) | Cmax(μg/mL)b) | t1/2(h)b) | AUC0-96(μg・h/mL)b) |
| ゾニサミドOD錠25mg | 6.0(1.0-12.0) | 0.101±0.027 | 119.1±39.2 | 6.83±1.54 |
| ゾニサミド錠25mg | 4.0(1.0-12.0) | 0.100±0.023 | 102.4±36.4 | 6.77±1.50 |
16.1.2 反復投与
<パーキンソン病>
1日1回25mg又は50mgを4週間経口投与したときの定常状態でのトラフ濃度は、それぞれ1.14±0.48μg/mL(108例の平均値±標準偏差)、2.57±0.86μg/mL(105例の平均値±標準偏差)であった2)。(ゾニサミド錠のデータ)
<レビー小体型認知症に伴うパーキンソニズム>
1日1回25mg又は50mg注)を4週間経口投与したときの定常状態でのトラフ濃度は、それぞれ1.43±0.34μg/mL(39例の平均値±標準偏差)、3.43±1.34μg/mL(37例の平均値±標準偏差)であった3)。(ゾニサミド錠のデータ)
16.1.3 生物学的同等性
健康成人にゾニサミドOD錠25mgとゾニサミド錠25mgを、クロスオーバー法によりそれぞれ1錠(ゾニサミドとして25mg)、水あり(23例)及び水なし(23例)で1回経口投与して血漿中ゾニサミド濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された1)。
16.1.4 生物学的同等性試験
<ゾニサミドOD錠25mgTRE「フェルゼン」>
健康成人男子にゾニサミドOD錠25mgTRE「フェルゼン」とトレリーフOD錠25mgをクロスオーバー法により、それぞれ1錠(ゾニサミドとして25mg)を絶食時単回経口投与(水なしで服用又は水で服用)し、血漿中ゾニサミド濃度を測定した。得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、さらに、平均値の差がlog(0.90)〜log(1.11)の範囲にあり、両剤の生物学的同等性が確認された4)。
1)水なしで服用
| 判定パラメータ | 参考パラメータ | |||
| AUC0-72h(ng・h/mL) | Cmax(ng/mL) | Tmax(h) | t1/2(h) | |
| ゾニサミドOD錠25mgTRE「フェルゼン」 | 6248.31±645.46 | 115.67±13.51 | 3.7±2.4 | 97.0±36.7 |
| トレリーフOD錠25mg | 6114.74±622.55 | 115.23±13.67 | 4.4±3.0 | 89.2±22.1 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
2)水で服用
| 判定パラメータ | 参考パラメータ | |||
| AUC0-72h(ng・h/mL) | Cmax(ng/mL) | Tmax(h) | t1/2(h) | |
| ゾニサミドOD錠25mgTRE「フェルゼン」 | 6456.84±1019.75 | 119.49±21.65 | 4.1±2.5 | 94.4±27.6 |
| トレリーフOD錠25mg | 6351.68±1092.33 | 116.94±19.12 | 3.9±2.1 | 99.1±38.2 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.2.1 食事の影響
健康成人12例において、空腹時及び食後に25mg単回投与したときの薬物動態パラメータを比較した結果、バイオアベイラビリティに対する食事の影響はほとんど認められなかった5)。(ゾニサミド錠のデータ)
16.3 分布
16.3.1 血清蛋白結合率
48.6%(in vitro、ヒト血清、限外ろ過法)6)
16.4 代謝
16.5 排泄
16.5.1 排泄経路
主として尿中7)
16.5.2 排泄率
経口投与後2週間における尿中排泄率は、未変化体として28.9〜47.8%、主代謝物(イソキサゾール環開裂体のグルクロン酸抱合体)として12.4〜18.7%であった。これらは投与量の47.6〜60.2%であった7)(健康成人、200mg1回、200mg/日又は400mg/日注)2日間投与)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
| クレアチニンクリアランス(mL/min) | Tmax(h) | Cmax(μg/mL) | t1/2(h) | CLra)(mL/min) | Aeb)(%) |
| >60 | 3.3 | 3.64 | 58 | 3.42 | 16.8 |
| 20〜60 | 4.3 | 3.73 | 58 | 2.50 | 11.9 |
| <20 | 2.9 | 4.08 | 63 | 2.23 | 13.3 |
腎クリアランス及び尿中排泄率で正常腎機能患者との間に差が認められた。
注)本剤のパーキンソン病に対する承認用量は1日25〜50mg、レビー小体型認知症に伴うパーキンソニズムに対する承認用量は1日25mgである。
16.8 その他
<ゾニサミドOD錠50mgTRE「フェルゼン」>
ゾニサミドOD錠50mgTRE「フェルゼン」は、「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン」に基づき、ゾニサミドOD錠25mgTRE「フェルゼン」を標準製剤としたとき、溶出挙動に基づき生物学的に同等とみなされた10)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
ゾニサミド錠の国内臨床試験成績は以下のとおりであった。
<パーキンソン病>
17.1.1 国内後期第II相/第III相試験
レボドパ製剤による治療で十分な効果が得られていないパーキンソン病患者347例を対象に、プラセボを対照とした二重盲検比較試験を実施した結果、25mg投与群ではプラセボ投与群に比べ主要評価項目としたUPDRS(Unified Parkinson’s Disease Rating Scale)Part III合計スコア(運動能力検査)が改善し、有効性が認められた11)12)。[7.参照]
| 投与群 | 症例数 | ベースライン | 最終評価時 | 変化量 | 検定b) | |
| 調整平均値a) | 標準誤差a) | |||||
| プラセボ群 | 81 | 22.9 | 21.0 | -2.0 | 0.8 | − |
| 25mg群 | 76 | 26.5 | 19.8 | -6.3 | 0.8 | p<0.001 |
| 50mg群 | 82 | 22.5 | 16.8 | -5.8 | 0.8 | p=0.003 |
ゾニサミドの副作用発現頻度は25mg群で40.5%(32/79例)、50mg群で49.4%(42/85例)であり、主な副作用(発現頻度が5%以上)は25mg群で体重減少(5.1%)、50mg群で傾眠(12.9%)、食欲減退(7.1%)、血中クレアチンホスホキナーゼ増加(7.1%)、気力低下(5.9%)であった。
17.1.2 国内第III相試験(運動機能スコアによる評価)
レボドパ製剤による治療で十分な効果が得られていないパーキンソン病患者(UPDRS Part III合計スコア10点以上)196例を対象に、プラセボを対照とした二重盲検比較試験を実施した結果、25mg投与群ではプラセボ投与群に比べ主要評価項目としたUPDRS Part III合計スコア(運動能力検査)が改善し、有効性が認められた13)14)。[7.参照]
| 投与群 | 症例数 | ベースライン | 最終評価時 | 変化量 | 検定b) | |
| 調整平均値a) | 標準誤差a) | |||||
| プラセボ群 | 63 | 21.5 | 18.7 | -2.9 | 0.9 | − |
| 25mg群 | 61 | 21.4 | 15.6 | -5.9 | 0.9 | p=0.029 |
| 50mg群 | 60 | 23.0 | 17.6 | -5.5 | 0.9 | p=0.073 |
ゾニサミドの副作用発現頻度は25mg群で30.2%(19/63例)、50mg群で34.9%(22/63例)であり、主な副作用(発現頻度が3%以上)は25mg群でジスキネジー、傾眠、幻覚、食欲減退(各3.2%)、50mg群で傾眠、悪心(各4.8%)、不眠症、ジスキネジー、無力症、幻覚(各3.2%)であった。
17.1.3 国内第III相試験(off 時間による評価)
レボドパ製剤による治療で十分な効果が得られていない、wearing-off現象を発現したパーキンソン病患者(off時間が1日2時間以上発現)389例を対象に、プラセボを対照とした二重盲検比較試験を実施した結果、50mg投与群ではプラセボ投与群に比べ主要評価項目としたoff時間が短縮し、有効性が認められた15)16)。
| 投与群 | 症例数 | ベースライン | 最終評価時 | 変化量 | 検定b) | |
| 調整平均値a) | 標準誤差a) | |||||
| プラセボ群 | 129 | 6.303 | 6.300 | -0.011 | 0.173 | − |
| 25mg群 | 125 | 6.435 | 5.991 | -0.436 | 0.176 | p=0.086 |
| 50mg群 | 121 | 6.377 | 5.657 | -0.719 | 0.179 | p=0.005 |
<レビー小体型認知症に伴うパーキンソニズム>
17.1.4 国内第III相試験
レボドパ製剤を12週間以上連続して服用中のパーキンソニズムを伴うレビー小体型認知症患者351例を対象に、プラセボを対照とした二重盲検比較試験を実施した結果、ゾニサミド25mg投与群はプラセボ投与群に比べ主要評価項目としたUPDRS Part III合計スコア(運動能力検査)が改善し、有効性が認められた17)18)(本試験では、ゾニサミドの投与群として25mg投与群、50mg投与群注)の2群を設定した。)。
| 投与群 | 症例数 | ベースライン | 最終評価時 | 変化量 | 検定b) | |
| 調整平均値a) | 標準誤差a) | |||||
| プラセボ群 | 118 | 30.5 | 29.2 | -1.4 | 0.6 | − |
| 25mg群 | 117 | 31.9 | 28.1 | -4.1 | 0.6 | p=0.005 |
ゾニサミドの副作用発現頻度は25mg群で15.4%(18/117例)であり、主な副作用(発現頻度が1%以上)は傾眠(3.4%)、体重減少(1.7%)、精神症状(1.7%)であった。
注)本剤のレビー小体型認知症に伴うパーキンソニズムに対する承認用量は1日25mgである。
18. 薬効薬理
18.1 作用機序
作用機序はまだ完全に解明されてはいないが、6-ヒドロキシドパミン(6-OHDA)により片側黒質線条体のドパミン神経を選択的に破壊したパーキンソン病モデルラット(片側6-OHDA処置ラット)を用いた脳微小透析法による実験において、レボドパ(ベンセラジド塩酸塩含有)併用下における破壊側線条体細胞外液中ドパミンレベルに対し有意な上昇作用を示す。また、ラット及びサル線条体ミトコンドリア・シナプトソーム膜標本中のMAO活性を阻害し、その阻害作用は比較的MAOのB型に選択性を示す19)。さらに、T型Caチャネル及びNaチャネル(ともにヒト遺伝子組換えタンパク質)に対して、それぞれのチャネルにおける電流の阻害作用を示す20)。
18.2 レボドパ作用の増強効果
レセルピン処置パーキンソン病モデルラットにおけるレボドパ(ベンセラジド塩酸塩含有)惹起運動亢進に対して増強効果を示す21)。
18.3 レボドパ作用の延長効果
片側6-OHDA処置ラットにおけるレボドパ(ベンセラジド塩酸塩含有)惹起回転運動の持続時間に対して延長効果を示す22)。
18.4 実験的wearing-off現象の改善効果
片側6-OHDA処置ラットへの高用量塩酸メチルドパ(ベンセラジド塩酸塩含有)反復投与により惹起した実験的wearing-off現象に対して改善効果を示す23)。
19. 有効成分に関する理化学的知見
19.1. ゾニサミド
20. 取扱い上の注意
アルミピロー開封後は湿気を避けて保存すること。
22. 包装
<ゾニサミドOD錠25mgTRE「フェルゼン」>
30錠[10錠(PTP)×3]
<ゾニサミドOD錠50mgTRE「フェルゼン」>
30錠[10錠(PTP)×3]
23. 主要文献
- 白倉健史ほか, BIO Clinica., 29 (13), 78-81, (2014)
- 反復投与[1](トレリーフ錠:2013年8月20日承認、審査報告書)
- 反復投与[2](トレリーフ錠・OD錠:2018年7月2日承認、申請資料概要2.5.3.1)
- 社内資料:生物学的同等性試験(ゾニサミドOD錠25mgTRE「フェルゼン」)
- 食事の影響(トレリーフ錠:2009年1月21日承認、申請資料概要2.7.1.2)
- Matsumoto K., et al., Arzneim-Forsch./Drug Res., 33, 961-968, (1983) »PubMed
- Ito T., et al., Arzneim-Forsch./Drug Res., 32, 1581-1586, (1982) »PubMed
- Nakasa H., et al., Mol. Pharmacol., 44, 216-221, (1993) »PubMed
- ゾニサミドの腎機能障害患者における薬物動態(トレリーフ錠:2009年1月21日承認、申請資料概要2.7.2.2)
- 社内資料:生物学的同等性試験(ゾニサミドOD錠50mgTRE「フェルゼン」)
- 国内後期第II相/第III相試験[1](トレリーフ錠:2009年1月21日承認、申請資料概要2.7.6.14)
- 国内後期第II相/第III相試験[2](トレリーフ錠:2009年1月21日承認、申請資料概要2.7.3.2)
- Murata M., et al., Neurol. Clin. Neurosci., 4, 10-15, (2016)
- 国内第III相試験(運動機能スコアによる評価)(トレリーフ錠:2009年1月21日承認、申請資料概要2.7.6.15)
- Murata M., et al., Mov. Disord., 30, 1343-1350, (2015) »PubMed
- 国内第III相試験(off時間による評価)(トレリーフ錠:2013年8月20日承認、審査報告書)
- レビー小体型認知症患者対象臨床試験(第3相試験)(トレリーフ錠・OD錠:2018年7月2日承認、申請資料概要2.7.6.2)
- UPDRS Part III合計スコア及び変化量(トレリーフ錠・OD錠:2018年7月2日承認、申請資料概要2.7.3.3)
- 脳内ドパミンレベル増加作用及びMAO阻害作用(トレリーフ錠:2009年1月21日承認、申請資料概要2.6.2.2)
- チャネル阻害作用(トレリーフ錠・OD錠:2018年7月2日承認、申請資料概要2.6.2.2)
- レボドパ作用の増強効果(トレリーフ錠:2009年1月21日承認、申請資料概要2.6.2.2)
- レボドパ作用の延長効果(トレリーフ錠:2009年1月21日承認、申請資料概要2.6.2.2)
- 実験的wearing-off現象の改善効果(トレリーフ錠:2009年1月21日承認、申請資料概要2.6.2.2)
24. 文献請求先及び問い合わせ先
文献請求先
株式会社フェルゼンファーマ
安全管理部
〒105-0001
東京都港区虎ノ門1丁目1番18号
電話:03-6368-5160
FAX:03-3580-1522
製品情報問い合わせ先
株式会社フェルゼンファーマ
安全管理部
〒105-0001
東京都港区虎ノ門1丁目1番18号
電話:03-6368-5160
FAX:03-3580-1522
26. 製造販売業者等
26.1 製造販売元
株式会社フェルゼンファーマ
札幌市中央区北10条西24丁目3番地