医薬品情報
| 総称名 | ベピオ |
|---|---|
| 一般名 | 過酸化ベンゾイル |
| 欧文一般名 | Benzoyl Peroxide |
| 製剤名 | 過酸化ベンゾイル製剤 |
| 薬効分類名 | 尋常性ざ瘡治療剤 |
| 薬効分類番号 | 2699 |
| ATCコード | D10AE01 |
| KEGG DRUG |
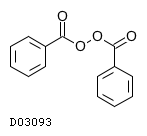
D03093
過酸化ベンゾイル
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年5月 改訂(第5版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ベピオゲル2.5% | BEPIO Gel | マルホ | 2699712Q1021 | 84.9円/g | 処方箋医薬品注) |
| ベピオローション2.5% | BEPIO Lotion | マルホ | 2699712Q2028 | 92.3円/g | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
5. 効能または効果に関連する注意
結節及び嚢腫には、他の適切な処置を行うこと。
6. 用法及び用量
1日1回、洗顔後、患部に適量を塗布する。
8. 重要な基本的注意
8.1 全身性の過敏反応や重度の皮膚刺激症状が認められた場合は本剤の使用を中止すること。
8.2 本剤の使用中に皮膚剥脱(鱗屑・落屑)、紅斑、刺激感、腫脹等があらわれることがある。紅斑や腫脹が顔面全体や頚部にまで及ぶ症例も報告されているので、観察を十分に行い、異常が認められた場合には本剤の使用を中止するなど適切な処置を行うこと。
8.3 本剤の使用中には日光への曝露を最小限にとどめ、日焼けランプの使用、紫外線療法は避けること。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。母乳中への移行は不明である。
9.7 小児等
12歳未満の小児等を対象とした臨床試験は実施していない。
11. 副作用
11.2 その他の副作用
| 5%以上 | 5%未満 | 頻度不明 | |
| 皮膚 | 皮膚剥脱(鱗屑・落屑)(15.3%)、紅斑(12.3%)、刺激感(11.4%)、乾燥 | そう痒、接触皮膚炎(アレルギー性接触皮膚炎を含む)、皮膚炎、湿疹、蕁麻疹、間擦疹、乾皮症、脂腺機能亢進、腫脹、ピリピリ感、灼熱感 | 汗疹、違和感、皮脂欠乏症、ほてり、浮腫、丘疹、疼痛、水疱、びらん、皮脂欠乏性湿疹 |
| その他 | 口角炎、眼瞼炎、白血球数減少、白血球数増加、血小板数増加、血中ビリルビン増加、ALT増加 | 血中コレステロール減少、血中尿素減少、AST増加、呼吸困難感 |
14. 適用上の注意
14.1 薬剤使用時の注意
14.1.1 本剤の有効成分濃度及び用法・用量は、過酸化ベンゾイル5%製剤と異なることに注意すること。
14.1.2 他の外用剤と併用する場合は、皮膚刺激症状が増すおそれがあるため注意すること。
14.1.3 本剤は漂白作用があるので、髪、衣料等に付着しないように注意すること。
14.1.4 外用としてのみ使用すること。
14.1.5 切り傷、すり傷、湿疹のある皮膚への塗布は避けること。
14.1.6 眼、口唇、鼻翼及び粘膜を避けながら、患部に塗布すること。眼の周囲に使用する場合には眼に入らないように注意すること。万一、眼に入った場合は直ちに水で洗い流すこと。
16. 薬物動態
16.1 血中濃度
尋常性ざ瘡患者の顔面全体(眼囲及び口唇を除く)にベピオゲル又はプラセボを各群9例に約0.5g塗布したとき注)の代謝物である安息香酸及び馬尿酸の薬物動態学的パラメータは次のとおりであった1)。
| 例数 | Cmax(μg/mL) | tmax(h) | AUC0〜t(μg・h/mL) | ||
| 平均±標準偏差 | 平均±標準偏差 | 平均±標準偏差 | |||
| 安息香酸 | ベピオゲル | 9 | 0.0197±0.0063 | 2.6±2.3 | 0.137±0.122 |
| プラセボ | 6 | 0.0189±0.0067 | 6.9±8.7 | 0.072±0.081 | |
| 馬尿酸 | ベピオゲル | 7 | 0.2617±0.1420 | 5.0±9.1 | 2.724±1.936 |
| プラセボ | 8 | 0.1969±0.1370 | 0.6±1.4 | 0.639±1.206 | |
16.2 吸収
ヒト正常皮膚を用いて14Cで標識したベピオゲルの皮膚透過性を検討した結果、24時間塗布した際の累積透過量及び皮膚中放射能量を合わせた吸収率は塗布量の10%程度であった2)(in vitro)。
16.3 分布
ヒト正常皮膚に過酸化ベンゾイルを経皮投与した際の皮膚内分布を検討した結果、表皮及び真皮中には過酸化ベンゾイル及び安息香酸が検出されたが、透過後はすべて安息香酸であることが確認された3)(in vitro)。
16.4 代謝
16.5 排泄
安息香酸は、ヒト及び主要な動物種において、ほぼすべてが尿中に排泄される6)。
注)ベピオゲルの承認された用法・用量は、「1日1回、洗顔後、患部に適量を塗布する。」である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<ゲル>
17.1.1 国内第II/III相臨床試験
顔面に尋常性ざ瘡を有する患者404例を対象として、ベピオゲル又はプラセボを12週間全顔に塗布する二重盲検比較試験7)を実施した。主要評価項目である最終評価時の炎症性皮疹数の減少率において、ベピオゲル群はプラセボ群と比較し統計的有意差(p<0.001)が認められた。
副作用発現頻度はベピオゲル群で37.3%(76/204例)であった。主な副作用は皮膚剥脱19.1%(39/204例)、適用部位紅斑13.7%(28/204例)、適用部位刺激感8.3%(17/204例)、適用部位そう痒感3.4%(7/204例)及び接触皮膚炎2.5%(5/204例)であった。
副作用発現頻度はベピオゲル群で37.3%(76/204例)であった。主な副作用は皮膚剥脱19.1%(39/204例)、適用部位紅斑13.7%(28/204例)、適用部位刺激感8.3%(17/204例)、適用部位そう痒感3.4%(7/204例)及び接触皮膚炎2.5%(5/204例)であった。
| ベピオゲル (203例) | プラセボ (201例) | 差※ (差の95%信頼区間) | |
| 炎症性皮疹数減少率(%) | 72.73 | 41.67 | 25.72 (19.23〜32.89) |
| 非炎症性皮疹数減少率(%) | 56.52 | 21.88 | 29.48 (21.38〜37.59) |
| 総皮疹数減少率(%) | 62.22 | 28.57 | 29.44 (22.73〜36.46) |
17.1.2 国内第III相臨床試験
顔面に尋常性ざ瘡を有する患者231例を対象として、ベピオゲルを52週間全顔に塗布する長期投与試験(非盲検試験)8)を実施した。その結果、総皮疹数は12週後まで経時的に減少し、その後も増加することなく最終評価時まで推移した。
副作用発現頻度は49.4%(114/231例)であった。主な副作用は適用部位刺激感19.0%(44/231例)、皮膚剥脱18.2%(42/231例)、適用部位紅斑13.9%(32/231例)、適用部位乾燥13.0%(30/231例)、適用部位そう痒感6.1%(14/231例)、接触皮膚炎3.0%(7/231例)であった。
副作用発現頻度は49.4%(114/231例)であった。主な副作用は適用部位刺激感19.0%(44/231例)、皮膚剥脱18.2%(42/231例)、適用部位紅斑13.9%(32/231例)、適用部位乾燥13.0%(30/231例)、適用部位そう痒感6.1%(14/231例)、接触皮膚炎3.0%(7/231例)であった。
<ローション>
17.1.3 国内第III相臨床試験
顔面に尋常性ざ瘡を有する患者222例を対象として、ベピオローション又はプラセボを12週間全顔に塗布する二重盲検比較試験9)を実施した。主要評価項目である治療開始12週後の総皮疹数の減少率において、ベピオローション群はプラセボ群と比較し統計的有意差(p<0.0001)が認められた。
副作用発現頻度はベピオローション群で11.9%(13/109例)であった。副作用は適用部位紅斑4.6%(5/109例)、適用部位そう痒感、適用部位乾燥2.8%(3/109例)、接触皮膚炎1.8%(2/109例)、適用部位刺激感、皮膚剥脱0.9%(1/109例)であった。
副作用発現頻度はベピオローション群で11.9%(13/109例)であった。副作用は適用部位紅斑4.6%(5/109例)、適用部位そう痒感、適用部位乾燥2.8%(3/109例)、接触皮膚炎1.8%(2/109例)、適用部位刺激感、皮膚剥脱0.9%(1/109例)であった。
| ベピオローション (109例) | プラセボ (113例) | 差 (差の95%信頼区間) | |
| 総皮疹数減少率(%) | 63.02 | 26.54 | 36.48 (26.28〜46.68) |
| 炎症性皮疹数減少率(%) | 71.35 | 36.72 | 34.63 (24.84〜44.42) |
| 非炎症性皮疹数減少率(%) | 57.04 | 22.14 | 34.90 (22.89〜46.92) |
18. 薬効薬理
18.1 作用機序
18.1.1 抗菌作用
18.1.2 角層剥離作用
18.2 抗菌作用
18.3 角層剥離作用
実験的ウサギ面皰モデルにおいて、過酸化ベンゾイルは角質細胞同士の結合を弛めて角層剥離を促し、毛漏斗部の角層肥厚を改善した14)。
19. 有効成分に関する理化学的知見
19.1. 過酸化ベンゾイル
22. 包装
<ゲル>
チューブ
15g×10
<ローション>
ボトル
15g×10
23. 主要文献
- 藤村昭夫ら, 臨床医薬, 30 (8), 639-649, (2014)
- 社内資料:ヒト皮膚透過性(in vitro)(ベピオゲル2.5%:2014年12月26日承認、CTD2.6.4.3.1.1)
- 社内資料:ヒト皮膚組織内での代謝(in vitro)(ベピオゲル2.5%:2014年12月26日承認、CTD2.6.4.4.1.1)
- Morsches B.,et al., Arzneim.-Forsch.(Drug Res.), 32 ((I)3), 298-300, (1982) »PubMed
- 社内資料:ヒト血漿中代謝安定性(in vitro)(ベピオゲル2.5%:2014年12月26日承認、CTD2.6.4.5.1.2.1)
- Bridges J.W.,et al., Biochem.J., 118, 47-51, (1970) »PubMed
- 川島 眞ら, 臨床医薬, 30 (8), 651-668, (2014)
- 川島 眞ら, 臨床医薬, 30 (8), 669-689, (2014)
- 社内資料:尋常性ざ瘡患者を対象とした国内第III相臨床試験(プラセボ対照試験)(ベピオローション2.5%)
- Burkhart C.N.,et al., Skin Pharmacol.Appl.Skin Physiol., 13 (5), 292-296, (2000) »PubMed
- Sagransky M.,et al., Expert Opin.Pharmacother., 10 (16), 2555-2562, (2009)
- Burkhart C.G.,et al., J.Cutan.Med.Surg., 4 (3), 138-141, (2000) »PubMed
- 吉川敏一, フリーラジカル, 5-7, (1988)
- Oh C.W.,et al., J.Dermatol., 23, 169-180, (1996) »PubMed
- Nakatsuji T.,et al., J.Invest.Dermatol., 129, 2480-2488, (2009) »PubMed
- Decker L.C.,et al., Antimicrob.Agents Chemother., 33 (3), 326-330, (1989) »PubMed
- Burkhart C.G.,et al., Br.J.Dermatol., 154, 341-344, (2006) »PubMed
- Eady E.A.,et al., Br.J.Dermatol., 131, 331-336, (1994) »PubMed
- Fourniat J.,et al., Int.J.Cosmet.Sci., 11, 253-258, (1989) »PubMed
- Cove J.H.,et al., J.Appl.Bacteriol., 54, 379-382, (1983) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
マルホ株式会社
製品情報センター
〒531-0071
大阪市北区中津1-11-1
電話:0120-12-2834
製品情報問い合わせ先
マルホ株式会社
製品情報センター
〒531-0071
大阪市北区中津1-11-1
電話:0120-12-2834
26. 製造販売業者等
26.1 製造販売
マルホ株式会社
大阪市北区中津1-5-22