医薬品情報
| 総称名 | ラモトリギン |
|---|---|
| 一般名 | ラモトリギン |
| 欧文一般名 | Lamotrigine |
| 製剤名 | ラモトリギン製剤 |
| 薬効分類名 | 抗てんかん剤 双極性障害治療薬 |
| 薬効分類番号 | 1139 1179 |
| ATCコード | N03AX09 |
| KEGG DRUG |
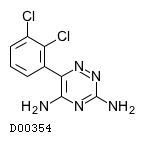
D00354
ラモトリギン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年3月 改訂(第4版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ラモトリギン錠小児用2mg「アメル」 | Lamotrigine Tablets for Pediatric「AMEL」 | 共和薬品工業 | 1139009F1072 | 6.3円/錠 | 劇薬, 処方箋医薬品 |
| ラモトリギン錠小児用5mg「アメル」 | Lamotrigine Tablets for Pediatric「AMEL」 | 共和薬品工業 | 1139009F2079 | 6.3円/錠 | 劇薬, 処方箋医薬品 |
| ラモトリギン錠25mg「アメル」 (後発品) | Lamotrigine Tablets「AMEL」 | 共和薬品工業 | 1139009F3040 | 10.4円/錠 | 劇薬, 処方箋医薬品 |
| ラモトリギン錠100mg「アメル」 (後発品) | Lamotrigine Tablets「AMEL」 | 共和薬品工業 | 1139009F4047 | 25.3円/錠 | 劇薬, 処方箋医薬品 |
1. 警告
本剤の投与により中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、薬剤性過敏症症候群等の全身症状を伴う重篤な皮膚障害があらわれることがあり、死亡に至った例も報告されているので、以下の事項に注意すること。
1.1 用法及び用量を超えて本剤を投与した場合に皮膚障害の発現率が高いことから、本剤の6.用法及び用量を遵守すること。
1.1.1 投与開始時は定められた用法及び用量を超えないこと。バルプロ酸ナトリウム併用時の投与開始2週間までは隔日投与にすること(成人のみ)。[7.1参照]
1.1.2 維持用量までの漸増時も定められた用法及び用量を超えないこと。また、増量時期を早めないこと。[7.1参照]
1.2 発疹発現時には早期に皮膚科専門医に相談し、適切な処置を行うこと。また、発疹に加え以下に示す症状があらわれた場合には重篤な皮膚障害に至ることがあるので、直ちに本剤の投与を中止すること。[11.1.1、11.1.2参照]
発熱(38℃以上)、眼充血、口唇・口腔粘膜のびらん、咽頭痛、全身倦怠感、リンパ節腫脹 等
1.4 患者又は家族に対して、発疹や上記の症状があらわれた場合には直ちに受診するよう指導すること。
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
ラモトリギン錠小児用2mg「アメル」
○てんかん患者の下記発作に対する単剤療法
定型欠神発作
○他の抗てんかん薬で十分な効果が認められないてんかん患者の下記発作に対する抗てんかん薬との併用療法
ラモトリギン錠小児用5mg「アメル」
○てんかん患者の下記発作に対する単剤療法
定型欠神発作
○他の抗てんかん薬で十分な効果が認められないてんかん患者の下記発作に対する抗てんかん薬との併用療法
ラモトリギン錠25mg「アメル」
○てんかん患者の下記発作に対する単剤療法
部分発作(二次性全般化発作を含む)
強直間代発作
定型欠神発作
○他の抗てんかん薬で十分な効果が認められないてんかん患者の下記発作に対する抗てんかん薬との併用療法
ラモトリギン錠100mg「アメル」
○てんかん患者の下記発作に対する単剤療法
部分発作(二次性全般化発作を含む)
強直間代発作
定型欠神発作
○他の抗てんかん薬で十分な効果が認められないてんかん患者の下記発作に対する抗てんかん薬との併用療法
5. 効能または効果に関連する注意
ラモトリギン錠小児用2mg「アメル」
<定型欠神発作>
5.1 15歳以上の患者における有効性及び安全性については確立していないため、15歳未満で本剤の治療を開始した患者において、15歳以降も継続して本剤を使用する場合には、患者の状態を十分観察し、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
ラモトリギン錠小児用5mg「アメル」
<定型欠神発作>
5.1 15歳以上の患者における有効性及び安全性については確立していないため、15歳未満で本剤の治療を開始した患者において、15歳以降も継続して本剤を使用する場合には、患者の状態を十分観察し、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
ラモトリギン錠25mg「アメル」
<定型欠神発作>
5.1 15歳以上の患者における有効性及び安全性については確立していないため、15歳未満で本剤の治療を開始した患者において、15歳以降も継続して本剤を使用する場合には、患者の状態を十分観察し、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
<双極性障害における気分エピソードの再発・再燃抑制>
5.2 双極性障害の気分エピソードの急性期治療に対する本剤の有効性及び安全性は確立していない。
ラモトリギン錠100mg「アメル」
<定型欠神発作>
5.1 15歳以上の患者における有効性及び安全性については確立していないため、15歳未満で本剤の治療を開始した患者において、15歳以降も継続して本剤を使用する場合には、患者の状態を十分観察し、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
<双極性障害における気分エピソードの再発・再燃抑制>
5.2 双極性障害の気分エピソードの急性期治療に対する本剤の有効性及び安全性は確立していない。
6. 用法及び用量
ラモトリギン錠小児用2mg「アメル」
・てんかん患者に用いる場合
小児(錠小児用2mg)
6.4 単剤療法の場合(定型欠神発作に用いる場合)
通常、ラモトリギンとして最初の2週間は1日0.3mg/kgを1日1回又は2回に分割して経口投与し、次の2週間は1日0.6mg/kgを1日1回又は2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大0.6mg/kgずつ漸増する。維持用量は1日1〜10mg/kgとし、1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大0.6mg/kgずつ、1日用量は最大200mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.5 バルプロ酸ナトリウムを併用する場合
通常、ラモトリギンとして最初の2週間は1日0.15mg/kgを1日1回経口投与し、次の2週間は1日0.3mg/kgを1日1回経口投与する。その後は、1〜2週間毎に1日量として最大0.3mg/kgずつ漸増する。維持用量は、バルプロ酸ナトリウムに加えて本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合は1日1〜5mg/kgとし、本剤のグルクロン酸抱合を誘導する薬剤注2)を併用していない場合は1日1〜3mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大200mgまでとする。
6.6 バルプロ酸ナトリウムを併用しない場合注1)
6.6.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、ラモトリギンとして最初の2週間は1日0.6mg/kgを1日2回に分割して経口投与し、次の2週間は1日1.2mg/kgを1日2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大1.2mg/kgずつ漸増する。維持用量は1日5〜15mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大400mgまでとする。
6.6.2 6.6.1以外の薬剤注3)を併用する場合
バルプロ酸ナトリウムを併用する場合に従う。
参考:てんかん患者に用いる場合(小児)
| 併用療法 | 6.4単剤療法の場合 (定型欠神発作に用いる場合) | ||||
| 本剤と併用する薬剤の種類 | 6.5バルプロ酸ナトリウムを併用する場合 | 6.6バルプロ酸ナトリウムを併用しない場合注1) | |||
| 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用しない場合 | 6.6.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.6.2 6.6.1以外の薬剤注3)を併用する場合 | ||
| 1・2週目 | 0.15mg/kg/日 (1日1回投与) | 0.15mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日2回に分割して投与) | 0.15mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回又は2回に分割して投与) |
| 3・4週目 | 0.3mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回投与) | 1.2mg/kg/日 (1日2回に分割して投与) | 0.3mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日1回又は2回に分割して投与) |
| 5週目以降 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大1.2mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.6mg/kg/日ずつ漸増する。 |
| 維持用量 | 1〜5mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 5〜15mg/kg/日 (最大400mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜10mg/kg/日 (最大200mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大0.6mg/kg/日ずつ) |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
ラモトリギン錠小児用5mg「アメル」
・てんかん患者に用いる場合
小児(錠小児用5mg)
6.4 単剤療法の場合(定型欠神発作に用いる場合)
通常、ラモトリギンとして最初の2週間は1日0.3mg/kgを1日1回又は2回に分割して経口投与し、次の2週間は1日0.6mg/kgを1日1回又は2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大0.6mg/kgずつ漸増する。維持用量は1日1〜10mg/kgとし、1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大0.6mg/kgずつ、1日用量は最大200mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.5 バルプロ酸ナトリウムを併用する場合
通常、ラモトリギンとして最初の2週間は1日0.15mg/kgを1日1回経口投与し、次の2週間は1日0.3mg/kgを1日1回経口投与する。その後は、1〜2週間毎に1日量として最大0.3mg/kgずつ漸増する。維持用量は、バルプロ酸ナトリウムに加えて本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合は1日1〜5mg/kgとし、本剤のグルクロン酸抱合を誘導する薬剤注2)を併用していない場合は1日1〜3mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大200mgまでとする。
6.6 バルプロ酸ナトリウムを併用しない場合注1)
6.6.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、ラモトリギンとして最初の2週間は1日0.6mg/kgを1日2回に分割して経口投与し、次の2週間は1日1.2mg/kgを1日2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大1.2mg/kgずつ漸増する。維持用量は1日5〜15mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大400mgまでとする。
6.6.2 6.6.1以外の薬剤注3)を併用する場合
バルプロ酸ナトリウムを併用する場合に従う。
参考:てんかん患者に用いる場合(小児)
| 併用療法 | 6.4単剤療法の場合 (定型欠神発作に用いる場合) | ||||
| 本剤と併用する薬剤の種類 | 6.5バルプロ酸ナトリウムを併用する場合 | 6.6バルプロ酸ナトリウムを併用しない場合注1) | |||
| 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用しない場合 | 6.6.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.6.2 6.6.1以外の薬剤注3)を併用する場合 | ||
| 1・2週目 | 0.15mg/kg/日 (1日1回投与) | 0.15mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日2回に分割して投与) | 0.15mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回又は2回に分割して投与) |
| 3・4週目 | 0.3mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回投与) | 1.2mg/kg/日 (1日2回に分割して投与) | 0.3mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日1回又は2回に分割して投与) |
| 5週目以降 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大1.2mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.6mg/kg/日ずつ漸増する。 |
| 維持用量 | 1〜5mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 5〜15mg/kg/日 (最大400mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜10mg/kg/日 (最大200mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大0.6mg/kg/日ずつ) |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
ラモトリギン錠25mg「アメル」
・てんかん患者に用いる場合
成人(錠25mg)
6.1 単剤療法の場合(部分発作(二次性全般化発作を含む)及び強直間代発作に用いる場合)
通常、ラモトリギンとして最初の2週間は1日25mgを1日1回経口投与し、次の2週間は1日50mgを1日1回経口投与し、5週目は1日100mgを1日1回又は2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大100mgずつ漸増する。維持用量は1日100〜200mgとし、1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大100mgずつ、1日用量は最大400mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.2 バルプロ酸ナトリウムを併用する場合
通常、ラモトリギンとして最初の2週間は1回25mgを隔日に経口投与し、次の2週間は1日25mgを1日1回経口投与する。その後は、1〜2週間毎に1日量として25〜50mgずつ漸増する。維持用量は1日100〜200mgとし、1日2回に分割して経口投与する。
6.3 バルプロ酸ナトリウムを併用しない場合注1)
6.3.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、ラモトリギンとして最初の2週間は1日50mgを1日1回経口投与し、次の2週間は1日100mgを1日2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大100mgずつ漸増する。維持用量は1日200〜400mgとし、1日2回に分割して経口投与する。
6.3.2 6.3.1以外の薬剤注3)を併用する場合
単剤療法の場合に従う。
参考:てんかん患者に用いる場合(成人)
| 併用療法 | 6.1単剤療法の場合 (部分発作(二次性全般化発作を含む)及び強直間代発作に用いる場合) | |||
| 本剤と併用する薬剤の種類 | 6.2バルプロ酸ナトリウムを併用する場合 | 6.3バルプロ酸ナトリウムを併用しない場合注1) | ||
| 6.3.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.3.2 6.3.1以外の薬剤注3)を併用する場合 | |||
| 1・2週目 | 25mgを隔日投与 | 50mg/日 (1日1回投与) | 25mg/日 (1日1回投与) | |
| 3・4週目 | 25mg/日 (1日1回投与) | 100mg/日 (1日2回に分割して投与) | 50mg/日 (1日1回投与) | |
| 5週目以降 | 1〜2週間毎に25〜50mg/日ずつ漸増する。 | 1〜2週間毎に最大100mg/日ずつ漸増する。 | 5週目は100mg/日 (1日1回又は2回に分割して投与) その後1〜2週間毎に最大100mg/日ずつ漸増する。 | |
| 維持用量 | 100〜200mg/日 (1日2回に分割して投与) | 200〜400mg/日 (1日2回に分割して投与) | 100〜200mg/日 (最大400mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大100mg/日ずつ) | |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
小児(錠25mg)
6.4 単剤療法の場合(定型欠神発作に用いる場合)
通常、ラモトリギンとして最初の2週間は1日0.3mg/kgを1日1回又は2回に分割して経口投与し、次の2週間は1日0.6mg/kgを1日1回又は2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大0.6mg/kgずつ漸増する。維持用量は1日1〜10mg/kgとし、1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大0.6mg/kgずつ、1日用量は最大200mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.5 バルプロ酸ナトリウムを併用する場合
通常、ラモトリギンとして最初の2週間は1日0.15mg/kgを1日1回経口投与し、次の2週間は1日0.3mg/kgを1日1回経口投与する。その後は、1〜2週間毎に1日量として最大0.3mg/kgずつ漸増する。維持用量は、バルプロ酸ナトリウムに加えて本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合は1日1〜5mg/kgとし、本剤のグルクロン酸抱合を誘導する薬剤注2)を併用していない場合は1日1〜3mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大200mgまでとする。
6.6 バルプロ酸ナトリウムを併用しない場合注1)
6.6.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、ラモトリギンとして最初の2週間は1日0.6mg/kgを1日2回に分割して経口投与し、次の2週間は1日1.2mg/kgを1日2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大1.2mg/kgずつ漸増する。維持用量は1日5〜15mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大400mgまでとする。
6.6.2 6.6.1以外の薬剤注3)を併用する場合
バルプロ酸ナトリウムを併用する場合に従う。
参考:てんかん患者に用いる場合(小児)
| 併用療法 | 6.4単剤療法の場合 (定型欠神発作に用いる場合) | ||||
| 本剤と併用する薬剤の種類 | 6.5バルプロ酸ナトリウムを併用する場合 | 6.6バルプロ酸ナトリウムを併用しない場合注1) | |||
| 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用しない場合 | 6.6.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.6.2 6.6.1以外の薬剤注3)を併用する場合 | ||
| 1・2週目 | 0.15mg/kg/日 (1日1回投与) | 0.15mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日2回に分割して投与) | 0.15mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回又は2回に分割して投与) |
| 3・4週目 | 0.3mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回投与) | 1.2mg/kg/日 (1日2回に分割して投与) | 0.3mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日1回又は2回に分割して投与) |
| 5週目以降 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大1.2mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.6mg/kg/日ずつ漸増する。 |
| 維持用量 | 1〜5mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 5〜15mg/kg/日 (最大400mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜10mg/kg/日 (最大200mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大0.6mg/kg/日ずつ) |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
・双極性障害における気分エピソードの再発・再燃抑制に用いる場合(錠25mg)
6.1 単剤療法の場合
通常、成人にはラモトリギンとして最初の2週間は1日25mgを1日1回経口投与、次の2週間は1日50mgを1日1回又は2回に分割して経口投与し、5週目は1日100mgを1日1回又は2回に分割して経口投与する。6週目以降は維持用量として1日200mgを1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大100mgずつ、1日用量は最大400mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.2 バルプロ酸ナトリウムを併用する場合
通常、成人にはラモトリギンとして最初の2週間は1回25mgを隔日に経口投与、次の2週間は1日25mgを1日1回経口投与し、5週目は1日50mgを1日1回又は2回に分割して経口投与する。6週目以降は維持用量として1日100mgを1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大50mgずつ、1日用量は最大200mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.3 バルプロ酸ナトリウムを併用しない場合注1)
6.3.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、成人にはラモトリギンとして最初の2週間は1日50mgを1日1回経口投与、次の2週間は1日100mgを1日2回に分割して経口投与し、5週目は1日200mgを1日2回に分割して経口投与する。6週目は1日300mgを1日2回に分割して経口投与し、7週目以降は維持用量として1日300〜400mgを1日2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大100mgずつ、1日用量は最大400mgまでとし、いずれも1日2回に分割して経口投与する。
6.3.2 6.3.1以外の薬剤注3)を併用する場合
単剤療法の場合に従う。
参考:双極性障害における気分エピソードの再発・再燃抑制に用いる場合(成人)
| 併用療法 | 6.1単剤療法の場合 | |||
| 本剤と併用する薬剤の種類 | 6.2バルプロ酸ナトリウムを併用する場合 | 6.3バルプロ酸ナトリウムを併用しない場合注1) | ||
| 6.3.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.3.2 6.3.1以外の薬剤注3)を併用する場合 | |||
| 1・2週目 | 25mgを隔日投与 | 50mg/日 (1日1回投与) | 25mg/日 (1日1回投与) | |
| 3・4週目 | 25mg/日 (1日1回投与) | 100mg/日 (1日2回に分割して投与) | 50mg/日 (1日1回又は2回に分割して投与) | |
| 5週目 | 50mg/日 (1日1回又は2回に分割して投与) | 200mg/日 (1日2回に分割して投与) | 100mg/日 (1日1回又は2回に分割して投与) | |
| 6週目以降 | 100mg/日 (最大200mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大50mg/日ずつ) | 6週目300mg/日 7週目以降300〜400mg/日 (最大400mg/日) (1日2回に分割して投与) (増量は1週間以上の間隔をあけて最大100mg/日ずつ) | 200mg/日 (最大400mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大100mg/日ずつ) | |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
ラモトリギン錠100mg「アメル」
・てんかん患者に用いる場合
成人(錠100mg)
6.1 単剤療法の場合(部分発作(二次性全般化発作を含む)及び強直間代発作に用いる場合)
通常、ラモトリギンとして最初の2週間は1日25mgを1日1回経口投与し、次の2週間は1日50mgを1日1回経口投与し、5週目は1日100mgを1日1回又は2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大100mgずつ漸増する。維持用量は1日100〜200mgとし、1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大100mgずつ、1日用量は最大400mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.2 バルプロ酸ナトリウムを併用する場合
通常、ラモトリギンとして最初の2週間は1回25mgを隔日に経口投与し、次の2週間は1日25mgを1日1回経口投与する。その後は、1〜2週間毎に1日量として25〜50mgずつ漸増する。維持用量は1日100〜200mgとし、1日2回に分割して経口投与する。
6.3 バルプロ酸ナトリウムを併用しない場合注1)
6.3.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、ラモトリギンとして最初の2週間は1日50mgを1日1回経口投与し、次の2週間は1日100mgを1日2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大100mgずつ漸増する。維持用量は1日200〜400mgとし、1日2回に分割して経口投与する。
6.3.2 6.3.1以外の薬剤注3)を併用する場合
単剤療法の場合に従う。
参考:てんかん患者に用いる場合(成人)
| 併用療法 | 6.1単剤療法の場合 (部分発作(二次性全般化発作を含む)及び強直間代発作に用いる場合) | |||
| 本剤と併用する薬剤の種類 | 6.2バルプロ酸ナトリウムを併用する場合 | 6.3バルプロ酸ナトリウムを併用しない場合注1) | ||
| 6.3.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.3.2 6.3.1以外の薬剤注3)を併用する場合 | |||
| 1・2週目 | 25mgを隔日投与 | 50mg/日 (1日1回投与) | 25mg/日 (1日1回投与) | |
| 3・4週目 | 25mg/日 (1日1回投与) | 100mg/日 (1日2回に分割して投与) | 50mg/日 (1日1回投与) | |
| 5週目以降 | 1〜2週間毎に25〜50mg/日ずつ漸増する。 | 1〜2週間毎に最大100mg/日ずつ漸増する。 | 5週目は100mg/日 (1日1回又は2回に分割して投与) その後1〜2週間毎に最大100mg/日ずつ漸増する。 | |
| 維持用量 | 100〜200mg/日 (1日2回に分割して投与) | 200〜400mg/日 (1日2回に分割して投与) | 100〜200mg/日 (最大400mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大100mg/日ずつ) | |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
小児(錠100mg)
6.4 単剤療法の場合(定型欠神発作に用いる場合)
通常、ラモトリギンとして最初の2週間は1日0.3mg/kgを1日1回又は2回に分割して経口投与し、次の2週間は1日0.6mg/kgを1日1回又は2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大0.6mg/kgずつ漸増する。維持用量は1日1〜10mg/kgとし、1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大0.6mg/kgずつ、1日用量は最大200mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.5 バルプロ酸ナトリウムを併用する場合
通常、ラモトリギンとして最初の2週間は1日0.15mg/kgを1日1回経口投与し、次の2週間は1日0.3mg/kgを1日1回経口投与する。その後は、1〜2週間毎に1日量として最大0.3mg/kgずつ漸増する。維持用量は、バルプロ酸ナトリウムに加えて本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合は1日1〜5mg/kgとし、本剤のグルクロン酸抱合を誘導する薬剤注2)を併用していない場合は1日1〜3mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大200mgまでとする。
6.6 バルプロ酸ナトリウムを併用しない場合注1)
6.6.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、ラモトリギンとして最初の2週間は1日0.6mg/kgを1日2回に分割して経口投与し、次の2週間は1日1.2mg/kgを1日2回に分割して経口投与する。その後は、1〜2週間毎に1日量として最大1.2mg/kgずつ漸増する。維持用量は1日5〜15mg/kgとし、1日2回に分割して経口投与する。なお、1日用量は最大400mgまでとする。
6.6.2 6.6.1以外の薬剤注3)を併用する場合
バルプロ酸ナトリウムを併用する場合に従う。
参考:てんかん患者に用いる場合(小児)
| 併用療法 | 6.4単剤療法の場合 (定型欠神発作に用いる場合) | ||||
| 本剤と併用する薬剤の種類 | 6.5バルプロ酸ナトリウムを併用する場合 | 6.6バルプロ酸ナトリウムを併用しない場合注1) | |||
| 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用しない場合 | 6.6.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.6.2 6.6.1以外の薬剤注3)を併用する場合 | ||
| 1・2週目 | 0.15mg/kg/日 (1日1回投与) | 0.15mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日2回に分割して投与) | 0.15mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回又は2回に分割して投与) |
| 3・4週目 | 0.3mg/kg/日 (1日1回投与) | 0.3mg/kg/日 (1日1回投与) | 1.2mg/kg/日 (1日2回に分割して投与) | 0.3mg/kg/日 (1日1回投与) | 0.6mg/kg/日 (1日1回又は2回に分割して投与) |
| 5週目以降 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大1.2mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.3mg/kg/日ずつ漸増する。 | 1〜2週間毎に最大0.6mg/kg/日ずつ漸増する。 |
| 維持用量 | 1〜5mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 5〜15mg/kg/日 (最大400mg/日) (1日2回に分割して投与) | 1〜3mg/kg/日 (最大200mg/日) (1日2回に分割して投与) | 1〜10mg/kg/日 (最大200mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大0.6mg/kg/日ずつ) |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
・双極性障害における気分エピソードの再発・再燃抑制に用いる場合(錠100mg)
6.1 単剤療法の場合
通常、成人にはラモトリギンとして最初の2週間は1日25mgを1日1回経口投与、次の2週間は1日50mgを1日1回又は2回に分割して経口投与し、5週目は1日100mgを1日1回又は2回に分割して経口投与する。6週目以降は維持用量として1日200mgを1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大100mgずつ、1日用量は最大400mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.2 バルプロ酸ナトリウムを併用する場合
通常、成人にはラモトリギンとして最初の2週間は1回25mgを隔日に経口投与、次の2週間は1日25mgを1日1回経口投与し、5週目は1日50mgを1日1回又は2回に分割して経口投与する。6週目以降は維持用量として1日100mgを1日1回又は2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大50mgずつ、1日用量は最大200mgまでとし、いずれも1日1回又は2回に分割して経口投与する。
6.3 バルプロ酸ナトリウムを併用しない場合注1)
6.3.1 本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合
通常、成人にはラモトリギンとして最初の2週間は1日50mgを1日1回経口投与、次の2週間は1日100mgを1日2回に分割して経口投与し、5週目は1日200mgを1日2回に分割して経口投与する。6週目は1日300mgを1日2回に分割して経口投与し、7週目以降は維持用量として1日300〜400mgを1日2回に分割して経口投与する。症状に応じて適宜増減するが、増量は1週間以上の間隔をあけて1日量として最大100mgずつ、1日用量は最大400mgまでとし、いずれも1日2回に分割して経口投与する。
6.3.2 6.3.1以外の薬剤注3)を併用する場合
単剤療法の場合に従う。
参考:双極性障害における気分エピソードの再発・再燃抑制に用いる場合(成人)
| 併用療法 | 6.1単剤療法の場合 | |||
| 本剤と併用する薬剤の種類 | 6.2バルプロ酸ナトリウムを併用する場合 | 6.3バルプロ酸ナトリウムを併用しない場合注1) | ||
| 6.3.1本剤のグルクロン酸抱合を誘導する薬剤注2)を併用する場合 | 6.3.2 6.3.1以外の薬剤注3)を併用する場合 | |||
| 1・2週目 | 25mgを隔日投与 | 50mg/日 (1日1回投与) | 25mg/日 (1日1回投与) | |
| 3・4週目 | 25mg/日 (1日1回投与) | 100mg/日 (1日2回に分割して投与) | 50mg/日 (1日1回又は2回に分割して投与) | |
| 5週目 | 50mg/日 (1日1回又は2回に分割して投与) | 200mg/日 (1日2回に分割して投与) | 100mg/日 (1日1回又は2回に分割して投与) | |
| 6週目以降 | 100mg/日 (最大200mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大50mg/日ずつ) | 6週目300mg/日 7週目以降300〜400mg/日 (最大400mg/日) (1日2回に分割して投与) (増量は1週間以上の間隔をあけて最大100mg/日ずつ) | 200mg/日 (最大400mg/日) (1日1回又は2回に分割して投与) (増量は1週間以上の間隔をあけて最大100mg/日ずつ) | |
本剤は主としてグルクロン酸転移酵素で代謝される。
注1)本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。
注2)本剤のグルクロン酸抱合を誘導する薬剤
注3)本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
7. 用法及び用量に関連する注意
<効能共通>
7.1 発疹等の皮膚障害の発現率は、定められた用法及び用量を超えて投与した場合に高いことが示されているので、併用する薬剤の組み合わせに留意して、6.用法及び用量を遵守すること。なお、体重換算等により調節した用量に一致する錠剤の組み合わせがない場合には、調節した用量に最も近く、かつ超えない用量になるよう錠剤を組み合わせて投与すること。[1.1.1、1.1.2、7.3、8.1、11.1.1、17.3.1、17.3.2参照]
7.2 併用する薬剤については以下のとおり分類されるので留意すること。なお、本剤のグルクロン酸抱合に対する影響が明らかでない薬剤による併用療法では、バルプロ酸ナトリウムを併用する場合の用法及び用量に従うこと。[6.、10.2、16.7.1、16.7.2参照]
・本剤のグルクロン酸抱合を誘導する薬剤
フェニトイン、カルバマゼピン、フェノバルビタール、プリミドン、リファンピシン、ロピナビル・リトナビル配合剤
・本剤のグルクロン酸抱合に対し影響を及ぼさない薬剤
アリピプラゾール、オランザピン、ゾニサミド、ガバペンチン、シメチジン、トピラマート、プレガバリン、リチウム、レベチラセタム、ペランパネル、ラコサミド
7.3 本剤による発疹等の皮膚症状のために投与を中止した場合には、治療上の有益性が危険性を上回ると判断される場合以外は再投与しないこと。再投与にあたっては、いかなる理由で投与を中止した患者においても、維持用量より低い用量から漸増すること。なお、投与中止から本剤の消失半減期の5倍の期間(バルプロ酸ナトリウムを併用した時は約350時間、バルプロ酸ナトリウムを併用せず本剤のグルクロン酸抱合を誘導する薬剤を併用した時は約65時間(いずれも外国人のデータ)、バルプロ酸ナトリウムも本剤のグルクロン酸抱合を誘導する薬剤も併用しなかった時は約170時間)を経過している場合は、初回用量から6.用法及び用量に従って再開することが推奨される。[7.1、10.2、16.7.1、16.7.2参照]
7.4 本剤投与中に、本剤のグルクロン酸抱合を阻害あるいは誘導する薬剤を投与開始又は投与中止する場合には、本剤の用量調節を考慮すること。
<各種てんかんの治療>
7.5 本剤を定型欠神発作以外の小児てんかん患者に用いる場合には、他の抗てんかん薬と併用して使用すること。定型欠神発作以外の国内臨床試験において、本剤単独投与での使用経験はない。[9.7.3参照]
7.6 小児てんかん患者へ投与する場合に、投与初期(1〜2週)に体重換算した1日用量が1〜2mgの範囲内であった場合は2mg錠を隔日に1錠服用する。体重換算した1日用量が1mg未満の場合は本剤を服用してはならない。本剤投与中は、体重変化を観察し、必要に応じ適切に用量の変更を行うこと。なお、2〜6歳の小児の場合は維持用量の上限付近の用量が必要な場合がある。
8. 重要な基本的注意
<効能共通>
8.1 本剤の投与による発疹は斑状・丘疹状にあらわれることが多く、重篤な皮膚障害の発現率は、本剤投与開始から8週間以内に高く、また、バルプロ酸ナトリウムと併用した場合、あるいは小児において高いことが示されているので、本剤の投与にあたっては十分に注意し、異常が認められた場合には、投与を中止し適切な処置を行うこと。[1.3、7.1、9.7.1、11.1.1、17.3.1、17.3.2参照]
<各種てんかんの治療>
8.5 眠気、注意力・集中力・反射運動能力等の低下が起こることがある。自動車の運転等危険を伴う機械操作の適否は、関連学会の留意事項1)を十分理解の上、医師が慎重に判断し、危険を伴う機械操作を行う場合には十分な注意が必要であることを適切に患者に指導すること。また、眠気等があらわれた場合には、自動車の運転等危険を伴う機械の操作に従事しないよう、患者に指導すること。
8.6 てんかん患者では、連用中における投与量の急激な減少ないし投与の中止により、てんかん発作の増悪又はてんかん重積状態があらわれることがあるので、投与を中止する場合には、発疹の発現等安全性の観点から直ちに投与を中止しなければならない場合を除き、少なくとも2週間以上かけて徐々に減量するなど慎重に行うこと。
<双極性障害における気分エピソードの再発・再燃抑制>
8.7 眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、本剤投与中の患者には自動車の運転等、危険を伴う機械の操作に従事させないよう注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 脳の器質的障害又は統合失調症の素因のある患者
精神症状を増悪させることがある。
9.1.3 他の抗てんかん薬に対しアレルギー歴又は発疹発現の既往歴がある患者
重篤ではない発疹の発現頻度が約3倍になる。
9.1.4 Brugada症候群の患者
Brugada症候群に特徴的な心電図変化(右脚ブロック及び右側胸部誘導(V1〜V3)のcoved型ST上昇)が顕在化したとの報告がある。
9.1.5 心不全、基礎心疾患(心筋梗塞、弁膜症、心筋症等)、刺激伝導障害のある患者
刺激伝導障害を起こす又は悪化させる可能性がある。In vitro試験においてヒト心筋型電位依存性Na+チャネル電流を抑制し、抗不整脈薬クラスIb群に属する薬剤と同様の特性を有することが示された。
9.2 腎機能障害患者
9.2.1 腎不全患者
腎クリアランスが低下しているために、主代謝物(グルクロン酸抱合体)の血漿中濃度が健康成人よりも高くなることがある。[16.6.1参照]
9.3 肝機能障害患者
減量を考慮すること。肝機能障害の程度に応じて本剤のクリアランスが低下し、消失半減期が延長することがある。[16.6.2参照]
9.5 妊婦
9.5.1 以下の報告を考慮し、妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
・海外での複数のプロスペクティブ調査において、妊娠第1三半期に本剤を単独投与された総計2000例以上の妊婦の情報が収集されている。本剤使用による大奇形発現リスクの実質的な増加は認められていないが、いくつかの妊娠調査において孤発性の口蓋口唇裂奇形発現リスクの増加が報告されている。ケースコントロール研究においては、他の奇形と比較して、本剤の使用に伴う口蓋口唇裂の発現リスクが高いとの結果は得られていない。本妊娠調査のデータは、多剤併用療法時の先天異常発現のリスクに対する本剤の影響について評価するのに十分なものではない。
・動物(ラット)において本剤の胎児への移行が認められたとの報告がある。
・動物を用いた生殖発生毒性試験において催奇形性作用は認められなかったが、本剤はジヒドロ葉酸還元酵素に対し弱い阻害作用を有するため、妊娠中に本剤を投与した場合、胎児奇形を誘発する危険性が考えられる。また、ラットでヒト最大用量である400mg/日の0.12倍以上の投与量[体表面積換算(mg/m2)に基づく]において母動物の一般状態の悪化に関連した胎児体重の低値、着床後胚・胎児死亡率及び死産児数の増加、胎児骨格変異の発現頻度増加、出生児における神経行動学的異常、出生児回収率(哺育中の巣から出生児を離し、5分以内に母動物が巣内に出生児を連れ戻す)の低下又は出生後の生存率低下がみられた。
9.5.2 妊娠により本剤の血中濃度や治療効果に影響がみられる可能性があるため(妊娠中に本剤の血中濃度が低下したという報告がある)、妊婦に対し本剤を投与する場合には、患者の状態等に十分注意すること。
9.6 授乳婦
本剤投与中は授乳を避けさせること。本剤はヒト乳汁中へ移行し、授乳中の乳児における血中濃度は、授乳中の女性の血中濃度の最大約50%に達したとの報告がある2)。また、授乳されている新生児、乳児において、無呼吸、傾眠、体重増加不良等を起こすことが報告されている。
9.7 小児等
<効能共通>
9.7.2 小児において、発疹の初期徴候は感染と誤診されやすいので、本剤投与開始8週間以内に発疹及び発熱等の症状が発現した場合には特に注意すること。
<各種てんかんの治療>
9.7.3 低出生体重児、新生児、乳児又は2歳未満の幼児、及び定型欠神発作以外の単剤療法に対する国内臨床試験は実施していない。[7.5参照]
<双極性障害における気分エピソードの再発・再燃抑制>
9.7.4 小児及び18歳未満の患者を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に、生理機能が低下している。
10. 相互作用
相互作用序文
ラモトリギンは主としてグルクロン酸転移酵素(主にUGT1A4)で代謝される。[16.4参照]
薬物代謝酵素用語
グルクロン酸転移酵素(主にUGT1A4)
10.2 併用注意
| バルプロ酸ナトリウム [7.2、7.3、16.7.1、16.7.2参照] | 本剤の消失半減期が約2倍延長するとの報告がある。 | 肝におけるグルクロン酸抱合が競合する。 |
| 本剤のグルクロン酸抱合を誘導する薬剤 フェニトイン カルバマゼピン フェノバルビタール プリミドン リファンピシン ロピナビル・リトナビル配合剤 [7.2、7.3、16.7.1、16.7.2参照] | 本剤の血中濃度が低下する。 | 肝における本剤のグルクロン酸抱合が促進される。 |
| アタザナビル+リトナビル [16.7.2参照] | アタザナビル及びリトナビル両剤と本剤を併用した場合に本剤の血中濃度が低下したとの報告がある。 本剤維持用量投与中にアタザナビルとリトナビルを投与開始又は投与中止する場合には、本剤の用量調節を考慮すること。 | 肝における本剤のグルクロン酸抱合が促進される。 |
| カルバマゼピン [6.参照] | 本剤とカルバマゼピンの併用により、めまい、失調、複視、霧視、嘔気等が発現したという報告があり、通常、これらの症状はカルバマゼピンの減量により回復する。 | 機序不明 |
| リスペリドン [16.7.2参照] | 本剤とリスペリドンの併用時には、それぞれの単独投与時に比較して、傾眠の報告が多いとの報告がある。 | 機序不明 |
| 経口避妊薬(卵胞ホルモン・黄体ホルモン配合剤) [16.7.2参照] | 本剤とエチニルエストラジオール・レボノルゲストレル配合剤との併用において、以下の報告がある。 1)本剤の血中濃度が減少したとの報告があるので、本剤維持用量投与中に経口避妊薬を投与開始又は投与中止する場合には、本剤の用量調節を考慮すること。 2)レボノルゲストレルの血中濃度が減少し、血中卵胞ホルモン(FSH)及び黄体形成ホルモン(LH)が上昇し、エストラジオールが僅かに上昇したとの報告がある。 | 1)肝における本剤のグルクロン酸抱合が促進される。 2)機序不明 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(0.5%)、多形紅斑(頻度不明)
11.1.2 薬剤性過敏症症候群(頻度不明)
発疹、発熱等が初期にみられることがあり、更にリンパ節腫脹、顔面浮腫、血液障害(好酸球増多、白血球増加、異型リンパ球の出現)及び臓器障害(肝機能障害等)の種々の全身症状があらわれることがある。薬剤性過敏症症候群の徴候又は症状3)は遅発性に発現する。薬剤性過敏症症候群の徴候が認められた場合には、本剤の投与を直ちに中止し、適切な処置を行うこと。
また、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがある。なお、過敏症の初期症状は、発疹を伴わないこともあるので、発疹以外の症状(発熱又はリンパ節腫脹等)の発現にも注意が必要である。[1.2参照]
また、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがある。なお、過敏症の初期症状は、発疹を伴わないこともあるので、発疹以外の症状(発熱又はリンパ節腫脹等)の発現にも注意が必要である。[1.2参照]
11.1.3 再生不良性貧血(頻度不明)、汎血球減少(頻度不明)、無顆粒球症(頻度不明)
11.1.4 血球貪食症候群(頻度不明)
発熱、発疹、神経症状、脾腫、リンパ節腫脹、血球減少、高フェリチン血症、高トリグリセリド血症、肝機能障害、血液凝固障害等の異常が認められた場合には、直ちに投与を中止し、適切な処置を行うこと。
11.1.5 肝炎、肝機能障害及び黄疸(0.1%)
11.1.6 無菌性髄膜炎(頻度不明)
項部硬直、発熱、頭痛、悪心・嘔吐又は意識混濁等の症状を伴う無菌性髄膜炎があらわれることがある。本剤の再投与により、さらに重篤な症状を伴う無菌性髄膜炎が投与後すぐに再発したとの報告がある。
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 皮膚 | 発疹 | 脱毛 | 光線過敏性反応 | |
| 全身症状 | 発熱、疲労、疼痛 | |||
| 精神神経系 | 傾眠(15%)、めまい | 頭痛、不眠、不安・焦燥・興奮、てんかん発作回数の増加 | 易刺激性、運動障害、失調、振戦、幻覚、眼振、攻撃性 | 平衡障害、チック、錯乱、パーキンソン症状の悪化、錐体外路症状、舞踏病アテトーゼ、悪夢 |
| 消化器 | 胃腸障害(嘔気・嘔吐、下痢等) | 食欲不振 | ||
| 肝臓 | 肝機能検査値異常 | |||
| 血液 | 白血球減少、好中球減少、貧血 | 血小板減少、リンパ節症 | 低ガンマグロブリン血症、偽リンパ腫 | |
| 眼 | 複視 | 霧視、結膜炎 | ||
| 筋骨格系 | 背部痛、関節痛 | |||
| その他 | ループス様反応 |
13. 過量投与
13.1 症状
QRS延長の発現が報告されている。用量上限の10〜20倍量により眼振、失調、意識障害、大発作痙攣、昏睡等の症状の発現が報告されている。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.2 本剤は少量の水と共にそのまま服用する、あるいは咀嚼又は少なくとも錠剤が浸る程度の少量の水に溶かして服用するよう指導すること。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 海外で実施された本剤を含む複数の抗てんかん薬における、てんかん、精神疾患等を対象とした199のプラセボ対照臨床試験の検討結果において、自殺念慮及び自殺企図の発現のリスクが、抗てんかん薬の服用群でプラセボ群と比較して約2倍高く(抗てんかん薬服用群:0.43%、プラセボ群:0.24%)、抗てんかん薬の服用群では、プラセボ群と比べ1000人あたり1.9人多いと計算された(95%信頼区間:0.6-3.9)。また、てんかん患者のサブグループでは、プラセボ群と比べ1000人あたり2.4人多いと計算されている。[8.2-8.4、9.1.1参照]
15.1.2 本剤はジヒドロ葉酸還元酵素に対し弱い阻害作用を有するため、長期投与により葉酸代謝を阻害する可能性がある。なお、ヒトにおける長期投与の成績において、投与1年目まではヘモグロビン値、平均赤血球容積、血清中及び赤血球中の葉酸濃度に有意な変化は認められず、また、投与5年目まで赤血球中の葉酸濃度に有意な変化は認められなかった。
16. 薬物動態
16.1 血中濃度
16.1.1 健康成人
健康成人6例にラモトリギン25〜200mgを単回経口投与した時、投与後1.7〜2.5時間でCmaxに達し、T1/2は約31〜38時間であった。Cmax及びAUC0-∞は投与量の増加に伴い増大した。また、健康成人6例にラモトリギン50mgを1日2回10日間反復経口投与した時、血漿中ラモトリギン濃度は投与6日目に定常状態に達した4)。
| 投与量(mg) | 例 | Cmax(μg/mL) | Tmax(hr) | T1/2(hr) | AUC0-∞(μg・hr/mL) | CLt/F(mL/min) | Vd/F(L) |
| 25 | 6 | 0.338±0.031 | 1.7±0.8 | 37.9±11.1 | 15.2±4.9 | 29.77±9.12 | 91.0±8.1 |
| 50 | 6 | 0.718±0.049 | 2.5±1.2 | 35.0±4.7 | 33.7±5.9 | 25.33±4.09 | 75.2±4.8 |
| 100 | 6 | 1.488±0.261 | 2.3±1.4 | 30.5±3.3 | 59.9±12.1 | 28.79±5.65 | 74.2±9.2 |
| 200 | 6 | 3.075±0.336 | 2.5±1.0 | 32.4±5.5 | 136.1±33.2 | 25.64±5.69 | 69.8±9.3 |
16.1.2 てんかん患者
成人てんかん患者を対象とした国内臨床試験において、ラモトリギン200mgを投与した時の血中ラモトリギン濃度は、バルプロ酸ナトリウムを併用し、ラモトリギンのグルクロン酸抱合を誘導する薬剤を併用しない場合は9.6μg/mL、バルプロ酸ナトリウムを併用せず、ラモトリギンのグルクロン酸抱合を誘導する薬剤を併用した場合は2.2μg/mLであった5)。
成人又は小児てんかん患者を対象とした国内臨床試験において、既存の抗てんかん薬の投与を受けている患者にラモトリギンを投与した時の定常状態における血中ラモトリギン濃度を以下に示した。併用抗てんかん薬によりラモトリギンの維持用量は異なるが、同様の血中濃度が示された。また、ラモトリギンの投与前後で併用抗てんかん薬の血中濃度に顕著な差は認められなかった5)。
成人又は小児てんかん患者を対象とした国内臨床試験において、既存の抗てんかん薬の投与を受けている患者にラモトリギンを投与した時の定常状態における血中ラモトリギン濃度を以下に示した。併用抗てんかん薬によりラモトリギンの維持用量は異なるが、同様の血中濃度が示された。また、ラモトリギンの投与前後で併用抗てんかん薬の血中濃度に顕著な差は認められなかった5)。
| 併用薬剤 | ラモトリギン維持用量(mg/日) | 患者数(サンプル数) | 血漿中ラモトリギン濃度注2)(μg/mL) | ||
| バルプロ酸ナトリウム | ラモトリギンのグルクロン酸抱合を誘導する薬剤注1) | ラモトリギンとの薬物相互作用が明らかでない抗てんかん薬 | |||
| 併用 | 併用又は非併用 | 併用又は非併用 | 100〜200 | 5(10) | 3.25(1.44〜9.58) |
| 非併用 | 併用 | 併用又は非併用 | 200〜400 | 60(99) | 2.81(0.32〜7.28) |
| 併用薬剤 | ラモトリギン維持用量(mg/kg/日) | 患者数(サンプル数) | 血漿中ラモトリギン濃度注2)(μg/mL) | ||
| バルプロ酸ナトリウム | ラモトリギンのグルクロン酸抱合を誘導する薬剤注1) | ラモトリギンとの薬物相互作用が明らかでない抗てんかん薬 | |||
| 併用 | 非併用 | 併用又は非併用 | 1〜3 | 18(45) | 3.85(1.07〜11.38) |
| 併用 | 1〜5 | 48(101) | 2.32(0.29〜5.91) | ||
| 非併用 | 非併用 | 併用 | |||
| 併用 | 併用又は非併用 | 5〜15 | 30(54) | 3.30(0.70〜9.82) | |
16.1.3 生物学的同等性試験
<ラモトリギン錠小児用2mg「アメル」、ラモトリギン錠小児用5mg「アメル」>
ラモトリギン錠小児用2mg「アメル」及びラモトリギン錠小児用5mg「アメル」と各標準製剤について、下記のとおりクロスオーバー法により健康成人男子に水あり(少量の水でそのまま咀嚼せずに服用)又は咀嚼(水あり)(咀嚼後、少量の水で服用)で絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された8)。
| 標準製剤 | 試験投与量 | |
| ラモトリギン錠小児用2mg「アメル」 | ラミクタール錠小児用2mg | それぞれ1錠(ラモトリギンとして2mg) |
| ラモトリギン錠小児用5mg「アメル」 | ラミクタール錠小児用5mg | それぞれ1錠(ラモトリギンとして5mg) |
| 判定パラメータ | 参考パラメータ | |||
| AUC(0→72)(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | |
| ラモトリギン錠小児用2mg「アメル」 | 1227±207 | 34.44±3.89 | 1.4±0.8 | 50.7±23.2 |
| ラミクタール錠小児用2mg | 1233±190 | 35.72±4.73 | 1.0±0.8 | 49.6±19.8 |
図1 血漿中未変化体濃度(生物学的同等性、水あり、少量の水でそのまま咀嚼せずに服用)
| 判定パラメータ | 参考パラメータ | |||
| AUC(0→72)(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | |
| ラモトリギン錠小児用2mg「アメル」 | 1152±138 | 33.31±3.70 | 0.9±0.7 | 46.8±9.7 |
| ラミクタール錠小児用2mg | 1137±157 | 34.03±4.10 | 1.0±0.8 | 43.8±8.8 |
図2 血漿中未変化体濃度(生物学的同等性、水あり、咀嚼後、少量の水で服用)
| 判定パラメータ | 参考パラメータ | |||
| AUC(0→72)(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | |
| ラモトリギン錠小児用5mg「アメル」 | 2279±298 | 65.48±8.36 | 1.3±0.8 | 44.7±8.5 |
| ラミクタール錠小児用5mg | 2327±261 | 67.26±9.12 | 1.2±0.8 | 45.9±9.0 |
図3 血漿中未変化体濃度(生物学的同等性、水あり、少量の水でそのまま咀嚼せずに服用)
| 判定パラメータ | 参考パラメータ | |||
| AUC(0→72)(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | |
| ラモトリギン錠小児用5mg「アメル」 | 2544±272 | 72.16±10.93 | 1.0±0.5 | 44.2±7.0 |
| ラミクタール錠小児用5mg | 2549±314 | 73.41±15.47 | 1.0±0.6 | 44.7±6.6 |
図4 血漿中未変化体濃度(生物学的同等性、水あり、咀嚼後、少量の水で服用)
<ラモトリギン錠100mg「アメル」>
ラモトリギン錠100mg「アメル」とラミクタール錠100mgを、クロスオーバー法によりそれぞれ1錠(ラモトリギンとして100mg)健康成人男子に水あり(少量の水でそのまま咀嚼せずに服用)又は咀嚼(水あり)(咀嚼後、少量の水で服用)で絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された8)。
| 判定パラメータ | 参考パラメータ | |||
| AUC(0→96)(μg・hr/mL) | Cmax(μg/mL) | Tmax(hr) | T1/2(hr) | |
| ラモトリギン錠100mg「アメル」 | 78.02±13.76 | 1.76±0.23 | 1.38±0.94 | 43.90±10.12 |
| ラミクタール錠100mg | 76.92±13.73 | 1.74±0.23 | 1.46±0.98 | 45.21±14.52 |
図5 血漿中未変化体濃度(生物学的同等性、水あり、少量の水でそのまま咀嚼せずに服用)
| 判定パラメータ | 参考パラメータ | |||
| AUC(0→96)(μg・hr/mL) | Cmax(μg/mL) | Tmax(hr) | T1/2(hr) | |
| ラモトリギン錠100mg「アメル」 | 77.90±11.01 | 1.79±0.32 | 1.46±1.06 | 49.66±13.16 |
| ラミクタール錠100mg | 77.36±11.32 | 1.75±0.21 | 1.18±0.89 | 48.07±11.91 |
図6 血漿中未変化体濃度(生物学的同等性、水あり、咀嚼後、少量の水で服用)
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.2.1 食事の影響
健康成人12例にラモトリギン150mgを空腹時及び食後に単回経口投与した時、食後投与では空腹時に比べ血漿中ラモトリギンのTmaxは遅延したが、AUCに有意な差を認めなかった9)(外国人データ)。
16.2.2 生物学的利用率
健康成人8例にラモトリギン75mgを単回経口投与した時の生物学的利用率は97.6%であった10)(外国人データ)。
16.3 分布
In vitroでのラモトリギン(1〜10μg/mL)のヒト血漿蛋白結合率は53.1〜56.2%であった11)。
16.4 代謝
16.5 排泄
健康成人6例に14C-ラモトリギン240mg(15μCi)を単回経口投与した時、投与後168時間までに糞中に約2%、尿中に約94%が排泄された。尿中へは主にラモトリギン-N2-グルクロン酸抱合体(約71%)として排泄され、以下未変化体(10%)、ラモトリギン-N5-グルクロン酸抱合体(5〜10%)及びラモトリギン-N2-メチル体(0.14%)の順であった15)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
16.6.2 肝機能障害患者
健康成人12例及び肝硬変患者24例にラモトリギン100mgを単回経口投与した時のラモトリギンの薬物動態パラメータを以下に示した。中等度肝硬変患者においてCmaxの低下がみられたものの、他のパラメータでは健康成人との間に顕著な差はみられなかった。重度肝硬変患者では健康成人と比較してCmax及びTmax以外のパラメータに差がみられ、AUC0-∞及びT1/2は腹水なしで約2倍、腹水ありで約4倍増加し、CL/Fは腹水なしで2/3、腹水ありで1/3に減少した18)19)(外国人データ)。[9.3参照]
| 健康被験者 (対照群) (12例) | 中等度肝硬変患者 (12例) | 重度肝硬変患者 | ||
| 腹水なし (7例) | 腹水あり (5例) | |||
| Child-Pugh分類 | − | A | B | C |
| Cmax(μg/mL) | 1.61(1.14-2.53) | 1.34(0.99-1.81) | 1.48(1.22-2.26) | 1.65(1.12-1.84) |
| Tmax(hr) | 1.00(1.00-8.00) | 1.00(1.00-4.00) | 1.00(1.00-4.00) | 2.00(1.00-9.52) |
| T1/2(hr) | 32.16(22.27-49.29) | 35.99(30.16-89.08) | 59.68(34.79-145.12) | 110.13(50.11-158.14) |
| AUC0-∞(μg・hr/mL) | 69.07(38.77-98.09) | 70.60(47.86-215.75) | 110.72(73.53-225.35) | 248.86(73.72-368.62) |
| CL/F(mL/min/kg) | 0.338(0.267-0.593) | 0.312(0.165-0.443) | 0.237(0.114-0.356) | 0.103(0.061-0.260) |
16.6.3 高齢者
高齢者12例(65歳以上、クレアチニンクリアランス:平均61mL/min)にラモトリギン150mgを単回経口投与した時、ラモトリギンのCmax、AUC0-∞、T1/2及びCL/Fの平均値(標準偏差)は各々2.35(0.40)μg/mL、93.8(21.0)μg・hr/mL、31.2(5.4)時間及び0.396(0.063)mL/min/kgであった。これらは、健康成人男性にラモトリギン150mgを単回経口投与した時のCmax、AUC0-∞、T1/2及びCL/Fの平均値(標準偏差)、各々2.45(0.18)μg/mL、117.30(24.61)μg・hr/mL、31.2(6.4)時間、0.313(0.087)mL/min/kgと顕著な差はなかった4)20)21)(外国人データ)。
16.7 薬物相互作用
16.7.1 本剤のグルクロン酸抱合における併用薬剤の影響[6.、7.2、7.3、10.2参照]
| 本剤とグルクロン酸抱合が競合する薬剤 | 本剤のグルクロン酸抱合を誘導(促進)する薬剤 | 本剤のグルクロン酸抱合に影響を及ぼさない薬剤 |
| バルプロ酸ナトリウム | フェニトイン カルバマゼピン フェノバルビタール プリミドン リファンピシン ロピナビル・リトナビル配合剤 アタザナビル+リトナビル エチニルエストラジオール・レボノルゲストレル配合剤(経口避妊薬) | アリピプラゾール オランザピン ゾニサミド ガバペンチン シメチジン トピラマート プレガバリン リチウム レベチラセタム ペランパネル ラコサミド |
16.7.2 他剤との併用試験
(1)バルプロ酸ナトリウム
健康成人男性にバルプロ酸ナトリウム500mg(1日2回)とラモトリギン50mg、100mg及び150mg(1日1回)を反復併用した時のラモトリギンの薬物動態を以下に示した。健康成人にラモトリギンのみを反復経口投与した時の成績と比べ、バルプロ酸ナトリウム併用時のラモトリギンのT1/2は2倍以上であり、CLt/Fは1/2以下であった。また、血漿中バルプロ酸濃度に変動はみられたものの一定の傾向はみられず、その有効濃度域を維持していた22)(外国人データ)。[7.2、7.3、10.2参照]
| ラモトリギン投与量 | 例 | Cmax(μg/mL) | Cmin(μg/mL) | Tmax(hr) | T1/2(hr) | AUCss(μg・hr/mL) | CLt/F(mL/min/kg) | Vd/F(L/kg) |
| 50mg | 18 | 3.45±0.61 | 2.53±0.46 | 1.83±0.98 | 75.3±14.1 | 66.7±10.9 | 0.17±0.03 | 0.94±0.10 |
| 100mg | 6.78±1.13 | 5.02±0.97 | 1.96±1.00 | 69.6±14.3 | 132.5±22.6 | 0.17±0.04 | 0.88±0.09 | |
| 150mg | 9.44±1.71 | 6.48±1.52 | 2.02±0.96 | 69.6±14.8 | 178.2±37.1 | 0.20±0.05 | 1.03±0.18 |
(2)リファンピシン
(3)ロピナビル・リトナビル配合剤
(4)アタザナビル+リトナビル
(5)リスペリドン
(6)経口避妊薬(エチニルエストラジオール30μg及びレボノルゲストレル150μg含有)
健康成人女性にラモトリギン300mgと経口避妊薬を併用した時、血清中ラモトリギンのAUC0-24及びCmaxはラモトリギンの単独投与時のそれぞれ48%及び61%であり、経口避妊薬との併用により血清中ラモトリギン濃度は明らかに低下した。経口避妊薬休薬期間(7日間)では、ラモトリギンの血中濃度が徐々に上昇し、休薬終了時には経口避妊薬服用期間と比較して平均約2倍となった。また、レボノルゲストレルのAUC0-24及びCmaxは経口避妊薬単独投与時のそれぞれ81%及び88%であった。一方、エチニルエストラジオールのAUC0-24は経口避妊薬単独投与時の93%であったが、Cmaxに違いはみられなかった27)(外国人データ)。[10.2参照]
(7)オランザピン
(8)ゾニサミド
(9)ガバペンチン
(10)トピラマート
(11)レベチラセタム
(12)ペランパネル
(13)ラコサミド
(14)プレガバリン
(15)シメチジン
(16)リチウム
(17)アリピプラゾール
16.7.3 In vitro試験
ラモトリギンは有機カチオントランスポーター(OCT2)を介した腎尿細管分泌を阻害する可能性が示された39)。
16.8 その他
ラモトリギン錠25mg「アメル」について、「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン(平成24年2月29日 薬食審査発0229第10号)」に基づき、ラモトリギン錠100mg「アメル」を標準製剤としたとき、溶出挙動が同等と判断され、生物学的に同等とみなされた40)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<各種てんかんの治療>
17.1.1 国際共同第III相試験(成人、単剤療法)
成人における部分発作又は強直間代発作を有する新たに診断されたてんかん患者及び再発したてんかん患者(未治療)65例(日本人39例)を対象に、日本及び韓国において非対照非盲検試験41)42)を実施した。維持用量を200mg/日となるよう設定して実施した。発作型別の維持療法期(漸増期終了時から24週間)における発作消失維持率は、下表のとおりであった。
| 発作型 | 評価例数 | 発作消失維持例 | 発作消失維持率注)(%)[95%信頼区間] |
| すべての発作型 | 65 | 28 | 43.1[30.85,55.96] |
| 部分発作 | 55 | 22 | 40.0[27.02,54.09] |
| 強直間代発作 | 10 | 8 | 80.0[44.39,97.48] |
維持投与期を終了した後の継続投与期(24週間)における発作消失維持率は、下表のとおりであった。なお、継続投与期は日本のみで実施された。
| 発作型 | 評価例数 | 発作消失維持例 | 発作消失維持率注)(%)[95%信頼区間] |
| すべての発作型 | 19 | 16 | 84.2[60.42,96.62] |
| 部分発作 | 13 | 12 | 92.3[63.97,99.81] |
| 強直間代発作 | 6 | 5 | 83.3[35.88,99.58] |
副作用発現頻度は、31%(20/65例)であった。主な副作用は、発疹15%(10/65例)、頭痛、めまい、及び胃腸障害各3%(2/65例)であった(承認時)。
17.1.2 国際共同第III相試験(小児、単剤療法)
小児における定型欠神発作を有する新たに診断された4歳から12歳のてんかん患者(未治療)20例(日本人16例)を対象に、日本及び韓国において単剤投与による非対照非盲検試験43)44)を実施した。維持用量は発作の状態や安全性を考慮して1.2〜10.2mg/kg/日又は400mg/日(いずれか低い用量)注)の範囲内で増減可能とした。
維持療法期終了時(維持療法期における12週時)においてHV-EEGにより定型欠神発作の消失が確認された被験者数は、治験薬投与症例数20例中7例であり、その割合(95%信頼区間)は、35.0(15.39〜59.22)%であった。
維持療法期を終了した後の継続投与期12週時において、HV-EEGにより定型欠神発作の消失が確認された被験者数は、継続投与期に移行した7例中6例であり、その割合(95%信頼区間)は85.7(42.13〜99.64)%であった。
副作用発現頻度は、35%(7/20例)であった。その内訳は、発疹25%(5/20例)、肝機能検査値異常及び頭痛各5%(1/20例)であった(承認時)。
維持療法期終了時(維持療法期における12週時)においてHV-EEGにより定型欠神発作の消失が確認された被験者数は、治験薬投与症例数20例中7例であり、その割合(95%信頼区間)は、35.0(15.39〜59.22)%であった。
維持療法期を終了した後の継続投与期12週時において、HV-EEGにより定型欠神発作の消失が確認された被験者数は、継続投与期に移行した7例中6例であり、その割合(95%信頼区間)は85.7(42.13〜99.64)%であった。
副作用発現頻度は、35%(7/20例)であった。その内訳は、発疹25%(5/20例)、肝機能検査値異常及び頭痛各5%(1/20例)であった(承認時)。
注)小児の定型欠神発作に対する承認された本剤の単剤投与の維持用量は1日1〜10mg/kg、最大200mgである。
17.1.3 海外第III相試験(小児及び成人、単剤療法)
部分発作又は強直間代発作を有する新たに診断されたてんかん患者及び再発したてんかん患者(未治療)343例(12〜72歳)を対象に、カルバマゼピン対照非盲検試験45)46)を実施した。ラモトリギンの維持用量を100mg/日又は200mg/日と設定した。維持投与期(漸増期終了時から24週間)における発作消失維持率は、下表のとおりであった。
| ラモトリギン100mg/日群 | ラモトリギン200mg/日群 | カルバマゼピン群 | |
| 評価例数 | 115 | 111 | 117 |
| 発作消失維持例 | 59 | 67 | 64 |
| 発作消失維持率注)(%)[95%信頼区間] | 51.3[41.81,60.73] | 60.4[50.63,69.52] | 54.7[45.23,63.92] |
ラモトリギン群における副作用発現頻度は、26%(58/226例)であった。
17.1.4 国内第III相試験(成人、併用療法)
成人における部分発作及び全般発作に対するAdd-on投与による第III相試験(二重盲検比較試験)47)48)49)を実施した。ラモトリギンの維持用量はバルプロ酸ナトリウム併用患者には150mg、バルプロ酸ナトリウム非併用患者には300mg、維持用量期間8週間と設定して実施した。有効性解析対象症例における最終全般改善度及び各発作型における最終全般改善度は以下のとおりであった。
| 投与群 | 症例数 | 最終全般改善度 | 検定 Wilcoxon | |||||
| 著明改善 | 改善 | やや改善 | 不変 | 悪化 | 判定不能 | |||
| ラモトリギン群 | 87 | 10(11%) | 20(23%) | 16(18%) | 26(30%) | 12(14%) | 3(3%) | p=0.0119 |
| プラセボ群 | 89 | 8(9%) | 13(15%) | 9(10%) | 34(38%) | 23(26%) | 2(2%) | |
| 発作型 | 投与群 | 症例数 | 著明改善 | 改善 | やや改善 | 不変 | 悪化 | 判定不能 | 改善率 |
| 部分発作 | ラモトリギン群 | 66 | 6 | 17 | 9 | 22 | 10 | 2 | 23(35%) |
| プラセボ群 | 66 | 6 | 12 | 7 | 20 | 20 | 1 | 18(27%) | |
| 強直間代発作 | ラモトリギン群 | 7 | 0 | 3 | 2 | 1 | 1 | 0 | 3(43%) |
| プラセボ群 | 11 | 1 | 1 | 1 | 7 | 1 | 0 | 2(18%) | |
| Lennox-Gastaut症候群の全般発作 | ラモトリギン群 | 11 | 1 | 3 | 3 | 2 | 2 | 0 | 4(36%) |
| プラセボ群 | 16 | 1 | 0 | 1 | 10 | 4 | 0 | 1(6%) |
ラモトリギン群における副作用発現頻度は、37%(32/87例)であった。主な副作用は、傾眠20%(17/87例)、浮動性めまい13%(11/87例)、頭痛及び複視各5%(4/87例)であった。
17.1.5 国内第III相試験(小児、併用療法)
小児における部分発作及び全般発作に対するAdd-on投与による第III相試験(単盲検比較試験)50)51)を実施した。ラモトリギンの維持用量はバルプロ酸ナトリウム併用患者には約1〜5mg/kg/日(バルプロ酸ナトリウムを併用し、グルクロン酸抱合を誘導する薬剤を非併用の患者には約1〜3mg/kg/日)、バルプロ酸ナトリウム非併用患者には約5〜15mg/kg/日、維持用量期間8週間と設定して実施した。有効性解析対象症例における最終全般改善度及び各発作型における最終全般改善度は以下のとおりであった。
| 投与群 | 症例数 | 最終全般改善度 | 検定 Wilcoxon | |||||
| 著明改善 | 改善 | やや改善 | 不変 | 悪化 | 判定不能 | |||
| ラモトリギン群 | 86 | 12(14%) | 26(30%) | 18(21%) | 18(21%) | 9(10%) | 3(3%) | p=0.0009 |
| ゾニサミド群 | 82 | 3(4%) | 17(21%) | 17(21%) | 22(27%) | 20(24%) | 3(4%) | |
| 発作型 | 投与群 | 症例数 | 著明改善 | 改善 | やや改善 | 不変 | 悪化 | 判定不能 | 改善率 |
| 部分発作 | ラモトリギン群 | 33 | 5 | 7 | 7 | 9 | 5 | 0 | 12(36%) |
| ゾニサミド群 | 39 | 3 | 11 | 9 | 8 | 6 | 2 | 14(36%) | |
| 強直間代発作 | ラモトリギン群 | 17 | 3 | 9 | 1 | 2 | 1 | 1 | 12(71%) |
| ゾニサミド群 | 12 | 0 | 1 | 3 | 4 | 4 | 0 | 1(8%) | |
| Lennox-Gastaut症候群の全般発作 | ラモトリギン群 | 33 | 3 | 11 | 8 | 6 | 4 | 1 | 14(42%) |
| ゾニサミド群 | 34 | 0 | 5 | 6 | 11 | 12 | 0 | 5(15%) |
ラモトリギン群における副作用発現頻度は、43%(37/87例)であった。主な副作用は、傾眠26%(23/87例)、浮動性めまい7%(6/87例)であった。
17.1.6 海外臨床試験(成人、併用療法)
成人における部分発作に対するAdd-on投与による二重盲検クロスオーバー比較試験52)53)54)を実施した。ラモトリギンの維持用量を400mg/日(バルプロ酸ナトリウム非併用)、維持用量期間9週間と設定して実施した結果、ラモトリギン群における発作頻度減少率はプラセボ群と比較して有意に高かった。
ラモトリギン投与期における副作用発現頻度は、70%(66/94例)であった。主な副作用は、浮動性めまい30%(28/94例)、失調27%(25/94例)、複視18%(17/94例)であった。
また、ラモトリギンの維持用量を300mg/日(バルプロ酸ナトリウム非併用)又は150mg/日(バルプロ酸ナトリウム併用)、維持用量期間12週間と設定して実施した結果、ラモトリギン群における発作頻度減少率はプラセボ群と比較して有意に高かった。
ラモトリギン投与期における副作用発現頻度は、71%(29/41例)であった。主な副作用は、浮動性めまい17%(7/41例)、悪心15%(6/41例)、頭痛及び失調各12%(5/41例)であった。
ラモトリギン投与期における副作用発現頻度は、70%(66/94例)であった。主な副作用は、浮動性めまい30%(28/94例)、失調27%(25/94例)、複視18%(17/94例)であった。
また、ラモトリギンの維持用量を300mg/日(バルプロ酸ナトリウム非併用)又は150mg/日(バルプロ酸ナトリウム併用)、維持用量期間12週間と設定して実施した結果、ラモトリギン群における発作頻度減少率はプラセボ群と比較して有意に高かった。
ラモトリギン投与期における副作用発現頻度は、71%(29/41例)であった。主な副作用は、浮動性めまい17%(7/41例)、悪心15%(6/41例)、頭痛及び失調各12%(5/41例)であった。
| 投与量 | 症例数 | 発作頻度減少率中央値注1) |
| 400mg | 88 | 25%*** |
| 150mg注2)又は300mg | 41 | 26%*** |
17.1.7 海外臨床試験(小児、併用療法)
小児における部分発作に対するAdd-on投与による二重盲検並行群間比較試験55)56)を実施した。ラモトリギンの維持用量をバルプロ酸ナトリウム併用患者には約5mg/kg/日(最大250mg/日)、バルプロ酸ナトリウム非併用患者には約15mg/kg/日(最大750mg/日)、維持用量期間12週間と設定して実施した結果、ラモトリギン群における発作頻度減少率はプラセボ群と比較して有意に高かった。
| 投与群 | 症例数 | 発作頻度減少率中央値 |
| ラモトリギン群 | 98 | 36%** |
| プラセボ群 | 101 | 7% |
ラモトリギン群における副作用発現頻度は、65%(64/98例)であった。主な副作用は、傾眠18%(18/98例)、浮動性めまい15%(15/98例)、失調10%(10/98例)であった。
17.1.8 海外臨床試験(小児及び成人、併用療法)
Lennox-Gastaut症候群(3〜25歳)における全般発作に対するAdd-on投与による二重盲検並行群間比較試験57)58)を実施した。ラモトリギンの維持用量をバルプロ酸ナトリウム併用患者には約5mg/kg/日(最大200mg/日)、バルプロ酸ナトリウム非併用患者には約15mg/kg/日(最大400mg/日)、維持用量期間10週間と設定して実施した結果、ラモトリギン群における発作頻度減少率はプラセボ群と比較して有意に高かった。
| 投与群 | 症例数 | 発作頻度減少率中央値 |
| ラモトリギン群 | 78 | 32%* |
| プラセボ群 | 89 | 9% |
ラモトリギン群における副作用発現頻度は、30%(24/79例)であった。主な副作用は、発疹8%(6/79例)、嘔吐、悪心及び失調各4%(3/79例)であった。
17.1.9 海外臨床試験(小児及び成人、併用療法)
強直間代発作(2〜55歳)に対するAdd-on投与による二重盲検並行群間比較試験59)を実施した。ラモトリギンの維持用量をバルプロ酸ナトリウム併用患者では、2〜12歳には約3mg/kg/日(最大200mg/日)、12歳超には200mg/日、バルプロ酸ナトリウム非併用患者では、2〜12歳には12mg/kg/日(最大400mg/日)、12歳超には400mg/日、維持用量期間12週間と設定して実施した結果、ラモトリギン群における発作頻度減少率はプラセボ群と比較して有意に高かった。
| 投与群 | 症例数 | 発作頻度減少率中央値 |
| ラモトリギン群 | 58 | 82%** |
| プラセボ群 | 59 | 43% |
ラモトリギン群における副作用発現頻度は、22%(13/58例)であった。主な副作用は、浮動性めまい、傾眠及び悪心各5%(3/58例)であった。
<双極性障害における気分エピソードの再発・再燃抑制>
17.1.10 国内第II/III相試験(成人)
双極I型障害を有する患者(215例)を対象に、第1期(8〜16週間)として非盲検下でラモトリギン200mgを投与し、第2期(26週間)として、症状が安定した患者を対象にプラセボ対照ランダム化治療中止試験60)を実施した。主要評価項目である第2期開始から治験を中止・脱落するまでの期間(Time to withdrawal from study:TWS)は、下表のとおりであり、イベント発現までの時間は、ラモトリギン群ではプラセボ群と比較して長く、統計学的な有意差が認められた(p=0.010、ログランク検定)。
| プラセボ群 | ラモトリギン群 | |
| 評価例数 | 58例 | 45例 |
| イベント発現割合 | 74.1%(43例) | 53.3%(24例) |
| TWS中央値[95%信頼区間](日) | 67.5[32.0,127.0] | 169.0[111.0,n/c] |
| プラセボ群との比較注) | p=0.010 |
第1期における副作用発現頻度は、32%(69/215例)であった。主な副作用は、発疹6.5%(14/215例)、頭痛4.2%(9/215例)、傾眠3.7%(8/215例)、悪心2.8%(6/215例)であった。
17.1.11 国内長期投与試験(成人)
第II/III相試験に継続して実施した52週間の非盲検長期投与試験において、併用薬により調節した用法及び用量(50〜400mg/日)でラモトリギンを投与した結果は、下表のとおりであった61)62)。
| 評価時期 | 例数 | CGI-S注1) | HAM-D17注2) | YMRS注3) | |||
| 合計点 | 変化量 | 合計点 | 変化量 | 合計点 | 変化量 | ||
| 試験開始時 | 92 | 2.9±1.1 | − | 9.7±8.0 | − | 3.0±5.5 | − |
| 6週 | 84 | 2.2±0.9 | −0.7±1.0 | 4.3±4.9 | −4.7±7.2 | 2.6±4.4 | −0.3±5.9 |
| 16週 | 78 | 2.1±0.9 | −0.7±1.2 | 5.2±6.0 | −3.8±7.5 | 1.7±3.0 | −1.3±6.1 |
| 28週 | 77 | 2.1±1.0 | −0.7±1.2 | 4.5±5.1 | −4.5±7.7 | 2.0±5.2 | −1.1±5.8 |
| 40週 | 70 | 2.1±1.0 | −0.6±1.2 | 4.7±5.5 | −3.9±7.7 | 1.7±4.0 | −1.1±6.7 |
| 52週 | 68 | 1.8±0.8 | −1.0±1.1 | 3.9±5.3 | −4.4±6.9 | 0.8±1.7 | −2.1±6.0 |
| 最終評価時注4) | 92 | 2.1±1.2 | −0.8±1.2 | 5.5±7.3 | −4.3±7.2 | 1.9±5.6 | −1.1±7.1 |
長期投与試験に移行した症例における副作用発現頻度は、21%(19/92例)であった。主な副作用は、胃腸障害7.6%(7/92例)であった(承認時)。
17.3 その他
17.3.1 国内臨床試験における用量の違いによる発疹等の皮膚障害の発現率(バルプロ酸ナトリウム併用患者)
17.3.2 国内臨床試験における皮膚粘膜眼症候群(Stevens-Johnson症候群)の発現率
18. 薬効薬理
18.1 作用機序
18.2 抗痙攣作用
各種てんかん動物モデルにおいて抗痙攣作用を示すことが報告されている。
18.2.1 マウス及びラットの最大電撃痙攣を抑制する68)。
18.2.2 薬物(ペンチレンテトラゾール、4-アミノピリジン及び6,7-dimethoxy-4-ethyl-β-carboline-3-carboxylate(DMCM))によりマウスに誘発される強直性痙攣を抑制する68)69)70)。
18.2.3 ラット及びイヌの海馬における電気刺激誘発後発射を抑制する71)。
18.2.6 ラットにおける協調性運動障害作用は弱く、治療係数(協調性運動障害を示すED50値/抗痙攣作用のED50値の比)は、フェニトインやジアゼパムよりも高い値を示す75)。
19. 有効成分に関する理化学的知見
19.1. ラモトリギン
21. 承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
<ラモトリギン錠小児用2mg「アメル」>
140錠[14錠(PTP)×10]
<ラモトリギン錠小児用5mg「アメル」>
140錠[14錠(PTP)×10]
<ラモトリギン錠25mg「アメル」>
140錠[14錠(PTP)×10]
<ラモトリギン錠100mg「アメル」>
140錠[14錠(PTP)×10]
23. 主要文献
- 日本てんかん学会:抗てんかん発作薬を服用しているてんかんのある人において、自動車運転や危険を伴う機械操作を行う際の留意事項(2026年3月17日)
- Newport DJ,et al., Pediatrics., 122, e223-231, (2008)
- 厚生労働省:重篤副作用疾患別対応マニュアル 薬剤性過敏症症候群
- 血中濃度(健康成人)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.2.2.2.1)
- 血中濃度(てんかん患者)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.2.2.2)
- Jawad S,et al., Epilepsy Res., 1, 194-201, (1987) »PubMed
- Anderson GD,et al., Clin Pharmacol Ther., 60, 145-156, (1996) »PubMed
- 社内資料:生物学的同等性試験[錠小児用2mg、錠小児用5mg、錠100mg]
- 吸収(食事の影響)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.1.1.2)
- Yuen WC,et al., Br J Clin Pharmacol., 26, 242P, (1988)
- 分布(ラミクタール錠:2008年10月16日承認、申請資料概要2.6.4.4.3)
- Magdalou J,et al., J Pharmacol Exp Ther., 260, 1166-1173, (1992) »PubMed
- Green MD,et al., Drug Metab Dispos., 23, 299-302, (1995) »PubMed
- 代謝(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.2.2.1.7)
- 排泄(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.2.2.2.1.4)
- Fillastre JP,et al., Drugs Exp Clin Res., 19, 25-32, (1993) »PubMed
- 腎機能障害患者(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.2.2.2.3.3)
- Marcellin P,et al., Br J Clin Pharmacol, 51, 410-414, (2001) »PubMed
- 肝機能障害患者(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.2.2.2.3.1)
- Posner J,et al., J Pharm Med., 1, 121-128, (1991)
- 血中濃度(高齢者)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.2.3.5)
- 他剤との併用試験(バルプロ酸ナトリウム)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.2.1.7)
- Ebert U,et al., Eur J Clin Pharmacol., 56, 299-304, (2000) »PubMed
- van der Lee MJ,et al., Clin Pharmacol Ther., 80, 159-168, (2006) »PubMed
- Burger DM,et al., Clin Pharmacol Ther., 84, 698-703, (2008) »PubMed
- 他剤との併用試験(リスペリドン)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.2.4.4)
- 他剤との併用試験(経口避妊薬)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.2.4.1)
- 他剤との併用試験(オランザピン)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.2.2.2.4.2,2.7.6.2.4.2)
- Levy RH,et al., Ther Drug Monit., 27, 193-198, (2005) »PubMed
- Weintraub D,et al., Arch Neurol., 62, 1432-1436, (2005) »PubMed
- Doose DR,et al., Epilepsia., 44, 917-922, (2003) »PubMed
- Gidal BE,et al., Epilepsy Res., 64, 1-11, (2005) »PubMed
- Perucca E,et al., Epilepsy Res., 53, 47-56, (2003) »PubMed
- Majid O,et al., Br J Clin Pharmacol., 82, 422-430, (2016) »PubMed
- Halasz P,et al., Epilepsia., 50, 443-453, (2009) »PubMed
- Brodie MJ,et al., Epilepsia., 46, 1407-1413, (2005) »PubMed
- 他剤との併用試験(リチウム)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.2.4.3)
- Schieber FC,et al., Hum Psychopharmacol., 24, 145-152, (2009) »PubMed
- In vitro試験(ラミクタール錠:2011年7月1日承認、申請資料概要2.7.4.6)
- 社内資料:生物学的同等性試験(溶出挙動比較)
- Yamamoto T,et al., Epilepsy & Seizure Journal of Japan Epilepsy Society., 7, 55-65, (2014)
- 国際共同第III相試験(成人、単剤療法)(ラミクタール錠:2014年8月29日承認、審査報告書)
- Yasumoto S,et al., Brain Dev., 38, 407-413, (2016) »PubMed
- 国際共同第III相試験(小児、単剤療法)(ラミクタール錠:2015年9月24日承認、申請資料概要2.7.6.LAM115377試験)
- Reunanen M,et al., Epilepsy Res., 23, 149-155, (1996) »PubMed
- 海外第III相試験(小児及び成人、単剤療法)(ラミクタール錠:2014年8月29日承認、審査報告書)
- 村崎光邦,他, 臨床精神薬理, 11, 117-134, (2008)
- 国内第III相試験(成人、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.3.1.2)
- 国内第III相試験(成人、併用療法)(ラミクタール錠:2008年10月16日承認、審査報告書)
- 大田原俊輔,他, てんかん研究, 25, 425-440, (2008) »DOI
- 国内第III相試験(小児、併用療法)(ラミクタール錠:2008年10月16日承認、審査報告書)
- Messenheimer J,et al., Epilepsia., 35, 113-121, (1994) »PubMed
- Schapel GJ,et al., J Neurol Neurosurg Psychiatry., 56, 448-453, (1993) »PubMed
- 海外臨床試験(成人、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.3.3.2.2.1,2.7.6.3.1.5,2.7.6.3.1.6)
- Duchowny M,et al., Neurology., 53, 1724-1731, (1999) »PubMed
- 海外臨床試験(小児、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.3.1.8)
- Motte J,et al., N Engl J Med., 337, 1807-1812, (1997) »PubMed
- 海外臨床試験(小児及び成人、併用療法)(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.3.1.9)
- Biton V,et al., Neurology., 65, 1737-1743, (2005) »PubMed
- 小山司,他, 臨床精神医学, 40, 369-383, (2011)
- 国内長期投与試験(成人)(ラミクタール錠:2011年7月1日承認、申請資料概要2.7.4.7,2.7.6 SCA106052試験)
- 国内長期投与試験(成人)(ラミクタール錠:2011年7月1日承認、審査報告書)
- 厚生労働省医薬食品局:医薬品・医療機器等安全性情報,No.287, (2012)
- 国内臨床試験における皮膚障害の発現率(ラミクタール錠:2008年10月16日承認、申請資料概要2.7.6.3.2.9)
- 国内臨床試験における皮膚粘膜眼症候群(Stevens-Johnson症候群)の発現率(ラミクタール錠:2008年10月16日承認、申請資料概要2.5.5.4)
- Xie X,et al., Pflugers Arch., 430, 437-446, (1995) »PubMed
- Leach MJ,et al., Epilepsia., 27, 490-497, (1986) »PubMed
- Miller AA,et al., Epilepsia., 27, 483-489, (1986) »PubMed
- Cramer CL,et al., Life Sci., 54, PL271-275, (1994)
- Dalby NO,et al., Epilepsy Res., 28, 63-72, (1997) »PubMed
- Wheatley PL,et al., Epilepsia., 30, 34-40, (1989) »PubMed
- Otsuki K,et al., Epilepsy Res., 31, 101-112, (1998) »PubMed
- Stratton SC,et al., Epilepsy Res., 53, 95-106, (2003) »PubMed
- De Sarro G,et al., Neuropharmacology., 35, 153-158, (1996) »PubMed
- Smith SE,et al., Epilepsy Res., 15, 101-111, (1993) »PubMed
- Hosford DA,et al., Epilepsia., 38, 408-414, (1997) »PubMed
- 遺伝的てんかんモデル動物での評価(ELマウス)(ラミクタール錠:2008年10月16日承認、申請資料概要2.6.2.2.1.4)
24. 文献請求先及び問い合わせ先
文献請求先
共和薬品工業株式会社
お問い合わせ窓口
〒530-0005
大阪市北区中之島3-2-4
電話:0120-041-189
FAX:06-6121-2858
製品情報問い合わせ先
共和薬品工業株式会社
お問い合わせ窓口
〒530-0005
大阪市北区中之島3-2-4
電話:0120-041-189
FAX:06-6121-2858
26. 製造販売業者等
26.1 製造販売元
共和薬品工業株式会社
大阪市北区中之島3-2-4