医薬品情報
| 総称名 | ベムリディ |
|---|---|
| 一般名 | テノホビル アラフェナミドフマル酸塩 |
| 欧文一般名 | Tenofovir Alafenamide Fumarate |
| 製剤名 | テノホビル アラフェナミドフマル酸塩錠 |
| 薬効分類名 | 抗ウイルス化学療法剤 |
| 薬効分類番号 | 6250 |
| ATCコード | J05AF13 |
| KEGG DRUG |
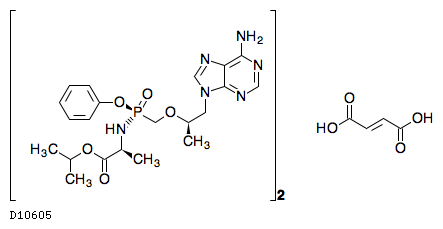
D10605
テノホビルアラフェナミドフマル酸塩
|
| KEGG DGROUP |
DG01223
テノホビル
DG03107
抗HIV薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年9月 改訂(第3版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ベムリディ錠25mg | VEMLIDY Tablets 25mg | ギリアド・サイエンシズ | 6250045F1023 | 883.1円/錠 | 劇薬, 処方箋医薬品注) |
1. 警告
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
5. 効能または効果に関連する注意
5.1 本剤投与開始に先立ち、HBV-DNA定量により、ウイルスの増殖を確認すること。
5.2 本剤の投与開始時期、他の抗ウイルス剤に対する耐性がみられた患者への使用等については、国内外のガイドライン等を参考にすること。
6. 用法及び用量
通常、成人にはテノホビル アラフェナミドとして1回25mgを1日1回経口投与する。
7. 用法及び用量に関連する注意
7.1 本剤の投与期間、併用薬等については、国内外のガイドライン等を参考にすること。
7.2 本剤の有効成分であるテノホビル アラフェナミドの他、テノホビル ジソプロキシルフマル酸塩を含む製剤と併用しないこと。
7.3 本剤投与後、クレアチニン・クリアランスが15mL/分未満に低下した場合は、維持血液透析を行っている患者を除き、投与の中止を考慮すること。なお、透析日に本剤を投与する際は、透析後に1日用量を投与すること。[8.3、9.1.3、9.2.1、11.1.1、16.6.2参照]
8. 重要な基本的注意
8.1 本剤によるB型慢性肝疾患の治療は、投与中のみでなく投与終了後も十分な経過観察が必要であり、経過に応じて適切な処置が必要なため、B型慢性肝疾患の治療に十分な知識と経験を持つ医師のもとで開始すること。[1.、8.2参照]
8.2 本剤は、投与中止により肝機能の悪化又は肝炎の重症化を起こすことがある。本内容を患者に説明し、患者が自己の判断で投与を中止しないように十分指導すること。[1.、8.1参照]
8.3 投与開始時に、クレアチニン・クリアランスを測定するなど、腎機能障害の有無に注意すること。クレアチニン・クリアランスが15mL/分以上であること又は維持血液透析を行っていることを確認すること。また、本剤投与後も定期的な検査等により患者の状態を注意深く確認すること。[7.3、9.1.3、9.2.1、10.2、11.1.1、16.6.2参照]
8.4 本剤の投与を開始する前にHIV感染の有無を確認すること。[9.1.1参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 ヒト免疫不全ウイルス(HIV)/B型肝炎ウイルス(HBV)重複感染患者
本剤のみの投与は避けること。薬剤耐性HIVが出現する可能性がある。[8.4参照]
9.1.2 病的骨折の既往のある患者又はその他の慢性骨疾患を有する患者
観察を十分に行い、異常が認められた場合には本剤の投与を中止するなど適切な処置を行うこと。成人B型慢性肝疾患患者に対する本剤の48週間投与により、腰痛と寛骨の骨密度の低下が認められている。主な骨密度の低下は、腰椎と寛骨で投与開始後24週時にかけて発現した。
9.1.3 腎機能障害のリスクを有する患者
9.2 腎機能障害患者
9.2.1 末期腎不全患者
9.3 肝機能障害患者
9.3.1 非代償性肝硬変患者
非代償性肝硬変患者を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物試験でテノホビルの乳汁への移行が報告されており、テノホビル アラフェナミドのヒト乳汁への移行の有無については不明である。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能が低下しており、合併症や併用薬の使用が多くみられる。
10. 相互作用
相互作用序文
本剤はP糖蛋白(P-gp)の基質である。[16.7.1参照]
薬物代謝酵素用語
P糖蛋白(P-gp)
10.1 併用禁忌
10.2 併用注意
| リファブチン | テノホビル アラフェナミドの血漿中濃度が低下し、本剤の効果が減弱するおそれがある。 | P-gpの誘導作用により、テノホビル アラフェナミドの血漿中濃度が低下するおそれがある。 |
| カルバマゼピン フェノバルビタール フェニトイン ホスフェニトイン [16.7.2参照] | テノホビル アラフェナミドの血漿中濃度が低下し、本剤の効果が減弱するおそれがある。 | P-gpの誘導作用により、テノホビル アラフェナミドの血漿中濃度が低下するおそれがある。 |
| アシクロビル バラシクロビル塩酸塩 ガンシクロビル バルガンシクロビル塩酸塩 [8.3、9.1.3、11.1.1、16.6.2参照] | これらの薬剤又は本剤の血中濃度が上昇し、有害事象を増強する可能性がある。 | 尿細管への能動輸送により排泄される薬剤と併用する場合、排泄経路の競合により排泄が遅延するため。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 腎不全等の重度の腎機能障害(頻度不明)
11.1.2 乳酸アシドーシス及び脂肪沈着による重度の肝腫大(脂肪肝)(頻度不明)
11.2 その他の副作用
| 1%以上 | 0.5%以上1%未満 | 頻度不明 | |
| 消化器 | 悪心、腹部膨満 | 消化不良、下痢、放屁、上腹部痛、便秘 | |
| 一般・全身障害及び投与部位の状態 | 疲労 | ||
| 臨床検査 | ALT増加 | ||
| 筋・骨格系 | 関節痛 | ||
| 神経系 | 頭痛 | 浮動性めまい | |
| 精神系 | 不眠症 | ||
| 皮膚及び皮下組織 | そう痒症、発疹 | 血管性浮腫、蕁麻疹 |
13. 過量投与
13.1 処置
テノホビルは血液透析により約54%が除去される。1)
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
16.1.1 健康成人における薬物動態
日本人健康成人被験者を対象として、本剤25mgを食後に単回経口投与したときの薬物動態パラメータを表1に示す。2)
| テノホビル アラフェナミド (10例) | テノホビル (10例) | |
| Cmax(ng/mL)a | 165(57) | 10.0(23) |
| tmax(h)b | 1.25(0.25,2.50) | 2.25(1.50,3.00) |
| AUC0-inf(ng・h/mL)a | 213(46) | 305(36) |
| t1/2(h)b | 0.31(0.24,0.57) | 44.29(30.09,55.29) |
16.1.2 B型慢性肝疾患患者における薬物動態
B型慢性肝疾患患者(全体集団)における母集団薬物動態解析に基づく推定では、定常状態におけるAUCtau及びCmaxの平均値(変動係数)は、テノホビル アラフェナミド(698例)でそれぞれ215.5ng・hr/mL(66.6%)及び177.6ng/mL(53.4%)、テノホビル(856例)でそれぞれ321.9ng・hr/mL(31.5%)及び17.2ng/mL(35.2%)であった。日本人のB型慢性肝疾患患者での定常状態におけるAUCtau及びCmaxの平均値(変動係数)は、テノホビル アラフェナミド(49例)でそれぞれ213.8ng・hr/mL(58.4%)及び176.5ng/mL(44.2%)、テノホビル(55例)でそれぞれ363.2ng・hr/mL(27.7%)及び19.5ng/mL(30.2%)であった。最終モデルで検討された共変量は、テノホビル アラフェナミドでは、投与条件(絶食下又は食後)、感染状態及び性別、テノホビルでは、投与条件(絶食下又は食後)、推定eGFR値、感染状態、性別及び人種(黒人)であり、臨床的に有意な共変量は認められなかった。3)
16.2 吸収
16.2.1 食事の影響
健康成人被験者を対象として、本剤25mgを高脂肪/高カロリー食摂取後及び空腹時に単回経口投与したときの薬物動態パラメータを表2に示す。4)(外国人のデータ)
| テノホビル アラフェナミド | ||
| 食後 (40例) | 空腹時 (39例) | |
| Cmax(ng/mL)a | 252.6(46.4) | 266.3(46.9) |
| tmax(h)b | 1.00(0.50,1.50) | 0.50(0.25,0.50) |
| AUC0-inf(ng・h/mL)a | 288.9(39.2) | 171.5(33.6) |
| t1/2(h)b | 0.45(0.40,0.59) | 0.35(0.30,0.42) |
16.3 分布
16.4 代謝
ヒトに経口投与されたテノホビル アラフェナミドは、投与量の80%超が代謝により消失する。(外国人のデータ)
テノホビル アラフェナミドは、主として初代肝細胞内でカルボキシルエステラーゼ1を主要代謝酵素として加水分解されるほか、末梢血単核球(PBMC)及び他のHIV標的細胞内でカテプシンAによって加水分解され、テノホビル アラニンとなる。更に加水分解を受けてテノホビルとなった後、アデニル酸キナーゼ及びヌクレオシド二リン酸キナーゼによって連続的にリン酸化され、薬理学的に活性を有する代謝物であるテノホビル二リン酸となる。
B型慢性肝疾患患者を対象とした臨床試験で本剤25mgを経口投与したとき、テノホビル ジソプロキシルフマル酸塩300mg経口投与との比較で、血漿中テノホビル濃度は89%低かった。3)9)10)11)12)13)(外国人のデータ)
In vitroでは、テノホビル アラフェナミドはCYP3A4によってわずかに代謝される。
テノホビル アラフェナミドは、主として初代肝細胞内でカルボキシルエステラーゼ1を主要代謝酵素として加水分解されるほか、末梢血単核球(PBMC)及び他のHIV標的細胞内でカテプシンAによって加水分解され、テノホビル アラニンとなる。更に加水分解を受けてテノホビルとなった後、アデニル酸キナーゼ及びヌクレオシド二リン酸キナーゼによって連続的にリン酸化され、薬理学的に活性を有する代謝物であるテノホビル二リン酸となる。
B型慢性肝疾患患者を対象とした臨床試験で本剤25mgを経口投与したとき、テノホビル ジソプロキシルフマル酸塩300mg経口投与との比較で、血漿中テノホビル濃度は89%低かった。3)9)10)11)12)13)(外国人のデータ)
In vitroでは、テノホビル アラフェナミドはCYP3A4によってわずかに代謝される。
16.5 排泄
健康被験者に14C標識テノホビル アラフェナミド25mgを単回投与したとき、投与量の47.2%が糞中に、36.2%が尿中に排泄された。その主成分はテノホビルであり、糞中の99%、尿中の86%を占めた。また、投与量の1.4%がテノホビル アラフェナミドとして尿中に排泄された。(外国人のデータ)テノホビルは腎臓での糸球体ろ過と尿細管への能動輸送の両方により排泄された。9)
16.6 特定の背景を有する患者
16.6.1 肝機能障害を有する被験者における薬物動態
軽度又は中等度肝機能障害被験者に本剤25mgを投与した際のテノホビル アラフェナミドのAUCinf及びCmaxは、肝機能正常被験者と比較して、軽度の肝機能障害を有する被験者ではそれぞれ7.5%及び11.0%低く、中等度肝機能障害被験者ではそれぞれ12.7%及び18.7%高かった。軽度又は中等度肝機能障害被験者に本剤25mgを投与した際のテノホビルのAUCinf及びCmaxは、肝機能正常被験者と比較して、軽度の肝機能障害を有する被験者ではそれぞれ10.8%及び3.0%低く、中等度肝機能障害被験者ではそれぞれ2.8%及び12.4%低かった。重度肝機能障害被験者に本剤25mgを投与した際のテノホビル アラフェナミドのAUCinf及びCmaxは、肝機能正常被験者と比較して、それぞれ46.0%及び54.9%低く、また、テノホビルのAUCinf及びCmaxはそれぞれ36.9%及び10.1%低かった。蛋白結合率で補正したとき(重度肝機能障害被験者及び肝機能正常被験者ではそれぞれ37.8%、20.4%)、重度肝機能障害被験者の遊離型(非結合型)テノホビル アラフェナミドのAUCinf及びCmaxは、肝機能正常被験者と比較して、それぞれ5.6%及び17.8%低かった。5)6)(外国人のデータ)
16.6.2 腎機能障害を有する被験者における薬物動態
重度腎機能障害被験者(クレアチニン・クリアランス:15mL/分以上30mL/分未満)に本剤25mgを単回投与した際のテノホビル アラフェナミドのAUCinf及びCmaxは、腎機能正常被験者と比較してそれぞれ1.9倍及び1.8倍、テノホビルのAUCinf及びCmaxは、それぞれ5.7倍及び2.8倍高かった。維持血液透析を行っている末期腎不全(クレアチニン・クリアランス:15mL/分未満)のB型慢性肝疾患患者に本剤25mgを1日1回反復投与した際のテノホビル アラフェナミドのAUClast及びCmaxは、腎機能正常のB型慢性肝疾患患者と比較してそれぞれ1.2倍及び1.0倍、テノホビルのAUCtau及びCmaxは、それぞれ49倍及び37倍であった。7)14)43)44)(外国人のデータ)[7.3、8.3、9.1.3、9.2.1、10.2、11.1.1参照]
クレアチニン・クリアランスが15mL/分未満で維持血液透析を行っていない腎機能障害患者におけるテノホビル アラフェナミドの薬物動態は検討されていない。
クレアチニン・クリアランスが15mL/分未満で維持血液透析を行っていない腎機能障害患者におけるテノホビル アラフェナミドの薬物動態は検討されていない。
16.7 薬物相互作用
16.7.1 In vitro及びin vivo試験成績
16.7.2 臨床薬物相互作用試験
薬物相互作用試験の結果を表3及び表4に示す。16)(外国人のデータ)
| 併用薬 | 併用薬の投与量(mg) | テノホビル アラフェナミドの投与量(mg) | 例数 | テノホビル アラフェナミドの薬物動態パラメータ比 併用時/非併用時 (90%信頼区間)b | ||
| Cmax | AUC | Cmin | ||||
| カルバマゼピン11) [10.2参照] | 300 1日2回 | 25 1日1回c | 26 | 0.43 (0.36,0.51) | 0.45d (0.40,0.51) | NC |
| コビシスタットe,17) | 150 1日1回 | 8 1日1回f | 12 | 2.83 (2.20,3.65) | 2.65 (2.29,3.07) | NC |
| レジパスビル・ソホスブビル18) | 90/400 1日1回 | 25 1日1回g | 42 | 1.03 (0.94,1.14) | 1.32 (1.24,1.40) | NC |
| セルトラリン19) | 50 1日1回 | 10 1日1回f,h | 19 | 1.00 (0.86,1.16) | 0.96 (0.89,1.03) | NC |
| ソホスブビル・ベルパタスビル20) | 400/100 1日1回 | 10 1日1回f,h | 24 | 0.80 (0.68,0.94) | 0.87 (0.81,0.94) | NC |
| 併用薬 | 併用薬の投与量(mg) | テノホビル アラフェナミドの投与量(mg) | 例数 | 併用薬の薬物動態パラメータ比 併用時/非併用時 (90%信頼区間)b | ||
| Cmax | AUC | Cmin | ||||
| レジパスビル18) | レジパスビル 90 ソホスブビル 400 1日1回 | 25 1日1回d | 41 | 1.01 (0.97,1.05) | 1.02 (0.97,1.06) | 1.02 (0.98,1.07) |
| ソホスブビル18) | 0.96 (0.89,1.04) | 1.05 (1.01,1.09) | NC | |||
| GS-331007c,18) | 1.08 (1.05,1.11) | 1.08 (1.06,1.10) | 1.10 (1.07,1.12) | |||
| ミダゾラムe,21) | 2.5 1日1回 経口投与 | 25 1日1回 | 18 | 1.02 (0.92,1.13) | 1.12 (1.03,1.22) | NC |
| 1 1日1回 静脈内投与 | 0.99(0.89,1.11) | 1.08 (1.04,1.14) | NC | |||
| ノルエルゲストロミン22) | ノルゲスチメート 0.180/0.215/0.250 1日1回/ エチニルエストラジオール0.025 1日1回 | 25 1日1回f | 29 | 1.17 (1.07,1.26) | 1.12 (1.07,1.17) | 1.16 (1.08,1.24) |
| ノルゲストレル22) | 1.10 (1.02,1.18) | 1.09 (1.01,1.18) | 1.11 (1.03,1.20) | |||
| エチニルエストラジオール22) | 1.22 (1.15,1.29) | 1.11 (1.07,1.16) | 1.02 (0.93,1.12) | |||
| セルトラリン19) | 50 単回投与 | 10 1日1回g,h | 19 | 1.14 (0.94,1.38) | 1.09 (0.90,1.32) | NC |
| ソホスブビル20) | 400 1日1回 | 10 1日1回g,h | 23 | 1.23 (1.07,1.42) | 1.37 (1.24,1.52) | NC |
| GS-331007c,20) | 1.29 (1.25,1.33) | 1.48 (1.43,1.53) | 1.58 (1.52,1.65) | |||
| ベルパタスビル20) | 100 1日1回 | 15 | 1.30 (1.17,1.45) | 1.50 (1.35,1.66) | 1.60 (1.44,1.78) | |
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第3相臨床試験
B型慢性肝疾患(肝代償期)患者における本剤の有効性及び安全性を検討することを目的として、テノホビル ジソプロキシルフマル酸塩(300mg1日1回投与)を対照としたランダム化二重盲検並行群間比較試験(GS-US-320-0108試験、未治療及び既治療のHBe抗原陰性患者対象。425例<日本人患者27例>)を実施した結果を表1に示す。23)
テノホビル ジソプロキシルフマル酸塩(300mg1日1回投与)に対する非劣性が示された(非劣性マージン10%)。なお、その他の有効性パラメータ(48週時)を表2に示す。
テノホビル ジソプロキシルフマル酸塩(300mg1日1回投与)に対する非劣性が示された(非劣性マージン10%)。なお、その他の有効性パラメータ(48週時)を表2に示す。
| HBe抗原陰性 (GS-US-320-0108試験) | |||
| 本剤群 | TDF群 | ||
| 全体 | 94.0%(268/285例) | 92.9%(130/140例) | |
| 群間差[95%信頼区間]a | 1.8%[−3.6%,7.2%] | ||
| 核酸アナログによる治療歴の有無b | 無(未治療例) | 94.3%(216/229例) | 93.6%(102/109例) |
| 有(既治療例) | 95.2%(40/42例) | 95.8%(23/24例) | |
| 日本人 | 95.2%(20/21例) | 100%(6/6例) | |
| 外国人 | 93.9%(248/264例) | 92.5%(124/134例) | |
| HBe抗原陰性 (GS-US-320-0108試験) | ||
| 本剤群 (285例) | TDF群 (140例) | |
| ALT ALT正常化(中央検査機関)b | 83% | 75% |
| ALT正常化(AASLD)c | 50% | 32% |
| 血清学的解析 HBe抗原消失/セロコンバージョンd | N/A | N/A |
| HBs抗原消失/セロコンバージョン | 0/0 | 0/0 |
副作用の発現率は本剤群13.7%(39/285例)であった。本剤群で発現率が1%以上の副作用は、表3のとおりであった。
| 本剤群 (285例) | |
| 事象名 | |
| 腹部膨満 | 5例(1.8%) |
| 頭痛 | 5例(1.8%) |
| 悪心 | 4例(1.4%) |
| 疲労 | 4例(1.4%) |
| 関節痛 | 3例(1.1%) |
| 不眠 | 3例(1.1%) |
| そう痒症 | 3例(1.1%) |
17.1.2 国際共同第3相臨床試験
B型慢性肝疾患(肝代償期)患者における本剤の有効性及び安全性を検討することを目的として、テノホビル ジソプロキシルフマル酸塩(300mg1日1回投与)を対照としたランダム化二重盲検並行群間比較試験(GS-US-320-0110試験、未治療及び既治療のHBe抗原陽性患者対象。873例<日本人患者46例>)を実施した結果を表4に示す。24)
テノホビル ジソプロキシルフマル酸塩(300mg1日1回投与)に対する非劣性が示された(非劣性マージン10%)。なお、その他の有効性パラメータ(48週時)を表5に示す。
テノホビル ジソプロキシルフマル酸塩(300mg1日1回投与)に対する非劣性が示された(非劣性マージン10%)。なお、その他の有効性パラメータ(48週時)を表5に示す。
| HBe抗原陽性 (GS-US-320-0110試験) | |||
| 本剤群 | TDF群 | ||
| 全体 | 63.9%(371/581例) | 66.8%(195/292例) | |
| 群間差[95%信頼区間]a | −3.6%[−9.8%,2.6%] | ||
| 核酸アナログによる治療歴の有無b | 無(未治療例) | 68.1%(301/442例) | 71.0%(157/221例) |
| 有(既治療例) | 52.1%(49/94例) | 58.1%(25/43例) | |
| 日本人 | 62.9%(22/35例) | 81.8%(9/11例) | |
| 外国人 | 63.9%(349/546例) | 66.2%(186/281例) | |
| HBe抗原陽性 (GS-US-320-0110試験) | ||
| 本剤群 (581例) | TDF群 (292例) | |
| ALT ALT正常化(中央検査機関)b | 72% | 67% |
| ALT正常化(AASLD)c | 45% | 36% |
| 血清学的解析 HBe抗原消失/セロコンバージョンd | 14%/10% | 12%/8% |
| HBs抗原消失/セロコンバージョン | 1%/1% | <1%/0 |
副作用の発現率は本剤群14.5%(84/581例)であった。本剤群で発現率が1%以上の副作用は、表6のとおりであった。
| 本剤群 (581例) | |
| 事象名 | |
| 悪心 | 13(2.2%) |
| 疲労 | 8(1.4%) |
| 頭痛 | 7(1.2%) |
| 消化不良 | 6(1.0%) |
17.3 その他
17.3.1 心電図に対する影響
健康被験者48例を対象として心電図に対する影響を評価したとき、本剤25mg及び高用量(承認用量の5倍の125mg)のテノホビル アラフェナミドはQT/QTc間隔に影響を与えず、PR間隔を延長させなかった。25)(外国人のデータ)
18. 薬効薬理
18.1 作用機序
テノホビル アラフェナミドはテノホビル(2'-デオキシアデノシン一リン酸アナログ)をホスホンアミデートで修飾したプロドラッグである。テノホビル アラフェナミドは、受動輸送及び肝取込みトランスポーターであるOATP1B1及びOATP1B3により初代肝細胞に取り込まれる。テノホビル アラフェナミドは、初代肝細胞内では主にカルボキシルエステラーゼ1により、PBMCやその他のHIV標的細胞内では主にカテプシンAによる加水分解を受ける。細胞内のテノホビルはリン酸化されて活性代謝物であるテノホビル二リン酸となる。テノホビル二リン酸は、HBVの逆転写酵素によりウイルスDNA鎖へと取り込まれ、HBVの複製を阻害し、ウイルスDNA鎖の伸長は停止する。
テノホビルはHBVに特異的に作用する。テノホビル二リン酸のミトコンドリアDNAポリメラーゼγを含むほ乳類のDNAポリメラーゼに対する阻害作用は非常に弱く、ミトコンドリアDNAアッセイを含む複数のin vitro試験成績では、ミトコンドリアに対する毒性は認められていない。26)27)28)29)30)31)32)33)34)35)36)37)
テノホビルはHBVに特異的に作用する。テノホビル二リン酸のミトコンドリアDNAポリメラーゼγを含むほ乳類のDNAポリメラーゼに対する阻害作用は非常に弱く、ミトコンドリアDNAアッセイを含む複数のin vitro試験成績では、ミトコンドリアに対する毒性は認められていない。26)27)28)29)30)31)32)33)34)35)36)37)
18.2 抗ウイルス活性
ジェノタイプA〜HのHBV臨床分離株に対するテノホビル アラフェナミドの抗ウイルス活性を、HepG2細胞を用いて評価した。テノホビル アラフェナミドの分離株に対する50%効果濃度(EC50値)は34.7〜134.4nmol/Lの範囲であり、全株での平均EC50値は86.6nmol/Lであった。HepG2細胞に対する50%細胞毒性濃度(CC50値)は44400nmol/L超であった。38)In vitro相互作用試験において、テノホビルは核酸系逆転写酵素阻害剤であるアデホビル、エムトリシタビン、エンテカビル、ラミブジン及びtelbivudine(国内未承認)との併用により、拮抗作用を示さなかった。39)
18.3 薬剤耐性
GS-US-320-0108試験及びGS-US-320-0110試験で本剤を投与された未治療及び既治療患者の併合解析では、48週時までにウイルス学的ブレイクスルー(HBV DNA量が一度69IU/mL未満となった後、2回の来院時に連続して69IU/mL以上、又はHBV DNA量がナディア値から1.0 log10以上増加)に至った患者、又は24週時以降に早期中止し、中止時のHBV DNA量が69IU/mL以上であった患者を対象に、ベースライン及び投与後のHBV分離株を用いてHBV DNAの塩基配列を解析した。40)日本人患者2例を含む、24例中20例でHBV DNAの塩基配列が決定された。これらの分離株から、本剤への耐性と関連するアミノ酸の置換は検出されなかった。41)
18.4 交差耐性
既に知られている核酸系逆転写酵素阻害剤に対する耐性変異を含む、一連の臨床分離株に対するテノホビル アラフェナミドの抗ウイルス活性を、HepG2細胞を用いて評価した。ラミブジン耐性変異(rtV173L+rtL180M+rtM204V、rtL180M+rtM204V及びrtM204I)ウイルスは、テノホビル アラフェナミドに対して感受性を示した(耐性変異株におけるEC50値の野生型に対する平均変化倍率:2倍未満)。エンテカビル耐性変異(rtL180M+rtM204V+rtT184G、rtL180M+rtM204V+rtS202G及びrtL180M+rtM204V+rtM250V)ウイルスは、テノホビル アラフェナミドに対して感受性を示した。アデホビル ピボキシル耐性変異rtA181T、rtA181V又はrtN236Tの一残基の置換では、テノホビル アラフェナミドに対する感受性を示したが、rtA181V+rtN236T変異ウイルスでは、テノホビル アラフェナミドに対する感受性の低下が認められた(EC50値の平均変化倍率:3.7倍)。これら変異の臨床的意義は不明である。42)
19. 有効成分に関する理化学的知見
19.1. テノホビル アラフェナミドフマル酸塩
20. 取扱い上の注意
開栓後は容器を密閉し、湿気を避けて保存すること。
22. 包装
30錠[瓶、バラ、乾燥剤入り]
28錠[14錠(PTP)×2、乾燥剤入り]
23. 主要文献
- 社内資料:腎機能障害被験者における薬物動態試験(GS-01-919)(承認年月日:2016.12.19、CTD2.7.2.3)
- 社内資料:健康成人における薬物動態試験(GS-US-320-1228)(承認年月日:2016.12.19、CTD2.7.6.6)
- 社内資料:国際共同第3相臨床試験(GS-US-320-0108、GS-US-320-0110)の母集団薬物動態解析(承認年月日:2016.12.19、CTD2.7.2.3)
- 社内資料:食事の影響に関する試験(GS-US-320-1382)(承認年月日:2016.12.19、CTD2.7.6.20)
- 社内資料:肝機能障害患者における薬物動態試験(GS-US-120-0114)(承認年月日:2016.12.19、CTD2.7.6.8)
- 社内資料:肝機能障害患者における薬物動態試験(GS-US-320-1615)(承認年月日:2016.12.19、CTD2.7.6.9)
- 社内資料:腎機能障害被験者における薬物動態試験(GS-US-120-0108)(承認年月日:2016.12.19、CTD2.7.6.7)
- 社内資料:血漿蛋白結合に関する試験(P0504-00039.1)(承認年月日:2016.12.19、CTD2.6.4.4)
- 社内資料:マスバランス試験(GS-US-120-0109)(承認年月日:2016.12.19、CTD2.7.6.5)
- 社内資料:薬物代謝に関する試験(AD-120-2004)(承認年月日:2016.12.19、CTD2.6.4.5)
- 社内資料:カルバマゼピンとの薬物相互作用試験(GS-US-311-1387)(承認年月日:2016.12.19、CTD2.7.6.24)
- 社内資料:薬物代謝酵素(CYP)に関する検討(AD-120-2003)(承認年月日:2016.12.19、CTD2.6.4.7)
- 社内資料:薬物代謝酵素(UGT)に関する検討(AD-120-2006)(承認年月日:2016.12.19、CTD2.6.4.7)
- 社内資料:透析を必要とする末期腎不全患者における母集団薬物動態解析(QP 2015-1004 TAF ESRD)(承認年月日:2016.12.19、CTD2.7.2.3)
- 社内資料:トランスポーターに関する試験(AD-120-2018)(承認年月日:2016.12.19、CTD2.6.4.7)
- テノホビル アラフェナミド米国添付文書
- 社内資料:抗HIV薬との薬物相互作用試験(GS-US-311-0101)(承認年月日:2016.12.19、CTD2.7.6.16)
- 社内資料:レジパスビル/ソホスブビルとの薬物相互作用試験(GS-US-366-1689)(承認年月日:2016.12.19、CTD2.7.6.22)
- 社内資料:セルトラリンとの薬物相互作用試験(GS-US-292-1316)(承認年月日:2016.12.19、CTD2.7.6.15)
- 社内資料:抗HCV薬との薬物相互作用試験(GS-US-342-1167)(承認年月日:2016.12.19、CTD2.7.6.21)
- 社内資料:ミダゾラムとの薬物相互作用試験(GS-US-120-1538)(承認年月日:2016.12.19、CTD2.7.6.12)
- 社内資料:ホルモン避妊薬との薬物相互作用試験(GS-US-311-1790)(承認年月日:2016.12.19、CTD2.7.6.19)
- 社内資料:国際共同第3相臨床試験(GS-US-320-0108)(承認年月日:2016.12.19、CTD2.7.6.29)
- 社内資料:国際共同第3相臨床試験(GS-US-320-0110)(承認年月日:2016.12.19、CTD2.6.7.30)
- 社内資料:QT/QTc間隔への影響に関する試験(GS-US-120-0107)(承認年月日:2016.12.19、CTD2.7.6.25)
- Murakami E et al., Antimicrob Agents Chemother, 59 (6), 3563-9, (2015)
- Birkus G et al., Antimicrob Agents Chemother, 51 (2), 543-50, (2007)
- Birkus G et al., Mol Pharmaco, 74 (1), 92-100, (2008)
- Eisenberg EJ et al., Nucleosides Nucleotides Nucleic Acids, 20 (4-7), 1091-8, (2001) »PubMed »DOI
- Robbins BL et al., Pharmacotherapy, 23 (6), 695-701, (2003)
- Delaney WE et al., Antimicrob Agents Chemother, 50 (7), 2471-7, (2006)
- Cherrington JM et al., Antivir Chem Chemother, 6 (4), 217-21, (1995)
- 社内資料:ヒト及び動物ウイルスに対する活性に関する検討(PC-120-2003)(承認年月日:2016.12.19、CTD2.6.2.2)
- Kramata P et al., Collection Symposium Series(Holy A and Tocik Z,eds),Institute of Organic Chemistry and Biochemistry,Academy of Sciences of Czech Republic,Prague,Czech Republic, 1, 188-91, (1996)
- 社内資料:ミトコンドリアに対する作用の検討(PC-120-2006)(承認年月日:2016.12.19、CTD2.6.2.3)
- 社内資料:ミトコンドリアに対する作用の検討(P1278-00042)(承認年月日:2016.12.19、CTD2.6.2.3)
- 社内資料:ミトコンドリアに対する作用の検討(TX-104-2001)(承認年月日:2016.12.19、CTD2.6.2.3)
- 社内資料:抗HBV活性に関する試験(PC-320-2003)(承認年月日:2016.12.19、CTD2.6.2.2)
- 社内資料:既存の核酸系逆転写酵素阻害剤との併用による抗HBV活性に関する試験(PC-174-2006)(承認年月日:2016.12.19、CTD2.6.2.5)
- 社内資料:耐性発現に関する検討(PC-320-2009)(承認年月日:2016.12.19、CTD2.6.2.2)
- 社内資料:日本人での耐性発現に関する検討(PC-320-2010)(承認年月日:2016.12.19、CTD2.6.2.2)
- 社内資料:交差耐性に関する検討(PC-320-2007)(承認年月日:2016.12.19、CTD2.6.2.2)
- 社内資料:腎機能障害を有するHIV陽性被験者にゲンボイヤ配合錠を投与した試験(GS-US-292-1825)
- 社内資料:腎機能障害を有するHBV感染被験者を対象とした試験(GS-US-320-4035)
24. 文献請求先及び問い合わせ先
文献請求先
ギリアド・サイエンシズ株式会社
メディカルサポートセンター 受付時間:9:00〜17:30(土・日・祝日及び会社休日を除く)
〒100-6616
東京都千代田区丸の内一丁目9番2号 グラントウキョウサウスタワー
電話:フリーダイアル 0120-506-295
FAX:03-5958-2959
製品情報問い合わせ先
ギリアド・サイエンシズ株式会社
メディカルサポートセンター 受付時間:9:00〜17:30(土・日・祝日及び会社休日を除く)
〒100-6616
東京都千代田区丸の内一丁目9番2号 グラントウキョウサウスタワー
電話:フリーダイアル 0120-506-295
FAX:03-5958-2959
26. 製造販売業者等
26.1 製造販売元
ギリアド・サイエンシズ株式会社
〒100-6616
東京都千代田区丸の内1-9-2 グラントウキョウサウスタワー