医薬品情報
| 総称名 | ホスミシン |
|---|---|
| 一般名 | ホスホマイシンカルシウム水和物 |
| 欧文一般名 | Fosfomycin Calcium Hydrate |
| 製剤名 | ホスホマイシンカルシウム水和物錠 |
| 薬効分類名 | ホスホマイシン系抗生物質製剤 |
| 薬効分類番号 | 6135 |
| ATCコード | J01XX01 S02AA17 |
| KEGG DRUG |
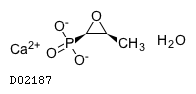
D02187
ホスホマイシンカルシウム水和物
|
| KEGG DGROUP |
DG00633
ホスホマイシン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年7月 改訂(第1版)

|
4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ホスミシン錠250 | FOSMICIN TABLETS | Meiji Seikaファルマ | 6135001F1029 | 52.3円/錠 | 処方箋医薬品注) |
| ホスミシン錠500 | FOSMICIN TABLETS | Meiji Seikaファルマ | 6135001F2025 | 88円/錠 | 処方箋医薬品注) |
4. 効能または効果
<適応菌種>
<適応症>
深在性皮膚感染症、膀胱炎、腎盂腎炎、感染性腸炎、涙嚢炎、麦粒腫、瞼板腺炎、中耳炎、副鼻腔炎
5. 効能または効果に関連する注意
<感染性腸炎、中耳炎、副鼻腔炎>
「抗微生物薬適正使用の手引き」1)を参照し、抗菌薬投与の必要性を判断した上で、本剤の投与が適切と判断される場合に投与すること。
6. 用法及び用量
通常、成人はホスホマイシンとして1日量2〜3g(力価)を3〜4回に分け、小児はホスホマイシンとして1日量40〜120mg(力価)/kgを3〜4回に分け、それぞれ経口投与する。
なお、年齢、症状に応じて適宜増減する。
なお、年齢、症状に応じて適宜増減する。
8. 重要な基本的注意
本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
肝障害が悪化するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、投与しないことが望ましい。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.8 高齢者
減量するなど注意すること。本剤は、主として腎臓から排泄されるが、高齢者では、一般に腎機能が低下している。[16.5参照]
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 偽膜性大腸炎等の血便を伴う重篤な大腸炎(0.1%未満)
腹痛、頻回の下痢があらわれた場合には、直ちに投与を中止し、適切な処置を行うこと。
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 肝臓 | AST、ALT、Al-P、LDHの上昇等の肝機能異常 | ||
| 消化器 | 嘔気、腹痛、下痢・軟便 | 食欲不振、消化不良、胃部不快感、胃もたれ、胸やけ、腹部膨満感、嘔吐 | |
| 腎臓 | 浮腫、BUN上昇 | ||
| 皮膚 | 発疹 | 蕁麻疹、そう痒感 | |
| 血液 | 好酸球増多、血小板減少 | ||
| 神経系 | 頭痛、耳鳴、眩暈 | ||
| 菌交代症 | 口内炎 | ||
| その他 | ほてり、発赤、発熱、心悸亢進、倦怠感 | 菌交代により非感受性のクレブシエラ・オキシトカがあらわれることがある。 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
健康成人(n=20)にクロスオーバー法で、本剤又は旧製剤(カプセル剤)の1,000mg(力価)を1回経口投与したときの血清中濃度、薬物動態パラメータは以下に示すとおりであった。この結果より、本剤とカプセル剤の生物学的同等性が証明された2)。
| 製剤 | 血清中濃度(μg/mL) | 薬物動態パラメータ | ||||
| 2.5時間 | 6時間 | 10時間 | Tmax(時間) | Cmax(μg/mL) | T1/2(時間) | |
| 錠剤 | 5.36 | 2.68 | 1.54 | 2.63 | 5.86 | 4.35 |
| カプセル剤 | 5.19 | 2.32 | 1.42 | 2.43 | 5.64 | 4.55 |
図 血清中濃度推移
16.3 分布
16.3.1 蛋白結合
平衡透析法により測定したヒト血清蛋白との結合率は2.16%であった。
16.4 代謝
ホスホマイシンは、体内で代謝されずに、大部分が未変化体のまま尿中に排泄される。
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内一般臨床試験
17.1.2 国内臨床試験(カプセル剤、ドライシロップ剤)
本剤とカプセル剤は生物学的同等性が確認されている。カプセル剤、ドライシロップ剤における比較試験及び一般臨床試験での臨床効果は次のとおりであった8)9)10)11)12)13)14)15)16)17)。
・深在性皮膚感染症(せつ、せつ症)に対して78.4%(40/51例)の有効率を示した。
・感染性腸炎(腸炎、細菌性赤痢)に対して96.0%(406/423例)の有効率を示した。
・膀胱炎、腎盂腎炎に対して74.7%(280/375例)の有効率を示した。
・麦粒腫、瞼板腺炎、涙嚢炎に対して93.8%(91/97例)の有効率を示した。
・中耳炎に対して68.6%(153/223例)、副鼻腔炎に対して81.8%(81/99例)の有効率を示した。
18. 薬効薬理
18.1 作用機序
ホスホマイシンは、UDP-GlcNAcエノールピルビン酸エーテル生成を触媒するUDP-GlcNAcエノールピルビルトランスフェラーゼを不可逆的に失活させ、細胞壁ペプチドグリカン生合成の初期反応を阻害することにより抗菌活性を示す18)。
18.2 in vitro抗菌作用
ホスホマイシンは、グラム陽性菌、グラム陰性菌に対して殺菌的に作用した19)。
19. 有効成分に関する理化学的知見
19.1. ホスホマイシンカルシウム水和物
22. 包装
<ホスミシン錠250>
PTP包装 100錠(10錠×10)
<ホスミシン錠500>
PTP包装 100錠(10錠×10) 500錠(10錠×50)
23. 主要文献
- 厚生労働省健康局結核感染症課編:抗微生物薬適正使用の手引き
- 社内資料:ホスホマイシンの生物学的同等性試験
- 川畑徳幸ほか, Chemotherapy., 23 (5), 1880-1885, (1975) »DOI
- 藤田公生ほか, Jpn.J.Antibiot., 41 (5), 567-570, (1988) »PubMed
- 中澤 昭ほか, 眼科臨床医報, 82 (8), 1523-1528, (1988)
- 高山幹子ほか, 耳鼻と臨床, 34 (3), 801-809, (1988) »DOI
- 川久保淳ほか, 耳鼻と臨床, 34 (4), 1043-1058, (1988) »DOI
- 松原義雄ほか, 感染症学雑誌, 49 (12), 843-855, (1975) »PubMed
- 真下啓明ほか, Chemotherapy., 23 (5), 1713-1716, (1975) »DOI
- 安田利顕ほか, 臨床皮膚科, 29 (12), 1081-1088, (1975)
- 石神襄次ほか, 泌尿紀要, 21 (10), 971-977, (1975)
- 石神襄次ほか, 泌尿紀要, 24 (9), 757-778, (1978)
- 宍戸仙太郎ほか, 泌尿紀要, 24 (9), 779-797, (1978)
- 平石 浩ほか, 感染症学雑誌, 54 (7), 343-352, (1980) »PubMed
- 馬場駿吉ほか, 耳鼻と臨床, 29 (5), 584-617, (1983) »DOI
- 富岡 昌ほか, 耳鼻臨床, 76 (4), 1291-1305, (1983) »DOI
- 大石正夫ほか, 眼科臨床医報, 77 (7), 1095-1104, (1983)
- 泉 孝英ほか, ホスホマイシン−新たなる展開−(臨床医薬研究協会), 28-33, (1995)
- 宮内慶之輔ほか, Jpn.J.Antibiot., 28 (3), 320-330, (1975) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
Meiji Seikaファルマ株式会社
くすり相談室
〒104-8002
東京都中央区京橋2-4-16
電話:フリーダイヤル0120-093-396
03-3273-3539
03-3273-3539
FAX:03-3272-2438
製品情報問い合わせ先
Meiji Seikaファルマ株式会社
くすり相談室
〒104-8002
東京都中央区京橋2-4-16
電話:フリーダイヤル0120-093-396
03-3273-3539
03-3273-3539
FAX:03-3272-2438
26. 製造販売業者等
26.1 製造販売元
Meiji Seikaファルマ株式会社
東京都中央区京橋2-4-16