医薬品情報
| 総称名 | アスピリン |
|---|---|
| 一般名 | アスピリン |
| 欧文一般名 | Aspirin |
| 薬効分類名 | 解熱鎮痛消炎剤 川崎病用剤 |
| 薬効分類番号 | 1143 3399 |
| ATCコード | A01AD05 B01AC06 N02BA01 |
| KEGG DRUG |
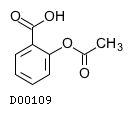
D00109
アスピリン
|
| KEGG DGROUP |
DG01504
非ステロイド性抗炎症薬 (NSAID)
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年1月 改訂(第4版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 15.その他の注意 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アスピリン「ホエイ」 | ヴィアトリス・ヘルスケア | 1143001X1112 | 3.56円/g |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
○下記疾患の解熱・鎮痛
急性上気道炎(急性気管支炎を伴う急性上気道炎を含む)
6. 用法及び用量
<関節リウマチ、リウマチ熱、変形性関節症、強直性脊椎炎、関節周囲炎、結合織炎、術後疼痛、歯痛、症候性神経痛、関節痛、腰痛症、筋肉痛、捻挫痛、打撲痛、痛風による痛み、頭痛、月経痛>
通常、成人にはアスピリンとして、1回0.5〜1.5g、1日1.0〜4.5gを経口投与する。
なお、年齢、疾患、症状により適宜増減する。ただし、上記の最高量までとする。
なお、年齢、疾患、症状により適宜増減する。ただし、上記の最高量までとする。
<急性上気道炎(急性気管支炎を伴う急性上気道炎を含む)の解熱・鎮痛>
通常、成人にはアスピリンとして、1回0.5〜1.5gを頓用する。
なお、年齢、疾患、症状により適宜増減する。ただし、原則として1日2回までとし、1日最大4.5gを限度とする。また、空腹時の投与は避けさせることが望ましい。
なお、年齢、疾患、症状により適宜増減する。ただし、原則として1日2回までとし、1日最大4.5gを限度とする。また、空腹時の投与は避けさせることが望ましい。
<川崎病(川崎病による心血管後遺症を含む)>
急性期有熱期間は、アスピリンとして1日体重1kgあたり30〜50mgを3回に分けて経口投与する。解熱後の回復期から慢性期は、アスピリンとして1日体重1kgあたり3〜5mgを1回経口投与する。なお、症状に応じて適宜増減する。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
<効能共通>
8.1 解熱鎮痛剤による治療は原因療法ではなく対症療法であることに留意すること。
8.2 過度の体温下降、虚脱、四肢冷却等があらわれることがあるので、特に高熱を伴う小児及び高齢者又は消耗性疾患の患者においては、投与後の患者の状態に十分注意すること。
8.3 慢性疾患(関節リウマチ、変形性関節症等)に対し本剤を用いる場合には、次の事項を考慮すること。
・長期投与する場合には、定期的に尿検査、血液検査及び肝機能検査等を行うこと。また、異常が認められた場合には減量、休薬等の適切な措置を講ずること。
・薬物療法以外の療法も考慮すること。
8.4 急性疾患に対し本剤を用いる場合には、次の事項を考慮すること。
・疼痛、発熱の程度を考慮し投与すること。
・原則として同一の薬剤の長期投与を避けること。
・原因療法があればこれを行うこと。
<川崎病(川崎病による心血管後遺症を含む)>
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
<効能共通>
9.1.1 消化性潰瘍の既往歴のある患者
9.1.2 血液の異常又はその既往歴のある患者(川崎病以外の効能又は効果で重篤な血液の異常のある患者を除く)
9.1.3 心機能異常のある患者(川崎病以外の効能又は効果で重篤な心機能不全のある患者を除く)
心機能をさらに悪化させるおそれがある。腎のプロスタグランジン生合成を抑制し、浮腫、循環体液量の増加が起こり、心臓の仕事量が増加する。[2.8参照]
9.1.4 気管支喘息のある患者(アスピリン喘息又はその既往歴のある患者を除く)
9.1.5 非ステロイド性消炎鎮痛剤の長期投与による消化性潰瘍のある患者で、本剤の長期投与が必要であり、かつミソプロストールによる治療が行われている患者
本剤を継続投与する場合には、十分経過を観察し、慎重に投与すること。ミソプロストールは非ステロイド性消炎鎮痛剤により生じた消化性潰瘍を効能・効果としているが、ミソプロストールによる治療に抵抗性を示す消化性潰瘍もある。
9.1.6 アルコール常飲者
9.1.7 手術、心臓カテーテル検査又は抜歯前1週間以内の患者
術前の投与は慎重に行うこと。手術、心臓カテーテル検査又は抜歯時の失血量を増加させるおそれがある。また、手術前1週間以内にアスピリンを投与した例では失血量が有意に増加したとの報告がある。
9.1.8 感染症を合併している患者
必要に応じて適切な抗菌剤を併用し、観察を十分に行い慎重に投与すること。感染症を不顕性化するおそれがある。
<川崎病以外の効能又は効果>
9.2 腎機能障害患者
<川崎病以外の効能又は効果>
9.2.1 重篤な腎機能障害のある患者
投与しないこと。腎機能障害をさらに悪化させるおそれがある。[2.7参照]
<効能共通>
9.2.2 腎機能障害又はその既往歴のある患者(川崎病以外の効能又は効果で重篤な腎機能障害のある患者を除く)
腎機能障害を悪化又は再発させるおそれがある。
9.3 肝機能障害患者
<川崎病以外の効能又は効果>
<効能共通>
9.3.2 肝機能障害又はその既往歴のある患者(川崎病以外の効能又は効果で重篤な肝機能障害のある患者を除く)
肝機能障害を悪化又は再発させるおそれがある。[11.1.6参照]
9.5 妊婦
9.5.1 出産予定日12週以内の妊婦
9.5.2 妊婦(出産予定日12週以内の妊婦は除く)又は妊娠している可能性のある女性
<効能共通>
(1)治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。シクロオキシゲナーゼ阻害剤(経口剤、坐剤)を妊婦に使用し、胎児の腎機能障害及び尿量減少、それに伴う羊水過少症が起きたとの報告がある。動物実験(ラット)で催奇形性作用があらわれたとの報告5)がある。妊娠期間の延長、過期産につながるおそれがある。
<川崎病以外の効能又は効果>
(2)投与する際には、必要最小限にとどめ、羊水量、胎児の動脈管収縮を疑う所見を妊娠週数や投与日数を考慮して適宜確認するなど慎重に投与すること。シクロオキシゲナーゼ阻害剤(全身作用を期待する製剤)を妊娠中期の妊婦に使用し、胎児の動脈管収縮が起きたとの報告がある。
9.6 授乳婦
授乳中の女性には本剤投与中は授乳を避けさせること。母乳中へ移行することが報告されている。
9.7 小児等
<効能共通>
9.7.1 副作用の発現に特に注意し、必要最小限の使用にとどめるなど患者の状態を観察しながら慎重に投与すること。副作用があらわれやすい。
9.7.2 本剤を15歳未満の水痘、インフルエンザの患者に投与しないことを原則とするが、やむを得ず投与する場合には、慎重に投与し、投与後の患者の状態を十分に観察すること。サリチル酸系製剤の使用実態は我が国と異なるものの、米国においてサリチル酸系製剤とライ症候群注)との関連性を示す疫学調査報告がある6)。
<川崎病(川崎病による心血管後遺症を含む)>
9.7.3 本剤投与中の15歳未満の患者が水痘、インフルエンザを発症した場合には、投与を中断することを原則とするが、やむを得ず投与を継続する場合には、慎重に投与し、投与後の患者の状態を十分に観察すること。サリチル酸系製剤の使用実態は我が国と異なるものの、米国においてサリチル酸系製剤とライ症候群注)との関連性を示す疫学調査報告がある6)。
注)ライ症候群:小児において極めてまれに水痘、インフルエンザ等のウイルス性疾患の先行後、激しい嘔吐、意識障害、痙攣(急性脳浮腫)と肝臓ほか諸臓器の脂肪沈着、ミトコンドリア変形、AST・ALT・LDH・CKの急激な上昇、高アンモニア血症、低プロトロンビン血症、低血糖等の症状が短期間に発現する高死亡率の病態である。
9.8 高齢者
副作用の発現に特に注意し、少量から投与を開始し必要最小限の使用にとどめるなど患者の状態を観察しながら慎重に投与すること。副作用があらわれやすい。
10. 相互作用
10.2 併用注意
| 抗凝固剤 クマリン系抗凝固剤 (ワルファリンカリウム) [11.1.2参照] | クマリン系抗凝固剤の作用を増強し、出血時間の延長、消化管出血等を起こすことがあるので、クマリン系抗凝固剤を減量するなど、慎重に投与すること。 | 本剤は血漿蛋白に結合したクマリン系抗凝固剤と置換し、遊離させる。また、本剤は血小板凝集抑制作用、消化管刺激による出血作用を有する。 |
| 抗凝固剤 血液凝固阻止剤 (ヘパリン製剤、ダナパロイドナトリウム、第Xa因子阻害剤(リバーロキサバン等)、抗トロンビン剤(ダビガトランエテキシラートメタンスルホン酸塩等)、トロンボモデュリン アルファ等) [11.1.2参照] | 出血の危険性が増大するおそれがあるので、観察を十分に行い、注意すること。 | 本剤は血小板凝集抑制作用を有するため、これら薬剤との併用により出血傾向が増強されるおそれがある。 |
| 血小板凝集抑制作用を有する薬剤 (チクロピジン塩酸塩、シロスタゾール、クロピドグレル硫酸塩、トロンボキサン合成酵素阻害剤(オザグレルナトリウム)、プロスタグランジンE1製剤、E1及びI2誘導体製剤(ベラプロストナトリウム等)、サルポグレラート塩酸塩、イコサペント酸エチル等) [11.1.2参照] | 出血の危険性が増大するおそれがあるので、観察を十分に行い、注意すること。 | 本剤は血小板凝集抑制作用を有するため、これら薬剤との併用により出血傾向が増強されるおそれがある。 |
| 血栓溶解剤 (ウロキナーゼ、t-PA製剤等) [11.1.2参照] | 出血の危険性が増大するおそれがあるので、観察を十分に行い、注意すること。 | 本剤は血小板凝集抑制作用を有するため、これら薬剤との併用により出血傾向が増強されるおそれがある。 |
| 糖尿病用剤 (ヒトインスリン等) | 糖尿病用剤の作用を増強し、低血糖を起こすことがあるので糖尿病用剤を減量するなど、慎重に投与すること。 | 本剤は血漿蛋白に結合した糖尿病用剤を遊離させる。また、本剤は大量で血糖降下作用を有する。 |
| メトトレキサート | メトトレキサートの副作用(骨髄抑制、肝・腎・消化器障害等)が増強されることがある。 | 本剤は血漿蛋白に結合したメトトレキサートと置換し、遊離させる。また、本剤はメトトレキサートの腎排泄を阻害すると考えられている。 |
| バルプロ酸ナトリウム | バルプロ酸ナトリウムの作用を増強し、振戦等を起こすことがある。 | 本剤は血漿蛋白に結合したバルプロ酸ナトリウムを遊離させる。 |
| フェニトイン | 総フェニトイン濃度を低下させるが、非結合型フェニトイン濃度を低下させないとの報告があるので、総フェニトイン濃度に基づいて増量する際には臨床症状等を慎重に観察すること。 | 本剤は血漿蛋白に結合したフェニトインと置換し、遊離させる。 |
| 炭酸脱水酵素阻害剤 (アセタゾラミド等) | これら薬剤の副作用を増強し、嗜眠、錯乱等の中枢神経系症状、代謝性アシドーシス等を起こすことが報告されている。 | 本剤は血漿蛋白に結合したこれら薬剤と置換し、遊離させる。 |
| 副腎皮質ホルモン剤 (ベタメタゾン、プレドニゾロン、メチルプレドニゾロン等) | サリチル酸中毒を起こすことが報告されている。 | 機序は不明である。併用時に、副腎皮質ホルモン剤を減量するとサリチル酸系製剤の血中濃度が増加したとの報告がある。 |
| リチウム製剤 (炭酸リチウム) | 類薬(インドメタシン等)でリチウム中毒を起こすことが報告されている。 | 類薬(インドメタシン等)は腎のプロスタグランジン生合成を抑制し、リチウムの腎排泄を低下させる。 |
| チアジド系利尿剤 (ヒドロクロロチアジド) | 類薬(インドメタシン等)でチアジド系利尿剤の作用を減弱させることが報告されている。 | 類薬(インドメタシン等)は腎のプロスタグランジン生合成を抑制し、チアジド系利尿剤の作用を減弱させることがある。 |
| 尿酸排泄促進剤 (プロベネシド、ベンズブロマロン) | これらの薬剤の作用を減弱させることがある。 | サリチル酸製剤は尿酸の排泄を抑制することが知られているため、これら薬剤の効果が減弱すると考えられる。 |
| 乳酸ナトリウム | 本剤の作用を減弱させることがある。 | 乳酸ナトリウムにより尿がアルカリ性となり、サリチル酸の尿中排泄が増加し、血中濃度が治療域以下になることがある。 |
| 非ステロイド系解熱鎮痛消炎剤 インドメタシン、ジクロフェナクナトリウム等 [7.1、11.1.2参照] | (1)これら薬剤の血中濃度を低下させるおそれがある。 (2)消化器系の副作用を増強させるおそれがある。 (3)出血及び腎機能低下を起こすことがある。 | (1)本剤との併用により、これら薬剤の血漿蛋白結合部位からの遊離置換によると考えられる。 (2)、(3)機序不明 |
| 非ステロイド系解熱鎮痛消炎剤 オキシカム系消炎鎮痛剤 (ピロキシカム等) [7.1、11.1.7参照] | 両剤又は一方の薬剤の副作用の発現頻度を増加させ、消化性潰瘍、胃腸出血の発現が高まるおそれがある。 | 両剤ともにプロスタグランジン生合成阻害作用を有するためと考えられている。 |
| 非ステロイド系解熱鎮痛消炎剤 スリンダク [7.1参照] | 消化器系の副作用の発現率が上昇する。また、スリンダクの活性代謝物(スルフィド体)の血中濃度が低下する。 | 機序不明 |
| 非ステロイド系解熱鎮痛消炎剤 イブプロフェン、ナプロキセン、ピロキシカム、スルピリン [7.1参照] | 本剤の血小板凝集抑制作用を減弱するとの報告がある。 | 血小板のシクロオキシゲナーゼ-1(COX-1)と本剤の結合を阻害するためと考えられる。 |
| 非ステロイド系解熱鎮痛消炎剤 COX-2選択的阻害剤 (セレコキシブ) [7.1参照] | 低用量の本剤(1日325mg以下)とセレコキシブを併用した場合、セレコキシブのみを服用したときに比べて消化性潰瘍等の発生率が高くなることが報告されている。 | 主に本剤併用によるNSAIDsの消化管障害誘発によると考えられる。 |
| ドネペジル塩酸塩 [11.1.7参照] | 消化性潰瘍を起こすことがある。 | コリン系が賦活され胃酸分泌が促進される。 |
| β-遮断剤 (プロプラノロール塩酸塩等) | 降圧作用が減弱することがある。 | 本剤がプロスタグランジン生合成を抑制することにより、プロスタグランジンを介した降圧効果を減弱させる。 |
| アンジオテンシン変換酵素阻害剤 (カプトプリル等) アンジオテンシン受容体ネプリライシン阻害剤 (サクビトリルバルサルタンナトリウム水和物) アンジオテンシンII受容体拮抗剤 (バルサルタン等) 直接的レニン阻害剤 (アリスキレン) | (1)降圧作用が減弱することがある。 (2)腎機能を悪化させるおそれがある。 | (1)本剤がプロスタグランジン生合成を抑制することにより、プロスタグランジンを介した降圧効果を減弱させる。 (2)本剤の腎プロスタグランジン合成阻害作用により、腎血流量が低下するためと考えられる。 |
| ループ利尿剤 (フロセミド等) | (1)これらの薬剤の利尿作用を減弱させるおそれがある。 (2)サリチル酸中毒が発現するおそれがある。 | (1)本剤が腎のプロスタグランジン生合成を抑制することにより、これら薬剤の作用を減弱させるためと考えられる。 (2)腎の排泄部位において両剤の競合が起こり、サリチル酸誘導体の排泄が遅れるためと考えられる。 |
| ニトログリセリン | ニトログリセリンの作用を減弱させるおそれがある。 | 本剤がプロスタグランジン生合成を抑制することにより、ニトログリセリンの血管拡張作用を減弱させる。 |
| タクロリムス水和物、シクロスポリン | 腎機能障害が発現することがある。 | 腎機能障害の副作用が相互に増強されると考えられる。 |
| プロスタグランジンD2、トロンボキサンA2受容体拮抗剤 (セラトロダスト、ラマトロバン) | ヒト血漿蛋白結合に対する相互作用の検討(in vitro)において、本剤によりこれら薬剤の非結合型分率が上昇することがある。 | これら薬剤が本剤と血漿蛋白結合部位で置換し、遊離型血中濃度が上昇すると考えられる。 |
| 選択的セロトニン再取り込み阻害剤(SSRI) (フルボキサミンマレイン酸塩、塩酸セルトラリン等) [11.1.2参照] | 皮膚の異常出血(斑状出血、紫斑等)、出血症状(胃腸出血等)が報告されている。 | SSRIの投与により血小板凝集が阻害され、本剤との併用により出血傾向が増強すると考えられる。 |
| アルコール [9.1.6、11.1.2参照] | 消化管出血が増強されるおそれがある。 | アルコールによる胃粘膜障害と本剤のプロスタグランジン合成阻害作用により、相加的に消化管出血が増強すると考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
ショックやアナフィラキシー(呼吸困難、全身潮紅、血管性浮腫、蕁麻疹等)があらわれることがある。
11.1.2 出血(頻度不明)
11.1.3 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、剥脱性皮膚炎(いずれも頻度不明)
11.1.6 肝機能障害、黄疸(いずれも頻度不明)
11.1.7 消化性潰瘍、小腸・大腸潰瘍(いずれも頻度不明)
11.1.8 アレルギー反応に伴う急性冠症候群(頻度不明)
11.2 その他の副作用
| 頻度不明 | |
| 消化器 | 食欲不振、胸やけ、悪心・嘔吐、胃痛、腹痛、胃腸障害、便秘、下痢、食道炎、口唇腫脹、吐血、胃部不快感 |
| 過敏症 | 蕁麻疹、発疹、浮腫、鼻炎様症状 |
| 血液注1) | 貧血、血小板機能低下(出血時間の延長) |
| 皮膚 | そう痒、発汗 |
| 精神神経系 | めまい、頭痛、興奮 |
| 肝臓注1) | AST上昇、ALT上昇 |
| 腎臓注1) | 腎機能障害 |
| 循環器 | 血圧低下、血管炎、心窩部痛 |
| 呼吸器 | 気管支炎 |
| 感覚器 | 耳鳴、難聴、角膜炎、結膜炎 |
| その他注2) | 過呼吸、代謝性アシドーシス、倦怠感、低血糖 |
13. 過量投与
13.1 徴候と症状
耳鳴、めまい、頭痛、悪心・嘔吐、消化管出血・潰瘍、難聴、軽度の頻呼吸等の初期症状から血中濃度の上昇に伴い、重度の過呼吸、呼吸性アルカローシス、代謝性アシドーシス等の酸塩基平衡障害、痙攣、昏睡等の中枢神経系障害、心血管虚脱、呼吸不全等が認められる。
13.2 処置
催吐、胃洗浄を行い、その上で活性炭や下剤を投与する。ブドウ糖輸液などにより体液と電解質のバランスの維持を図る。小児の高熱には、スポンジ浴を行う。炭酸水素ナトリウムの静脈注射などによりアシドーシスを補正すると共に尿のアルカリ化を図る。重篤な場合、血液透析、腹膜灌流などを考慮する。
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 炭酸水素ナトリウム、炭酸マグネシウム等のアルカリ性製剤と配合しないこと。
14.1.2 湿潤しやすい製剤との配合は望ましくない。
14.2 薬剤投与時の注意
本剤は空腹時の服用を避けることが望ましい。
15. その他の注意
15.1 臨床使用に基づく情報
非ステロイド性消炎鎮痛剤を長期間投与されている女性において、一時的な不妊が認められたとの報告がある。
15.2 非臨床試験に基づく情報
in vitroの試験において、アスピリン等のグルクロン酸抱合により代謝される薬剤が抗ウイルス剤(ジドブジン)のグルクロン酸抱合を阻害したとの報告7)がある。
18. 薬効薬理
18.1 作用機序
<川崎病以外の効能又は効果>
<川崎病(川崎病による心血管後遺症を含む)>
18.1.2 シクロオキシゲナーゼ-1(COX-1)を阻害することにより、トロンボキサンA2(TXA2)の合成を阻害し、血小板凝集抑制作用を示す。血小板におけるCOX-1阻害作用は不可逆的である。また、プロスタグランジン(PG)の合成過程でアラキドン酸からPGE2などの合成を阻害し、抗炎症作用を示す1)。
19. 有効成分に関する理化学的知見
19.1. アスピリン
20. 取扱い上の注意
本品は吸湿によって脱アセチル化が起こり、この際生じる酢酸が更に変化を促進するので、乾燥をよほど厳密にしないと瓶中に蓄えることはかえって良くない14)。
22. 包装
500g[袋]
23. 主要文献
- 日本小児循環器学会, 川崎病急性期治療のガイドライン(平成24年改訂版).日本小児循環器学会雑誌, 28 (Suppl.3), S1-S28, (2012)
- 日本循環器学会、日本心臓病学会、日本小児科学会、日本小児循環器学会、日本胸部外科学会合同研究班, 川崎病心臓血管後遺症の診断と治療に関するガイドライン(2013年改訂版).Circ J., 1-38, (2013) »PubMed
- 赤木禎冶ほか, 綜合臨牀, 44 (10), 2410-2413, (1995)
- 厚生省薬務局安全課, 医薬品副作用情報No.66, (1984)
- 長浜萬蔵ほか, 日本先天異常学会会報, 6 (1), 20-31, (1966) »DOI
- 厚生省医薬安全局, 医薬品等安全性情報No.151, (1998)
- Sim SM,et al., Br J Clin Pharmac., 32 (1), 17-21, (1991)
- たか折修二ほか監訳, グッドマン・ギルマン薬理書(上).第12版, 1225-1285, (2013), (廣川書店)
- 熊谷洋ほか, 臨床薬理学大系, 4, 8-66, (1969)
- 熊谷洋ほか, 臨床薬理学大系, 6, 58-79, (1969)
- 高木敬次郎ほか, 薬物学, 214-223, (1984)
- 坂登光夫, 薬局, 35 (3), 23-27, (1984)
- たか折修二ほか監訳, グッドマン・ギルマン薬理書(上).第12版, 1102-1103, (2013), (廣川書店)
- 第十八改正 日本薬局方解説書, C-119-124, (2021), (廣川書店)
24. 文献請求先及び問い合わせ先
文献請求先
ヴィアトリス製薬合同会社
メディカルインフォメーション部
〒106-0041
東京都港区麻布台一丁目3番1号
電話:フリーダイヤル 0120-419-043
製品情報問い合わせ先
ヴィアトリス製薬合同会社
メディカルインフォメーション部
〒106-0041
東京都港区麻布台一丁目3番1号
電話:フリーダイヤル 0120-419-043
26. 製造販売業者等
26.1 製造販売元
ヴィアトリス・ヘルスケア合同会社
東京都港区麻布台一丁目3番1号
26.2 販売元
ヴィアトリス製薬合同会社
東京都港区麻布台一丁目3番1号