医薬品情報
| 総称名 | ベイスン |
|---|---|
| 一般名 | ボグリボース |
| 欧文一般名 | Voglibose |
| 薬効分類名 | 食後過血糖改善剤 |
| 薬効分類番号 | 3969 |
| ATCコード | A10BF03 |
| KEGG DRUG |
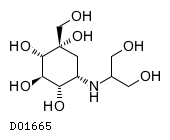
D01665
ボグリボース
|
| KEGG DGROUP |
DG01663
α-グルコシダーゼ阻害薬
DG02044
血糖降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年11月 改訂(第4版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ベイスン錠0.2 | BASEN Tablets | T’s製薬 | 3969004F1020 | 12.8円/錠 | 処方箋医薬品注) |
| ベイスン錠0.3 | BASEN Tablets | T’s製薬 | 3969004F2027 | 12.9円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 重症ケトーシス、糖尿病性昏睡又は前昏睡の患者[輸液及びインスリンによる速やかな高血糖の是正が必須となるので本剤の投与は適さない。]
2.2 重症感染症、手術前後、重篤な外傷のある患者[インスリン注射による血糖管理が望まれるので本剤の投与は適さない。]
2.3 本剤の成分に対する過敏症の既往歴のある患者
4. 効能または効果
<ベイスン錠0.2>
○糖尿病の食後過血糖の改善
(ただし、食事療法・運動療法を行っている患者で十分な効果が得られない場合、又は食事療法・運動療法に加えて経口血糖降下剤若しくはインスリン製剤を使用している患者で十分な効果が得られない場合に限る)
(ただし、食事療法・運動療法を行っている患者で十分な効果が得られない場合、又は食事療法・運動療法に加えて経口血糖降下剤若しくはインスリン製剤を使用している患者で十分な効果が得られない場合に限る)
○耐糖能異常における2型糖尿病の発症抑制(錠0.2のみ)
(ただし、食事療法・運動療法を十分に行っても改善されない場合に限る)
(ただし、食事療法・運動療法を十分に行っても改善されない場合に限る)
<ベイスン錠0.3>
○糖尿病の食後過血糖の改善
(ただし、食事療法・運動療法を行っている患者で十分な効果が得られない場合、又は食事療法・運動療法に加えて経口血糖降下剤若しくはインスリン製剤を使用している患者で十分な効果が得られない場合に限る)
(ただし、食事療法・運動療法を行っている患者で十分な効果が得られない場合、又は食事療法・運動療法に加えて経口血糖降下剤若しくはインスリン製剤を使用している患者で十分な効果が得られない場合に限る)
5. 効能または効果に関連する注意
ベイスン錠0.2
<効能共通>
5.1 本剤の適用はあらかじめ糖尿病治療及び糖尿病発症抑制の基本である食事療法、運動療法を十分に行ったうえで効果が不十分な場合に限り考慮すること。
<糖尿病の食後過血糖の改善>
5.2 糖尿病治療の基本である食事療法・運動療法のみを行っている患者では、投与の際の食後血糖2時間値は200mg/dL以上を示す場合に限る。
5.3 食事療法、運動療法に加えて経口血糖降下剤又はインスリン製剤を使用している患者では、投与の際の空腹時血糖値は140mg/dL以上を目安とする。
<耐糖能異常における2型糖尿病の発症抑制(錠0.2のみ)>
5.4 本剤の適用は、耐糖能異常(空腹時血糖が126mg/dL未満かつ75g経口ブドウ糖負荷試験の血糖2時間値が140〜199mg/dL)と判断され、糖尿病発症抑制の基本である食事療法・運動療法を3〜6ヵ月間行っても改善されず、かつ高血圧症、脂質異常症(高トリグリセリド血症、低HDLコレステロール血症等)、肥満(Body Mass Index:BMI 25kg/m2以上)、2親等以内の糖尿病家族歴のいずれかを有する場合に限定すること。
ベイスン錠0.3
<効能共通>
5.1 本剤の適用はあらかじめ糖尿病治療及び糖尿病発症抑制の基本である食事療法、運動療法を十分に行ったうえで効果が不十分な場合に限り考慮すること。
<糖尿病の食後過血糖の改善>
5.2 糖尿病治療の基本である食事療法・運動療法のみを行っている患者では、投与の際の食後血糖2時間値は200mg/dL以上を示す場合に限る。
5.3 食事療法、運動療法に加えて経口血糖降下剤又はインスリン製剤を使用している患者では、投与の際の空腹時血糖値は140mg/dL以上を目安とする。
6. 用法及び用量
ベイスン錠0.2
<糖尿病の食後過血糖の改善>
通常、成人にはボグリボースとして1回0.2mgを1日3回毎食直前に経口投与する。なお、効果不十分な場合には、経過を十分に観察しながら1回量を0.3mgまで増量することができる。
<耐糖能異常における2型糖尿病の発症抑制(錠0.2のみ)>
通常、成人にはボグリボースとして1回0.2mgを1日3回毎食直前に経口投与する。
ベイスン錠0.3
<糖尿病の食後過血糖の改善>
通常、成人にはボグリボースとして1回0.2mgを1日3回毎食直前に経口投与する。なお、効果不十分な場合には、経過を十分に観察しながら1回量を0.3mgまで増量することができる。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
<効能共通>
8.1 本剤は低血糖症状を起こすことがあるので、糖尿病患者又は耐糖能異常を有する者に対し低血糖症状及びその対処方法について十分説明すること。[11.1.1参照]
8.2 高所作業、自動車の運転等に従事している糖尿病患者又は耐糖能異常を有する者に投与するときには注意すること。[11.1.1参照]
<糖尿病の食後過血糖の改善>
8.3 本剤投与中は、血糖を定期的に検査するとともに、経過を十分に観察し、常に投与継続の必要性について注意を払うこと。本剤を2〜3ヵ月投与しても食後血糖に対する効果が不十分な場合(静脈血漿で食後血糖2時間値が200mg/dL以下にコントロールできないなど)には、より適切と考えられる治療への変更を考慮すること。
なお、食後血糖の十分なコントロール(静脈血漿で食後血糖2時間値が160mg/dL以下)が得られ、食事療法・運動療法又はこれらに加えて経口血糖降下剤若しくはインスリンを使用するのみで十分と判断される場合には、本剤の投与を中止して経過観察を行うこと。
なお、食後血糖の十分なコントロール(静脈血漿で食後血糖2時間値が160mg/dL以下)が得られ、食事療法・運動療法又はこれらに加えて経口血糖降下剤若しくはインスリンを使用するのみで十分と判断される場合には、本剤の投与を中止して経過観察を行うこと。
<耐糖能異常における2型糖尿病の発症抑制(錠0.2のみ)>
8.4 本剤の投与開始後は、1〜3ヵ月毎を目安に空腹時血糖、随時血糖、HbA1c等の糖代謝関連検査及び体重測定を実施するとともに、6〜12ヵ月毎を目安に75g経口ブドウ糖負荷試験を実施して十分に経過観察し、常に投与継続の必要性に留意すること。
また、血糖高値(空腹時血糖、75g経口ブドウ糖負荷試験の血糖2時間値)や糖負荷後初期インスリン分泌低下等を有する場合には、糖尿病発症リスクが高くなるとの報告があるので、十分な観察を行うこと。なお、2型糖尿病と診断された場合には、適切と考えられる治療への変更を考慮すること。また、本剤投与開始後に耐糖能異常が改善し、食事療法・運動療法のみで十分と判断される場合には、本剤の投与を中止して糖代謝関連検査等による経過観察を行うこと。
また、血糖高値(空腹時血糖、75g経口ブドウ糖負荷試験の血糖2時間値)や糖負荷後初期インスリン分泌低下等を有する場合には、糖尿病発症リスクが高くなるとの報告があるので、十分な観察を行うこと。なお、2型糖尿病と診断された場合には、適切と考えられる治療への変更を考慮すること。また、本剤投与開始後に耐糖能異常が改善し、食事療法・運動療法のみで十分と判断される場合には、本剤の投与を中止して糖代謝関連検査等による経過観察を行うこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 開腹手術の既往又は腸閉塞の既往のある患者
腸内ガス等の増加により腸閉塞が発現しやすい。[11.1.2参照]
9.1.2 消化・吸収障害を伴った慢性腸疾患の患者
本剤の作用により病態が悪化することがある。
9.1.3 ロエムヘルド症候群、重度のヘルニア、大腸の狭窄・潰瘍等の患者
腸内ガス等の増加により症状が悪化することがある。
9.2 腎機能障害患者
9.2.1 重篤な腎障害のある患者
代謝状態が変化することがあるため血糖管理状況が大きく変化するおそれがある。
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
代謝状態が変化することがあるため血糖管理状況が大きく変化するおそれがある。また、重篤な肝硬変例で、高アンモニア血症が増悪し意識障害を伴うことがある。[11.1.4参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に高齢者では生理機能が低下している。[7.参照]
10. 相互作用
10.2 併用注意
| 糖尿病用薬 スルホニルアミド系及びスルホニルウレア系薬剤 ビグアナイド系薬剤 インスリン製剤 インスリン抵抗性改善剤 [11.1.1参照] | インスリン及びスルホニルウレア系薬剤と併用した際に、低血糖発現の報告があるので、左記薬剤との併用時には、低血糖発現の可能性を考慮し、低用量から投与を開始するなど慎重に投与すること。 | 左記糖尿病用薬の血糖降下作用に本剤の糖質吸収遅延作用が加わる。 |
| 糖尿病用薬及びその血糖降下作用を増強又は減弱する薬剤を併用している場合 糖尿病用薬の血糖降下作用を増強する薬剤 β-遮断剤 サリチル酸剤 モノアミン酸化酵素阻害剤 フィブラート系の高脂血症治療剤 ワルファリン等 糖尿病用薬の血糖降下作用を減弱する薬剤 アドレナリン 副腎皮質ホルモン 甲状腺ホルモン等 | 左記の併用に加え更に本剤を併用する場合には、糖尿病用薬の使用上の注意に記載の相互作用に留意するとともに、本剤の糖質吸収遅延作用が加わることによる影響に十分注意すること。 | 左記薬剤により他の糖尿病用薬の血糖降下作用が増強又は減弱されるところに、本剤の糖質吸収遅延作用が加わる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 低血糖(他の糖尿病用薬との併用の場合0.1〜5%未満、併用しない場合頻度不明)
11.1.2 腸閉塞(頻度不明)
腹部膨満、鼓腸、放屁増加等があらわれ、腸内ガス等の増加により、腸閉塞があらわれることがある。観察を十分に行い、持続する腹痛、嘔吐等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。[7.、9.1.1参照]
11.1.3 劇症肝炎、重篤な肝機能障害、黄疸(頻度不明)
劇症肝炎、AST、ALTの上昇等を伴う重篤な肝機能障害、黄疸があらわれることがある。
11.1.4 意識障害を伴う高アンモニア血症(頻度不明)
重篤な肝硬変例に投与した場合、便秘等を契機として高アンモニア血症が増悪し、意識障害を伴うことがあるので、排便状況等を十分に観察し、異常が認められた場合には直ちに投与を中止すること。[9.3.1参照]
11.2 その他の副作用
| 5%以上 | 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 消化器 | 下痢、放屁、腹部膨満 | 軟便、腹鳴、腹痛、便秘、食欲不振、悪心、嘔吐、胸やけ、口渇 | 口内炎、味覚異常、腸管嚢胞様気腫症 | |
| 過敏症 | 発疹、そう痒、光線過敏症 | |||
| 肝臓 | AST、ALT、LDH、γ-GTP、Al-Pの上昇 | |||
| 精神神経系 | めまい | 頭痛、ふらつき、眠気 | ||
| 血液 | 貧血 | 血小板減少 | 顆粒球減少 | |
| その他 | しびれ、顔面等の浮腫、眼のかすみ、ほてり、倦怠感、脱力感、高カリウム血症、血清アミラーゼ上昇、HDLコレステロール低下、発汗、脱毛 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男子(10名)に2mg注)を単回投与した場合、血漿中にボグリボースは検出されない3)。
16.1.2 反復投与
健康成人男子(6名)に1回0.2mg1日3回、7日間反復投与した場合、血漿中にボグリボースは検出されない3)。
16.3 分布
ラットに[14C]ボグリボース1mg/kg単回投与した試験で胎児及び乳汁中への移行が認められている4)。
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
<糖尿病の食後過血糖の改善>
17.1.1 国内第II・III相試験
インスリン非依存型糖尿病、インスリン依存型糖尿病の各患者を対象に、1日0.6又は0.9mgを、投与した二重盲検比較対照試験を含む各種臨床試験において、最終血糖総合改善度が評価された877例の糖尿病の病型別改善率は表のとおりである5)6)7)8)9)10)11)12)13)14)15)16)17)18)19)20)21)。
| 糖尿病の病型 | 例数 | 中等度改善以上 | 軽度改善以上 |
| インスリン非依存型糖尿病 | 812 | 371(45.7) | 613(75.5) |
| インスリン依存型糖尿病 | 65 | 31(47.7) | 47(72.3) |
| 計 | 877 | 402(45.8) | 660(75.3) |
上記のインスリン非依存型糖尿病患者を対象とした二重盲検比較対照試験の結果、本剤の有用性が認められている5)6)。
また、食事療法のみの症例のみならず、インスリン製剤使用中7)8)9)10)あるいは経口血糖降下剤使用中11)12)13)14)15)の患者においても食後過血糖の改善を初めとする有用性が認められている。さらに、長期投与試験(平均投与期間約7ヵ月)では効果の持続が確認され、安定した血糖コントロールが得られている16)17)18)19)20)。
承認時までの試験では、1日0.6mg又は0.9mgを投与した965例中154例(16.0%)に臨床検査値の異常を含む副作用が認められている。主な副作用は下痢(4.0%)、放屁増加(4.0%)、腹部膨満(3.5%)等であった。なお、臨床薬理試験結果より、これらの代表的副作用(放屁増加、腹部膨満、下痢及び軟便等)は、薬理作用に起因する未吸収糖質の分解・発酵に基づくものであると考えられる。
また、食事療法のみの症例のみならず、インスリン製剤使用中7)8)9)10)あるいは経口血糖降下剤使用中11)12)13)14)15)の患者においても食後過血糖の改善を初めとする有用性が認められている。さらに、長期投与試験(平均投与期間約7ヵ月)では効果の持続が確認され、安定した血糖コントロールが得られている16)17)18)19)20)。
承認時までの試験では、1日0.6mg又は0.9mgを投与した965例中154例(16.0%)に臨床検査値の異常を含む副作用が認められている。主な副作用は下痢(4.0%)、放屁増加(4.0%)、腹部膨満(3.5%)等であった。なお、臨床薬理試験結果より、これらの代表的副作用(放屁増加、腹部膨満、下痢及び軟便等)は、薬理作用に起因する未吸収糖質の分解・発酵に基づくものであると考えられる。
<耐糖能異常における2型糖尿病の発症抑制>
17.1.2 国内第III相試験
耐糖能異常を有し、かつ高血圧症、高脂血症、肥満(Body Mass Index:BMI 25kg/m2以上)あるいは2親等以内の糖尿病家族歴のいずれかを有する者を対象に、食事療法・運動療法に加えて1回0.2mgを1日3回投与した二重盲検比較試験(平均投与日数336.7±254.0日間)の結果、最終評価時点における2型糖尿病移行例数は、本剤投与群で50/897例、プラセボ群で106/881例である。
プラセボ群に対する本剤投与群のハザード比(両側95%信頼区間)は0.595(0.4334-0.8177)である(層別ログランク検定:p=0.0014)21)。
なお、2型糖尿病累積移行率は図表のとおりである。
プラセボ群に対する本剤投与群のハザード比(両側95%信頼区間)は0.595(0.4334-0.8177)である(層別ログランク検定:p=0.0014)21)。
なお、2型糖尿病累積移行率は図表のとおりである。
| 2型糖尿病累積移行率 | ||
| 投与開始48週時点 | 投与開始96週時点 | |
| 本剤投与群 | 2.6%(1.53-3.68) | 4.8%(3.13-6.44) |
| プラセボ群 | 7.0%(5.23-8.73) | 13.2%(10.59-15.85) |
承認時までの試験では、1日0.6mgを投与した951例中452例(47.5%)に臨床検査値の異常を含む副作用が認められている。主な副作用は鼓腸(17.4%)、腹部膨満(13.1%)、下痢(12.0%)等であった。
18. 薬効薬理
18.1 作用機序
18.1.1 本剤は、腸管において二糖類から単糖への分解を担う二糖類水解酵素(α-グルコシダーゼ)を阻害し、糖質の消化・吸収を遅延させることにより食後の過血糖を改善する22)23)24)25)26)27)28)29)。
18.1.2 ブタ小腸由来マルターゼとスクラーゼに対してアカルボースよりそれぞれ約20倍及び30倍強い阻害作用を示し、ラット小腸由来マルターゼ及びスクラーゼ阻害活性はそれぞれアカルボースの約270倍及び190倍である(in vitro)。一方ブタ及びラット膵α-アミラーゼに対する阻害作用はアカルボースの約1/3,000であり、β-グルコシダーゼに対しては阻害活性を示さない22)(in vitro)。
18.1.3 ラット小腸由来のスクラーゼ−イソマルターゼの複合体の二糖類水解酵素に対する阻害様式は競合拮抗的である22)(in vitro)。
18.2 血糖上昇抑制作用
19. 有効成分に関する理化学的知見
19.1. ボグリボース
22. 包装
<ベイスン錠0.2>
100錠[10錠(PTP)×10]、500錠[10錠(PTP)×50]
<ベイスン錠0.3>
100錠[10錠(PTP)×10]、500錠[10錠(PTP)×50]
23. 主要文献
- Morseth S.L.et al., 薬理と治療, 19, 4325-4340, (1991)
- Morseth S.L.et al., 薬理と治療, 19, 4375-4396, (1991)
- 平賀興吾, 基礎と臨床, 26, 283-294, (1992)
- 前芝良宏 他, 薬理と治療, 19, 3639-3649 , (1991)
- 後藤由夫 他, 医学のあゆみ, 160, 943-971 , (1992)
- 神谷文雅 他, 臨床成人病, 22, 573-591 , (1992)
- 池田義雄 他, 新薬と臨牀, 41, 20-28, (1992)
- 中埜幸治 他, 診療と新薬, 28, 2315-2323, (1991)
- 森島豊彦 他, 臨牀と研究, 69, 3997-4010, (1992)
- 河盛隆造 他, 糖尿病, 35, 633-640, (1992) »DOI
- 柴田 昭 他, Progress in Medicine., 12, 239-250, (1992) »DOI
- 田港朝彦 他, 新薬と臨牀, 41, 193-205, (1992)
- 西澤良記 他, 医学と薬学, 27, 123-135, (1992)
- 松岡 瑛 他, 診療と新薬, 29, 255-265, (1992)
- 加来浩平 他, 薬理と治療, 20, 887-899, (1992)
- 三村和郎 他, 臨牀と研究, 69, 919-932 , (1992)
- 三村和郎 他, 臨牀と研究, 69, 235-244, (1992)
- 中村光男 他, 新薬と臨牀, 41, 2-18 , (1992)
- 小泉順二 他, 診療と新薬, 29, 241-252 , (1992)
- 梅田文夫 他, 臨牀と研究, 69, 1309-1322, (1992)
- Kawamori R.et al, Lancet., 373, 1607-1614, (2009)
- 小高裕之 他, 日本栄養・食糧学会誌, 45, 27-31, (1992) »DOI
- 後藤由夫 他, 臨床成人病, 22, 451-458, (1992)
- 池田 衡 他, 薬理と治療, 19, 4105-4117, (1991)
- Odaka H.et al., J.Nutr.Sci.Vitaminol., 38, 27-37, (1992) »PubMed »DOI
- 池田 衡 他, 薬理と治療, 19, 4451-4456, (1991)
- 小高裕之 他, 日本栄養・食糧学会誌, 45, 33-38, (1992) »DOI
- 高見健治 他, 薬理と治療, 19, 4457-4467, (1991)
- 小高裕之 他, 薬理と治療, 19, 4829-4834, (1991)
24. 文献請求先及び問い合わせ先
文献請求先
T's製薬株式会社
ティーズDIセンター
〒451-0045
名古屋市西区名駅二丁目27番8号
電話:0120-923-093 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
製品情報問い合わせ先
T's製薬株式会社
ティーズDIセンター
〒451-0045
名古屋市西区名駅二丁目27番8号
電話:0120-923-093 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
25. 保険給付上の注意
耐糖能異常における2型糖尿病の発症抑制(ただし、食事療法及び運動療法を十分に行っても改善されない場合に限る。)を目的に使用する場合、保険適用上の取扱いを以下のとおりとすること。
1.耐糖能異常(空腹時血糖が126mg/dL未満かつ75g経口ブドウ糖負荷試験の血糖2時間値が140〜199mg/dL)と判断され、糖尿病発症抑制の基本である食事療法及び運動療法を3〜6ヵ月間行っても改善されず、かつ高血圧症、脂質異常症(高トリグリセリド血症、低HDLコレステロール血症等)のいずれかを基礎疾患として有する患者を対象とする場合に限り、保険適用されるものとする。
2.診療報酬明細書の摘要欄には、耐糖能異常と判断した根拠(判断した年月日とその結果)、食事療法及び運動療法を3〜6ヵ月間行っても改善されなかった旨及び高血圧症又は脂質異常症の診断名を記載する。
26. 製造販売業者等
26.1 製造販売元
T's製薬株式会社
大阪市中央区道修町四丁目1番1号
26.2 販売
武田薬品工業株式会社
大阪市中央区道修町四丁目1番1号