医薬品情報
| 総称名 | ダイアップ |
|---|---|
| 一般名 | ジアゼパム |
| 欧文一般名 | Diazepam |
| 製剤名 | ジアゼパム坐剤 |
| 薬効分類名 | 小児用抗けいれん剤 |
| 薬効分類番号 | 1139 |
| KEGG DRUG |
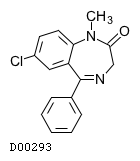
D00293
ジアゼパム
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年2月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ダイアップ坐剤4 | DIAPP Suppositories | 高田製薬 | 1124701J1022 | 44.6円/個 | 向精神薬(第三種), 処方箋医薬品 |
| ダイアップ坐剤6 | DIAPP Suppositories | 高田製薬 | 1124701J2029 | 50.3円/個 | 向精神薬(第三種), 処方箋医薬品 |
| ダイアップ坐剤10 | DIAPP Suppositories | 高田製薬 | 1124701J3025 | 57.1円/個 | 向精神薬(第三種), 処方箋医薬品 |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
小児に対して次の目的に用いる
熱性けいれん及びてんかんのけいれん発作の改善
6. 用法及び用量
通常、小児にジアゼパムとして1回0.4〜0.5mg/kgを1日1〜2回、直腸内に挿入する。
なお、症状に応じて適宜増減するが、1日1mg/kgを超えないようにする。
なお、症状に応じて適宜増減するが、1日1mg/kgを超えないようにする。
8. 重要な基本的注意
8.1 本剤は小児用の製剤である。
8.2 眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、投与後の患者の状態に十分注意すること。
8.3 熱性けいれんに用いる場合には、発熱時の間歇投与とし、37.5℃の発熱を目安に、すみやかに直腸内に挿入する。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心障害のある患者
症状が悪化するおそれがある。
9.1.2 脳に器質的障害のある患者
作用が強くあらわれる。
9.1.3 衰弱患者
作用が強くあらわれる。
9.1.4 中等度又は重篤な呼吸不全のある患者
症状が悪化するおそれがある。
9.2 腎機能障害患者
排泄が遅延するおそれがある。
9.3 肝機能障害患者
排泄が遅延するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.5.1 妊娠中にジアゼパム製剤の投与を受けた患者の中に奇形を有する児等の障害児を出産した例が対照群と比較して有意に多いとの疫学的調査報告がある。
9.5.2 ベンゾジアゼピン系薬剤で新生児に哺乳困難、嘔吐、活動低下、筋緊張低下、過緊張、嗜眠、傾眠、呼吸抑制・無呼吸、チアノーゼ、易刺激性、神経過敏、振戦、低体温、頻脈等を起こすことが報告されている。
なお、これらの症状は、離脱症状あるいは新生児仮死として報告される場合もある。また、ベンゾジアゼピン系薬剤で新生児に黄疸の増強を起こすことが報告されている。
なお、これらの症状は、離脱症状あるいは新生児仮死として報告される場合もある。また、ベンゾジアゼピン系薬剤で新生児に黄疸の増強を起こすことが報告されている。
9.5.3 分娩前に連用した場合、出産後新生児に離脱症状があらわれることが、ベンゾジアゼピン系薬剤で報告されている。
9.6 授乳婦
授乳を避けさせること。ヒト母乳中へ移行し、新生児に嗜眠、体重減少等を起こすことがあり、また、黄疸を増強する可能性がある。
9.7 小児等
9.7.1 乳児
慎重に投与すること。作用が強くあらわれる。一般的に代謝排泄機能が未熟であることが考えられる。
乳児(1歳未満)に対し投与された244例のうち、13例(5.33%)に副作用が発現したが、1歳以上の症例の副作用発現率6.94%(273例/3,934例)と有意差はなかった。
乳児(1歳未満)に対し投与された244例のうち、13例(5.33%)に副作用が発現したが、1歳以上の症例の副作用発現率6.94%(273例/3,934例)と有意差はなかった。
9.7.2 低出生体重児・新生児
投与しないこと。低出生体重児・新生児を対象とした有効性及び安全性を指標とした臨床試験は実施していない。[2.3参照]
10. 相互作用
10.1 併用禁忌
| リトナビル ノービア ニルマトレルビル・リトナビル パキロビッド [2.4参照] | 過度の鎮静や呼吸抑制等を起こすおそれがある。 | これらの薬剤のCYPに対する競合的阻害作用により、併用した場合、本剤の血中濃度が大幅に上昇することが予測される。 |
10.2 併用注意
| 中枢神経抑制剤 フェノチアジン誘導体、 バルビツール酸誘導体等 | 作用が増強されることがある。 | 相互に中枢神経抑制作用を増強することが考えられている。 |
| アルコール(飲酒) | 作用が増強されることがある。 | 相互に中枢神経抑制作用を増強することが考えられている。 |
| オピオイド鎮痛剤 | 作用が増強されることがある。 | 相互に中枢神経抑制作用を増強することが考えられている。 |
| モノアミン酸化酵素阻害剤 | 作用が増強されることがある。 | 機序は不明。 |
| シメチジン、 オメプラゾール、 エソメプラゾール、 ランソプラゾール | 作用が増強されることがある。 | シメチジン・オメプラゾールにより肝臓のCYPによる代謝が阻害され、本剤のクリアランスが減少し、血中濃度が上昇することによる。 本剤の代謝、排泄を遷延させるおそれがある。 |
| シプロフロキサシン | 作用が増強されることがある。 | 本剤のクリアランスがシプロフロキサシンとの併用により低下することが報告されている。 |
| フルボキサミンマレイン酸塩 | 作用が増強されることがある。 | 本剤の代謝が阻害されることにより本剤のクリアランスが低下することが報告されている。 |
| 強いCYP3Aを阻害する薬剤 コビシスタットを含有する製剤、 ボリコナゾール等 | 本剤の血中濃度が上昇する可能性がある。 | これら薬剤のCYP3A阻害作用により、本剤の代謝が阻害されるため。 |
| CYP3A4で代謝される薬剤 アゼルニジピン、 ホスアンプレナビル等 | 本剤又はこれらの薬剤の作用が増強されるおそれがある。 | 本剤とこれらの薬剤がCYP3A4を競合的に阻害することにより、相互のクリアランスが低下すると考えられる。 |
| エトラビリン | 本剤の血中濃度が上昇する可能性がある。 | エトラビリンのCYP2C9、CYP2C19阻害作用により、本剤の代謝が阻害される。 |
| マプロチリン塩酸塩 | 1)中枢神経抑制作用を増強することがある。 2)併用中の本剤を急速に減量又は中止するとけいれん発作が起こることがある。 | 1)相互に中枢神経抑制作用を増強することが考えられている。 2)本剤の抗けいれん作用により抑制されていたマプロチリン塩酸塩のけいれん誘発作用が、本剤の急速な減量又は中止によりあらわれることが考えられている。 |
| ミルタザピン | 鎮静作用が増強されるおそれがある。 また、ミルタザピンとの併用により精神運動機能及び学習獲得能力が減退するとの報告がある。 | 相加的な鎮静作用を示すことが考えられる。 |
| バルプロ酸ナトリウム | 本剤の作用が増強することがある。 | 本剤の非結合型の血中濃度を上昇させる。 |
| ダントロレンナトリウム水和物、 ボツリヌス毒素製剤 | 筋弛緩作用を増強することがある。 | 相互に筋弛緩作用を増強することが考えられている。 |
| リファンピシン | 本剤の血中濃度が低下し、作用が減弱するおそれがある。 | リファンピシンのCYP3A4誘導作用により、本剤の代謝が誘導され、血中濃度が低下する可能性がある。 |
| アパルタミド | 本剤の血中濃度が低下し、作用が減弱するおそれがある。 | アパルタミドのCYP2C19誘導作用により、本剤の代謝が誘導され、血中濃度が低下する可能性がある。 |
| シナカルセト、 エボカルセト | これら薬剤の血中濃度に影響を与えるおそれがある。 | 血漿蛋白結合率が高いことによる。 |
| 無水カフェイン | 本剤の血中濃度が減少することがある。 | 不明 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 依存性(頻度不明)
連用により薬物依存を生じることがあるので、観察を十分に行い、用量及び使用期間に注意し慎重に投与すること。また、連用中における投与量の急激な減少ないし投与の中止により、けいれん発作、せん妄、振戦、不眠、不安、幻覚、妄想等の離脱症状があらわれることがあるので、投与を中止する場合には、徐々に減量するなど慎重に行うこと。
11.1.2 刺激興奮、錯乱等(頻度不明)
11.1.3 呼吸抑制(頻度不明)
慢性気管支炎等の呼吸器疾患に用いた場合、呼吸抑制があらわれることがある。
注)発現頻度は使用成績調査を含む
11.2 その他の副作用
| 1%以上 | 1%未満 | 頻度不明 | |
| 精神神経系 | 眠気、ふらつき | 歩行失調、頭痛、言語障害、興奮、振戦 | 眩暈、失禁、霧視、複視、多幸症 |
| 肝臓 | 黄疸 | ||
| 呼吸器 | 喘鳴、気道分泌過多 | ||
| 血液 | 白血球減少症 | 顆粒球減少症 | |
| 循環器 | 頻脈、血圧低下 | ||
| 消化器 | 悪心、嘔吐、食欲不振、下痢、流涎 | 便秘、口渇 | |
| 過敏症 | 発疹 | ||
| その他 | 脱力感、四肢冷感、頻尿 | けん怠感、浮腫、低体温 |
13. 過量投与
13.1 処置
本剤の過量投与が明白又は疑われた場合の処置としてフルマゼニル(ベンゾジアゼピン受容体拮抗剤)を投与する場合には、使用前にフルマゼニルの使用上の注意を必ず読むこと。
14. 適用上の注意
14.1 薬剤投与時の注意
直腸投与のみに使用し、経口投与はしないこと。
15. その他の注意
15.1 臨床使用に基づく情報
投与した薬剤が特定されないままにフルマゼニル(ベンゾジアゼピン受容体拮抗剤)を投与された患者で、新たに本剤を投与する場合、本剤の鎮静・抗けいれん作用が変化、遅延するおそれがある。
16. 薬物動態
16.1 血中濃度
健康成人14例に本剤(10mg)を1回直腸内投与した時の平均最高血中濃度は321ng/mL、平均最高血中濃度到達時間は1.2時間、平均消失半減期は34.9時間であった。
また、小児6例(平均14.8ヵ月)に0.5mg/kgを1回直腸内投与した時の平均最高血中濃度は379ng/mL、平均最高血中濃度到達時間は1.5時間、平均消失半減期は32.8時間であった。
また、小児6例(平均14.8ヵ月)に0.5mg/kgを1回直腸内投与した時の平均最高血中濃度は379ng/mL、平均最高血中濃度到達時間は1.5時間、平均消失半減期は32.8時間であった。
図16-1 小児における平均血漿中濃度推移
17. 臨床成績
17.1 有効性及び安全性に関する試験
18. 薬効薬理
18.1 作用機序
中枢における抑制性伝達物質GABAの受容体には、GABAA受容体とGABAB受容体があるが、GABAA受容体は、GABA結合部位、ベンゾジアゼピン結合部位、バルビツール酸誘導体結合部位、などからなる複合体を形成し、中央にCl−を通す陰イオンチャネル(Cl−チャネル)が存在する。GABAがその結合部位に結合するとCl−チャネルが開口し、それにより神経細胞は過分極し、神経機能の全般的な抑制がもたらされる。ベンゾジアゼピン系薬物がこの複合体の結合部位に結合すると、GABAによる過分極誘起作用すなわち神経機能抑制作用を促進する10)。
18.2 マウスにおける経口投与との比較
| 試験法 | 投与後30分のED50値(mg/kg) | |
| 直腸内投与 | 経口投与 | |
| 抗Bemegrideけいれん | 0.25 | 0.56 |
| 抗電撃けいれん | 0.45 | 0.71 |
19. 有効成分に関する理化学的知見
19.1. ジアゼパム
20. 取扱い上の注意
アルミピロー開封後は湿気を避けて遮光して保存すること。
22. 包装
<ダイアップ坐剤4>
50個[5個×10]
<ダイアップ坐剤6>
50個[5個×10]
<ダイアップ坐剤10>
50個[5個×10]
23. 主要文献
- 原沢孝夫他, 薬理と治療, 9 (7), 261-271, (1981)
- 竹重博子他, 小児科臨床, 35 (1), 25-38, (1982)
- 釜萢敏他, 小児科臨床, 35 (2), 130-138, (1982)
- 高江洲悦子他, 小児科臨床, 34 (11), 40-48, (1981)
- 三宅捷太他, 小児科診療, 45 (4), 132-138, (1982)
- 牧野定夫他, 小児科診療, 45 (3), 113-116, (1982)
- 高橋寛他, 薬理と治療, 10 (7), 343-368, (1982)
- 山脇英範他, 小児科臨床, 38 (10), 73-78, (1985)
- 福山幸夫他, 小児科臨床, 44 (3), 111-133, (1991)
- 日本薬局方解説書編集委員会編, 第十八改正 日本薬局方解説書, (2021), (廣川書店)
- 花井道夫他, 薬理と治療, 13 (12), 225-234, (1985)
24. 文献請求先及び問い合わせ先
文献請求先
高田製薬株式会社
文献請求窓口
〒336-8666
さいたま市南区沼影1丁目11番1号
電話:0120-989-813
FAX:048-816-4183
製品情報問い合わせ先
高田製薬株式会社
文献請求窓口
〒336-8666
さいたま市南区沼影1丁目11番1号
電話:0120-989-813
FAX:048-816-4183
25. 保険給付上の注意
25.1 投薬期間制限医薬品に関する情報
本剤は厚生労働省告示第97号(平成20年3月19日付)に基づき、投薬量は1回14日分を限度とされています。
26. 製造販売業者等
26.1 製造販売元
高田製薬株式会社
さいたま市西区宮前町203番地1