医薬品情報
| 総称名 | ニトロール |
|---|---|
| 一般名 | 硝酸イソソルビド |
| 欧文一般名 | Isosorbide Dinitrate |
| 薬効分類名 | 硝酸イソソルビド注射剤 |
| 薬効分類番号 | 2171 |
| ATCコード | C01DA08 |
| KEGG DRUG |
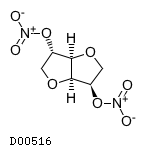
D00516
硝酸イソソルビド
|
| KEGG DGROUP |
DG01270
硝酸イソソルビド
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年3月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ニトロール注5mg | Nitorol injection | エーザイ | 2171404A1026 | 151円/管 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 重篤な低血圧又は心原性ショックのある患者[血管拡張作用によりさらに血圧を低下させ、症状を悪化させるおそれがある。][9.1.1参照]
2.2 Eisenmenger症候群又は原発性肺高血圧症の患者[血圧低下によりショックを起こすことがある。]
2.3 右室梗塞の患者[血圧低下によりショックを起こすことがある。]
2.4 脱水症状のある患者[血圧低下によりショックを起こすことがある。]
2.5 神経循環無力症の患者[本剤の効果がなく、本剤投与により血圧低下等があらわれることがある。]
2.6 閉塞隅角緑内障の患者[眼圧を上昇させるおそれがある。]
2.7 硝酸・亜硝酸エステル系薬剤に対し過敏症の既往歴のある患者
2.8 頭部外傷又は脳出血のある患者[頭蓋内圧を上昇させるおそれがある。]
2.9 ホスホジエステラーゼ5阻害作用を有する薬剤(シルデナフィルクエン酸塩、バルデナフィル塩酸塩水和物、タダラフィル)又はグアニル酸シクラーゼ刺激作用を有する薬剤(リオシグアト)を投与中の患者[10.1参照]
4. 効能または効果
6. 用法及び用量
<急性心不全>
通常、成人には、本剤を注射液そのまま、又は生理食塩液、5%ブドウ糖注射液等で希釈して0.05〜0.001%溶液とし、硝酸イソソルビドとして1時間あたり1.5〜8mgを点滴静注する。投与量は患者の病態に応じて適宜増減するが、増量は1時間あたり10mgまでとする。
<不安定狭心症>
通常、成人には、本剤を注射液そのまま、又は生理食塩液、5%ブドウ糖注射液等で希釈して0.05〜0.001%溶液とし、硝酸イソソルビドとして1時間あたり2〜5mgを点滴静注する。投与量は患者の病態に応じて適宜増減する。
<冠動脈造影時の冠攣縮寛解>
通常、成人には、冠動脈造影時に本剤を注射液そのまま、硝酸イソソルビドとして5mgをカテーテルを通し、バルサルバ洞内に1分以内に注入する。なお、投与量は、患者の症状に応じて適宜増減するが、投与量の上限は10mgまでとする。
7. 用法及び用量に関連する注意
7.1 冠動脈造影時に冠攣縮を誘発した場合は、迅速に攣縮寛解のための処置を行うこと。また、まれに完全閉塞寛解時にreperfusion injuryによると考えられる心室細動などの危険な不整脈や血圧低下を起こすことがあるので電気的除細動などの適切な処置を行うこと。
8. 重要な基本的注意
8.1 本剤投与中は、頻回の血圧測定と血行動態のモニターを行うこと。また、投与量の調節は患者の血行動態、症状をみて徐々に行うこと。[11.1.1参照]
8.2 投与中に血圧低下等の異常が観察された場合には、減量又は投与を中止すること。また、必要に応じて昇圧剤投与等の適切な処置を行うこと。[11.1.1参照]
8.3 血圧低下の可能性のある患者や心拍出量が低下している患者に投与する場合には、カテコールアミン系薬剤等と併用することが望ましい。
8.4 投与中に左心不全状態が改善した場合は、患者の様子をみて投与を中止すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 低血圧の患者(重篤な低血圧のある患者を除く)
さらに血圧を低下させるおそれがある。[2.1参照]
9.1.2 左室充満圧の低い患者
血圧低下及び心拍出量低下のおそれがある。
9.1.3 遺伝性果糖不耐症の患者
本剤の添加剤D-ソルビトールが体内で代謝されて生成した果糖が正常に代謝されず、低血糖、肝不全、腎不全等が誘発されるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
本剤は、主として肝臓で代謝されるが、一般に肝機能が低下していることが多いため、高い血中濃度が持続するおそれがある。
10. 相互作用
10.1 併用禁忌
| ホスホジエステラーゼ5阻害作用を有する薬剤 シルデナフィルクエン酸塩 (バイアグラ、レバチオ) バルデナフィル塩酸塩水和物 (レビトラ) タダラフィル (シアリス、アドシルカ、ザルティア) [2.9参照] | 併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 | 本剤はcGMPの産生を促進し、一方、ホスホジエステラーゼ5阻害作用を有する薬剤はcGMPの分解を抑制することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
| グアニル酸シクラーゼ刺激作用を有する薬剤 リオシグアト (アデムパス) [2.9参照] | 併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 | 本剤とグアニル酸シクラーゼ刺激作用を有する薬剤は、ともにcGMPの産生を促進することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
10.2 併用注意
| 利尿剤 | 血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 | 血圧低下作用を増強させる。 |
| 血管拡張剤 硝酸・亜硝酸エステル系薬剤 | 血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 | 血管拡張作用が増強される。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック(0.1〜5%未満)
11.1.2 心室細動、心室頻拍
冠動脈造影時の冠攣縮寛解に際し、reperfusion injuryによると考えられる心室細動等の危険な不整脈(0.1%未満)があらわれることがある。このような場合には、電気的除細動などの適切な処置を行うこと。
発現頻度は製造販売後調査を含む。
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 循環器 | 血圧低下、めまい、動悸、四肢浮腫、心拍出量低下 | 徐脈、期外収縮、心房細動 | |
| 精神神経系 | 頭痛 | 全身倦怠感、興奮、陽気 | |
| 消化器 | 嘔気、嘔吐 | 食欲低下 | |
| 血液 | 動脈血酸素分圧の低下 | メトヘモグロビン血症 | |
| 肝臓 | AST、ALT等の上昇 | ||
| 過敏症 | 発疹 |
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 輸液セットへの吸着
硝酸イソソルビドは、一般に使用されているポリ塩化ビニル製の輸液容器及び輸液セットに吸着するが、ガラス製、ポリエチレン製の容器、器具には吸着しない。硝酸イソソルビドのポリ塩化ビニル製輸液セットに対する吸着率は、図に示す通りで点滴速度に影響され、ポリ塩化ビニル管100cmでは点滴速度60mL/時間(1mL/分)以上であれば、投与量の80%以上が静脈内に注入される。また、硝酸イソソルビドの吸着率は配合濃度に影響されないが、輸液セットが長い程高くなるので注意すること。
点滴速度による影響
16. 薬物動態
16.1 血中濃度
16.1.1 持続投与(健康成人男子)
健康成人男子に硝酸イソソルビドを5mg/hrで静脈内持続注入した際、硝酸イソソルビドの血漿中濃度は緩やかに上昇し、注入開始後1.5時間でほぼ定常濃度に達した。その後、注入停止とともに半減期6.3±1.0分(分布相)及び109.1±35.7分(排泄相)の2相性を示し、速やかに低下した。
| t1/2α(min) | t1/2β(min) | AUC(ng・min/mL) | CL(L/hr) |
| 6.3±1.0 | 109.1±35.7 | 2,694±54.0 | 144±28.2 |
16.1.2 単回投与(心不全患者)
心不全患者に硝酸イソソルビド5mgを静脈内単回投与注)したとき、血漿中硝酸イソソルビド濃度は2相性を示し、半減期3.9±1.2分(分布相)及び78.0±24.0分(排泄相)であった。また、AUC及びクリアランスはそれぞれ2,328±478ng・min/mL及び134.0±22.2L/hrであった1)。
| t1/2α(min) | t1/2β(min) | Vss(L) | AUC(ng・min/mL) | CL(L/hr) |
| 3.9±1.2 | 78.0±24.0 | 124.0±51.2 | 2,328±478 | 134.0±22.2 |
硝酸イソソルビド血漿中濃度
注)静脈内単回投与は承認外用法である。
16.1.3 単回投与(狭心症患者)
狭心症患者に硝酸イソソルビド5mgをバルサルバ洞内に投与したとき、5分後の血漿中濃度は246±122ng/mLを示した。血漿中硝酸イソソルビド濃度は2相性を示し、半減期1.5分(分布相)及び27分(排泄相)であった。また、AUCは5,305±2,352ng・min/mLであった2)。
硝酸イソソルビド血漿中濃度
| Cmax注)(ng/mL) | t1/2α(min) | t1/2β(min) | AUC(ng・min/mL) |
| 246±122 | 1.5 | 27.0 | 5,305±2,352 |
17. 臨床成績
17.1 有効性及び安全性に関する試験
18. 薬効薬理
18.1 作用機序
18.2 病態モデル動物における作用
18.2.1 心臓の前負荷、後負荷を軽減
急性うっ血性心不全イヌによる実験で、本薬は静脈系容量血管を拡張することにより、静脈還流を減少させ、左室拡張終期圧の低下(前負荷の軽減)をもたらし、同時に末梢動脈を拡張して、総末梢血管抵抗を減少(後負荷の軽減)させた。これらの作用により、うっ血性心不全の血行動態を改善した14)。
18.2.2 心筋の局所血流量を増加
18.2.3 虚血部心筋組織内ノルアドレナリンの増加
梗塞イヌによる実験で虚血部心筋からのノルアドレナリンの放出が抑制され、虚血部心筋組織内ノルアドレナリンを増加させ、血行動態的には心係数、左室収縮力の改善を認めた17)。
18.3 血管拡張作用
19. 有効成分に関する理化学的知見
19.1. 硝酸イソソルビド
20. 取扱い上の注意
20.1 外箱開封後は光を遮り保存すること。
22. 包装
10管(ガラスアンプル)
23. 主要文献
- 長村好章ら, 臨牀と研究, 62 (8), 2672-2676, (1985)
- 延吉正清ら, 臨牀と研究, 64 (7), 2308-2311, (1987)
- 広沢弘七郎ら, 呼吸と循環, 33 (7), 903-912, (1985)
- 牧野克俊ら, 臨牀と研究, 61 (8), 2744-2750, (1984)
- Kodama K.et al., Jpn.Circ.J., 48 (4), 380-387, (1984)
- 広沢弘七郎ら, 医学のあゆみ, 134 (4), 310-320, (1985)
- Saito T.et al., Jpn.Circ.J., 50 (1), 30-36, (1986)
- 伊藤正明ら, 呼吸と循環, 33 (5), 679-684, (1985)
- Hirota Y.et al., Jpn.Circ.J., 51 (6), 617-623, (1987)
- 滝島 任ら, 循環器科, 21 (3), 276-286, (1987)
- 延吉正清ら, 臨牀と研究, 64 (7), 2295-2307, (1987)
- Kukovetz W.R., Cardiology, 74 (S.1), 12-19, (1987)
- 高田 芳伸ら, 薬局, 42 (7), 937-944, (1991)
- 大原秀人ら, 日本薬理学雑誌, 82 (5), 343-350, (1983) »PubMed
- 高山幸男ら, 脈管学, 21 (5), 351-357, (1981)
- Tonooka I.et al., Am.Heart J., 111 (3), 525-533, (1986)
- 李 詔, 日大医学雑誌, 41 (6), 637-652, (1982)
- Ishikawa S.et al., Br.J.Pharmacol., 79 (3), 737-750, (1983)
- Matlib M.A.et al., Am.Heart J., 110 (1), 204-212, (1985)
24. 文献請求先及び問い合わせ先
文献請求先
エーザイ株式会社
hhcホットライン
〒112-8088
東京都文京区小石川4-6-10
電話:フリーダイヤル 0120-419-497
製品情報問い合わせ先
エーザイ株式会社
hhcホットライン
〒112-8088
東京都文京区小石川4-6-10
電話:フリーダイヤル 0120-419-497
26. 製造販売業者等
26.1 製造販売元
エーザイ株式会社
東京都文京区小石川4-6-10