医薬品情報
| 総称名 | 次硝酸ビスマス |
|---|---|
| 一般名 | 次硝酸ビスマス |
| 欧文一般名 | Bismuth Subnitrate |
| 薬効分類名 | 止しゃ剤 |
| 薬効分類番号 | 2315 |
| ATCコード | A02BX12 |
| KEGG DRUG |
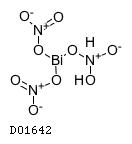
D01642
次硝酸ビスマス
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年11月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 9.特定の背景を有する患者に関する注意 11.副作用 13.過量投与 14.適用上の注意 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| 次硝酸ビスマスシオエ | Bismuth Subnitrate SIOE | シオエ製薬 | 2315002X1088 | 8.3円/g |
2. 禁忌
次の患者には投与しないこと
2.1 慢性消化管通過障害又は重篤な消化管潰瘍のある患者[ビスマスの吸収による副作用が起こるおそれがある。]
2.2 出血性大腸炎の患者[腸管出血性大腸菌(O157等)や赤痢菌等の重篤な細菌性下痢患者では、症状の悪化、治療期間の延長をきたすおそれがある。][9.1.1参照]
4. 効能または効果
下痢症
6. 用法及び用量
次硝酸ビスマスとして、通常成人1日2gを2〜3回に分割経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
7. 用法及び用量に関連する注意
精神神経系障害があらわれるおそれがあるので長期連続投与を避け、やむを得ない場合には、原則として1ヵ月に20日程度(1週間に5日以内)の投与にとどめること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 細菌性下痢のある患者(出血性大腸炎の患者は除く)
治療上やむを得ないと判断される場合を除き、投与しないこと。治療期間の延長をきたすおそれがある。[2.2参照]
9.1.2 便秘の患者
本剤は下痢症を適応とするため、症状が悪化するおそれがある。
9.1.3 結腸瘻造設術、回腸瘻造設術又は人工肛門造設術を受けた患者
9.1.4 消化管憩室のある患者
ビスマスが吸収されやすいため、血液中に移行する量が多くなるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。投与する場合は、投与量、投与期間等に注意して投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。投与量、投与期間等に注意して投与すること。
9.7 小児等
投与量、投与期間等に注意して投与すること。小児等を対象とした臨床試験は実施していない。
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 精神神経系障害(頻度不明)
ビスマス塩類(次硝酸ビスマス、次没食子酸ビスマス)1日3〜20gの連続経口投与(1ヵ月〜数年間)により、間代性痙攣、昏迷、錯乱、運動障害等の精神神経系障害(初期症状:不安、不快感、記憶力減退、頭痛、無力感、注意力低下、振戦等)があらわれたとの報告がある。これらの報告によれば、症状は投与中止後数週間〜数ヵ月で回復している1)。
11.1.2 血液障害(頻度不明)
亜硝酸中毒(メトヘモグロビン血症、血圧降下、皮膚の紅潮)があらわれることがある。また、便秘があらわれた場合には、亜硝酸中毒を起こすおそれがある1)。
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 消化器 | 嘔気、食欲不振 | |
| 粘膜 | 歯齦縁、舌、口腔内等に青色又は青黒色の着色 |
13. 過量投与
13.1 症状
以下の症状があらわれることがある1)。
・臭い口臭、口内炎と歯肉炎、金属味、食欲不振、悪心、嘔吐、下痢、腹痛、頭痛、不快感と脱力感、発熱、リウマチ様疼痛、蕁麻疹、落屑性皮膚炎、歯肉の黒色線条及び頬粘膜の黒色斑点、血圧低下、腎障害(近位尿細管障害、腎不全)、肝障害。
・小児に次硝酸ビスマスを大量投与した結果、メトヘモグロビン血症を起こして死亡した例がある。
13.2 処置
以下の治療を行うことが望ましい1)。
・下剤:硫酸マグネシウム(30g→水200mL)又はクエン酸マグネシウム(34g→水200mL)の投与。
・輸液(肝保護剤を加える)。
・キレート剤(重症の場合のみ):ジメルカプロールの筋注(1回投与量2.5mg/kg)。
〔中等症まで〕初日、6時間毎に4回、2日目以降6日間1日1回投与。
〔重症〕最初の2日間は4時間毎に1日6回、3日目は1日4回、以後回復するまで毎日2回投与。
(注意)腎機能低下のある場合には体内に蓄積するため減量投与すること。
・チオ硫酸ナトリウムの静注。
・塩化アンモニウムの点滴。
・血液透析(HD):ビスマスの血中濃度が非常に高い場合。
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 浣腸には使用しないこと。
14.1.2 本剤の服用によって便の色が黒くなることがある。(ビスマスが黒色の硫化ビスマスになるため。)
16. 薬物動態
16.2 吸収
次サリチル酸ビスマスの場合約1%2)
16.5 排泄
次サリチル酸ビスマスの場合、ほとんど糞便中に排泄される。吸収されたビスマスの血漿中半減期は約5日で、唾液、尿及び胆汁中に排泄される2)。
18. 薬効薬理
18.1 作用機序
本剤は収れん並びに粘膜面、潰瘍面を被覆保護する作用を有し、また腸内異常発酵によって生じる硫化水素と結合するため、下痢に効果があるとされている2)。
19. 有効成分に関する理化学的知見
19.1. 次硝酸ビスマス
22. 包装
500g(ポリ袋)
23. 主要文献
- 日本薬局方 医薬品情報集, 750, (2011), ((株)じほう)
- 第十八改正日本薬局方解説書, C-2210-C-2213, (2021), (廣川書店)
24. 文献請求先及び問い合わせ先
文献請求先
シオエ製薬株式会社
製品情報担当
〒661-0976
兵庫県尼崎市潮江3丁目1番11号
電話:06-6470-2102
FAX:06-6499-8132
製品情報問い合わせ先
シオエ製薬株式会社
製品情報担当
〒661-0976
兵庫県尼崎市潮江3丁目1番11号
電話:06-6470-2102
FAX:06-6499-8132
26. 製造販売業者等
26.1 製造販売元
シオエ製薬株式会社
兵庫県尼崎市潮江3丁目1番11号
26.2 販売
日本新薬株式会社
京都市南区吉祥院西ノ庄門口町14