医薬品情報
| 総称名 | ボンゾール |
|---|---|
| 一般名 | ダナゾール |
| 欧文一般名 | Danazol |
| 製剤名 | ダナゾール錠 |
| 薬効分類名 | 子宮内膜症治療剤 |
| 薬効分類番号 | 2499 |
| ATCコード | G03XA01 |
| KEGG DRUG |
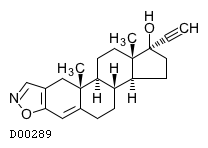
D00289
ダナゾール
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年12月 改訂(第3版 D16)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ボンゾール錠200mg | BONZOL tablets | 田辺ファーマ | 2499007F2028 | 242.4円/錠 | 処方箋医薬品注) |
1. 警告
2. 禁忌
次の患者には投与しないこと
2.1 血栓症の既往歴のある患者[血栓症を起こすおそれがある。][11.1.1参照]
2.2 アンチトロンビンIII、プロテインC、プロテインSなどの凝固制御因子の欠損又は減少のある患者[血栓症を起こすおそれがある。][11.1.1参照]
2.4 重篤な心疾患のある患者[浮腫等の症状が強くあらわれるおそれがある。][9.1.1参照]
2.5 重篤な腎疾患のある患者[9.2.1参照]
2.6 ポルフィリン症の患者[症状を悪化させるおそれがある。]
2.7 アンドロゲン依存性腫瘍のある患者[症状を悪化させるおそれがある。]
2.8 診断のつかない異常性器出血のある患者[このような患者では悪性腫瘍の疑いがある。][8.4参照]
2.9 妊婦又は妊娠している可能性のある女性[7.、9.5参照]
2.10 授乳婦[9.6参照]
4. 効能または効果
6. 用法及び用量
通常、成人にはダナゾールとして1日200〜400mgを2回に分け、月経周期第2〜5日より、約4カ月間連続経口投与する。症状により増量する。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
8.1 投与にあたり、既往歴・家族歴を十分に聴取し、血栓症の発生に十分配慮すること。血栓症を起こしやすい因子・合併症を有する患者に投与する場合は、末梢血液一般検査(血小板数、ヘマトクリット値等)を行うことが望ましい。[1.、11.1.1参照]
8.2 血栓症の危険性は高齢者、特に40歳以上で高くなる。また外国では、喫煙が類薬(経口避妊薬)による重篤な副作用(血栓症等)の危険性を増大させ、また、この危険性は年齢及び喫煙量により増大すると報告されている。[1.、11.1.1参照]
8.3 投与により、血栓症を引き起こすおそれがあるので、下肢の疼痛・浮腫、激しい頭痛、嘔吐、吐き気、めまい等の症状があらわれた場合には、投与を中止すること。また、患者に対しては、異常が認められた場合には直ちに医師等に相談するよう、あらかじめ説明すること。[1.、11.1.1参照]
8.4 投与に際して、類似疾患(悪性腫瘍、子宮筋腫等)との鑑別に留意し、投与中腫瘤が増大したり、臨床症状の改善がみられない場合は投与を中止すること。[2.8参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心疾患のある患者又はその既往歴のある患者(重篤な心疾患のある患者を除く)
浮腫等の症状が強くあらわれるおそれがある。[2.4参照]
9.1.2 てんかん患者、片頭痛のある患者
浮腫等により症状が強くあらわれるおそれがある。
9.1.3 糖尿病患者
十分コントロールを行いながら投与すること。耐糖能の異常がみられるおそれがある。
9.2 腎機能障害患者
9.2.1 重篤な腎疾患のある患者
投与しないこと。浮腫等の症状が強くあらわれるおそれがある。[2.5参照]
9.2.2 腎疾患のある患者又はその既往歴のある患者(重篤な腎疾患のある患者を除く)
浮腫等の症状が強くあらわれるおそれがある。
9.3 肝機能障害患者
9.3.1 重篤な肝機能障害、肝疾患のある患者
9.3.2 肝機能障害、肝疾患のある患者(重篤な肝機能障害、肝疾患のある患者を除く)
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、投与しないこと。女性胎児の男性化を起こすことが報告されている。[2.9、7.参照]
9.6 授乳婦
投与しないこと。動物実験(ラット)で、母乳中へ移行することが報告されている。[2.10参照]
9.8 高齢者
減量(例えば1日100mg)するなど注意すること。一般に生理機能が低下している。
10. 相互作用
相互作用序文
本剤は、CYP3A4に対する阻害作用を有する。
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| ワルファリンカリウム | 出血傾向(血尿・吐血等)を増強することが考えられる。 | 肝細胞でクマリンのレセプター部位への親和性増加と、ビタミンK依存性因子の産生阻害・異化促進によりワルファリンカリウムの作用が増強するためと考えられる。また、ダナゾールが抗凝血性を高めるとの報告もある。 |
| カルバマゼピン | カルバマゼピンの作用を増強することが考えられる。 | カルバマゼピンの代謝を抑制するためと考えられる。 |
| シクロスポリン | シクロスポリンの作用を増強することが考えられる。 | 機序は明らかにされていないがシクロスポリンの血中濃度が上昇すると報告されている。 |
| タクロリムス水和物 | タクロリムスの作用を増強することが考えられる。 | タクロリムスの脱メチル及び水酸化による代謝を抑制するためと考えられる。 |
| インスリン製剤 (ヒトインスリン等) | 高血糖症状があらわれることがある。 | インスリン抵抗性を増強するおそれがある。 |
| アルファカルシドール | 血中カルシウム値が上昇したとの報告がある。 | 機序は不明である。 |
| シンバスタチン アトルバスタチンカルシウム水和物 | ミオパシー、横紋筋融解症が発現したとの報告がある。 | 本剤のCYP3A4に対する阻害作用により、左記薬剤の代謝が阻害され、これらの血中濃度が上昇する可能性がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 血栓症(頻度不明)
11.1.2 心筋梗塞(頻度不明)
11.1.5 間質性肺炎(頻度不明)
注1)発現頻度は、製造販売後調査の結果を含み、子宮内膜症及び乳腺症に対する試験の結果に基づき算出した。
11.2 その他の副作用
| 10%以上 | 0.5〜10%未満 | 0.5%未満 | 頻度不明 | |
| 肝臓 | ALT上昇(13.53%) | LDH上昇、AST上昇 | 黄疸、ALP上昇 | γ-GTP上昇 |
| 皮膚 | ざ瘡(16.25%) | 発疹、色素沈着、皮脂の分泌増加 | 脱毛、紅斑(多形滲出性紅斑等)、はだあれ、蕁麻疹、点状出血 | 光線過敏症 |
| 男性化現象 | 嗄声、多毛 | 陰核肥大 | ||
| 電解質代謝 | 浮腫(10.31%) | 体重増加 | ||
| 子宮 | 性器出血 | 帯下の増加、無月経 | ||
| 乳房 | 乳房変化(乳房縮小、乳頭痛等) | |||
| 血液 | 白血球減少 | 白血球増多、赤血球増多、血小板増多、血小板減少 | ||
| 消化器 | 悪心・嘔吐、胃不快感、胃痛、便秘、食欲亢進 | 下痢、食欲不振、口内炎、口渇 | ||
| 筋肉 | 筋肉痛、関節痛、しびれ、肩こり | 筋拘縮、痙攣、四肢の感覚異常 | 手根管症候群、CK上昇 | |
| 精神神経系 | 神経過敏、頭痛、めまい、倦怠感 | 眠気、耳鳴、不眠、精神不安 | 良性頭蓋内圧亢進注2)、抑うつ | |
| 低エストロゲン症状 | 熱感 | そう痒、発汗、顔面潮紅、腟炎、乾燥感 | ||
| その他 | 心悸亢進、眼精疲労、味覚異常、性欲減退、性欲亢進、コレステロール上昇 | 耐糖能の異常、立ちくらみ、血圧上昇 |
12. 臨床検査結果に及ぼす影響
本剤は、テストステロン又は血漿蛋白の臨床検査結果に影響を及ぼすおそれがある。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
本剤の使用によって子宮内膜症治療患者における卵巣癌発現のリスクが増大するとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人女性6例にダナゾールを1回100mgあるいは200mg経口投与したところ、血漿中濃度は、それぞれ投与後2.5±0.5及び2.7±0.8時間で最高に達し、その後緩やかに減少した1)。(カプセル剤の成績)
16.1.2 反復投与
健康成人女性9例にダナゾールを1回100mgあるいは200mgを1日2回、14日間経口投与したところ、投与量と血漿中濃度には相関がみられ、7〜14日でほぼ定常状態に達した2)(外国人でのデータ)。(カプセル剤の成績)
16.2 吸収
本剤の吸収部位は消化管である。
16.3 分布
雌性ラットに14C-ダナゾール10mg/kgを単回経口投与したとき、大脳、下垂体、肝臓、腎臓、副腎及び子宮等ほとんどの組織で1.5時間後に最高濃度を示し、肝臓及び副腎で高濃度であった。以後、血中濃度に対応して減少した3)。
16.4 代謝
本剤の主な代謝は肝臓で行われている。
16.5 排泄
雌性ラットに14C-ダナゾール10mg/kgを単回経口投与したとき、投与後48時間の尿、糞及び呼気中の排泄率はそれぞれ投与量の17.8%、81.3%及び0.6%であった3)。
17. 臨床成績
18. 薬効薬理
18.1 作用機序
子宮内膜症に対し、下垂体に作用してゴナドトロピン分泌を抑制するとともに、卵巣、子宮内膜症組織に直接作用して、異所性子宮内膜組織を萎縮・壊死させる。
18.2 抗ゴナドトロピン作用
18.2.1 健康成人女性にダナゾールを200mg/日投与すると、血中FSH、LHのmid-cycle surgeを抑制した6)。
18.2.2 一側性卵巣摘除ラットを用いた実験で、ダナゾールは代償性の卵巣肥大を抑制し、腟発情日数を減少させた7)。
18.2.3 幼若去勢ラットを用いたin vivo実験で、ダナゾールは去勢による血中FSH、LHの上昇を有意に(p<0.01)抑制した8)。
18.3 卵巣におけるステロイドホルモン産生酵素活性抑制作用
18.4 ステロイドレセプターとの相互作用
ヒト子宮内膜を用いたin vitro実験で、ダナゾールはアンドロゲンレセプター及びプロゲステロンレセプターに結合することが認められた11)。
18.5 子宮内膜への直接作用
ヒト子宮内膜細胞培養系を用いたin vitro実験で、ダナゾールは3H-thymidine取込みでみたDNA合成を抑制した12)。
19. 有効成分に関する理化学的知見
19.1. ダナゾール
22. 包装
100錠[10錠(PTP)×10]
23. 主要文献
- 田村昭蔵,他, 産婦人科の実際, 29 (12), 1193-1206, (1980)
- Lloyd-Jones JG,et al., J Int Med Res., 5 (Suppl.3), 18-24, (1977)
- 常磐知宣, 他, 応用薬理, 22 (4), 605-620, (1981)
- 杉本 修,他, 診療と新薬, 31 (9), 1520-1533, (1994)
- 水口弘司,他, 新薬と臨床, 43 (9), 1812-1825, (1994)
- Guillebaud J,et al., J Int Med Res., 5 (Suppl.3), 57-66, (1977)
- Potts G O,et al., Fertil Steril., 25 (4), 367-372, (1974) »PubMed
- Eldridge J C,et al., Biol Reprod., 10 (4), 438-446, (1974) »PubMed
- Barbieri R L,et al., Obstet Gynecol., 57 (6), 722-724, (1981) »PubMed
- Barbieri R L,et al., Fertil Steril., 28 (8), 809-813, (1977) »PubMed
- Tamaya T,et al., Fertil Steril., 41 (5), 732-735, (1984) »PubMed
- 武谷雄二,他, 産科と婦人科, 52 (8), 1363-1365, (1985)
24. 文献請求先及び問い合わせ先
文献請求先
田辺ファーマ株式会社
くすり相談センター
〒541-8505
大阪市中央区道修町3-2-10
電話:0120-753-280
製品情報問い合わせ先
田辺ファーマ株式会社
くすり相談センター
〒541-8505
大阪市中央区道修町3-2-10
電話:0120-753-280
26. 製造販売業者等
26.1 製造販売元
田辺ファーマ株式会社
大阪市中央区道修町3-2-10