医薬品情報
| 総称名 | ダルメート |
|---|---|
| 一般名 | フルラゼパム塩酸塩 |
| 欧文一般名 | Flurazepam Hydrochloride |
| 製剤名 | フルラゼパム塩酸塩カプセル |
| 薬効分類名 | 不眠症治療剤 |
| 薬効分類番号 | 1124 |
| ATCコード | N05CD01 |
| KEGG DRUG |
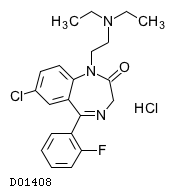
D01408
フルラゼパム塩酸塩
|
| KEGG DGROUP |
DG03202
睡眠薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年12月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ダルメートカプセル15 | Dalmate Capsules | 共和薬品工業 | 1124002M2022 | 6.3円/カプセル | 向精神薬(第三種), 習慣性医薬品, 処方箋医薬品 |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分又はベンゾジアゼピン系薬剤に対し過敏症の既往歴のある患者
2.2 急性閉塞隅角緑内障の患者(抗コリン作用により眼圧が上昇し、症状を悪化させることがある。)
2.3 重症筋無力症の患者(重症筋無力症の症状を悪化させるおそれがある。)
2.4 リトナビルを投与中の患者[10.1参照]
4. 効能または効果
○不眠症
○麻酔前投薬
6. 用法及び用量
通常成人1回、1〜2カプセルを就寝前または手術前に経口投与する。ただし、フルラゼパム塩酸塩として、10〜30mgとする。
なお、年齢・症状により、適宜増減する。
なお、年齢・症状により、適宜増減する。
7. 用法及び用量に関連する注意
<不眠症>
7.1 就寝の直前に服用させること。また、服用して就寝した後、睡眠途中において一時的に起床して仕事等をする可能性があるときは服用させないこと。
8. 重要な基本的注意
<効能共通>
8.1 本剤の影響が翌朝以後に及び、眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、自動車の運転等の危険を伴う機械の操作に従事させないよう注意すること。
8.2 連用により薬物依存を生じることがあるので、漫然とした継続投与による長期使用を避けること。本剤の投与を継続する場合には、治療上の必要性を十分に検討すること。[11.1.1参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 肺性心、肺気腫、気管支喘息及び脳血管障害の急性期等で呼吸機能が高度に低下している患者
治療上やむを得ないと判断される場合を除き、投与しないこと。また、少量から投与を開始するなど注意すること。炭酸ガスナルコーシスを起こしやすい。[11.1.2参照]
9.1.2 心障害のある患者
少量から投与を開始するなど注意すること。ジアゼパムで循環器への影響があらわれたとの報告がある。
9.1.3 脳に器質的障害のある患者
少量から投与を開始するなど注意すること。作用が強くあらわれるおそれがある。
9.1.4 衰弱患者
少量から投与を開始するなど注意すること。
9.2 腎機能障害患者
少量から投与を開始するなど注意すること。作用が強くあらわれるおそれがある。
9.3 肝機能障害患者
少量から投与を開始するなど注意すること。作用が強くあらわれるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.5.1 妊娠中に他のベンゾジアゼピン系薬剤(ジアゼパム、クロルジアゼポキシド等)の投与を受けた患者の中に奇形児等の障害児を出産した例が対照群と比較して有意に多いとの疫学的調査報告がある。
9.5.2 ベンゾジアゼピン系薬剤で新生児に哺乳困難、嘔吐、活動低下、筋緊張低下、過緊張、嗜眠、傾眠、呼吸抑制・無呼吸、チアノーゼ、易刺激性、神経過敏、振戦、低体温、頻脈等を起こすことが報告されている。なお、これらの症状は、離脱症状あるいは新生児仮死として報告される場合もある。また、ベンゾジアゼピン系薬剤で新生児に黄疸の増強を起こすことが報告されている。
9.5.3 分娩前に連用した場合、出産後新生児に離脱症状があらわれることが、ベンゾジアゼピン系薬剤で報告されている。
9.6 授乳婦
授乳を避けさせること。ヒト母乳中へ移行し、新生児に嗜眠、体重減少等を起こすことが他のベンゾジアゼピン系薬剤(ジアゼパム)で報告されている。また、黄疸を増強する可能性がある。
9.7 小児等
少量から投与を開始するなど注意すること。小児等を対象とした臨床試験は実施していない。
9.8 高齢者
少量から投与を開始するなど注意すること。運動失調等の副作用が発現しやすい。
10. 相互作用
10.1 併用禁忌
| リトナビル (ノービア) [2.4参照] | 過度の鎮静や呼吸抑制を起こすおそれがある。 | リトナビルのチトクロームP450に対する競合的阻害作用により、併用した場合、本剤の血中濃度が大幅に上昇することが予測される。 |
10.2 併用注意
| アルコール (飲酒) | 本剤の作用が増強・持続されることがある(服用した翌日の飲酒によっても発現する場合がある)。 アルコールとの併用は避けることが望ましい。 | 相加作用が発現することが考えられる。 |
| 中枢神経抑制剤 フェノチアジン誘導体 バルビツール酸誘導体 鎮痛薬 麻酔薬 等 | 相互に中枢作用を増強することがある。 | 相加作用が発現することが考えられる。 |
| モノアミン酸化酵素阻害剤 | 相互に中枢作用を増強することがある。 | 相加作用が発現することが考えられる。 |
| モノアミン酸化酵素阻害剤 | クロルジアゼポキシドで舞踏病が発現したとの報告がある。 | 機序は不明である。 |
| シメチジン | 本剤の作用が増強されることがある。 | シメチジンが肝チトクロームP450を阻害し、本剤の代謝を阻害するおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 依存性(頻度不明)
連用により薬物依存を生じることがあるので、観察を十分に行い、用量及び使用期間に注意し慎重に投与すること。また、連用中における投与量の急激な減少ないし投与中止により、痙攣発作、せん妄、振戦、不眠、不安、幻覚、妄想等の離脱症状があらわれることがあるので、投与を中止する場合には、徐々に減量するなど慎重に行うこと。[8.2参照]
11.1.2 呼吸抑制、炭酸ガスナルコーシス(いずれも頻度不明)
呼吸機能が高度に低下している患者に投与した場合、炭酸ガスナルコーシスを起こすことがあるので、このような場合には気道を確保し、換気を図るなど適切な処置を行うこと。[9.1.1参照]
11.1.3 一過性前向性健忘、もうろう状態(いずれも頻度不明)
本剤を投与する場合には少量から開始するなど、慎重に行うこと。なお、十分に覚醒しないまま、車の運転、食事等を行い、その出来事を記憶していないとの報告がある。
11.2 その他の副作用
| 0.5%以上 | 0.1〜0.5%未満 | 0.1%未満 | 頻度不明 | |
| 精神神経系 | 昼間の眠気(2.1%)、ふらつき(1.8%)、頭重 | 眩暈、頭痛、不安感 | 焦躁感 | |
| 循環器 | 動悸 | |||
| 肝臓 | 肝障害(ビリルビン、AST、ALTの上昇) | |||
| 消化器 | 口渇 | 悪心 | 下痢、腹痛、食欲不振、口の苦み、嘔吐、唾液分泌過多 | |
| 過敏症 | 発疹 | |||
| 骨格筋 | 倦怠感(1.1%) | |||
| その他 | 発汗 |
13. 過量投与
13.1 処置
本剤の過量投与が明白又は疑われた場合の処置としてフルマゼニル(ベンゾジアゼピン受容体拮抗剤)を投与する場合には、使用前にフルマゼニルの使用上の注意を必ず読むこと。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている。
15. その他の注意
15.1 臨床使用に基づく情報
投与した薬剤が特定されないままにフルマゼニル(ベンゾジアゼピン受容体拮抗剤)を投与された患者で、新たに本剤を投与する場合、本剤の鎮静・抗痙攣作用が変化、遅延するおそれがある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
16.4 代謝
尿中の主代謝物は、ハイドロキシエチル体で総排泄量の86%を占めた1)。
16.5 排泄
健常成人男子にフルラゼパム塩酸塩30mgを経口投与したとき、48時間までに投与量の32〜59%が大部分代謝物として尿中に排泄された1)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
18. 薬効薬理
18.1 作用機序
18.2 睡眠作用
18.3 ヒト終夜脳波試験
19. 有効成分に関する理化学的知見
19.1. フルラゼパム塩酸塩
20. 取扱い上の注意
アルミピロー又はガラス瓶開封後は湿気を避けて遮光して保存すること。
22. 包装
100カプセル[10カプセル(PTP)×10]
1000カプセル[瓶、バラ]
23. 主要文献
- 長谷川護,他, 薬理と治療, 1 (3), 56-64, (1973)
- Eckert,M.,et al., Drugs Exptl.Clin.Res., 9 (1), 77-84, (1983)
- 社内資料:臨床試験
- 木村政資,他, 医学のあゆみ, 89 (3), 118-138, (1974)
- 橘直矢,他, 医学のあゆみ, 87 (12), 640-654, (1973)
- 伊東和人,他, 薬理と治療, 1 (3), 217-236, (1973)
- 中村圭二,他, ファルマシアレビュー, 10, 85-99, (1983)
- Mohler,H.,et al., The Benzodiazepines,ed.by Costa,E., 93-115, (1983), (Raven Press.,New York.)
- 君島健次郎,他, 米子医学雑誌, 23 (1), 63-72, (1972)
- 橋本惟,他, 応用薬理, 7 (3), 381-398, (1973)
- Kales,A.,et al., Arch.Gen.Psychiat., 23, 219-225, (1970) »PubMed
- 石山陽事,他, 臨床脳波, 15, 625-632, (1973)
24. 文献請求先及び問い合わせ先
文献請求先
共和薬品工業株式会社
お問い合わせ窓口
〒530-0005
大阪市北区中之島3-2-4
電話:0120-041-189
FAX:06-6121-2858
製品情報問い合わせ先
共和薬品工業株式会社
お問い合わせ窓口
〒530-0005
大阪市北区中之島3-2-4
電話:0120-041-189
FAX:06-6121-2858
25. 保険給付上の注意
本剤は厚生労働省告示第75号(平成24年3月5日付)に基づき、1回30日分を限度として投薬する。
26. 製造販売業者等
26.1 製造販売元
共和薬品工業株式会社
大阪市北区中之島3-2-4