医薬品情報
| 総称名 | ミネラミック |
|---|---|
| 一般名 | 塩化第二鉄 塩化マンガン 硫酸亜鉛水和物 硫酸銅 ヨウ化カリウム |
| 薬効分類名 | 高カロリー輸液用微量元素製剤 |
| 薬効分類番号 | 3229 |
| KEGG DRUG |
D04956
塩化第二鉄・塩化マンガン・硫酸亜鉛水和物・硫酸銅・ヨウ化カリウム
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年11月 改訂(第3版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ミネラミック注 | MINERAMIC INJECTION | 東和薬品 | 3229501A1078 | 94円/管 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤又は本剤配合成分に過敏症の既往歴のある患者
2.2 胆道閉塞のある患者[排泄障害により、マンガンの全血中濃度、及び銅などの微量元素の血漿中濃度を上昇させるおそれがある。][8.2参照]
4. 効能または効果
経口、経腸管栄養補給が不能又は不十分で高カロリー静脈栄養に頼らざるを得ない場合の亜鉛、鉄、銅、マンガン及びヨウ素の補給
6. 用法及び用量
通常、成人には1日2mLを高カロリー静脈栄養輸液に添加し、点滴静注する。
なお、年齢、症状に応じて適宜増減する。
なお、年齢、症状に応じて適宜増減する。
7. 用法及び用量に関連する注意
高カロリー輸液用基本液等には微量元素が含まれた製剤があるので、それらの微量元素量に応じて適宜減量すること。
8. 重要な基本的注意
8.1 本剤を長期連用する場合には、以下の点に注意すること。[8.2参照]
・臨床症状の推移を十分観察したうえで、慎重に投与すること。また、必要に応じ、マンガンの全血中濃度及びその他の微量元素の血漿中濃度を測定することが望ましい。
・特にマンガンについては、マンガン20μmol配合微量元素製剤※の投与により全血中濃度の上昇がみられたり、脳内蓄積によって脳MRI検査(T1強調画像)で高信号を示したり、パーキンソン様症状があらわれたとの報告がある。このような所見がみられた場合には、休薬、減量もしくは投与中止等を考慮すること。
※)マンガン20μmol、鉄35μmol、亜鉛60μmol、銅5μmol、ヨウ素1μmol配合製剤
9. 特定の背景を有する患者に関する注意
9.2 腎機能障害患者
微量元素の血漿・全血中濃度を上昇させるおそれがある。
9.3 肝機能障害患者
微量元素の血漿・全血中濃度を上昇させるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
11. 副作用
11.2 その他の副作用
| 頻度不明 | |
| 過敏症 | 発疹 |
| 肝臓 | 肝機能異常(AST上昇、ALT上昇、Al-P上昇等)、ビリルビン上昇 |
| 精神神経系 | パーキンソン様症状 |
| その他 | 血中マンガン上昇 |
16. 薬物動態
16.3 分布
16.5 排泄
各放射性元素(65Zn、54Mn、64Cu、125I、59Fe)を含むマンガン20μmol配合微量元素製剤※をラットに静脈内投与した時、主な排泄経路は、ヨウ素は尿中、他の元素は糞中であった。3)
※)マンガン20μmol、鉄35μmol、亜鉛60μmol、銅5μmol、ヨウ素1μmol配合製剤
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験(一般臨床成績)
マンガン20μmol配合微量元素製剤※を用いた臨床試験成績は次のとおりである。
高カロリー輸液法による栄養補給を2週間以上行った食道癌、胃癌等の患者180例に対し、微量元素製剤を2〜4週間高カロリー輸液剤に添加して投与した。血漿中微量元素濃度の基準濃度範囲内維持効果により評価した結果、有効率は78.3%(141/180例)であった。副作用は微量元素製剤との因果関係は明らかではないが、1例の好酸球増多が認められた。5)
17.1.2 国内第III相試験(長期臨床試験)
マンガン20μmol配合微量元素製剤※を用いた臨床試験成績は次のとおりである。
高カロリー輸液法による栄養補給を8週間以上行ったクローン病、短腸症候群、食道癌等の患者19例に対し、最初の4週間を微量元素無投与期間とし、その後4〜8週間微量元素製剤を高カロリー輸液剤に添加して投与した。その結果、微量元素無投与時での血漿中微量元素の低下傾向が微量元素製剤投与により基準値内に回復、維持されることが明らかとなった。微量元素製剤の有効率は89.5%(17/19例)で、副作用は認められなかった。6)
※)マンガン20μmol、鉄35μmol、亜鉛60μmol、銅5μmol、ヨウ素1μmol配合製剤
17.2 製造販売後調査等
17.2.1 特別調査(長期:1年以上)
マンガン1μmol配合微量元素製剤を投与されている在宅中心静脈栄養法施行中の患者20症例について血中の微量元素濃度を調査した。1年以上(最長2年4ヵ月)の投与患者において、全血中のマンガン濃度、血清中の鉄、亜鉛及び銅濃度の平均値が基準濃度範囲内に維持されていた症例の割合は、マンガン:78.9%(15/19例)、鉄:68.4%(13/19例)、亜鉛:81.8%(9/11例)、銅:89.5%(17/19例)であった。
また、本調査において全血中マンガン濃度は長期間の投与でも上昇する傾向は認められなかった。7)
また、本調査において全血中マンガン濃度は長期間の投与でも上昇する傾向は認められなかった。7)
17.2.2 特別調査(長期:1ヵ月以上)
1ヵ月以上の長期にわたりマンガン1μmol配合微量元素製剤が投与される高カロリー静脈栄養輸液療法の患者を対象とし、長期投与における有効性を調査した結果、有効率は99.3%(266/268例)であった。8)
18. 薬効薬理
18.1 作用機序
本剤は亜鉛、鉄、銅、マンガン及びヨウ素を含有し、高カロリー静脈栄養輸液に添加して微量元素を補給する。
18.2 微量元素補給効果
微量元素欠乏ラット及び正常ラットに、1週間、マンガン20μmol配合微量元素製剤※を添加した高カロリー輸液施行群と微量元素製剤を添加しない高カロリー輸液施行群における微量元素製剤の補給効果を比較検討した。その結果、微量元素製剤を添加しない群では血漿あるいは組織中の微量元素濃度は低下し、また微量元素欠乏に基づくと考えられる貧血症状、アルカリフォスファターゼ活性の低下、トリヨードチロニン及びチロキシン濃度の低下などが認められたが、微量元素製剤を添加した群ではこれらの変化は正常レベルに回復あるいは回復する傾向が認められた。9)
※)マンガン20μmol、鉄35μmol、亜鉛60μmol、銅5μmol、ヨウ素1μmol配合製剤
19. 有効成分に関する理化学的知見
19.1. 塩化第二鉄
| 一般的名称 | 塩化第二鉄 |
|---|---|
| 分子式 | FeCl3・6H2O |
| 分子量 | 270.30 |
| 物理化学的性状 | 黄褐色の結晶又は塊である。水に極めて溶けやすく、エタノール(95)又はジエチルエーテルにやや溶けやすい。湿気によって潮解する。 |
| 理化学知見その他 | 19.1 塩化第二鉄 |
| KEGG DRUG |
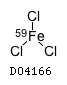
|
19.2. 塩化マンガン
| 一般的名称 | 塩化マンガン |
|---|---|
| 分子式 | MnCl2・4H2O |
| 分子量 | 197.91 |
| 物理化学的性状 | 淡紅色の結晶又は結晶性の粉末である。水に極めて溶けやすく、エタノール(95)にやや溶けやすい。吸湿性である。 |
| 理化学知見その他 | 19.2 塩化マンガン |
| KEGG DRUG |
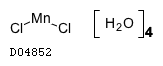
|
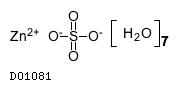
19.3. 硫酸亜鉛水和物
| 一般的名称 | 硫酸亜鉛水和物 |
|---|---|
| 分子式 | ZnSO4・7H2O |
| 分子量 | 287.55 |
| 物理化学的性状 | 無色の結晶又は白色の結晶性の粉末である。水に極めて溶けやすく、エタノール(99.5)に極めて溶けにくい。乾燥空気中で風解する。 |
| 理化学知見その他 | 19.3 硫酸亜鉛水和物 |
| KEGG DRUG |
|
19.4. 硫酸銅
| 一般的名称 | 硫酸銅 |
|---|---|
| 分子式 | CuSO4・5H2O |
| 分子量 | 249.69 |
| 物理化学的性状 | 青色の結晶もしくは粒又は濃青色の粉末である。水に溶けやすく、エタノール(95)にほとんど溶けない。乾燥した空気中で徐々に風解する。グリセリンに徐々に溶ける。 |
| 理化学知見その他 | 19.4 硫酸銅 |
| KEGG DRUG |
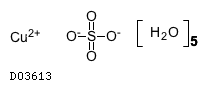
|
19.5. ヨウ化カリウム
20. 取扱い上の注意
20.1 外箱開封後は遮光して保存すること。
20.2 光により濁る場合があるので、液の性状を観察し、液の澄明でないものは使用しないこと。
22. 包装
2mL×50管
23. 主要文献
- 寺島建樹,他, Biomed Res Trace Elements., 5 (3), 265-266, (1994)
- 寺島建樹,他, JJPEN., 10 (3), 369-372, (1988)
- 北川泰久,他, JJPEN, 9 (6), 898-900, (1987)
- 松田晃彦,他, 日本衛生学雑誌, 44 (4), 887-893, (1989) »DOI
- 岡田 正,他, 薬理と治療, 17 (7), 3675-3690, (1989)
- 岡田 正,他, 薬理と治療, 17 (7), 3655-3673, (1989)
- 永濱 忍,他, 診療と新薬, 41 (12), 1213-1220, (2004)
- 永濱 忍,他, 診療と新薬, 44 (1), 3-12, (2007)
- 横井克彦,他, 日本衛生学雑誌, 44 (4), 831-838, (1989) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
東和薬品株式会社
学術部DIセンター
〒570-0081
大阪府守口市日吉町2丁目5番15号
電話:0120-108-932
FAX:06-7177-7379
製品情報問い合わせ先
東和薬品株式会社
学術部DIセンター
〒570-0081
大阪府守口市日吉町2丁目5番15号
電話:0120-108-932
FAX:06-7177-7379
26. 製造販売業者等
26.1 製造販売元
東和薬品株式会社
大阪府門真市新橋町2番11号