医薬品情報
| 総称名 | ロイコン |
|---|---|
| 一般名 | アデニン |
| 欧文一般名 | Adenine |
| 製剤名 | アデニン錠 |
| 薬効分類名 | 白血球減少症治療剤 |
| 薬効分類番号 | 4191 |
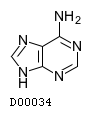
| KEGG DRUG |
D00034
アデニン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年10月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ロイコン錠10mg | LEUCON TABLETS 10mg | 大原薬品工業 | 4191001F1037 | 6.3円/錠 |
2. 禁忌
次の患者には投与しないこと
2.1 痛風、尿路結石のある患者[症状を悪化させることがある。]
2.2 本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
放射線曝射ないし薬物による白血球減少症
6. 用法及び用量
アデニンとして、通常成人1日20〜60mgを経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 高尿酸血症の患者
症状を悪化させることがある。[11.1.1参照]
9.2 腎機能障害患者
排泄障害により副作用があらわれることがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。妊娠(10日目)マウスに腹腔内投与した実験で、胎仔死亡、成長抑制及び前頭脳ヘルニア、口蓋裂、兎唇、前肢欠損、尾欠損等の奇形が認められている1)。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.8 高齢者
少量から投与を開始するなど慎重に投与すること。一般に生理機能が低下している。
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなどの適切な処置を行うこと。
11.1.2 急性腎障害(頻度不明)[8.1参照]
11.1.3 尿路結石(頻度不明)[8.1参照]
11.2 その他の副作用
| 頻度不明 | |
| 過敏症 | 発疹、そう痒感 |
| 消化器 | 便秘 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
17. 臨床成績
17.1 有効性及び安全性に関する試験
本剤の臨床試験は、悪性腫瘍の放射線療法及び化学療法時に起こる白血球減少症を対象に実施され、本剤投与前後の白血球数の変動について検討された結果、おおむね1週〜1ヵ月の投与で白血球数の増加による治療効果が認められた。
18. 薬効薬理
18.1 作用機序
14C標識アデニンによるin vitro実験(ウサギ)において、アデニンは骨髄細胞のRNA、DNAによくとりこまれ、核酸合成に利用される2)。
18.2 実験的白血球減少症に対する作用
18.3 実験的放射線障害防禦作用
放射線照射に対する防禦作用及び白血球減少の抑制ならびに回復促進効果が認められる(マウス)8)(in vivo)。
19. 有効成分に関する理化学的知見
19.1. アデニン
22. 包装
(PTP)
100錠(10錠×10)
1,000錠(10錠×100)
(バラ)
1,000錠
23. 主要文献
- Fujii T., et al., Okajimas Folia anat.Jpn., 49 (1), 47-53, (1972) »PubMed
- 中村 徹他, 日本血液学会雑誌, 25 (3-4), 490-491, (1962)
- 稲津佳彦他, 高峰研究所年報, 11, 162-175, (1959)
- 岡本良平他, 京都府立医科大学雑誌, 69, 505-510, (1961)
- 北川司良他, 外科の領域, 9, 290-296, (1961)
- Lecoq R., Int.Z.Vitaminforsch Beih., 27 (3), 291-300, (1957) »PubMed
- Paolino W., et al., Panminerva Med., 2, 5-8, (1960) »PubMed
- 宮崎 亨他, 和歌山医学, 13 (3-4), 107-112, (1962)
24. 文献請求先及び問い合わせ先
文献請求先
大原薬品工業株式会社
お客様相談室
〒104-6591
東京都中央区明石町8-1 聖路加タワー36階
電話:0120-419-363
FAX:03-6740-7702
製品情報問い合わせ先
大原薬品工業株式会社
お客様相談室
〒104-6591
東京都中央区明石町8-1 聖路加タワー36階
電話:0120-419-363
FAX:03-6740-7702
26. 製造販売業者等
26.1 製造販売元
大原薬品工業株式会社
滋賀県甲賀市甲賀町鳥居野121-15