医薬品情報
| 総称名 | ニトロール |
|---|---|
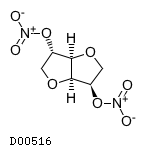
| 一般名 | 硝酸イソソルビド |
| 欧文一般名 | Isosorbide Dinitrate |
| 薬効分類名 | 虚血性心疾患治療剤 |
| 薬効分類番号 | 2171 |
| ATCコード | C01DA08 |
| KEGG DRUG |
D00516
硝酸イソソルビド
|
| KEGG DGROUP |
DG01270
硝酸イソソルビド
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年9月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ニトロール錠5mg | Nitorol tablets | エーザイ | 2171016F1082 | 10.8円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 重篤な低血圧又は心原性ショックのある患者[血管拡張作用によりさらに血圧を低下させ、症状を悪化させるおそれがある。][9.1.1参照]
2.2 閉塞隅角緑内障の患者[眼圧を上昇させるおそれがある。]
2.3 頭部外傷又は脳出血のある患者[頭蓋内圧を上昇させるおそれがある。]
2.4 高度な貧血のある患者[血圧低下により貧血症状(めまい、立ちくらみ等)を悪化させるおそれがある。]
2.5 硝酸・亜硝酸エステル系薬剤に対し過敏症の既往歴のある患者
2.6 ホスホジエステラーゼ5阻害作用を有する薬剤(シルデナフィルクエン酸塩、バルデナフィル塩酸塩水和物、タダラフィル)又はグアニル酸シクラーゼ刺激作用を有する薬剤(リオシグアト)を投与中の患者[10.1参照]
4. 効能または効果
6. 用法及び用量
<経口>
通常成人は、1回1〜2錠(硝酸イソソルビドとして1回5〜10mg)を1日3〜4回経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
<舌下>
狭心発作時には、通常成人1回1〜2錠(硝酸イソソルビドとして1回5〜10mg)を舌下投与する。
狭心発作時以外には、通常成人1回1〜2錠(硝酸イソソルビドとして5〜10mg)を1日3〜4回舌下投与する。
なお、年齢、症状により適宜増減する。
狭心発作時以外には、通常成人1回1〜2錠(硝酸イソソルビドとして5〜10mg)を1日3〜4回舌下投与する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
8.1 過度の血圧低下が起こった場合には、本剤の投与を中止し下肢の挙上あるいは昇圧剤の投与等、適切な処置を行うこと。
8.2 起立性低血圧を起こすことがあるので注意すること。
8.3 本剤の投与開始時には、他の硝酸・亜硝酸エステル系薬剤と同様に血管拡張作用による頭痛等の副作用が起こりやすく、これらの副作用のために注意力・集中力・反射運動能力等の低下が起こることがあるので、このような場合には、自動車の運転等の危険を伴う機械の操作に従事させないように注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 低血圧の患者(重篤な低血圧のある患者を除く)
血管拡張作用により、さらに血圧を低下させるおそれがある。[2.1参照]
9.1.2 心筋梗塞の急性期の患者
血圧を低下させるおそれがある。
9.1.3 原発性肺高血圧症の患者
心拍出量が低下し、ショックを起こすことがある。
9.1.4 肥大型閉塞性心筋症の患者
心室内圧較差の増強をもたらし、症状を悪化させるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
本剤は、主として肝臓で代謝されるが、一般に肝機能が低下していることが多いため、高い血中濃度が持続するおそれがある。
10. 相互作用
10.1 併用禁忌
| ホスホジエステラーゼ5阻害作用を有する薬剤 シルデナフィルクエン酸塩 (バイアグラ、レバチオ) バルデナフィル塩酸塩水和物 (レビトラ) タダラフィル (シアリス、アドシルカ、ザルティア) [2.6参照] | 併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 | 本剤はcGMPの産生を促進し、一方、ホスホジエステラーゼ5阻害作用を有する薬剤はcGMPの分解を抑制することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
| グアニル酸シクラーゼ刺激作用を有する薬剤 リオシグアト (アデムパス) [2.6参照] | 併用により、降圧作用を増強することがあるので、本剤投与前にこれらの薬剤を服用していないことを十分確認すること。また、本剤投与中及び投与後においてこれらの薬剤を服用しないよう十分注意すること。 | 本剤とグアニル酸シクラーゼ刺激作用を有する薬剤は、ともにcGMPの産生を促進することから、両剤の併用によりcGMPの増大を介する本剤の降圧作用が増強する。 |
10.2 併用注意
| アルコール | 血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 | 血管拡張作用が増強される。 |
| 利尿剤 | 血圧低下等が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 | 血圧低下作用を増強させる。 |
| 血管拡張剤 硝酸・亜硝酸エステル系薬剤 | 頭痛、血圧低下等の副作用が増強されるおそれがある。過度の血圧低下が起こった場合には、減量又は投与を中止し、必要に応じて昇圧剤投与等の適切な処置を行うこと。 | 血管拡張作用が増強される。 |
11. 副作用
11.2 その他の副作用
| 5%以上 | 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 循環器 | めまい、血圧低下、潮紅、動悸 | 熱感、失神 | ||
| 精神神経系 | 頭痛 | 脱力感 | 不快感 | |
| 過敏症 | 発疹 | |||
| 消化器 | 悪心・嘔吐、胃部不快感、食欲不振 | |||
| 肝臓 | AST、ALTの上昇等 |
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 本剤は、無包装開放状態で含量の低下が認められているので、自動分包機内での保存は避けること。また、長期の分包処方は避けること。
14.1.2 分包後は、なるべく涼しいところで保管するよう注意すること。
14.2 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 本剤使用中に本剤又は他の硝酸・亜硝酸エステル系薬剤に対し耐薬性を生じ、作用が減弱することがある。
なお、類似化合物(ニトログリセリン)の経皮吸収型製剤での労作狭心症に対するコントロールされた外国の臨床試験成績によると、休薬時間を置くことにより、耐薬性が軽減できたとの報告がある。
なお、類似化合物(ニトログリセリン)の経皮吸収型製剤での労作狭心症に対するコントロールされた外国の臨床試験成績によると、休薬時間を置くことにより、耐薬性が軽減できたとの報告がある。
15.1.2 硝酸イソソルビド製剤の投与によって、メトヘモグロビン血症があらわれたとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男子5名に本剤1錠(硝酸イソソルビドとして5mg)を経口投与した際、投与後25.6分に最高血漿中濃度(Cmax=5.8ng/mL)を示した。その後血漿中硝酸イソソルビド濃度は2相性を示し、消失半減期は18.2分(α相)、93.5分(β相)であった。投与6時間後の血漿中濃度は0.07ng/mLであった。なお、AUC(0→∞)は7.5ng・hr/mLであった。
ニトロール錠5mg経口投与後の血漿中硝酸イソソルビド濃度
| Cmax(ng/mL) | tmax(min) | AUC(ng・hr/mL) | t1/2α(min) | t1/2β(min) |
| 5.8±0.7 | 25.6±4.9 | 7.5±1.3 | 18.2±1.4 | 93.5±20.0 |
健康成人男子12名に本剤1錠(硝酸イソソルビドとして5mg)を舌下投与した際、投与後18.2分に最高血漿中濃度(Cmax=35.7ng/mL)に達した。その後血漿中濃度は2相性を示し、消失半減期は7.5分(α相)、55.2分(β相)であった。なお、AUC(0→∞)は21.0ng・hr/mLであった1)。
ニトロール錠5mg舌下投与後の血漿中硝酸イソソルビド濃度
| Cmax(ng/mL) | tmax(min) | AUC(ng・hr/mL) | t1/2α(min) | t1/2β(min) |
| 35.7±6.4 | 18.2±3.2 | 21.0±2.7 | 7.5 | 55.2 |
16.5 排泄
本剤1錠(硝酸イソソルビドとして5mg)を5名の健康成人に経口投与した場合、投与後48時間迄の尿中排泄量は遊離型2-一硝酸イソソルビド及び遊離型5-一硝酸イソソルビドとしてそれぞれ0.23%、4.02%、それらのグルクロン酸抱合体として0.47%、10.03%であった。
17. 臨床成績
17.1 有効性及び安全性に関する試験
18. 薬効薬理
18.1 作用機序
18.2 前負荷、後負荷の軽減作用
18.3 冠血管拡張作用
麻酔イヌによる実験で、本薬は比較的太い冠動脈(conductive vessel)を拡張し、冠血管抵抗を減少させるとともに側副血行路も拡張し、冠血流量の増加は軽微であるが、虚血部心筋、特に内膜下層心筋への血流供給の再配分をうながして、心筋の酸素供給を増加することが認められている9)。
18.4 cGMP産生作用
KClであらかじめ、収縮させた子ウシの摘出冠動脈に本薬を添加すると、冠動脈の弛緩作用に比例してcGMPの産生が増加する10)。
19. 有効成分に関する理化学的知見
19.1. 硝酸イソソルビド
20. 取扱い上の注意
20.1 温度、湿度の高いところに長期間保存すると錠剤表面に結晶が析出することがある。
22. 包装
100錠[10錠(PTP)×10]、1,000錠[10錠(PTP)×100]
23. 主要文献
- 深見健一ら, 臨床薬理, 18 (3), 515-522, (1987) »DOI
- 塩田憲三ら, 総合臨床, 13 (12), 2365-2373, (1964)
- 森博愛ら, 臨牀と研究, 41 (10), 1847-1851, (1964)
- 原岡昭一ら, 診療, 18 (4), 521-525, (1965)
- Kukovetz W.R., Cardiology,, 74 (S.1), 12-19, (1987)
- 高田 芳伸ら, 薬局, 42 (7), 937-944, (1991)
- 平川千里ら, 最新医学, 29 (1), 170-176, (1974)
- Wendt R.L., J.Pharmacol.Exp.Ther., 180 (3), 732-742, (1972) »PubMed
- 高山幸男ら, 脈管学, 21 (5), 351-357, (1981)
- Matlib M.A.et al., Am.Heart J., 110 (1), 204-212, (1985)
24. 文献請求先及び問い合わせ先
文献請求先
エーザイ株式会社
hhcホットライン
〒112-8088
東京都文京区小石川4-6-10
電話:フリーダイヤル 0120-419-497
製品情報問い合わせ先
エーザイ株式会社
hhcホットライン
〒112-8088
東京都文京区小石川4-6-10
電話:フリーダイヤル 0120-419-497
26. 製造販売業者等
26.1 製造販売元
エーザイ株式会社
東京都文京区小石川4-6-10