医薬品情報
| 総称名 | ゼフナート |
|---|---|
| 一般名 | リラナフタート |
| 欧文一般名 | Liranaftate |
| 製剤名 | リラナフタート(Liranaftate)製剤 |
| 薬効分類名 | 抗真菌薬 |
| 薬効分類番号 | 2659 |
| ATCコード | D01AE25 |
| KEGG DRUG |
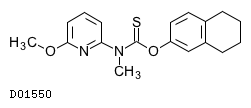
D01550
リラナフタート
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年8月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ゼフナートクリーム2% | ZEFNART CREAM 2% | 全薬工業 | 2659712N1020 | 22.7円/g | |
| ゼフナート外用液2% | ZEFNART SOLUTION 2% | 全薬工業 | 2659712Q1026 | 22.7円/mL |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対して過敏症の既往歴のある患者
2.2 他の外用抗真菌剤に対して過敏症の既往歴のある患者
2.3 臨床所見上皮膚カンジダ症あるいは汗疱、掌蹠膿疱症、膿皮症、他の皮膚炎等との鑑別が困難な患者[本剤は白癬菌以外に対して効果が期待できず、状態悪化のおそれがあるため]
4. 効能または効果
6. 用法及び用量
1日1回患部に塗布する。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
11. 副作用
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | |
| 皮膚 | 接触性皮膚炎、そう痒症、発赤、紅斑、刺激感、疼痛、小水疱性皮疹 | 皮膚炎、自家感作性皮膚炎、潮紅 |
14. 適用上の注意
14.1 薬剤投与時の注意
<製剤共通>
14.1.1 眼科用として角膜、結膜には使用しないこと。
14.1.2 著しいびらん面には使用しないこと。
14.1.3 誤って眼に入った場合は、直ちに大量の水で洗った後、専門医の処置をうけること。
<外用液>
14.1.4 刺激を生じることがあるので、亀裂、びらん面には注意して使用すること。
16. 薬物動態
16.2 吸収
健康成人の背部皮膚にゼフナートクリーム2% 5gを単回又は7日間塗布し、未変化体をガスクロマトグラフ法により経時的に測定(検出限界:1ng/mL)した結果、単回塗布では、塗布後336時間までの血漿中、尿中に検出されなかった。
7日間塗布においても同様であった1)。
7日間塗布においても同様であった1)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 前期臨床第II相試験
足白癬、体部白癬、股部白癬に対して本剤(クリーム剤)を1日1回塗布した前期臨床第II相試験の結果は以下のとおりであった2)。
| 疾患名 | 有効率(%) | 有効例数/評価例数 |
| 足白癬 | 76.4 | 55/72 |
| 体部白癬 | 94.7 | 18/19 |
| 股部白癬 | 95.0 | 19/20 |
安全性評価症例122例(足79例、体部21例、股部22例)のうち、副作用は2例(1.6%)に認められた。発現した副作用はいずれも接触性皮膚炎であった。
17.1.2 後期臨床第II相試験
足白癬、体部白癬、股部白癬に対して本剤(クリーム剤)を1日1回塗布した後期臨床第II相試験(無作為化並行用量反応試験)の結果は以下のとおりであった3)。
| 疾患名 | 有効率(%) | 有効例数/評価例数 |
| 足白癬 | 80.4 | 86/107 |
| 体部白癬 | 94.1 | 48/51 |
| 股部白癬 | 95.0 | 38/40 |
安全性評価症例254例(足134例、体部64例、股部56例)のうち、副作用は4例(1.6%)に認められた。発現した副作用は接触性皮膚炎1例(0.4%)、皮膚炎1例(0.4%)、刺激感1例(0.4%)、発赤・掻痒1例(0.4%)であった。
17.1.3 臨床第III相比較試験
足白癬、体部白癬、股部白癬に対して本剤(クリーム剤)または対照薬(ビホナゾール)を1日1回塗布した二重盲検無作為化比較試験の結果は以下のとおりであり、両群に統計学的な有意差はなかった4)。
| 疾患名 | リラナフタート群 | 対照薬群 | ||
| 有効率(%) | 有効例数/評価例数 | 有効率(%) | 有効例数/評価例数 | |
| 足白癬 | 81.0 | 115/142 | 80.6 | 112/139 |
| 体部白癬 | 85.3 | 64/75 | 81.6 | 62/76 |
| 股部白癬 | 89.8 | 53/59 | 97.0 | 65/67 |
リラナフタート群の安全性評価症例319例(足172例、体部81例、股部66例)のうち、副作用は5例(1.6%)に認められ、主な副作用は接触性皮膚炎3例(0.9%)であった。
17.1.4 臨床第III相試験(一般臨床試験)
足白癬、体部白癬、股部白癬に対して本剤(クリーム剤)を1日1回塗布した第III相一般臨床試験の結果は以下のとおりであった5)。
| 疾患名 | 有効率(%) | 有効例数/評価例数 |
| 足白癬 | 68.6 | 94/137 |
| 体部白癬 | 85.2 | 52/61 |
| 股部白癬 | 94.1 | 32/34 |
安全性評価症例299例(足183例、体部73例、股部43例)のうち、副作用は3例(1.0%)に認められた。発現した副作用はいずれも接触性皮膚炎であった。
17.1.5 臨床第III相試験(一般臨床試験)
足白癬、体部白癬、股部白癬に対して本剤(クリーム剤)を1日1回塗布した第III相一般臨床試験の結果は以下のとおりであった6)。
| 疾患名 | 有効率(%) | 有効例数/評価例数 |
| 足白癬 | 78.9 | 75/95 |
| 体部白癬 | 85.7 | 48/56 |
| 股部白癬 | 97.5 | 39/40 |
安全性評価症例240例(足126例、体部63例、股部51例)のうち、副作用は7例(2.9%)に認められ、主な副作用は接触性皮膚炎4例(1.7%)であった。
17.1.6 臨床第III相比較試験
股部白癬に対して本剤(クリーム剤)または対照薬(ビホナゾール)を1日1回塗布した二重盲検無作為化比較試験の結果は以下のとおりであった7)。
| 疾患名 | リラナフタート群 | 対照薬群 | ||
| 有効率(%) | 有効例数/評価例数 | 有効率(%) | 有効例数/評価例数 | |
| 股部白癬 | 98.7 | 76/77 | 91.3 | 84/92 |
| p値 | 0.041(Fisher検定) | |||
リラナフタート群の安全性評価症例115例のうち、副作用は6例(5.2%)に認められ、主な副作用は接触性皮膚炎3例(2.6%)であった。
17.1.7 臨床第III相比較試験(クリーム剤/液剤)
足白癬に対して本剤(クリーム剤又は液剤)を1日1回塗布し、液剤のクリーム剤に対する非劣性を確認した非盲検群間比較試験の結果は以下のとおりであった8)。
| 疾患名 | クリーム剤 | 液剤 | ||
| 有効率(%) | 有効例数/評価例数 | 有効率(%) | 有効例数/評価例数 | |
| 足白癬 | 94.9 | 130/137 | 97.0 | 131/135 |
安全性評価症例290例のうち、副作用は7例(2.4%)に認められ、主な副作用は接触性皮膚炎3例(1.0%)、紅斑3例(1.0%)であった。
18. 薬効薬理
18.1 作用機序
リラナフタートは真菌細胞のスクワレン・エポキシ化反応を阻害し、細胞膜構成成分であるエルゴステロールの生合成阻害により抗真菌作用を発揮する9)。
18.2 抗真菌作用
18.2.1 リラナフタートは、皮膚糸状菌(Trichophyton属、Microsporum属、Epidermophyton属)に対して強い抗真菌作用を有し、黒色真菌、二形性真菌及びその他の糸状菌に対しても抗真菌作用を示した10)11)。
18.2.2 リラナフタートの主な皮膚糸状菌の新鮮臨床分離株に対するMIC値は下表のとおりであり、優れた抗真菌作用を示した10)11)。
| 菌種(株数) | MIC(MIC90)†(μg/mL) |
| Trichophyton rubrum(57) | 0.009〜0.078(0.078) |
| Trichophyton mentagrophytes(23) | 0.004〜0.078(0.039) |
| Trichophyton tonsurans(2) | 0.019,0.039 |
| Microsporum canis(18) | 0.009〜0.078(0.019) |
| Epidermophyton floccosum(14) | 0.009〜0.156(0.039) |
18.2.4 T.mentagrophytesによるモルモット実験的白癬モデルにおいて、感染3日前にリラナフタートを塗布した場合、発症を認めなかった13)。
18.2.5 リラナフタートは、T.mentagrophytesに対し、1ng/mLで菌糸の発育を阻害し、1μg/mLで細胞壁の剥離、細胞膜の破壊を示した14)。
18.2.6 リラナフタートは、T.mentagrophytesに対して、耐性を発現しなかった15)。
19. 有効成分に関する理化学的知見
19.1. リラナフタート
20. 取扱い上の注意
<製剤共通>
20.1 小児の手の届かない所に保管すること。
<外用液>
20.2 合成樹脂を軟化したり、塗料を溶かしたりすることがあるので注意すること。
20.3 火気を避けて保管すること。
22. 包装
<ゼフナートクリーム2%>
チューブ[10g×10、10g×50]
<ゼフナート外用液2%>
ガラス瓶[10mL×10]
23. 主要文献
- 伊藤正俊 ほか, 薬理と治療, 20, 4501-4508, (1992)
- 高橋 久 ほか, 薬理と治療, 20, 4759-4768, (1992)
- 高橋 久 ほか, 西日本皮膚科, 55, 735-746, (1993) »DOI
- 高橋 久 ほか, 西日本皮膚科, 55, 747-758, (1993) »DOI
- 高橋 久 ほか, 西日本皮膚科, 55, 759-770, (1993) »DOI
- 高橋 久 ほか, 薬理と治療, 21, 3273-3286, (1993)
- 高橋 久 ほか, 西日本皮膚科, 62, 788-802, (2000) »DOI
- 種田明生 ほか, 西日本皮膚科, 69, 300-308, (2007) »DOI
- Morita T,et al., J.Med.Veter.Mycol., 27, 17-25, (1989) »PubMed
- Iwata K,et al., Antimicrob.Agents Chemother., 33, 2118-2125, (1989) »PubMed
- 奥 幸夫 ほか, 日本医真菌学会雑誌, 34, 185-192, (1993) »DOI
- 井上恒男 ほか, 日本医真菌学会雑誌, 34, 193-197, (1993) »DOI
- 川手 喬 ほか, 全薬工業研究報告「M-732の抗真菌活性に関する研究-実験的白癬菌感染に対する予防効果の検討」[未発表]
- Osumi M,et al., Chemotherapy., 41, 555-567, (1993) »DOI
- Iwata K,et al., Chemotherapy., 38, 435-443, (1990) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
鳥居薬品株式会社
お客様相談室
〒103-8439
東京都中央区日本橋本町3-4-1
電話:0120-316-834
FAX:03-3231-6890
製品情報問い合わせ先
鳥居薬品株式会社
お客様相談室
〒103-8439
東京都中央区日本橋本町3-4-1
電話:0120-316-834
FAX:03-3231-6890
26. 製造販売業者等
26.1 製造販売元
全薬工業株式会社
東京都文京区大塚5-6-15
26.2 販売元
鳥居薬品株式会社
東京都中央区日本橋本町3-4-1