医薬品情報
| 総称名 | ネオレスタール |
|---|---|
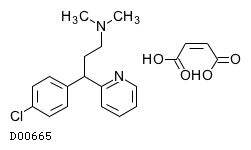
| 一般名 | クロルフェニラミンマレイン酸塩 |
| 欧文一般名 | Chlorpheniramine Maleate |
| 薬効分類名 | 抗ヒスタミン剤 |
| 薬効分類番号 | 4419 |
| ATCコード | R06AB04 |
| KEGG DRUG |
D00665
クロルフェニラミンマレイン酸塩
|
| KEGG DGROUP |
DG01482
ヒスタミンH1受容体拮抗薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年12月 改訂(第2版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ネオレスタール注射液10mg | NEORESTAR injections | 富士製薬工業 | 4419401A3055 | 104円/管 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分又は類似化合物に対し過敏症の既往歴のある患者
2.2 閉塞隅角緑内障の患者[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
2.3 前立腺肥大等下部尿路に閉塞性疾患のある患者[抗コリン作用により排尿困難、尿閉等があらわれ、症状が増悪することがある。]
2.4 低出生体重児・新生児[9.7.1参照]
4. 効能または効果
6. 用法及び用量
dl-クロルフェニラミンマレイン酸塩として、通常、成人1回5〜10mgを1日1〜2回、皮下、筋肉内または静脈内注射する。なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
8.1 眠気を催すことがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械の操作には従事させないよう十分注意すること。
8.2 再生不良性貧血、無顆粒球症があらわれることがあるので、血液検査を行うなど観察を十分に行うこと。[11.1.3参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 開放隅角緑内障の患者
抗コリン作用により眼圧が上昇し、症状を悪化させることがある。
9.1.2 眼内圧亢進のある患者
抗コリン作用により眼内圧が上昇し、症状が増悪するおそれがある。
9.1.3 甲状腺機能亢進症のある患者
抗コリン作用により症状が増悪するおそれがある。
9.1.4 狭窄性消化性潰瘍、幽門十二指腸通過障害のある患者
抗コリン作用により平滑筋の運動抑制、緊張低下が起こり、症状が増悪するおそれがある。
9.1.5 循環器系疾患のある患者
抗コリン作用による心血管系への作用により、症状が増悪するおそれがある。
9.1.6 高血圧症のある患者
抗コリン作用により血管拡張が抑制され、血圧が上昇するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意
| 中枢神経抑制剤 ペントバルビタールカルシウム クロザピン等 アルコール | 相互に作用を増強することがあるので、併用する場合には減量するなど慎重に投与すること。 | 本剤の中枢抑制作用により、作用が増強される。 |
| MAO阻害剤 | 相互に作用を増強することがあるので、併用する場合には減量するなど慎重に投与すること。 | 本剤の解毒機構に干渉し、作用を遷延化し増強することがある。 |
| 抗コリン作用を有する薬剤 アトロピン硫酸塩 ブチルスコポラミン臭化物 チキジウム臭化物等 | 相互に作用を増強することがあるので、併用する場合には減量するなど慎重に投与すること。 | 機序は不明である。 |
| ドロキシドパ ノルアドレナリン | 併用により血圧の異常上昇を来すおそれがある。 | 本剤はヒスタミンによる毛細血管拡張を抑制する。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック(頻度不明)
チアノーゼ、呼吸困難、胸内苦悶、血圧低下等の症状があらわれた場合には、投与を中止し、適切な処置を行うこと。
11.1.2 痙攣、錯乱(いずれも頻度不明)
痙攣、錯乱があらわれることがあるので、観察を十分に行い、異常があらわれた場合には、減量又は休薬等適切な処置を行うこと。
11.2 その他の副作用
| 頻度不明 | |
| 過敏症 | 発疹、光線過敏症等 |
| 精神神経系 | 鎮静、神経過敏、頭痛、焦燥感、複視、眠気、不眠、めまい、耳鳴、前庭障害、多幸症、情緒不安、ヒステリー、振戦、神経炎、協調異常、感覚異常、霧視等 |
| 消化器 | 口渇、胸やけ、食欲不振、悪心・嘔吐、腹痛、便秘、下痢等 |
| 泌尿器 | 頻尿、排尿困難、尿閉等 |
| 循環器 | 低血圧、心悸亢進、頻脈、期外収縮、微弱脈 |
| 呼吸器 | 鼻及び気道の乾燥、気管分泌液の粘性化、喘鳴、鼻閉等 |
| 血液1) | 溶血性貧血、血小板減少 |
| 肝臓 | 肝機能障害(AST・ALT・Al-Pの上昇) |
| その他 | 悪寒、発汗異常、疲労感、胸痛、月経異常、顔面蒼白 |
14. 適用上の注意
14.1 薬剤投与時の注意
16. 薬物動態
16.1 血中濃度
健常人(外国人)に3H標識クロルフェニラミンマレイン酸塩を静脈内投与した場合、投与5分後に最高血漿中濃度に達し、その値はクロルフェニラミン14.89ng/mLに相当し、半減期はα相が15分、β相が28時間である3)。
16.3 分布
16.3.1 血漿蛋白結合率
ヒト血漿蛋白結合率は、0.28μg/mL及び1.24μg/mLの濃度でそれぞれ72%及び69%であった(in vitro)3)。
16.4 代謝
16.5 排泄
健常人(外国人)に3H標識クロルフェニラミンマレイン酸塩の4mgを静脈内投与したときの投与後48時間までの尿及び糞中放射能排泄率は、それぞれ投与量の36%及び0.2%であった3)。
18. 薬効薬理
18.1 作用機序
クロルフェニラミンマレイン酸塩は、ヒスタミンH1受容体遮断薬である。H1受容体を介するヒスタミンによるアレルギー性反応(毛細血管の拡張と透過性亢進、気管支平滑筋の収縮、知覚神経終末刺激によるそう痒など)を抑制する。dl体である6)。
19. 有効成分に関する理化学的知見
19.1. クロルフェニラミンマレイン酸塩
20. 取扱い上の注意
外箱開封後は遮光して保存すること。
22. 包装
1mL[10アンプル]
23. 主要文献
- Deringer.P.M.et al., Lancet.I., 432, (1976)
- Kanoh.T.et al., Lancet.I., 546, (1976)
- Peets,E.A.et al., J.Pharmacol.Exp.Ther., 180 (2), 464-474, (1972)
- Huang,S.M.et al., Eur.J.Clin.Pharmacol., 22, 359-365, (1982) »PubMed
- Kasuya,F.et al., Xenobiotica., 21 (1), 97-109, (1991) »PubMed
- 第十八改正日本薬局方解説書, C-1832-1838, (2021), (廣川書店)
24. 文献請求先及び問い合わせ先
文献請求先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
製品情報問い合わせ先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
26. 製造販売業者等
26.1 製造販売元
富士製薬工業株式会社
富山県富山市水橋辻ヶ堂1515番地