医薬品情報
| 総称名 | ベネシッド |
|---|---|
| 一般名 | プロベネシド |
| 欧文一般名 | Probenecid |
| 薬効分類名 | 痛風治療剤 |
| 薬効分類番号 | 3942 |
| ATCコード | M04AB01 |
| KEGG DRUG |
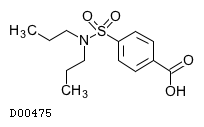
D00475
プロベネシド
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年2月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 12.臨床検査結果に及ぼす影響 13.過量投与 14.適用上の注意 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ベネシッド錠250mg | BENECID Tablets | 科研製薬 | 3942001F1040 | 18.7円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
○痛風
○ペニシリン・パラアミノサリチル酸の血中濃度維持
6. 用法及び用量
<痛風>
プロベネシドとして、通常、成人1日0.5〜2gを分割経口投与し、その後維持量として1日1〜2gを2〜4回に分割経口投与する。なお、年齢、症状により適宜増減する。
<ペニシリン・パラアミノサリチル酸の血中濃度維持>
プロベネシドとして、通常、成人1日1〜2gを4回に分割経口投与する。なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
<効能共通>
8.1 溶血性貧血、再生不良性貧血があらわれることがあるので、定期的に血液学的検査を行うなど観察を十分に行うこと。[11.1.1参照]
8.2 肝壊死があらわれることがあるので、定期的に肝機能検査を行うなど観察を十分に行うこと。[11.1.3参照]
<痛風>
8.3 急性痛風発作がおさまるまで、本剤の投与を開始しないこと。
8.4 投与初期に尿酸の移動により痛風発作の一時的な増強をみることがある。
8.5 本剤投与中に痛風が増悪した場合には、コルヒチン、インドメタシン等を併用すること。
8.6 尿が酸性の場合、痛風患者に尿酸結石及びこれに由来する血尿、腎仙痛、肋骨脊椎痛等の症状を起こしやすいので、これを防止するため、水分の摂取による尿量の増加及び尿のアルカリ化をはかること。なお、この場合には、患者の酸・塩基平衡に注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 消化性潰瘍の既往歴のある患者
消化性潰瘍が再発するおそれがある。
9.2 腎機能障害患者
9.2.1 高度の腎障害のある患者
投与しないこと。尿中尿酸排泄量の増大により症状を悪化させるおそれがある。なお、本剤は慢性腎不全(特に糸球体濾過値30mL/分以下)の患者には無効とされている。[2.2参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
9.7.1 2歳未満の乳幼児
投与しないこと。[2.5参照]
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意
| サリチル酸系薬剤 アスピリン等 | 本剤の尿酸排泄作用に拮抗する。 | 機序は不明であるが、腎尿細管分泌部位での阻害、血漿アルブミンの結合部位の競合によると考えられている。 |
| インドメタシン ナプロキセン | これら薬剤の半減期の延長、AUCの増加等の報告があるので、併用する場合には減量するなど注意すること。 | 本剤が併用薬の腎尿細管からの分泌、胆汁中への排泄を抑制するためと考えられている。 |
| ジドブジン | これら薬剤の半減期の延長、AUCの増加等の報告があるので、併用する場合には減量するなど注意すること。 | 本剤がジドブジンのグルクロン酸抱合を阻害し、また、抱合体の腎排泄を抑制するためと考えられている。 |
| 経口糖尿病用剤 スルホニルウレア系 スルホニルアミド系 パントテン酸 セファロスポリン系抗生物質 ペニシリン系抗生物質 アンピシリン水和物等 アシクロビル バラシクロビル塩酸塩 ザルシタビン ガチフロキサシン水和物 ジアフェニルスルホン | これら薬剤の半減期の延長、AUCの増加等の報告があるので、併用する場合には減量するなど注意すること。 | 本剤がこれら薬剤の腎尿細管分泌を阻害し、尿中排泄を低下させるためと考えられている。 |
| メトトレキサート | メトトレキサートの中毒症状(口内炎、汎血球減少)があらわれたとの報告があるので、併用する場合には減量するなど注意すること。 | 本剤がこれら薬剤の腎尿細管分泌を阻害し、尿中排泄を低下させるためと考えられている。 |
| 経口抗凝血剤 ワルファリン サルファ剤 | これら薬剤の作用を増強するおそれがある。 | 本剤がこれら薬剤の腎尿細管分泌を阻害し、尿中排泄を低下させるためと考えられている。 |
| ガンシクロビル | ガンシクロビルの半減期が延長し、AUCが増加するおそれがある。 | 本剤がこれら薬剤の腎尿細管分泌を阻害し、尿中排泄を低下させるためと考えられている。 |
| ノギテカン塩酸塩 | ノギテカン塩酸塩の腎クリアランスが低下するおそれがある。 | 動物実験において、ノギテカン塩酸塩の腎排泄に有機アニオントランスポーターが関与していることが示唆されているため。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 溶血性貧血、再生不良性貧血(いずれも頻度不明)[8.1参照]
11.1.2 アナフィラキシー(頻度不明)
11.1.3 肝壊死(頻度不明)[8.2参照]
11.1.4 ネフローゼ症候群(頻度不明)
注)発現頻度は再評価結果を含む。
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 血液 | 貧血 | |
| 過敏症 | 皮膚炎 | 発熱、そう痒 |
| 消化器 | 食欲不振、胃部不快感 | 悪心・嘔吐 |
| その他 | 頭痛 | めまい、頻尿、歯肉痛、潮紅 |
12. 臨床検査結果に及ぼす影響
12.1 ベネディクト試薬による尿糖検査では偽陽性を呈することがある。
12.2 次の化合物の尿中排泄を抑制することがある。
パラアミノ馬尿酸、フェノールスルホンフタレイン、17-ケトステロイド
12.3 スルホブロモフタレインの肝及び腎からの排泄を抑制することがある。
13. 過量投与
13.1 症状
昏睡や中枢神経系が刺激され痙攣、呼吸不全を引き起こすことがある。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
健常成人6人にプロベネシド2gを朝食2時間後に経口投与した場合、吸収は速やかで最高血漿中濃度に達する時間は1〜5時間である。更に、健常成人3人にプロベネシド2gを経口投与した場合、血漿中半減期は6〜12時間である1)(外国人のデータ)。
16.3 分布
16.5 排泄
健常成人2人に14C-標識プロベネシド2gを経口投与した場合、投与48時間以内で投与量の約40%がグルクロン酸抱合体として尿中に排泄され、未変化体の排泄は少ない(<4%)。他の代謝物は、n-プロピル側鎖の2位(7.2〜12.5%)及び末端(1.6〜3.7%)が水酸化された誘導体、及びカルボキシ体(6.2〜9.2%)、N-脱プロピル体(4.6〜8.0%)であり、これらは大部分が遊離の形で排泄される3)(外国人のデータ)。
注)本剤の承認された用量は、次のとおりである。
痛風の場合
プロベネシドとして1日0.5〜2gを分割経口投与し、その後維持量として1日1〜2gを2〜4回に分割経口投与する。
ペニシリン・パラアミノサリチル酸の血中濃度維持の場合
プロベネシドとして1日1〜2gを4回に分割経口投与する。
18. 薬効薬理
18.1 作用機序
尿細管における尿酸の分泌と再吸収を阻害するが、遠位尿細管での分泌抑制よりも近位尿細管での再吸収抑制が強いので、結果的に尿酸排泄を促進する。また、ペニシリン、パラアミノサリチル酸については、排泄抑制作用の方が強いので、これらの血中濃度を維持する2)。
18.2 尿酸排泄作用
18.3 ペニシリン、パラアミノサリチル酸の血中濃度維持作用
19. 有効成分に関する理化学的知見
19.1. プロベネシド
22. 包装
500錠[10錠(PTP)×50]
100錠[瓶、バラ]
23. 主要文献
- Dayton,P.G.et al., J.Pharmacol.Exp.Ther., 140, 278-286, (1963) »PubMed
- 第十八改正日本薬局方解説書
- Perel,J.M.et al., Life Sci., 9 (1), 1337-1343, (1970)
- Sirota,J.H.et al., J.Clin.Invest., 31, 692-701, (1952) »PubMed
- Pitts,F.W.et al., U.S.Armed Forces Med.J., 3 (8), 1219-1224, (1952) »PubMed
- Bartels,E.C., Med.Clin.N.Amer., 44, 453-463, (1960) »PubMed
- Boger,W.P.et al., Ann.Int.Med., 33, 18-31, (1950) »PubMed
- 上田泰 他, 化学療法, 12, 5-7, (1957)
24. 文献請求先及び問い合わせ先
文献請求先
科研製薬株式会社
医薬品情報サービス室
〒113-8650
東京都文京区本駒込二丁目28番8号
電話:フリーダイヤル 0120-519-874
製品情報問い合わせ先
科研製薬株式会社
医薬品情報サービス室
〒113-8650
東京都文京区本駒込二丁目28番8号
電話:フリーダイヤル 0120-519-874
26. 製造販売業者等
26.1 製造販売元
科研製薬株式会社
東京都文京区本駒込二丁目28番8号