医薬品情報
| 総称名 | ウブレチド |
|---|---|
| 一般名 | ジスチグミン臭化物 |
| 欧文一般名 | Distigmine Bromide |
| 薬効分類名 | コリンエステラーゼ阻害薬 |
| 薬効分類番号 | 1231 |
| ATCコード | N07AA03 |
| KEGG DRUG |
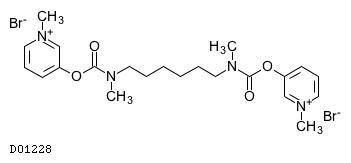
D01228
ジスチグミン臭化物
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年7月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ウブレチド錠5mg | UBRETID TAB.5mg | 鳥居薬品 | 1231014F1054 | 11.3円/錠 | 毒薬, 処方箋医薬品注) |
1. 警告
本剤の投与により意識障害を伴う重篤なコリン作動性クリーゼを発現し、致命的な転帰をたどる例が報告されているので、投与に際しては下記の点に注意し、医師の厳重な監督下、患者の状態を十分観察すること。
1.1 本剤投与中にコリン作動性クリーゼの徴候(初期症状:悪心・嘔吐、腹痛、下痢、唾液分泌過多、気道分泌過多、発汗、徐脈、縮瞳、呼吸困難等、臨床検査:血清コリンエステラーゼ低下)が認められた場合には、直ちに投与を中止すること。[1.2、1.3、8.1.1-8.1.3、8.3.1、9.8、11.1.1、13.1参照]
2. 禁忌
次の患者には投与しないこと
2.1 消化管又は尿路の器質的閉塞のある患者[消化管機能を亢進させ、症状を悪化させるおそれがある。また、尿の逆流を引き起こすおそれがある。]
2.2 迷走神経緊張症のある患者[迷走神経の緊張を増強させるおそれがある。]
2.3 脱分極性筋弛緩剤(スキサメトニウム)を投与中の患者[10.1参照]
2.4 本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
○手術後及び神経因性膀胱などの低緊張性膀胱による排尿困難
6. 用法及び用量
<手術後及び神経因性膀胱などの低緊張性膀胱による排尿困難>
ジスチグミン臭化物として、成人1日5mgを経口投与する。
<重症筋無力症>
ジスチグミン臭化物として、通常成人1日5〜20mgを1〜4回に分割経口投与する。なお、症状により適宜増減する。
7. 用法及び用量に関連する注意
<重症筋無力症>
医師の厳重な監督下、通常成人1日5mgから投与を開始し、患者の状態を十分観察しながら症状により適宜増減すること。
8. 重要な基本的注意
<効能共通>
8.1 本剤の投与により意識障害を伴うコリン作動性クリーゼがあらわれることがあるので、以下の点に注意すること。
8.2 本剤の使用により効果が認められない場合には、漫然と投与せず他の治療法を検討すること。
<重症筋無力症>
8.3 ときに筋無力症状の重篤な悪化、呼吸困難、嚥下障害(クリーゼ)をみることがあるので、このような場合には、臨床症状でクリーゼを鑑別し、困難な場合には、エドロホニウム塩化物2mgを静脈内投与し、クリーゼを鑑別し、次の処置を行うこと。
8.3.1 コリン作動性クリーゼ
8.3.2 筋無力性クリーゼ
呼吸困難、唾液排出困難、チアノーゼ、全身の脱力等の症状が認められた場合、又はエドロホニウム塩化物を投与したとき、症状の改善が認められた場合は本剤の投与量を増加する。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 コリン作動薬やコリンエステラーゼ阻害薬を投与中の患者
相互に作用を増強し、副作用が発現しやすくなるおそれがある。[10.2参照]
9.1.2 気管支喘息の患者
気管支喘息の症状を悪化させるおそれがある。
9.1.3 甲状腺機能亢進症の患者
甲状腺機能亢進症の症状を悪化させるおそれがある。
9.1.4 徐脈・心疾患(冠動脈疾患、不整脈)のある患者
心拍数低下、冠動脈の収縮、冠れん縮による狭心症、不整脈の増悪、心拍出量低下を起こすおそれがある。
9.1.5 消化性潰瘍の患者
消化管機能を亢進させ潰瘍の症状を悪化させるおそれがある。
9.1.6 てんかんの患者
てんかんの症状を悪化させるおそれがある。
9.1.7 パーキンソン症候群の患者
パーキンソン症候群の症状を悪化させるおそれがある。
9.2 腎機能障害患者
本剤は腎臓から排泄されるため、血中濃度が上昇するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
10. 相互作用
10.1 併用禁忌
| 脱分極性筋弛緩剤 スキサメトニウム塩化物水和物 スキサメトニウム注、 レラキシン注 [2.3参照] | 脱分極性筋弛緩剤の作用を増強する。 | 1)脱分極性筋弛緩剤はコリンエステラーゼにより代謝されるため、本剤により代謝が阻害されることが考えられる。 2)本剤による直接ニコチン様作用には脱分極性筋弛緩作用がある。 |
10.2 併用注意
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 コリン作動性クリーゼ(頻度不明)
11.1.2 狭心症、不整脈(いずれも頻度不明)
狭心症、不整脈(心室頻拍、心房細動、房室ブロック、洞停止等)があらわれることがある。
注)発現頻度は再評価結果を含む
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 0.5〜1%未満 | 0.5%未満 | 頻度不明 | |
| 骨格筋 | 筋力低下、線維性ちく搦(ちくでき=クローヌス)、筋痙攣 | 線維束れん縮 | |||
| 消化器 | 下痢 | 腹痛、悪心・不快感 | 嘔気・嘔吐、腹鳴、胃腸症状 | 便失禁、心窩部不快感、流唾、テネスムス(しぶり腹)、口渇 | |
| 精神神経系 | めまい、頭痛 | 睡眠障害 | |||
| 泌尿器 | 尿失禁 | 頻尿、尿道痛 | |||
| 肝臓 | AST・ALTの上昇 | ||||
| その他 | 発汗 | 流涙、全身倦怠感、神経痛悪化、動悸、舌のしびれ、発熱、自律神経失調、ざ瘡、胸部圧迫感、耳鳴 | 血清コリンエステラーゼ値低下 |
13. 過量投与
13.1 徴候・症状
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
健康成人に14Cジスチグミン臭化物5mgを単回経口投与した結果、血漿中濃度は投与後1.58時間で最高値4.40ng/mLとなり、その後、二相性に漸減した。半減期はα相で4.47±2.03時間、β相で69.5±5.1時間であった4)(外国人データ)。
16.2 吸収
16.2.1 食事の影響
イヌにジスチグミン臭化物(0.02%w/v水溶液)として1.0mg/kgを、絶食時又は給餌後に単回経口投与し、血漿中濃度を測定した際、絶食群は給餌群に比し、Cmaxが約9.4倍、AUC0-24が約6.6倍高値であった5)。
| 例数 | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | AUC0-24(ng/mL・hr) | |
| 絶食群 | 5 | 166±75 | 0.8±0.3 | 2.6±1.8 | 539±187 |
| 給餌群 | 5 | 17.6±8.4 | 0.9±0.2 | 4.1±2.0 | 82.0±23.8 |
16.5 排泄
健康成人に14Cジスチグミン臭化物5mgを単回経口投与した結果、投与216時間後までの尿及び糞中への累積排泄率は、それぞれ6.5%及び88.0%であった。0.5mgを単回静脈内投与した結果、尿及び糞中への累積排泄率は、それぞれ85.3%及び3.9%であった。
これらのことから、主な排泄部位は腎である4)(外国人データ)。
これらのことから、主な排泄部位は腎である4)(外国人データ)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床成績
| 疾患名 | 有効率%(有効例/症例数) | ||
| 1日投与量5mg | |||
| 排尿障害 | 前立腺症 | 前立腺肥大症 | 71.0(22/31) |
| 膀胱頸部硬化症 | 69.2(9/13) | ||
| 神経因性膀胱機能障害 | 神経因性膀胱 | 72.4(71/98) | |
| 脳性疾患 | 50.0(3/6) | ||
| 脊髄疾患 | 65.4(68/104) | ||
| 末梢神経疾患 | 76.3(71/93) | ||
| 手術後の排尿障害 | 90.2(119/132) | ||
| 計 | 76.1(363/477) | ||
| 疾患名 | 1日投与量別有効率% (有効例/症例数) | 計 | ||
| 5mg | 10mg | 15mg | ||
| 重症筋無力症 | 84.8 (56/66) | 78.8 (41/52) | 93.8 (15/16) | 83.6 (112/134) |
18. 薬効薬理
18.1 作用機序
ジスチグミン臭化物は、可逆的にコリンエステラーゼを阻害しアセチルコリンの分解を抑制することにより、間接的にアセチルコリンの作用を増強、持続させ、副交感神経支配臓器でムスカリン様作用を、また、骨格筋接合部でニコチン様作用を示す。
18.2 コリンエステラーゼ阻害作用
本品100μg/kg及びネオスチグミン100〜400μg/kgをラットに1回腹腔内投与したとき、血中コリンエステラーゼ活性はそれぞれ約80%及び30〜60%阻害された6)。
18.3 アセチルコリン作用の増強
ラットの血涙反応では、対照値のアセチルコリンED50値を1/5に減ずるに要する用量は、本品で8.6μg/kg、ネオスチグミンで16.6μg/kgであった。また本品の作用は、投与後2時間で最大となり、少なくとも48時間以上持続した6)。
18.4 抗クラーレ作用
19. 有効成分に関する理化学的知見
19.1. ジスチグミン臭化物
20. 取扱い上の注意
包装開封後は湿気を避けて保存すること。
22. 包装
PTP包装
100錠(10錠×10)、500錠(10錠×50)
バラ包装(瓶)
500錠
23. 主要文献
- 寺嶋正佳ほか, 臨床麻酔, 15 (7), 931-932, (1991)
- 植木正明ほか, 中毒研究, 4, 383-385, (1991)
- 岩壁秀樹ほか, 内科, 70 (4), 765-767, (1992)
- Vree TB,et al., Int.J.Clin.Pharmacol.Ther., 37 (8), 393-403, (1999) »PubMed
- 社内資料:ジスチグミン臭化物のビーグル犬を用いた経口投与による血漿中濃度測定試験
- 社内資料:ウブレチドの薬理学的研究
- Herzfeld E,et al., Wien Klin.Wochenschr., 69 (14), 245-248, (1957) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
鳥居薬品株式会社
お客様相談室
〒103-8439
東京都中央区日本橋本町3-4-1
電話:0120-316-834
FAX:03-3231-6890
製品情報問い合わせ先
鳥居薬品株式会社
お客様相談室
〒103-8439
東京都中央区日本橋本町3-4-1
電話:0120-316-834
FAX:03-3231-6890
26. 製造販売業者等
26.1 製造販売元
鳥居薬品株式会社
東京都中央区日本橋本町3-4-1