医薬品情報
| 総称名 | ウルグート |
|---|---|
| 一般名 | ベネキサート塩酸塩 ベータデクス |
| 欧文一般名 | Benexate Hydrochloride Betadex |
| 製剤名 | ベネキサート塩酸塩 ベータデクスカプセル |
| 薬効分類名 | 胃粘膜防御機構増強 胃炎・胃潰瘍治療剤 |
| 薬効分類番号 | 2329 |
| KEGG DRUG |
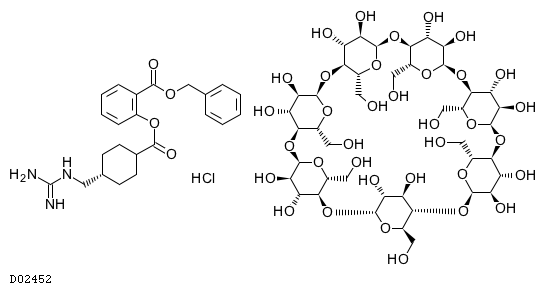
D02452
ベネキサート塩酸塩 ベータデクス
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年12月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ウルグートカプセル200mg | Ulgut Capsules | 共和薬品工業 | 2329019M1040 | 8.8円/カプセル |
2. 禁忌
次の患者には投与しないこと
妊婦又は妊娠している可能性のある女性[9.5参照]
4. 効能または効果
○下記疾患の胃粘膜病変(びらん、出血、発赤、浮腫)の改善
急性胃炎、慢性胃炎の急性増悪期
○胃潰瘍
6. 用法及び用量
通常、成人にはベネキサート塩酸塩 ベータデクスとして、1回400mgを1日2回朝食後及び就寝前に経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
<急性胃炎、慢性胃炎の急性増悪期>
8.1 胃炎に対して胃粘膜病変(びらん、出血、発赤、浮腫)の改善がみられない場合、長期にわたって漫然と使用すべきでない。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 血栓(脳血栓、心筋梗塞、血栓性静脈炎等)のある患者
in vitro で抗プラスミン作用が報告されている1)。
9.1.2 消費性凝固障害のある患者
in vitro で抗プラスミン作用が報告されている1)。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。動物試験(ラット)で臨床用量の150倍(2000mg/kg)投与により催奇形作用が報告されている2)。[2.参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能が低下していることが多い。
11. 副作用
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | |
| 皮膚 | そう痒感、発疹 | |
| 消化器 | 便秘、下痢 | 口渇、悪心・嘔吐、腹部不快感・膨満感 |
| 肝臓 | ASTの軽度上昇、ALTの軽度上昇 | |
| 精神神経系 | 頭痛、頭重感 | |
| その他 | 胸部絞扼感、浮遊感、歯が浮く感じ | 浮腫 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.3 分布
胃切除患者6例にベネキサート塩酸塩 ベータデクスカプセル400mgを経口投与したとき、HPLCにて測定された投与30分後の摘出胃の胃体部正常部位におけるベネキサート塩酸塩濃度(μg/g)は、胃粘液:102.7〜945.6、胃粘膜:2.1〜66.4(ただし、1例は検出されず)、筋層:1.8〜9.1であった3)。
16.4 代謝
健康成人男性3例にベネキサート塩酸塩 ベータデクスカプセル600mgを空腹時又は軽食後単回経口投与したとき、血漿中及び尿中に有効成分であるベネキサート塩酸塩は検出されず、速やかに代謝された。代謝物として、血漿中ではサリチル酸が、尿中ではサリチル尿酸及びグアニジノメチルシクロヘキサンカルボン酸が多く排泄された4)。(1回600mgは承認外用量であり、承認用量は、通常、1回400mgである。)
17. 臨床成績
17.1 有効性及び安全性に関する試験
<急性胃炎、慢性胃炎の急性増悪期>
17.1.1 国内第III相二重盲検比較試験5)
内視鏡検査により急性胃炎または慢性胃炎と診断され、びらん、出血、発赤、浮腫のいずれかの所見を有している患者292例を対象として、本剤の有効性及び安全性について塩酸セトラキサートを対照に多施設二重盲検比較試験を実施した。投与期間は4週間とした。
その結果、4週投与後の全般改善度評価対象例255例の改善率(中等度改善以上)は、本剤群81.1%(103/127)、塩酸セトラキサート群75.8%(97/128)であり、両群間に有意な差は認められなかった。4週投与後の内視鏡総合改善度(中等度改善以上)は、本剤群79.5%(101/127)、塩酸セトラキサート群73.4%(94/128)であり、両群間に有意な差は認められなかった。
副作用発現率は、本剤群では2.2%(3/137)であり下痢、心窩部痛・嘔吐・嘔気、肝機能異常が各1例認められた。
その結果、4週投与後の全般改善度評価対象例255例の改善率(中等度改善以上)は、本剤群81.1%(103/127)、塩酸セトラキサート群75.8%(97/128)であり、両群間に有意な差は認められなかった。4週投与後の内視鏡総合改善度(中等度改善以上)は、本剤群79.5%(101/127)、塩酸セトラキサート群73.4%(94/128)であり、両群間に有意な差は認められなかった。
副作用発現率は、本剤群では2.2%(3/137)であり下痢、心窩部痛・嘔吐・嘔気、肝機能異常が各1例認められた。
17.1.2 国内一般臨床試験(第II相用量検討試験)6)
内視鏡検査により急性胃炎または慢性胃炎と診断され、びらん、出血のいずれかの所見を有している患者77例を対象として、至適用量を検討することを目的とした用量検討試験を二重盲検にて実施した。投与期間は4週間とした。その結果、4週投与後の全般改善度評価対象例65例の改善率(中等度改善以上)は、1日400mg投与群79.4%(27/34)、1日800mg投与群80.6%(25/31)であり、両群間に有意な差は認められなかった。4週投与後の内視鏡総合改善度(中等度改善以上)は、1日400mg投与群79.4%(27/34)、1日800mg投与群80.6%(25/31)であり、両群間に有意な差は認められなかった。副作用発現率は1日800mg投与群では2.6%(1/38)であり白血球減少1例が認められた。
<胃潰瘍>
17.1.3 国内第III相二重盲検比較試験7)
内視鏡検査により胃潰瘍が確認された患者416例を対象として、ベネキサート塩酸塩 ベータデクスの有効性及び安全性について塩酸セトラキサートを対照に多施設二重盲検比較試験を実施した。投与期間は8週間とした。その結果、8週投与後の全般改善度評価対象例363例の改善率(中等度改善以上)は、本剤群73.0%(135/185)、塩酸セトラキサート群64.6%(115/178)であり、両群間に有意な差は認められなかった。8週投与後の内視鏡治癒判定(治癒率)は、本剤群58.9%(86/146)、塩酸セトラキサート群54.6%(71/130)であり、両群間に有意な差は認められなかった。副作用発現率は、本剤群では3.6%(7/192)であり悪心、便秘、頬部しびれ感・頭痛、掻痒感・胸部絞扼感が各1例、肝機能異常が3例認められた。
内視鏡検査により胃潰瘍が確認された患者を対象として、有効性及び安全性を検討することを目的とした臨床試験を実施した。投与期間は8週間とした。その結果、8週投与後の全般改善度評価対象例183例の改善率(中等度改善以上)は87.4%(160/183)であり、8週投与後の内視鏡治癒判定(治癒率)は70.8%(102/144)であった。
18. 薬効薬理
18.1 作用機序
胃粘膜に直接作用し、胃粘膜の血流量を増加させるほか、種々の胃粘膜防御機能を増強させる。
18.2 胃粘膜血流量増加作用
18.2.1 急性胃炎患者にベネキサート塩酸塩 ベータデクス200mgを生理食塩液に溶解し胃体部(n=29)及び前庭部(n=23)に注入したとき、内視鏡的レーザードップラー法にて測定された両部位の粘膜血流量は、注入直後(1分)から測定終了(5分)まで注入前に比べ有意に増加した16)。
18.2.2 ベネキサート塩酸塩 ベータデクスはモルモット摘出血管において血管収縮を抑制した17)。
18.2.3 ラットにベネキサート塩酸塩 ベータデクス100mg/kg、300mg/kgを経口投与したとき、水素ガスクリアランス法にて測定された投与5分後の胃粘膜血流量は、用量反応性に増加した。また、300mg/kg投与において1時間以上血流量増加の持続が認められた18)。
18.3 胃粘膜内高分子糖蛋白質の生合成促進作用及び減少抑制作用
18.3.1 ラットにベネキサート塩酸塩 ベータデクス300mg/kg単独経口投与したとき、胃粘膜内高分子糖蛋白質を約1.5倍増加させた19)。
18.3.2 ラットにベネキサート塩酸塩 ベータデクス300mg/kgをアスピリン300mg/kgと併用して経口投与したとき、また、アスピリン300mg/kg投与1時間前に経口投与したとき、いずれの場合もアスピリン投与によって起こる胃粘膜内高分子糖蛋白質の減少を抑制した19)。
18.4 胃粘膜の内因性プロスタグランジンE2及びI2増加作用
ラットにベネキサート塩酸塩 ベータデクス300mg/kg、1000mg/kgを胃内に注入したとき、インドメタシンあるいは拘束水浸ストレス負荷により低下した胃粘膜の内因性プロスタグランジンE2及びI2をほぼ用量依存性に増加させた20)。
18.5 酸(水素イオン)の胃粘膜への逆拡散防止作用
ラットにベネキサート塩酸塩 ベータデクス300mg/kgをアスピリン(胃粘膜関門障害物質)と併用して胃内に注入留置したとき、留置15分後の時点でアスピリンによって起こる胃粘膜への水素イオンの逆拡散を有意に抑制した21)。
18.6 各種実験潰瘍、実験胃粘膜病変に対する抑制作用
19. 有効成分に関する理化学的知見
19.1. ベネキサート塩酸塩 ベータデクス
22. 包装
100カプセル[10カプセル(PTP)×10]
23. 主要文献
- 村松睦,他, Prog. Med., 6 (Supple.1), 2142-2152, (1986)
- 小林文彦,他, 社内資料(ラットにおける器官形成期投与試験、1986)
- 板東隆文, Prog. Med., 15 (5), 641-644, (1995)
- 菅野浩一,他, Prog. Med., 6 (Supple.1), 2229-2237, (1986)
- 三好秋馬,他, Prog. Med., 9 (3), 1094-1117, (1989)
- 三好秋馬,他, Prog. Med., 9 (2), 609-620, (1989)
- 三好秋馬,他, Prog. Med., 6 (Supple.1), 2273-2295, (1986)
- 三好秋馬,他, Prog. Med., 6 (Supple.1), 2259-2272, (1986)
- 佐藤正伸,他, Prog. Med., 6 (Supple.1), 2296-2305, (1986)
- ちょ贊発, 他, Prog. Med., 6 (Supple.1), 2307-2314, (1986)
- 山本義樹,他, Prog. Med., 6 (Supple.1), 2315-2322, (1986)
- 田中延善,他, Prog. Med., 6 (Supple.1), 2323-2330, (1986)
- 佐藤茂範,他, Prog. Med., 6 (Supple.1), 2331-2339, (1986)
- 野村喜重郎,他, Prog. Med., 6 (Supple.1), 2341-2350, (1986)
- 宮井満久,他, Prog. Med., 6 (Supple.1), 2352-2360, (1986)
- 原澤茂,他, Prog. Med., 13 (4), 811-819, (1993)
- 佐藤初夫,他, Prog. Med., 6 (Supple.1), 2085-2091, (1986)
- 青野充,他, Prog. Med., 6 (Supple.1), 2077-2084, (1986)
- 安海義曜,他, Prog. Med., 6 (Supple.1), 2092-2098, (1986)
- 荒川哲男,他, 日本消化器病学会雑誌, 81 (7), 1554-1558, (1984) »DOI
- 大江慶治,他, 臨牀と研究, 63 (5), 1687-1692, (1986)
- 岡部進,他, 応用薬理, 27 (5), 829-836, (1984)
- 田中郁夫,他, Prog. Med., 9 (2), 601-607, (1989)
24. 文献請求先及び問い合わせ先
文献請求先
共和薬品工業株式会社
お問い合わせ窓口
〒530-0005
大阪市北区中之島3-2-4
電話:0120-041-189
FAX:06-6121-2858
製品情報問い合わせ先
共和薬品工業株式会社
お問い合わせ窓口
〒530-0005
大阪市北区中之島3-2-4
電話:0120-041-189
FAX:06-6121-2858
26. 製造販売業者等
26.1 製造販売元
共和薬品工業株式会社
大阪市北区中之島3-2-4