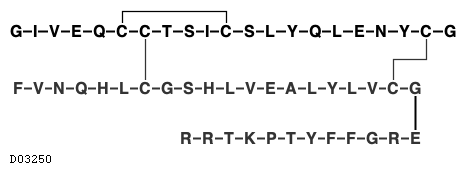医薬品情報
| 総称名 | ランタス |
|---|---|
| 一般名 | インスリン グラルギン(遺伝子組換え) |
| 欧文一般名 | Insulin Glargine(Genetical Recombination) |
| 薬効分類名 | 持効型溶解インスリンアナログ製剤 |
| 薬効分類番号 | 2492 |
| ATCコード | A10AE04 |
| KEGG DRUG |
D03250
インスリングラルギン
|
| KEGG DGROUP |
DG01636
インスリン製剤
|
| JAPIC | 添付文書(PDF) |
添付文書情報2020年5月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ランタス注ソロスター | LANTUS SoloStar S.C.Injection | サノフィ | 2492416G2024 | 888円/キット | 劇薬, 処方箋医薬品 |
2. 禁忌
次の患者には投与しないこと
2.1 低血糖症状を呈している患者[11.1.1参照]
2.2 本剤の成分又は他のインスリン グラルギン製剤に対し過敏症の既往歴のある患者
4. 効能または効果
インスリン療法が適応となる糖尿病
5. 効能または効果に関連する注意
2型糖尿病においては、急を要する場合以外は、あらかじめ糖尿病治療の基本である食事療法、運動療法を十分行ったうえで適用を考慮すること。
6. 用法及び用量
通常、成人では、初期は1日1回4〜20単位を皮下注射するが、ときに他のインスリン製剤を併用することがある。注射時刻は朝食前又は就寝前のいずれでもよいが、毎日一定とする。投与量は、患者の症状及び検査所見に応じて増減する。なお、その他のインスリン製剤の投与量を含めた維持量は、通常1日4〜80単位である。
ただし、必要により上記用量を超えて使用することがある。
ただし、必要により上記用量を超えて使用することがある。
7. 用法及び用量に関連する注意
7.1 適用にあたっては本剤の作用時間、1mLあたりのインスリン含有単位と患者の病状に留意し、その製剤的特徴に適する場合に投与すること。
7.2 糖尿病性昏睡、急性感染症、手術等緊急の場合は、本剤のみで処置することは適当でなく、速効型インスリン製剤を使用すること。
7.3 中間型又は持続型インスリン製剤から本剤に変更する場合、以下を参考に本剤の投与を開始し、その後の患者の状態に応じて用量を増減するなど、本剤の作用特性を考慮の上慎重に行うこと。[16.1.1参照]
7.3.1 インスリン グラルギン300単位/mL製剤から本剤に変更する場合
通常初期用量は、前治療のインスリン グラルギン300単位/mL製剤の1日投与量と同単位よりも低用量を目安として投与を開始する。[8.3参照]
7.3.2 インスリン グラルギン300単位/mL製剤以外の中間型又は持続型インスリン製剤から本剤に変更する場合
・1日1回投与の中間型又は持続型インスリン製剤から本剤に変更する場合、通常初期用量は、前治療の中間型又は持続型インスリン製剤の1日投与量と同単位を目安として投与を開始する。
・1日2回投与の中間型インスリン製剤から本剤への切り替えに関しては、国内では使用経験がない。[17.1.2参照]
7.4 インスリン グラルギン300単位/mL製剤又は中間型インスリン製剤から本剤への切り替え直後に低血糖を起こすことがあるので、中間型又は持続型インスリン製剤から本剤に変更する場合、併用している速効型インスリン製剤、超速効型インスリンアナログ製剤又は他の糖尿病用薬の投与量及び投与スケジュールの調整が必要となることがあるので注意すること。[17.1.1参照]
7.5 インスリン製剤以外の他の糖尿病用薬から本剤に変更する場合又はインスリン製剤以外の他の糖尿病用薬と本剤を併用する場合、投与にあたっては低用量から開始するなど、本剤の作用特性を考慮の上慎重に行うこと。[16.1.1参照]
8. 重要な基本的注意
8.1 本剤の自己注射にあたっては、以下の点に留意すること。
・投与法について十分な教育訓練を実施したのち、患者自ら確実に投与できることを確認した上で、医師の管理指導のもとで実施すること。
・本剤の使用にあたっては、必ず添付の取扱説明書を読むよう指導すること。
・すべての器具の安全な廃棄方法について指導を徹底すること。
8.3 インスリン グラルギン300単位/mL製剤から本剤への切り替え時には、前治療の1日投与量よりも低用量での切り替えを考慮するとともに、切り替え時及びその後しばらくの間は血糖モニタリングを慎重に行うこと。本剤とインスリン グラルギン300単位/mL製剤では薬物動態が異なる。インスリン グラルギン300単位/mL製剤から本剤への切り替え時に低血糖の発現が増加した。[7.3.1、11.1.1参照]
8.4 ヒトインスリンに対する獲得抗体を有し、高用量のインスリンを必要としている患者では、他のインスリン製剤から本剤に変更することによって、本剤の需要量が急激に変化することがあるので、経過を観察しながら慎重に投与すること。
8.5 急激な血糖コントロールに伴い、糖尿病網膜症の顕在化又は増悪、眼の屈折異常、治療後神経障害(主として有痛性)があらわれることがあるので注意すること。
8.6 本剤と他のインスリン製剤を取り違えないよう、毎回注射する前に本剤のラベル等を確認するよう患者に十分指導すること。
8.7 低血糖を起こすことがあるので、高所作業、自動車の運転等に従事している患者に投与するときには注意すること。[11.1.1参照]
8.8 同一箇所への繰り返し投与により、注射箇所に皮膚アミロイドーシス又はリポジストロフィーがあらわれることがあるので、定期的に注射箇所を観察するとともに、以下の点を患者に指導すること。
・本剤の注射箇所は、少なくとも前回の注射箇所から2〜3cm離すこと。[14.2.2参照]
・注射箇所の腫瘤や硬結が認められた場合には、当該箇所への投与を避けること。
8.9 皮膚アミロイドーシス又はリポジストロフィーがあらわれた箇所に本剤を投与した場合、本剤の吸収が妨げられ十分な血糖コントロールが得られなくなることがある。血糖コントロールの不良が認められた場合には、注射箇所の腫瘤や硬結の有無を確認し、注射箇所の変更とともに投与量の調整を行うなどの適切な処置を行うこと。血糖コントロールの不良に伴い、過度に増量されたインスリン製剤が正常な箇所に投与されたことにより、低血糖に至った例が報告されている。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 手術、外傷、感染症等の患者
インスリン需要の変動が激しい。
9.1.2 自律神経障害のある患者
低血糖の自覚症状が明確でないことがある。
9.1.3 低血糖を起こしやすい以下の患者又は状態
9.2 腎機能障害患者
9.2.1 重篤な腎障害のある患者
低血糖を起こすおそれがある。[11.1.1参照]
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
低血糖を起こすおそれがある。[11.1.1参照]
9.5 妊婦
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。妊娠した場合、あるいは妊娠が予測される場合には医師に知らせるよう指導すること。妊娠中、周産期等にはインスリンの需要量が変化しやすいため、用量に留意し、定期的に検査を行い投与量を調整すること。通常インスリン需要量は、妊娠初期は減少し、中期及び後期は増加する。
9.6 授乳婦
用量に留意し、定期的に検査を行い投与量を調整すること。インスリンの需要量が変化しやすい。
9.7 小児等
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。生理機能が低下していることが多く、低血糖が起こりやすい。[11.1.1参照]
10. 相互作用
10.2 併用注意
| 糖尿病用薬 ビグアナイド系薬剤 スルホニルウレア系薬剤 速効型インスリン分泌促進剤 α-グルコシダーゼ阻害剤 チアゾリジン系薬剤 DPP-4阻害薬 GLP-1受容体作動薬 SGLT2阻害剤 等 | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | 血糖降下作用が増強される。 |
| モノアミン酸化酵素(MAO)阻害剤 | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | インスリン分泌促進、糖新生抑制作用による血糖降下作用を有する。 |
| 三環系抗うつ剤 ノルトリプチリン塩酸塩 等 | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | 機序は不明であるが、インスリン感受性を増強するなどの報告がある。 |
| サリチル酸誘導体 アスピリン エテンザミド | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | 糖に対するβ細胞の感受性の亢進やインスリン利用率の増加等による血糖降下作用を有する。また、末梢で弱いインスリン様作用を有する。 |
| 抗腫瘍剤 シクロホスファミド水和物 | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | インスリンが結合する抗体の生成を抑制し、その結合部位からインスリンを遊離させる可能性がある。 |
| クマリン系薬剤 ワルファリンカリウム | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | 機序不明 |
| クロラムフェニコール | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | 機序不明 |
| サルファ剤 | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | 膵臓でのインスリン分泌を増加させることにより、低血糖を起こすと考えられている。腎機能低下、空腹状態の遷延、栄養不良、過量投与が危険因子となる。 |
| シベンゾリンコハク酸塩 ジソピラミド ピルメノール塩酸塩水和物 | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | インスリン分泌作用を認めたとの報告がある。 |
| フィブラート系薬剤 | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | インスリン感受性増強等の作用により、本剤の作用を増強する。 |
| レセルピン | 血糖降下作用の増強による低血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。[11.1.1参照] | 低血糖に対する交感神経系の症状(振戦、動悸等)をマスクし、低血糖を遷延させる可能性がある。 |
| チアジド系利尿剤 トリクロルメチアジド ループ利尿剤 フロセミド | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | カリウム喪失が関与すると考えられている。 カリウム欠乏時には、血糖上昇反応に対するβ細胞のインスリン分泌能が低下する可能性がある。 |
| 副腎皮質ステロイド プレドニゾロン トリアムシノロン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、筋肉組織・脂肪組織からのアミノ酸や脂肪酸の遊離促進、末梢組織でのインスリン感受性低下等による血糖上昇作用を有する。 |
| ACTH テトラコサクチド酢酸塩 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 副腎皮質刺激作用により糖質コルチコイドの分泌が増加する。糖質コルチコイドは、糖新生亢進、筋肉組織・脂肪組織からのアミノ酸や脂肪酸の遊離促進、末梢組織でのインスリン感受性低下等による血糖上昇作用を有する。 |
| アドレナリン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、末梢での糖利用抑制、インスリン分泌抑制による血糖上昇作用を有する。 |
| グルカゴン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、肝グリコーゲン分解促進による血糖上昇作用を有する。 |
| 甲状腺ホルモン レボチロキシンナトリウム水和物 乾燥甲状腺 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、肝グリコーゲン分解促進による血糖上昇作用を有する。 |
| 成長ホルモン ソマトロピン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 抗インスリン様作用による血糖上昇作用を有する。 |
| 卵胞ホルモン エチニルエストラジオール 結合型エストロゲン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 末梢組織でインスリンの作用に拮抗する。 |
| 経口避妊薬 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 末梢組織でインスリンの作用に拮抗する。 |
| ニコチン酸 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 末梢組織でのインスリン感受性を低下させるため耐糖能障害を起こす。 |
| 濃グリセリン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 代謝されて糖になるため、血糖値が上昇する。 |
| イソニアジド | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 炭水化物代謝を阻害することによる血糖上昇作用を有する。 |
| ダナゾール | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン抵抗性を増強するおそれがある。 |
| フェニトイン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン分泌抑制作用を有する。 |
| ブセレリン酢酸塩 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 耐糖能を悪化させることがある。 |
| フェノチアジン誘導体 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明であるが、動物実験(ラット)において、インスリン分泌が低下したとの報告がある。 |
| 蛋白同化ステロイド メスタノロン | 血糖降下作用の増強による低血糖症状、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 |
| ソマトスタチンアナログ製剤 オクトレオチド酢酸塩 等 | 血糖降下作用の増強による低血糖症状、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン、グルカゴン及び成長ホルモン等互いに拮抗的に調節作用をもつホルモン間のバランスが変化することがある。 |
| ペンタミジンイセチオン酸塩 | 血糖降下作用の増強による低血糖症状、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 膵臓のβ細胞に作用し、初期に低血糖、それに引き続いて高血糖を起こすことがある。 |
| β-遮断剤 プロプラノロール塩酸塩 アテノロール ピンドロール セリプロロール塩酸塩 等 | 血糖降下作用の増強による低血糖症状、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | アドレナリンによる低血糖からの回復反応を抑制する。また、低血糖に対する交感神経系の症状(振戦、動悸等)をマスクし、低血糖を遷延させる可能性がある。また、インスリン感受性は薬剤により増強あるいは減弱することが報告されている。 |
| 炭酸リチウム | 血糖降下作用の増強による低血糖症状、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 インスリン分泌が減少したとの報告、逆に低血糖が発現したとの報告がある。 |
| クロニジン | 血糖降下作用の増強による低血糖症状、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 血糖値が低下したとの報告、逆に血糖値を上昇させたとの報告がある。また、低血糖に対する交感神経系の症状(振戦、動悸等)をマスクし、低血糖を遷延させる可能性がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 低血糖(0.7%)
脱力感、倦怠感、高度の空腹感、冷汗、顔面蒼白、動悸、振戦、頭痛、めまい、嘔気、視覚異常、不安、興奮、神経過敏、集中力低下、精神障害、痙攣、意識障害(意識混濁、昏睡)等があらわれることがある。無処置の状態が続くと低血糖昏睡等を起こし、重篤な転帰(中枢神経系の不可逆的障害、死亡等)をとるおそれがある。
長期にわたる糖尿病、糖尿病性神経障害、β-遮断剤投与あるいは強化インスリン療法が行われている場合では、低血糖の初期の自覚症状(冷汗、振戦等)が通常と異なる場合や、自覚症状があらわれないまま、低血糖あるいは低血糖性昏睡に陥ることがある。
症状が認められた場合には糖質を含む食品を摂取する等、適切な処置を行うこと。α-グルコシダーゼ阻害剤との併用時にはブドウ糖を投与すること。経口摂取が不可能な場合は、ブドウ糖の静脈内投与やグルカゴンの筋肉内投与等、適切な処置を行うこと。
低血糖は臨床的に回復した場合にも、再発することがあるので継続的に観察すること。[2.1、8.2、8.3、8.7、9.1.3、9.2.1、9.3.1、9.8、10.2参照]
長期にわたる糖尿病、糖尿病性神経障害、β-遮断剤投与あるいは強化インスリン療法が行われている場合では、低血糖の初期の自覚症状(冷汗、振戦等)が通常と異なる場合や、自覚症状があらわれないまま、低血糖あるいは低血糖性昏睡に陥ることがある。
症状が認められた場合には糖質を含む食品を摂取する等、適切な処置を行うこと。α-グルコシダーゼ阻害剤との併用時にはブドウ糖を投与すること。経口摂取が不可能な場合は、ブドウ糖の静脈内投与やグルカゴンの筋肉内投与等、適切な処置を行うこと。
低血糖は臨床的に回復した場合にも、再発することがあるので継続的に観察すること。[2.1、8.2、8.3、8.7、9.1.3、9.2.1、9.3.1、9.8、10.2参照]
11.1.2 ショック、アナフィラキシー(いずれも頻度不明)
全身性皮膚反応、血管神経性浮腫、気管支痙攣、低血圧等の異常が認められた場合には投与を中止し、適切な処置を行うこと。
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 過敏症 | 発疹、蕁麻疹、そう痒感 | |
| 肝臓 | 肝機能異常(AST、ALTの上昇等) | |
| 眼 | 糖尿病網膜症の顕在化又は増悪 | |
| 注射部位 | 浮腫、疼痛、そう痒感、硬結 | 発赤、蕁麻疹、腫脹、炎症、リポジストロフィー(皮下脂肪の萎縮・肥厚等)、皮膚アミロイドーシス |
| その他 | ナトリウム貯留、浮腫 |
14. 適用上の注意
14.1 薬剤投与前の注意
14.1.1 本剤はJIS T 3226-2に準拠したA型専用注射針を用いて使用すること。
14.1.2 本剤とA型専用注射針との装着時に液漏れ等の不具合が認められた場合には、新しい注射針に取り替える等の処置方法を患者に十分指導すること。
14.1.3 本剤は他のインスリン製剤との混合により、濁りが生じたり、本剤の作用時間や効果が変化する可能性があるので、本剤のカートリッジにインスリン製剤を補充したり、他のインスリン製剤と混合しないこと。
14.1.4 本剤のカートリッジの内壁に付着物がみられたり、液中に塊や薄片がみられた場合、又は液が変色した場合は使用しないこと。
14.1.5 本剤のカートリッジにひびが入っている場合は使用しないこと。
14.2 薬剤投与時の注意
14.2.1 1本を複数の患者に使用しないこと。
14.2.2 皮下注射は、上腕部、大腿部、腹部、腰部等に行うが、同一部位内で投与する場合は前回の注射箇所より2〜3cm離して注射すること。[8.8参照]
14.2.3 静脈内に投与しないこと。皮下注射したとき、まれに注射針が血管内に入り、注射後直ちに低血糖を起こすことがあるので注意すること。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 インスリン又は経口血糖降下剤の投与中にアンジオテンシン変換酵素阻害剤を投与することにより、低血糖を起こしやすいとの報告がある1)。
15.1.2 ピオグリタゾンと併用した場合、浮腫が多く報告されている。併用する場合には、浮腫及び心不全の徴候を十分観察しながら投与すること。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
(1)正常血糖クランプ試験
日本人健康成人男子15例に、本剤及びNPHヒトインスリン0.4単位/kg注)を腹部に単回皮下投与し、30時間正常血糖クランプ法により本剤の作用を検討したとき、本剤投与後の血清中インスリン濃度は、最初に上昇した後、投与30時間後まで比較的平坦な推移を示した。一方、NPHヒトインスリン投与後においては、投与後2.5〜15時間の間、やや高い濃度で推移し、その後徐々に低下した。また、血糖降下作用を示すグルコース注入率の推移は、NPHヒトインスリン投与時では、投与後2〜6時間の間に明らかなピークを示したが、本剤投与時では投与初期に上昇した後、比較的一定に推移した。グルコース注入率のAUC(0-30hr)に両製剤間で有意な差は認められなかった2)。[7.3、7.5、7.6参照]
日本人健康成人にランタス注及びNPHヒトインスリンを単回皮下投与したときのグルコース注入率の推移(幾何平均値及びフィットカーブ)
(2)作用持続時間
1型糖尿病患者20例に本剤及びNPHヒトインスリン0.3単位/kg注)を大腿部に単回皮下投与し、正常血糖クランプ法で本剤の作用を検討したとき、グルコース注入率の推移から投与時から作用が消失するまでの持続時間は、NPHヒトインスリンでは14.5時間(中央値)であったのに対し、本剤ではほぼ24時間であった。本剤投与時のグルコース注入率はNPHヒトインスリンと比べてより平坦に推移し、明らかなピークは認められなかった。このときの血清中遊離インスリン濃度の推移はグルコース注入率と同様であった3)(外国人データ)。[7.3、7.5、7.6参照]
1型糖尿病患者(外国人)にランタス注及びNPHヒトインスリンを単回皮下投与したときのグルコース注入率の推移
1型糖尿病患者(外国人)にランタス注及びNPHヒトインスリンを単回皮下投与したときの血清中遊離インスリン濃度(幾何平均値)
16.1.2 反復投与
1型糖尿病患者15例に各患者の至適用量(14〜34単位)を11日間、腹部に反復皮下投与したとき、本剤を用いて補正した血清中遊離インスリン濃度推移から本剤の蓄積性は認められなかった4)(外国人データ)。
16.2 吸収
16.2.1 投与部位による比較
健康成人男子12例に、125I-インスリン グラルギン0.2単位/kg注)を上腕部、大腿部及び腹部に単回皮下投与したとき、血清中インスリン濃度、血清中外因性インスリン濃度並びに血糖値の推移に差はみられなかった。また、血清中インスリン濃度及び外因性インスリン濃度のAUC及びCmax、血糖値のAUC及び最大降下度に投与部位間で有意な差は認められなかった。これらのことから本剤の薬理作用に投与部位による差はないと考えられた5)(外国人データ)。
16.8 その他
16.8.1 持続静脈内投与時の血糖降下作用
健康成人20例に本剤及び速効型ヒトインスリンを0.1単位/kgを30分間かけて持続静脈内投与注)し、正常血糖クランプ法を用いて検討したとき、グルコース注入率のAUC(0-6h)の90%信頼区間は同等の許容域の範囲内であり、両剤の血糖降下作用は同等であると判断された6)(外国人データ)。
注)本剤の承認用量は、1日1回4〜20単位を皮下注射するが、その他のインスリン製剤を併用する場合の投与量を含めた維持量は、1日4〜80単位である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第2/3相試験
(1)1型糖尿病試験成績
1型糖尿病試験(1日4回頻回注射法、就寝前投与、28週間:速効型インスリン製剤との併用)は本剤群:128例、NPHヒトインスリン群:130例を対象に行われた。本剤はNPHヒトインスリンと比べHbA1c値(JDS値)の変化度において非劣性であることが検証された(p<0.0001)。また、本剤はNPHヒトインスリンと比べFBG値を有意に低下させた。1日血糖プロファイルでは、投与開始時に比べ28週時で朝食前、夕食前及び夕食後の血糖値を有意に低下させた。症候性低血糖は対照群と比べ切り替え直後(4週間)は増加したが投与期間全体では両群間で差はなかった。夜間低血糖は本剤群で発現件数が少なかった。また、重症低血糖はNPHヒトインスリン群では就寝時間帯に集中するのに対して、本剤群では発現が特定の時間帯に集中することはなかった。有害事象、重篤な低血糖及び抗体産生において群間に有意差は認められなかった。副作用の発現率は、本剤群10.1%(14/138例)であり、主な副作用は、重篤な低血糖症及び糖尿病性網膜症がそれぞれ1.4%(2/138例)であった7)8)。[7.4参照]
| 評価項目 | ランタス注 | NPHヒトインスリン | 検定注1) | ||||||
| n | 投与開始時 | 投与終了時 | 変化度 | n | 投与開始時 | 投与終了時 | 変化度 | ||
| HbA1c(JDS値)(%) | 128 | 7.71 | 7.57 | −0.15 | 130 | 7.84 | 7.83 | −0.00 | p<0.0001 |
| FBG(mg/dL) | 126 | 176.91 | 139.21 | −37.71 | 126 | 169.41 | 173.76 | 4.35 | p=0.0003 |
(2)2型糖尿病試験成績
2型糖尿病試験(1日1回朝食前投与、28週間:スルホニルウレア剤、α-グルコシダーゼ阻害剤及びビグアナイド剤との併用)は本剤群:141例、NPHヒトインスリン群:134例を対象に行われた。本剤NPHヒトインスリンと比べHbA1c値(JDS値)の変化度において非劣性であることが検証された(p<0.0001)。本剤はNPHヒトインスリンと比べFPG及びFBG値を有意に低下させ、朝食前投与でも翌日の朝食前血糖値を低下させた。本試験では、NPHヒトインスリンと比べ昼食前の低血糖発現が少なく、重症低血糖においても1日を通じて特定の時間に集中して発現することはなかった。また、因果関係が否定できない有害事象において両薬剤間で差はなかった。副作用の発現率は、本剤群7.0%(11/158例)であり、主な副作用は、糖尿病性網膜症が2.5%(4/158例)であった。投与28週間後に両薬剤群で抗体上昇が一部で認められたが、臨床症状・検査値には関連する所見はなかった9)10)。[7.4参照]
| 評価項目 | ランタス注 | NPHヒトインスリン | 検定注2) | ||||||
| n | 投与開始時 | 投与終了時 | 変化度 | n | 投与開始時 | 投与終了時 | 変化度 | ||
| HbA1c(JDS値)(%) | 141 | 9.07 | 7.97 | −1.10 | 134 | 9.11 | 8.06 | −1.05 | p<0.0001 |
| FPG(mg/dL) | 132 | 204.42 | 158.14 | −46.29 | 128 | 200.93 | 173.02 | −27.91 | p=0.0052 |
17.1.2 海外第3相臨床試験
(1)中間型インスリン製剤から本剤への切り替え
欧州及び米国で実施された成人の試験におけるNPHヒトインスリン1日2回投与からの切り替え用量の減量の割合は、それぞれ14%及び21%であった。なお、NPHヒトインスリン1日1〜2回投与を受けていた患者を対象に実施した主要な1型糖尿病試験の有効性と安全性成績を以下に示す。
| 1型糖尿病試験(成人)・欧州 | 1型糖尿病試験(成人)・米国 | |||
| ランタス注 | NPHヒトインスリン | ランタス注 | NPHヒトインスリン | |
| GHb変化度(%) | 0.21(283) | 0.10(274) | −0.16(256) | −0.21(262) |
| 空腹時血中グルコース変化度(mmol/L) | −1.17(280) | −0.89(274) | −1.12(244) | −0.94(258) |
| 副作用(%) | 12.7(292) | 13.3(293) | 22.0(264) | 18.1(270) |
(2)小児1型糖尿病
6〜15歳の1型糖尿病患者349例を対象として行われた臨床試験(NPHヒトインスリン対照、28週間投与)において、本剤はNPHヒトインスリンと比べFBG値を有意に低下させた。安全性については、成人と同様に、NPHヒトインスリンと比べて特に差は認められなかった。副作用の発現率は、本剤群7.5%(13/174例)であり、主な副作用は、注射部位腫瘤及び重篤な低血糖反応がそれぞれ1.7%(3/174例)であった。
なお、NPHヒトインスリン1日1回投与からは同単位で切り替えられ、1日2回投与からの切り替え用量の減量の割合は29%であった11)13)。[9.7参照]
なお、NPHヒトインスリン1日1回投与からは同単位で切り替えられ、1日2回投与からの切り替え用量の減量の割合は29%であった11)13)。[9.7参照]
| 1型糖尿病試験(小児) | ||
| ランタス注 | NPHヒトインスリン | |
| GHb変化度(%) | 0.28(155) | 0.27(156) |
| 空腹時血中グルコース変化度(mmol/L) | −1.29(173) | −0.68(172) |
| 副作用(%) | 7.5(174) | 7.4(175) |
17.2 製造販売後調査等
17.2.1 海外市販後臨床試験(小児1型糖尿病)
1〜5歳注3)の1型糖尿病患者125例を対象として行われた臨床試験(NPHヒトインスリン対照、24週間投与)において、主要評価項目を低血糖症発現率として検討した結果、本剤はNPHヒトインスリンに対し、低血糖症発現率に関して非劣性は確認できなかった(非劣性限界値:1.15)。平均1日血中グルコース及びHbA1cの変化量は以下のとおりであった。
| 1型糖尿病試験(小児) | ||
| ランタス注(n=61) | NPHヒトインスリン(n=64) | |
| 低血糖症発現率(件/人年) | 192.75 | 168.91 |
| 発現率比[95%CI]:1.18[0.97-1.44] | ||
| 平均1日血中グルコース変化量(mmol/L) | −0.2 | 0.5 |
| HbA1c変化量(%) | −0.048 | 0.045 |
注3)本剤群において、評価対象症例は2歳以上であった。
18. 薬効薬理
18.1 作用機序
インスリン グラルギンは中性のpH領域で低い溶解性を示すように設計されたヒトインスリンアナログである。インスリン グラルギンの注射剤である本剤は約pH4の無色澄明な溶液であるが、皮下に投与すると直ちに生理的pHにより微細な沈殿物を形成する。皮下に滞留したこの沈殿物からインスリン グラルギンが緩徐に溶解し、皮下から血中に移行することから、24時間にわたりほぼ一定の濃度で明らかなピークを示さない血中濃度推移を示す。
インスリン及びインスリン グラルギンを含むその誘導体の主要な活性は、グルコース代謝の調節にある。インスリン及びその誘導体は、末梢におけるグルコースの取り込み、特に骨格筋及び脂肪による取り込みを促進し、また肝におけるグルコース産生を阻害することによって血糖値を降下させる。更に、蛋白分解を阻害し、蛋白合成を促進するとともに、脂肪細胞における脂肪分解を阻害する。[7.6参照]
インスリン及びインスリン グラルギンを含むその誘導体の主要な活性は、グルコース代謝の調節にある。インスリン及びその誘導体は、末梢におけるグルコースの取り込み、特に骨格筋及び脂肪による取り込みを促進し、また肝におけるグルコース産生を阻害することによって血糖値を降下させる。更に、蛋白分解を阻害し、蛋白合成を促進するとともに、脂肪細胞における脂肪分解を阻害する。[7.6参照]
19. 有効成分に関する理化学的知見
19.1. インスリン グラルギン(遺伝子組換え)
20. 取扱い上の注意
20.1 外箱開封後は遮光して保存すること。
20.2 使用開始後は、遮光して室温保存すること。
20.3 使用中は本剤を冷蔵庫に保存しないこと。
20.4 使用開始後4週間を超えたものは使用しないこと。使用時の安定性試験に基づく。
22. 包装
3mL×2本
23. 主要文献
- Herings R M C,et al., Lancet., 345, 1195-8, (1995)
- 社内資料:健康成人における正常血糖クランプ試験
- 社内資料:1型糖尿病患者における作用持続時間
- Heise T,et al., Diabetic Medicine., 19 (6), 490-5, (2002) »PubMed
- 社内資料:健康成人における投与部位による比較
- 社内資料:健康成人における静脈内投与時の血糖降下作用
- 河盛隆造 他, 臨床医薬, 19 (5), 423-44, (2003)
- 社内資料:国内第2/3相臨床試験/1型糖尿病臨床試験
- 河盛隆造 他, 臨床医薬, 19 (5), 445-64, (2003)
- 社内資料:国内第2/3相臨床試験/2型糖尿病臨床試験
- 社内資料:1型糖尿病患者における1日2回NPH投与からの切り替え
- 社内資料:海外第3相臨床試験/1型糖尿病
- 社内資料:小児1型糖尿病臨床試験
- Danne T,et al., Pediatr Diabetes., 14 (8), 593-601, (2013) »PubMed
- 社内資料:小児1型糖尿病市販後臨床試験
24. 文献請求先及び問い合わせ先
文献請求先
サノフィ株式会社
コールセンター くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
製品情報問い合わせ先
サノフィ株式会社
コールセンター くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
26. 製造販売業者等
26.1 製造販売元
サノフィ株式会社
〒163-1488
東京都新宿区西新宿三丁目20番2号