医薬品情報
| 総称名 | ゼポラス |
|---|---|
| 一般名 | フルルビプロフェン |
| 欧文一般名 | Flurbiprofen |
| 製剤名 | フルルビプロフェンテープ剤 |
| 薬効分類名 | 経皮吸収型鎮痛・消炎剤 |
| 薬効分類番号 | 2649 |
| ATCコード | M01AE09 M02AA19 |
| KEGG DRUG |
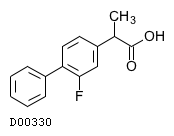
D00330
フルルビプロフェン
|
| KEGG DGROUP |
DG00755
フルルビプロフェン
DG01504
非ステロイド性抗炎症薬 (NSAID)
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年10月 改訂(第2版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ゼポラステープ20mg | ZEPOLAS TAPE20mg | 三笠製薬 | 2649732S3043 | 13.1円/枚 | |
| ゼポラステープ40mg | ZEPOLAS TAPE40mg | 三笠製薬 | 2649732S2047 | 18.2円/枚 |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
下記疾患並びに症状の鎮痛・消炎
変形性関節症、肩関節周囲炎、腱・腱鞘炎、腱周囲炎、上腕骨上顆炎(テニス肘等)、筋肉痛、外傷後の腫脹・疼痛
6. 用法及び用量
1日2回、患部に貼付する。
8. 重要な基本的注意
8.1 消炎鎮痛剤による治療は原因療法ではなく対症療法であることに留意すること。
8.2 慢性疾患(変形性関節症等)に対し本剤を用いる場合には薬物療法以外の療法も考慮すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 気管支喘息のある患者(アスピリン喘息又はその既往歴のある患者を除く)
9.1.2 皮膚感染症のある患者
感染を伴う炎症に対して用いる場合には適切な抗菌剤又は抗真菌剤を併用し、観察を十分に行い、慎重に使用すること。皮膚の感染症を不顕性化するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。シクロオキシゲナーゼ阻害剤を妊娠中期以降の妊婦に使用し、胎児動脈管収縮が起きたとの報告がある。また、シクロオキシゲナーゼ阻害剤(経口剤、坐剤)を妊婦に使用し、胎児の腎機能障害及び尿量減少、それに伴う羊水過少症が起きたとの報告がある。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
貼付部の皮膚の状態に注意しながら慎重に使用すること。
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には使用を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
胸内苦悶、悪寒、冷汗、呼吸困難、四肢しびれ感、血圧低下、血管浮腫、蕁麻疹等があらわれた場合には使用を中止し、適切な処置を行うこと。
11.1.2 喘息発作の誘発(アスピリン喘息)(頻度不明)
11.2 その他の副作用
| 0.1〜5%未満注) | 0.1%未満注) | |
| 皮膚 | そう痒、発赤、発疹 | かぶれ、ヒリヒリ感 |
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 損傷皮膚及び粘膜に使用しないこと。
14.1.2 湿疹又は発疹の部位に使用しないこと。
16. 薬物動態
16.1 血中濃度
16.1.1 健康成人
(1)単回投与
健康成人による単回貼付(14時間、1枚中フルルビプロフェン40mg含有貼付剤)時の最高血中濃度到達時間は13.8±1.3hr、最高血中濃度は38.5±5.9ng/mLであり、半減期は10.4±0.8hrであった1)。(平均値±S.E. n=10)
(2)反復投与
健康成人による反復貼付(1日2回、29日間、1枚中フルルビプロフェン40mg含有貼付剤)による血中濃度は、4日目以降に定常状態となり、剥離48時間後には血中より消失し、蓄積性は認められなかった2)。
16.1.2 生物学的同等性試験
ゼポラステープ20mgと標準製剤(フルルビプロフェン貼付剤、20mg含有)を、それぞれ12枚(直径3cmの円形に打ち抜いたもの)を健康成人男子8名の背中に貼付し、両剤の薬物分布量から生物学的同等性を検討した。その結果、両剤の薬物分布量の平均値の差の90%信頼区間はlog(1.0053)〜log(1.1862)であり、生物学的同等性の判定基準であるlog(0.70)〜log(1.43)の範囲内にあり、両剤の生物学的同等性が確認された3)。
16.3 分布
16.3.1 組織内移行
変形性膝関節症等の患者に1枚中フルルビプロフェン40mg含有貼付剤を適用した場合の薬物の組織移行性を、同量のフルルビプロフェン(40mg)経口投与時と比較した結果、滑膜中濃度はやや低いが、皮下脂肪、筋肉内濃度はほぼ近似した傾向が認められた4)。
貼付剤、内服剤投与時の組織内濃度(6時間値)
16.4 代謝
健康成人による単回貼付(14時間、1枚中フルルビプロフェン40mg含有貼付剤)時の代謝物は経口投与時とほぼ同一であった1)。
16.5 排泄
健康成人による単回貼付(14時間、1枚中フルルビプロフェン40mg含有貼付剤)時の72時間までの尿中総排泄量は1.94%であった1)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 二重盲検比較試験を含む国内143施設、414例について実施された1枚中フルルビプロフェン40mg含有貼付剤の臨床試験の概要は次のとおりである。なお、投与方法は、1日2回であり、投与期間は3日〜4週間である4)5)6)7)8)9)10)11)12)13)14)15)16)17)18)。(有効率は“有効と認められるもの”以上を集計した。)
| 疾患名 | 有効率 (“有効と認められるもの”以上例数/評価例数) |
| 変形性関節症 | 57.8%(52/90) |
| 肩関節周囲炎 | 64.0%(48/75) |
| 腱・腱鞘炎、腱周囲炎 | 64.7%(44/68) |
| 上腕骨上顆炎(テニス肘等) | 59.3%(32/54) |
| 筋肉痛 | 75.0%(33/44) |
| 外傷後の腫脹・疼痛 | 80.7%(67/83) |
18. 薬効薬理
18.1 作用機序
フルルビプロフェンは、プロスタグランジンの合成を阻害することが報告されている(in vitro)19)。シクロオキシゲナーゼ活性を阻害することによりプロスタグランジンの生成を抑制し、鎮痛・抗炎症作用を示すと考えられる。
18.2 鎮痛作用
18.3 抗炎症作用
18.3.1 急性炎症に対する作用
18.3.2 慢性炎症に対する作用
19. 有効成分に関する理化学的知見
19.1. フルルビプロフェン
20. 取扱い上の注意
内袋開封後はチャックを閉めて保存すること。
22. 包装
ゼポラステープ20mg
140枚(7枚×20)
840枚(7枚×120)
ゼポラステープ40mg
140枚(7枚×20)
700枚(7枚×100)
23. 主要文献
- 清水正啓 他, 貼付時の体内動態(社内資料)
- 坪井 実 他, 反復貼付時の血清中薬物濃度(社内資料)
- 三笠製薬株式会社社内資料:生物学的同等性に関する資料
- 菅原幸子 他, Therapeutic Research., 6, 289-294, (1987)
- 菅原幸子 他, 至適濃度の検討等(社内資料)
- 塩川優一 他, 炎症, 7, 203-211, (1987) »DOI
- 七川歓次 他, 炎症, 3, 79-94, (1983) »DOI
- 安田和則 他, 薬理と治療, 10, 3635-3644, (1982)
- 小竹英義 他, 薬理と治療, 10, 4207-4218, (1982)
- 平沼 晃 他, 薬理と治療, 10, 3645-3656, (1982)
- 今泉 司 他, 薬理と治療, 10, 4229-4241, (1982)
- 舘崎慎一郎 他, 薬理と治療, 10, 4219-4227, (1982)
- 林 正岳 他, 薬理と治療, 10, 3657-3669, (1982)
- 服部 奨 他, 薬理と治療, 10, 4243-4255, (1982)
- 青木虎吉 他, 炎症, 9, 335-344, (1989) »DOI
- 青木虎吉 他, 医学と薬学, 20, 1615-1625, (1988)
- 青木虎吉 他, 炎症, 9, 255-262, (1989) »DOI
- 小松原良雄他, 医学と薬学, 21, 761-769, (1989)
- 舛本省三 他, 日本薬理学雑誌, 72, 1025-1031, (1976) »PubMed
- 北川晴雄 他, 医薬品研究, 13, 869-878, (1982)
- 清水敬介 他, Therapeutic Research., 8, 235-236, (1988)
- 久木浩平 他, 医薬品研究, 15, 293-298, (1984)
- 舛本省三 他, 医薬品研究, 13, 879-885, (1982)
24. 文献請求先及び問い合わせ先
文献請求先
三笠製薬株式会社
営業本部学術課
〒176-8585
東京都練馬区豊玉北二丁目3番1号
電話:03-3557-7287
FAX:03-3994-7462
製品情報問い合わせ先
三笠製薬株式会社
営業本部学術課
〒176-8585
東京都練馬区豊玉北二丁目3番1号
電話:03-3557-7287
FAX:03-3994-7462
26. 製造販売業者等
26.1 製造販売元
三笠製薬株式会社
東京都練馬区豊玉北2-3-1