医薬品情報
| 総称名 | ロプレソール |
|---|---|
| 一般名 | メトプロロール酒石酸塩 |
| 欧文一般名 | Metoprolol Tartrate |
| 製剤名 | メトプロロール酒石酸塩徐放錠 |
| 薬効分類名 | 徐放性降圧剤 |
| 薬効分類番号 | 2149 |
| ATCコード | C07AB02 |
| KEGG DRUG |
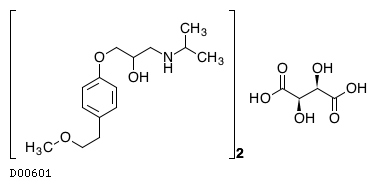
D00601
メトプロロール酒石酸塩
|
| KEGG DGROUP |
DG03231
血圧降下薬
DG01653
抗不整脈薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年1月 改訂(第4版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ロプレソールSR錠120mg | Lopresor SR Tablets 120mg | サンファーマ | 2149010G1055 | 57円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分及び他のβ遮断剤に対し過敏症の既往歴のある患者
2.2 糖尿病性ケトアシドーシス、代謝性アシドーシスのある患者[本症でみられる心筋収縮力抑制を増強するおそれがある。]
2.3 高度の徐脈(著しい洞性徐脈)、房室ブロック(II、III度)、洞房ブロック、洞不全症候群のある患者[心刺激伝導系を抑制し、症状を悪化させるおそれがある。]
2.4 心原性ショック、肺高血圧による右心不全、うっ血性心不全の患者[心筋収縮力を抑制し、症状を悪化させるおそれがある。]
2.5 重症の末梢循環障害(壊疽等)のある患者[症状を悪化させるおそれがある。]
2.6 未治療の褐色細胞腫又はパラガングリオーマの患者[7.、9.1.8参照]
2.7 妊婦又は妊娠している可能性のある女性[9.5参照]
4. 効能または効果
本態性高血圧症(軽症〜中等症)
6. 用法及び用量
通常、成人には1日1回1錠(メトプロロール酒石酸塩として120mg)を朝食後経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
8.1 投与が長期にわたる場合は心機能検査(脈拍・血圧・心電図・X線等)を定期的に行うこと。特に徐脈になったとき及び低血圧を起こした場合には減量又は中止すること。また、必要に応じアトロピンを投与するなど対症療法を行うこと。なお、肝機能、腎機能、血液像等に注意すること。
8.2 類似化合物(プロプラノロール塩酸塩)使用中の狭心症の患者で急に投与を中止したとき、症状が悪化したり、心筋梗塞を起こした症例が報告されているので、休薬を要する場合は徐々に減量し、観察を十分に行うこと。また、患者に医師の指示なしに服薬を中止しないよう注意すること。特に高齢者においては同様の注意をすること。[9.8参照]
8.3 手術前48時間は投与しないことが望ましい。
8.4 めまい、ふらつきがあらわれることがあるので、本剤投与中の患者(特に投与初期)には、自動車の運転等危険を伴う機械の操作に従事させないよう注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 気管支喘息、気管支痙攣のおそれのある患者
気管支拡張剤を併用するなど慎重に投与すること。喘息等の症状を誘発・悪化させるおそれがある。
9.1.2 うっ血性心不全のおそれのある患者
観察を十分に行い、ジギタリス剤を併用するなど慎重に投与すること。心筋収縮力を抑制し、症状を誘発するおそれがある。
9.1.3 低血糖症、コントロール不十分な糖尿病、長期間絶食状態の患者
血糖値に注意すること。低血糖症状を起こしやすく、かつ低血糖の前駆症状である頻脈等の症状をマスクしやすい。
9.1.4 徐脈、房室ブロック(I度)のある患者
心機能に注意すること。心刺激伝導系を抑制し、症状を悪化させるおそれがある。
9.1.5 異型狭心症の患者
症状を悪化させるおそれがある。
9.1.6 甲状腺中毒症の患者
(1)休薬を要する場合には徐々に減量し、観察を十分に行うこと。急に投与を中止すると、症状を悪化させることがある。
(2)頻脈等の中毒症状をマスクするおそれがある。
9.1.7 末梢循環障害(レイノー症候群、間欠性跛行症等)のある患者
症状を悪化させるおそれがある。
9.1.8 褐色細胞腫又はパラガングリオーマの患者
本剤の単独投与により急激に血圧が上昇することがある。[2.6、7.参照]
9.2 腎機能障害患者
9.2.1 重篤な腎障害のある患者
排泄が遅延するおそれがある。
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
代謝が遅延するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。[2.7参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続または中止を検討すること。母乳中へ移行することが報告されている。
9.7 小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.8 高齢者
次の点に注意し、少量から投与を開始するなど患者の状態を観察しながら慎重に投与すること。
・一般に過度の降圧は好ましくないとされている。脳梗塞等が起こるおそれがある。
・休薬を要する場合は、徐々に減量する。[8.2参照]
10. 相互作用
相互作用序文
本剤は、主として肝代謝酵素CYP2D6で代謝されることから、本酵素の活性に影響する薬剤との併用には注意すること。[16.4参照]
薬物代謝酵素用語
CYP2D6
10.2 併用注意
| 交感神経系に対し抑制的に作用する他の薬剤 β遮断剤(チモロール等の点眼剤を含む)等 | 過剰の交感神経抑制を来し、徐脈、血圧低下等があらわれるおそれがあるので、用量に注意すること。 | 共に交感神経抑制作用を有するため。 |
| 血糖降下剤 インスリン グリベンクラミド等 | 血糖降下作用を増強することがある。また、低血糖症状(頻脈等)をマスクすることがあるので、血糖値に注意すること。 | 本剤のβ遮断作用により、低血糖からの回復が遅れることがあり、また、低血糖に伴う交感神経系の症状をマスクする。 |
| カルシウム拮抗剤 ベラパミル ジルチアゼム等 | 相互に作用が増強され、過度の降圧又は心機能抑制があらわれることがあるので、用量に注意すること。 | 共に陰性変時・変力作用、降圧作用を有するため。 |
| クロニジン | クロニジンの投与中止後のリバウンド現象(血圧上昇)を増強するおそれがある。クロニジンの投与を中止する場合には、本剤を数日前に中止し、経過を観察してから行うこと。 | クロニジンの投与中止により血中ノルアドレナリンが増加した場合、本剤のβ遮断作用によりα刺激作用(血管収縮作用)が優位となるため。 |
| ClassI抗不整脈剤 ジソピラミド プロカインアミド等 ClassIII抗不整脈剤 アミオダロン等 | 過度の心機能抑制があらわれることがあるので、用量に注意すること。 | 共に心機能抑制作用を有するため。 |
| 抗不整脈剤 キニジン プロパフェノン アミオダロン等 | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
| ミラベグロン | 本剤のAUCが3.29倍上昇したとの報告があり、本剤の作用が増強するおそれがある。 | ミラベグロンのCYP2D6阻害作用により、本剤の血中濃度が上昇する可能性がある。 |
| 麻酔剤 セボフルラン等 | 過剰の交感神経の抑制を起こす可能性があるので心機能等に注意すること。 | 共に交感神経抑制作用を有するため。 |
| ジギタリス製剤 | 房室伝導時間が延長し、徐脈、房室ブロック等があらわれるおそれがあるので、心機能に注意すること。 | 共に刺激伝導速度の抑制作用を有するため。 |
| 非ステロイド性抗炎症剤 インドメタシン等 | 本剤の降圧作用が減弱することがあるので、用量に注意すること。 | 非ステロイド性抗炎症剤は、血管拡張作用を有する腎プロスタグランジンの合成・遊離を阻害し血圧を上昇させることがある。 |
| 降圧作用を有する他の薬剤 ニトログリセリン タダラフィル等 | 過度の降圧を来すおそれがあるので、用量に注意すること。 | 共に降圧作用を有するため。 |
| シメチジン | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
| 選択的セロトニン再取込み阻害剤 パロキセチン等 | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
| 抗ヒスタミン剤 ジフェンヒドラミン等 | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | これらの薬剤の肝代謝酵素阻害作用により本剤の代謝が抑制されると考えられる。 |
| ヒドララジン | 本剤の血中濃度が上昇し、作用が増強することがあるので、用量に注意すること。 | ヒドララジンは肝血流量を増加させ、本剤の初回通過効果を減少させると考えられる。 |
| リファンピシン | 本剤の血中濃度が低下し、作用が減弱することがあるので、用量に注意すること。 | リファンピシンの肝代謝酵素誘導作用により本剤の代謝が促進されると考えられる。 |
| リドカイン | リドカインの血中濃度を上昇させることがあるので、用量に注意すること。 | 本剤による肝血流量の減少及び肝代謝酵素活性阻害によりリドカインの代謝を遅延させると考えられる。 |
| フィンゴリモド | フィンゴリモドの投与開始時に本剤を併用すると重度の徐脈や心ブロックが認められることがある。 | 共に徐脈や心ブロックを引き起こすおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 心原性ショック(頻度不明)
11.1.2 うっ血性心不全(頻度不明)、房室ブロック(0.3%)、徐脈(2.3%)、洞機能不全(頻度不明)
11.1.3 喘息症状の誘発・悪化(頻度不明)
11.1.4 肝機能障害、黄疸(いずれも頻度不明)
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 眼 | 視覚障害(霧視等) | 涙液分泌減少、結膜炎 |
| 過敏症 | 発疹(乾癬型等) | 光線過敏症、そう痒 |
| 血液 | 血小板減少 | |
| 循環器 | 動悸 | 起立性低血圧注)心室性期外収縮、低血圧、末梢循環障害(四肢の冷え・しびれ等) |
| 呼吸器 | 鼻閉 | 鼻炎、気管支痙攣、息切れ |
| 精神神経系 | めまい・ふらつき、頭痛、不眠、眠気、悪夢 | 幻覚、感覚異常、注意力障害、神経過敏、不安、健忘、錯乱、抑うつ |
| 消化器 | 腹痛、悪心・嘔吐、食欲不振、胸やけ、口渇、腹部膨満感 | 下痢、便秘 |
| 肝臓 | AST上昇、ALT上昇 | |
| その他 | 倦怠感、胸部圧迫感、疲労感、耳鳴、発汗 | 脱毛、難聴、関節痛、筋痙直、体重増加、勃起障害、乾癬悪化、トリグリセライドの上昇、浮腫、性欲減退、CK(CPK)の上昇、味覚異常 |
13. 過量投与
13.1 症状
重度の低血圧、洞性徐脈、房室ブロック、心筋梗塞、心不全、心原性ショック、心停止、気管支痙攣、意識障害(又は昏睡)、痙攣、悪心、嘔吐、チアノーゼ等の症状が起こるおそれがある。
13.2 処置
13.2.1 過度の徐脈
アトロピンを静注する。効果不十分な場合にはβ1刺激剤(ドブタミン等)を投与する。又は一時的にペースメーカーを使用する。
13.2.2 過度の低血圧
低血圧には昇圧剤(アドレナリン、ドパミン、ドブタミン等)を投与する。
13.2.3 心不全
利尿剤、ジギタリス製剤を投与する。
13.2.4 気管支痙攣
β2刺激剤又はアミノフィリンを静注する。
これらの処置の間は患者を常に観察下におくこと。
また、過度の徐脈、過度の低血圧、心不全の処置には、グルカゴンが有効な場合もある。
これらの処置の間は患者を常に観察下におくこと。
また、過度の徐脈、過度の低血圧、心不全の処置には、グルカゴンが有効な場合もある。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.2 薬剤服用時の注意
本剤は二分割して服用可能であるが、徐放性製剤であることよりかまずに服用させること。
15. その他の注意
15.1 臨床使用に基づく情報
β遮断剤服用中の患者では、他の薬剤によるアナフィラキシー反応がより重篤になることがあり、また、通常用量のアドレナリンによる治療に抵抗するとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 血漿中濃度
健康成人を二群に分け、徐放錠(120mg)を朝食後1日1回、普通錠(40mg)を毎食後1日3回cross over投与した場合の平均血漿中濃度推移と各々の血漿中濃度より算出した薬物動態パラメーターは以下のとおりであり、両者のバイオアベイラビリティは同等であった1)。
| Cmax(ng/mL) | Tmax(h) | AUC0-24(ng・h/mL) | ||
| 徐放錠朝食後1日1回服用 | 平均±S.E. | 135.5±23.2 | 3.7±0.2 | 1,251.8±270.1 |
| 普通錠食後1日3回服用 | 平均±S.E. | 105.8±15.5 | 6.7±0.8 | 1,141.3±224.3 |
16.1.2 分割錠の徐放性
健康成人に徐放錠1錠とその1/2分割錠を単回投与した時、分割錠投与時のCmax、AUCは1錠投与時のほぼ半分となり、またT1/2はほとんど差がなく、非分割錠と同等な徐放特性が認められている。
16.1.3 蓄積性
健康成人に徐放錠を1日1回10日間連続投与し、血漿中濃度を検討した結果、蓄積性は認められていない2)。
16.2 吸収
16.2.1 食事の影響
健康成人に徐放錠1錠を投与した時、食後投与でのCmax、AUCは空腹時投与に比べ有意に高く、食事によるバイオアベイラビリティの増加が認められている3)。
16.4 代謝
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内一般臨床試験
本態性高血圧症138例を対象に本剤1日1回60〜240mgを8〜12週間投与した結果、有効率は68.4%(67/98)であり、年齢、罹病期間、投与前の血圧等と降圧効果の間には一定の傾向はなかった。副作用発現率は18.0%(23/128)であった。
17.1.2 国内一般臨床試験(長期投与試験)
本態性高血圧症患者28例を対象に本剤を1日1回、1年間投与した結果、良好な降圧効果が維持された。
副作用発現率は、20.0%(5/25)であり、その内訳は徐脈、項部のつっぱり感、足の冷感、立ちくらみ・風邪様症状、ふらふら感がそれぞれ1例であった8)。
副作用発現率は、20.0%(5/25)であり、その内訳は徐脈、項部のつっぱり感、足の冷感、立ちくらみ・風邪様症状、ふらふら感がそれぞれ1例であった8)。
17.1.3 国内二重盲検比較試験(普通錠との比較試験)
本態性高血圧患者を対象として本剤の単独療法時及びチアジド系利尿降圧剤併用時の有効性及び安全性を普通錠を対照薬として、二重盲検試験を行った。なお、試験対象患者は単独療法群222例(本剤群108例、普通錠群114例)、併用療法群118例(本剤群60例、普通錠群58例)であった。(本剤1日1回と普通錠のプラセボを1日3回服用又は普通錠1日3回と本剤のプラセボを1日1回服用を4〜8週間投与を行った。)徐放錠1日1回投与の有用性が認められている。
副作用発現率は、本剤の単独療法群で11.4%(12/105)、併用療法群で15.0%(9/60)であった。主な副作用は、単独療法群で徐脈3例、倦怠感・脱力感、胃重感等がそれぞれ1例あり、併用投与群で頭痛・頭重感3例、徐脈、倦怠感、胸やけ等がそれぞれ1例であった9)。
副作用発現率は、本剤の単独療法群で11.4%(12/105)、併用療法群で15.0%(9/60)であった。主な副作用は、単独療法群で徐脈3例、倦怠感・脱力感、胃重感等がそれぞれ1例あり、併用投与群で頭痛・頭重感3例、徐脈、倦怠感、胸やけ等がそれぞれ1例であった9)。
17.1.4 国内二重盲検比較試験(ピンドロールとの比較試験)
本態性高血圧患者235例(本剤群122例、ピンドロール群113例)を対象として本剤1錠と対照薬であるピンドロールのプラセボ1カプセル及びチアジド系利尿薬を併用又本剤のプラセボ1錠と対照薬1カプセル及びチアジド系利尿薬を併用して1日1回を12週間投与した二重盲検試験を行った。その結果、有効率は本剤群で78.1%であり両群間に有意差は認められなかった。
副作用発現率は、本剤群で10.2%(12/118)であった。主な副作用は、めまい・ふらつき・起立性低血圧4例、頭痛・頭重感2例、嘔気・嘔吐2例等であった10)。
副作用発現率は、本剤群で10.2%(12/118)であった。主な副作用は、めまい・ふらつき・起立性低血圧4例、頭痛・頭重感2例、嘔気・嘔吐2例等であった10)。
18. 薬効薬理
18.1 作用機序
本剤の降圧作用機序については、まだ十分に解明されていないが、従来のβ遮断剤と同様、長期投与による心拍出量の減少に適応した末梢血管抵抗の減少、レニン分泌抑制、中枢神経抑制、交感神経末端のシナプス前β受容体遮断作用等が考えられている。
18.2 β遮断作用−心血行動態に対する作用
メトプロロール酒石酸塩は健康成人の運動負荷による心拍数の増加、収縮期血圧の上昇をプロプラノロールと同程度に抑制する。その最大効果は、健康成人にメトプロロール酒石酸塩普通錠(以下普通錠と略す)を1回経口投与したとき、投与1〜2時間後にみられ、6〜8時間後においても抑制効果が認められている11)12)13)14)。一方、イソプロテレノール負荷による頻脈を抑制する作用はプロプラノロールより弱い12)。
健康成人に普通錠を1回経口投与したとき、安静時の心拍数、心拍出量は投与1時間後をピークとして有意に減少するが、血圧はほとんど変化を示さない15)。高血圧症患者に連続経口投与した場合には、心拍数、心拍出量の減少と共に血圧の有意な低下が認められている16)。なお、メトプロロール酒石酸塩には、内因性β受容体刺激作用は認められていない17)(ネコ)。
健康成人に普通錠を1回経口投与したとき、安静時の心拍数、心拍出量は投与1時間後をピークとして有意に減少するが、血圧はほとんど変化を示さない15)。高血圧症患者に連続経口投与した場合には、心拍数、心拍出量の減少と共に血圧の有意な低下が認められている16)。なお、メトプロロール酒石酸塩には、内因性β受容体刺激作用は認められていない17)(ネコ)。
18.3 β1選択性
18.4 降圧効果
18.5 血圧日内変動
本態性高血圧症患者にメトプロロール酒石酸塩徐放錠を1日1回投与したとき、24時間にわたって安定した降圧効果が持続し、血圧日内変動幅には影響を与えないことが認められている25)。
19. 有効成分に関する理化学的知見
19.1. メトプロロール酒石酸塩
22. 包装
100錠[10錠(PTP)×10]
23. 主要文献
- 清水秀利ほか, 薬物動態, 6 (4), 567-572, (1991) »DOI
- 清水秀利ほか, 薬物動態, 6 (4), 579-585, (1991) »DOI
- 清水秀利ほか, 薬物動態, 6 (4), 573-578, (1991) »DOI
- Bertz,R.J.et al., Clin.Pharmacokinet., 32 (3), 210-258, (1997) »PubMed
- Regardh,C.G.et al., J.Pharmacokinet.Biopharm., 2 (4), 347-364, (1974) »PubMed
- Borg,K.O.et al., Acta Pharmacol.Toxicol., 36 (Suppl.V), 125-135, (1975)
- Kendall,M.J.et al., Eur.J.Drug Metab.Pharmacokinet., 2 (2), 73-80, (1977)
- 柊山幸志郎ほか, 臨牀と研究, 64 (1), 243-252, (1987)
- 吉利 和ほか, 薬理と治療, 15 (1), 209-241, (1987)
- 武田忠直ほか, 臨床医薬, 7 (4), 835-873, (1991)
- 榊原 博ほか, 薬理と治療, 7 (5), 1334-1340, (1979)
- Johnsson,G.et al., Acta Pharmacol.Toxicol., 36 (Suppl.V), 69-75, (1975)
- Johnsson,G.et al., Acta Pharmacol.Toxicol., 36 (Suppl.V), 31-44, (1975)
- Regardh,C.G.et al., Acta Pharmacol.Toxicol., 36 (Suppl.V), 45-58, (1975)
- 松下 哲ほか, 心臓, 10 (7), 676-680, (1978) »DOI
- 築山久一郎ほか, 心臓, 9 (8), 698-707, (1977) »DOI
- Ablad,B.et al., Life Sci., 12/I (3), 107-119, (1973)
- 滝島 任ほか, 臨牀と研究, 54 (10), 3353-3360, (1977)
- Thiringer,G.et al., Eur.J.Clin.Pharmacol., 10 (3/4), 163-170, (1976)
- 可部順三郎ほか, アレルギー, 30 (1), 33-44, (1981) »DOI
- 牧野荘平ほか, アレルギーの臨床, 1 (5), 57-64, (1981)
- 滝島 任ほか, 薬理と治療, 8 (7), 2451-2457, (1980)
- Johnsson,G., Acta Pharmacol.Toxicol., 36 (Suppl.V), 59-68, (1975)
- 山下秀光ほか, 臨牀と研究, 57 (3), 907-914, (1980)
- 吉利 和ほか, 薬理と治療, 15 (1), 173-187, (1987)
24. 文献請求先及び問い合わせ先
文献請求先
サンファーマ株式会社
くすり相談センター
〒105-0011
東京都港区芝公園1-7-6
電話:0120-22-6880 受付時間:9時〜17時(土、日、祝日、その他当社の休業日を除く)
製品情報問い合わせ先
サンファーマ株式会社
くすり相談センター
〒105-0011
東京都港区芝公園1-7-6
電話:0120-22-6880 受付時間:9時〜17時(土、日、祝日、その他当社の休業日を除く)
26. 製造販売業者等
26.1 製造販売元
サンファーマ株式会社
東京都港区芝公園1-7-6