医薬品情報
| 総称名 | ノイエル |
|---|---|
| 一般名 | セトラキサート塩酸塩 |
| 欧文一般名 | Cetraxate Hydrochloride |
| 製剤名 | セトラキサート塩酸塩製剤 |
| 薬効分類名 | 粘膜防御性 胃炎・胃潰瘍治療剤 |
| 薬効分類番号 | 2329 |
| KEGG DRUG |
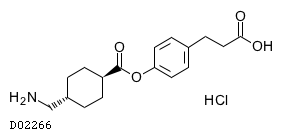
D02266
セトラキサート塩酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年2月 改訂(第1版)

|
4.効能または効果 6.用法及び用量 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ノイエルカプセル200mg | NEUER Capsules 200mg | アルフレッサファーマ | 2329004M1175 | 6.8円/カプセル | |
| ノイエル細粒40% | NEUER Fine Granules 40% | アルフレッサファーマ | 2329004C1129 |
4. 効能または効果
6. 用法及び用量
通常成人、セトラキサート塩酸塩として1回200mgを1日3〜4回食後及び就寝前に経口投与する。
年齢、症状により適宜増減する。
年齢、症状により適宜増減する。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 血栓のある患者(脳血栓、心筋梗塞、血栓性静脈炎等)
本剤は代謝されてトラネキサム酸を生じるので、血栓を安定化するおそれがある。
9.1.2 消費性凝固障害のある患者
本剤は代謝されてトラネキサム酸を生じるので、血栓を安定化するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
11. 副作用
11.2 その他の副作用
| 0.1〜1%未満 | 頻度不明 | |
| 消化器 | 口渇、悪心・嘔吐、下痢、便秘、胃部不快感・膨満感 | − |
| 過敏症 | 発疹、そう痒感 | − |
| その他 | − | AST上昇、ALT上昇等 |
14. 適用上の注意
<カプセル>
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
健康成人にセトラキサート塩酸塩200mgを単回経口投与した場合、未変化体は投与1時間後には、定量限界以下であった。
なお、主代謝物であるトラネキサム酸のTmaxは3.05±0.25時間、Cmaxは1.75±0.13μg/mL、t1/2は1.73±0.09時間であった。
なお、主代謝物であるトラネキサム酸のTmaxは3.05±0.25時間、Cmaxは1.75±0.13μg/mL、t1/2は1.73±0.09時間であった。
16.3 分布
ラットに14C-セトラキサート塩酸塩300mg/kgを経口投与すると、胃壁と副腎を除く全ての臓器において投与後8時間に最高放射能濃度が認められ、それらの推移は全血液中濃度推移と同様な傾向にあった。また、臓器別の放射能分布では、胃壁>腎>肝>副腎・肺>全血・膵・脾・心>筋>睾丸・脂肪・脳の順に高く、胃壁への取り込みは投与後、短時間で顕著であった。
16.4 代謝
13C-セトラキサート塩酸塩標識化合物を健康成人に投与して検討した結果、尿中に未変化体及びTranexamic acid(TA)、trans-4-hydroxymethylcyclohexanecarboxylic acid、trans-hexahydroterephthalic acid、N-acetyltranexamic acidが検出された。
未変化体及び上記4種類の代謝物を含めて、それらの総尿中排泄率は0〜24時間で投与量の約40%であった。このうち主代謝物はTAで全体の98%を占め、未変化体は極めて少なく、投与量の0.02〜0.04%であった。
未変化体及び上記4種類の代謝物を含めて、それらの総尿中排泄率は0〜24時間で投与量の約40%であった。このうち主代謝物はTAで全体の98%を占め、未変化体は極めて少なく、投与量の0.02〜0.04%であった。
16.5 排泄
健康成人にセトラキサート塩酸塩200mg単回投与後、6〜8時間まで微量ながら未変化のまま尿中に排泄が続き、総排泄量は13〜47μg(平均27.4μg)であった。この排泄量は投与量に対し0.007〜0.024%(平均0.014%)であり、8時間以後の尿中排泄はほとんど認められなかった。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<急性胃炎、慢性胃炎の急性増悪期>
17.1.1 国内臨床試験
胃内視鏡によりびらん、出血、発赤を主とした異常所見を有し、急性胃粘膜病変と診断された患者218例を対象に本剤の下記2用量の効果を二重盲検比較試験で検討した結果、800mg/日投与群での効果が優れている傾向が認められた。
| 改善率(%)〔改善例/総症例〕 | |
| 200mg/日投与群 | 63.1〔70/111〕 |
| 800mg/日投与群 | 73.8〔79/107〕 |
17.1.2 国内臨床試験
急性胃炎及び慢性胃炎の急性増悪と診断された患者を対象に本剤投与群に800mg/日並びにアルジオキサ投与群に400mg/日を4週間投与した二重盲検比較試験での改善率(全般改善度の中等度改善以上)は次のとおりであった。
| 改善率(%)〔改善例/総症例〕 | |||
| 1週 | 2週 | 4週 | |
| 本剤投与群 | 82.1〔23/28〕 | 75.9〔41/54〕 | 73.1〔57/78〕 |
| アルジオキサ投与群 | 68.4〔13/19〕 | 85.0〔34/40〕 | 77.6〔45/58〕 |
副作用の発生率は本剤群1.0%(発疹1例)、アルジオキサ群2.1%(便秘、悪心、各1例)であった。
17.1.3 国内臨床試験
びらん性胃炎、表層性胃炎等の胃炎患者を対象とした一般臨床試験では、72%(161/224)に改善効果が認められている。
<胃潰瘍>
17.1.4 国内臨床試験
胃潰瘍患者89例を対象に本剤投与群(本剤800mg/日+水酸化アルミゲル;44例)とプラセボ投与群(乳糖+水酸化アルミゲル;45例)の効果を二重盲検比較試験(8週間投与)で検討した結果、潰瘍治癒効果は本剤投与群が有意に優れていた1)。
| 治癒率(%)〔治癒例/総症例〕 | |
| 本剤投与群 | 88.6〔39/44〕注) |
| プラセボ投与群 | 62.2〔28/45〕注) |
17.1.5 国内第III相試験
消化性潰瘍患者を対象に本剤800mg/日並びにゲファルナート300mg/日を12週間投与した二重盲検比較試験での累積治癒率は次のとおりである。本剤投与群において、8週、12週で有意な差が認められた。
| 治癒率(%)〔治癒例/総症例〕 | |||
| 4週 | 8週注) | 12週注) | |
| 本剤投与群 | 28.2〔31/110〕 | 60.9〔67/110〕 | 72.7〔80/110〕 |
| ゲファルナート投与群 | 23.3〔27/116〕 | 46.6〔54/116〕 | 55.2〔64/116〕 |
副作用の種類及び出現率に両群間に差異は認められなかった。
17.1.6 国内臨床試験
胃潰瘍患者712症例を対象とした一般臨床試験の結果は、次のとおりであった。
| 治癒率(%)〔治癒例/総症例〕 | |
| 本剤単独 | 70.1〔384/548〕 |
| 他剤併用 (抗コリン薬、制酸薬、抗潰瘍薬) | 79.9〔131/164〕 |
18. 薬効薬理
18.1 作用機序
本剤は胃粘膜微小循環の改善を主作用とし、胃粘膜内プロスタグランジンE2、I2生合成増加作用、胃粘膜粘液の保持及び合成促進作用等のいわゆるcytoprotective(細胞保護)作用とともに、粘膜内でのペプシノーゲンの活性化抑制・生成抑制、抗カリクレイン作用による胃液分泌の抑制等の攻撃系因子抑制作用を併せもち、防御・攻撃因子の両面に作用することにより胃粘膜病変を治癒させる薬剤である。
18.2 各種実験胃粘膜病変に対する作用
18.3 胃粘膜微小循環の改善作用
18.4 胃粘膜内プロスタグランジンE2、I2生合成増加作用
ラット胃粘膜内プロスタグランジンE2、6-ケト-プロスタグランジンF1α増加作用を示した。このことはプロスタグランジンE2、I2の生合成を増加すると考えられる。
18.5 胃粘膜粘液保持・合成促進作用
ラット胃粘膜病変病態モデル(エチルアルコール、アスピリン、低酸素血症、熱傷ストレス、寒冷拘束ストレス・インドメタシン)において粘液の減少を抑制し、粘液成分としては、ヘキソサミン、シアル酸、糖蛋白等の維持が認められた。これらの作用は、粘液合成の促進に基づくと考えられている。
18.6 粘膜内ペプシノーゲンの活性化抑制作用
ラットのアスピリン投与時にみられる粘膜内ペプシノーゲンの活性化を抑制し、胃粘膜の自己消化を抑制することが認められている。また、その際にみられる水素イオンの逆拡散(back diffusion)及びタウロコール酸塩(胆汁酸塩)投与時の粘膜障害時にみられる水素イオンの逆拡散を抑制することが認められている。
18.7 抗カリクレイン作用による胃液分泌抑制作用
カリクレインに拮抗して、ラットにおける胃酸・ペプシンの分泌を抑制することが認められている。
19. 有効成分に関する理化学的知見
19.1. セトラキサート塩酸塩
20. 取扱い上の注意
<カプセル>
温度、湿度、光の影響により、カプセルの退色が認められることがあるため、開封後は、これらの影響を避けて保存することが望ましい。
22. 包装
<カプセル>
100カプセル[10カプセル(PTP)×10]
500カプセル[10カプセル(PTP)×50]
1000カプセル[10カプセル(PTP)×100]
2100カプセル[21カプセル(PTP)×100]
1000カプセル[プラスチック瓶、バラ]
<細粒>
0.5g×1200[6包×200、乾燥剤入り]
0.5g×2400[6包×400、乾燥剤入り]
0.5g×2520[3包×840、乾燥剤入り]
100g[アルミ袋、バラ]
1kg[アルミ袋、バラ]
23. 主要文献
- 三好秋馬 他, 内科宝函, 24 (4), 105-115, (1977)
- 橋爪武司 他, 応用薬理, 12 (5), 691-702, (1976)
- 川野 淳 他, 診療と新薬, 19 (1), 27-32, (1982)
- 宮本二郎 他, Prog.Med, 2 (6), 922-928, (1982)
24. 文献請求先及び問い合わせ先
文献請求先
アルフレッサファーマ株式会社
製品情報部
〒540-8575
大阪市中央区石町二丁目2番9号
電話:06-6941-0306
FAX:06-6943-8212
製品情報問い合わせ先
アルフレッサファーマ株式会社
製品情報部
〒540-8575
大阪市中央区石町二丁目2番9号
電話:06-6941-0306
FAX:06-6943-8212
26. 製造販売業者等
26.1 製造販売元
アルフレッサファーマ株式会社
大阪市中央区石町二丁目2番9号