医薬品情報
| 総称名 | エホチール |
|---|---|
| 一般名 | エチレフリン塩酸塩 |
| 欧文一般名 | Etilefrine Hydrochloride Etilefrine |
| 製剤名 | エチレフリン塩酸塩製剤 |
| 薬効分類名 | 昇圧剤 |
| 薬効分類番号 | 2119 |
| ATCコード | C01CA01 |
| KEGG DRUG |
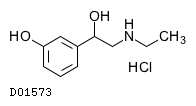
D01573
エチレフリン塩酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年7月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| エホチール注10mg | Effortil Injection | サノフィ | 2119401A1057 | 63円/管 | 劇薬, 処方箋医薬品 |
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
起立性低血圧、各種疾患若しくは状態に伴う急性低血圧又はショック時の補助治療
6. 用法及び用量
通常成人には、1回0.2〜1mL(エチレフリン塩酸塩として2〜10mg)を皮下注射、筋肉内注射又は静脈内注射する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
8.1 ショックの緊急治療の原則は換気の確保、輸液及び心拍出量の増加と昇圧である。ショック時の循環動態はショックを起こした原因及び病期によって異なるので、昇圧剤の選択及び使用時期については十分注意すること。
また、本剤は血圧下降等の応急処置剤として用いるべき薬剤であり、輸血又は輸液にかわるものではない。
また、本剤は血圧下降等の応急処置剤として用いるべき薬剤であり、輸血又は輸液にかわるものではない。
8.2 過度の昇圧反応を起こすことがあり、急性肺水腫、不整脈、心停止等があらわれることがあるので、過量投与にならないよう注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心室性頻拍のある患者
治療上やむを得ないと判断される場合を除き、投与しないこと。刺激伝導系の促進により、症状を悪化させるおそれがある。
9.1.2 高血圧の患者
血圧を上昇させるおそれがある。
9.1.3 重篤な動脈硬化症の患者
症状を悪化させるおそれがある。
9.1.4 甲状腺機能亢進症の患者
心悸亢進、頻脈等を悪化させるおそれがある。
9.1.5 心疾患のある患者
心筋酸素消費量の増大により、症状を悪化させるおそれがある。
9.1.6 徐脈のある患者
反射性の拍動数の増加を抑制するおそれがある。
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意
| ハロゲン化吸入麻酔剤 ハロタン | 期外収縮、徐脈等があらわれることがある。 | ハロタン等の麻酔剤は本剤に対する心筋の感受性を高めるため、不整脈がおこりやすくなる。 |
| 分娩促進剤 オキシトシン エルゴタミン | 血圧の異常上昇をきたすことがあるので、その様な場合はクロルプロマジンの静注を行う。 | 本剤の昇圧作用と麦角アルカロイドの末梢血管収縮作用により血圧が上昇する。 |
11. 副作用
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | |
| 循環器注) | 心悸亢進、胸内苦悶、徐脈、血圧異常上昇、呼吸困難 | |
| 精神神経系 | 頭痛 | 不眠、振戦 |
| 過敏症 | 発疹 |
13. 過量投与
13.1 症状
脳内出血、肺水腫、頭痛等があらわれることがあるので、特に感受性の高い患者には注意すること。
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 静脈内注射
下記の点に留意すること。
・血圧の異常上昇を来さないよう慎重に投与すること。
・点滴静注で大量の注射液が血管外に漏出した場合、局所の虚血性壊死があらわれることがあるので、注意すること。
・本剤により過度の血圧上昇を生じた場合には、α遮断剤(フェントールアミン等)を使用すること。
14.1.2 皮下・筋肉内注射
動物実験で充血、出血、変性等の局所障害が認められるので、組織・神経等への影響を避けるため、下記の点に留意すること。
・神経走行部位を避けるよう注意して注射すること。
・繰り返し注射する場合には、例えば左右交互に注射するなど、注射部位を変えて行うこと。
なお、乳幼小児には連用しないことが望ましい。
なお、乳幼小児には連用しないことが望ましい。
・注射針を刺入したとき、激痛を訴えたり、血液の逆流をみた場合には、直ちに針を抜き、部位を変えて注射すること。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人にエチレフリン塩酸塩0.75mg注1)を静脈内投与した場合、血中濃度の半減期は約2時間であった1)(外国人データ)。
注1)承認用量は0.2〜1mL(エチレフリン塩酸塩として2〜10mg)である。
16.3 分布
静脈内投与した場合、2分で全身に分布し、心筋及び肝に大量に分布した。脳内への分布は認められなかった2)(ラット)。
16.4 代謝
主代謝産物はエチレフリンのグルクロン酸及び硫酸抱合体であった1)(外国人データ)。
16.5 排泄
健康成人にエチレフリン塩酸塩0.75mg注2)を静脈内投与したとき、24時間で約78%が尿中に排泄された。未変化体の尿中排泄率は約28%であった1)(外国人データ)。
注2)承認用量は0.2〜1mL(エチレフリン塩酸塩として2〜10mg)である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
国内で実施された臨床試験の結果、承認された効能・効果に対する本剤の臨床効果が認められた。
17.2 製造販売後調査等
再評価時の調査症例1,025例中、本剤の副作用は6例(0.59%)であり、主な副作用は心悸亢進4例(0.39%)、頭痛3例(0.29%)であった。また、臨床検査値においては特に一定の傾向を示す変動は認められていない。
18. 薬効薬理
18.1 作用機序
本剤は交感神経刺激作用(α,β刺激)により、心拍出量を増加させる。また、静脈緊張度の改善により、循環血流量を増加させ、血圧を上昇させる。
18.2 心筋収縮力増強作用
18.3 血圧上昇作用
用量依存的に血圧を上昇させる4)(イヌ)。
18.4 臨床薬理
低血圧患者に皮下注射した場合、心拍出量の増加、血圧の上昇がみられる。末梢血管抵抗は減少する5)。
19. 有効成分に関する理化学的知見
19.1. エチレフリン塩酸塩
20. 取扱い上の注意
外箱開封後は遮光して保存すること。
22. 包装
1mL(1管)×10管
1mL(1管)×50管
23. 主要文献
- Hengstmann J H et al., Eur J Clin Pharmacol., 9, 179-87, (1975)
- 社内資料:薬物動態(ラット)
- Unna K et al., Arch Exp Pathol Pharmakol., 213, 207-34, (1951)
- 橋本虎六 ほか, 応用薬理, 3 (1), 27-33, (1969)
- 斉藤十六 ほか, 内科の領域, 9 (1), 75-80, (1961)
24. 文献請求先及び問い合わせ先
文献請求先
サノフィ株式会社
コールセンター くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
製品情報問い合わせ先
サノフィ株式会社
コールセンター くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
26. 製造販売業者等
26.1 製造販売元
サノフィ株式会社
〒163-1488
東京都新宿区西新宿三丁目20番2号