医薬品情報
| 総称名 | メイアクトMS |
|---|---|
| 一般名 | セフジトレン ピボキシル |
| 欧文一般名 | Cefditoren Pivoxil |
| 薬効分類名 | 経口用セフェム系抗生物質製剤 |
| 薬効分類番号 | 6132 |
| ATCコード | J01DD16 |
| KEGG DRUG |
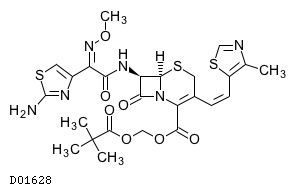
D01628
セフジトレンピボキシル
|
| KEGG DGROUP |
DG01488
セフェム系抗生物質
|
| JAPIC | 添付文書(PDF) |
添付文書情報2021年12月 改訂(第1版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 12.臨床検査結果に及ぼす影響 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| メイアクトMS小児用細粒10% | MEIACT MS FINE GRANULES | Meiji Seikaファルマ | 6132015C1103 | 192.8円/g | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
小児
<適応菌種>
<適応症>
成人(嚥下困難等により錠剤の使用が困難な場合)
<適応菌種>
<適応症>
5. 効能または効果に関連する注意
<咽頭・喉頭炎、扁桃炎(扁桃周囲炎、扁桃周囲膿瘍を含む)、急性気管支炎、中耳炎、副鼻腔炎>
「抗微生物薬適正使用の手引き」1)を参照し、抗菌薬投与の必要性を判断した上で、本剤の投与が適切と判断される場合に投与すること。
6. 用法及び用量
小児
<肺炎、中耳炎、副鼻腔炎の場合>
通常、小児にはセフジトレン ピボキシルとして1回3mg(力価)/kgを1日3回食後に経口投与する。
なお、必要に応じて1回6mg(力価)/kgまで投与できるが、成人での上限用量の1回200mg(力価)1日3回(1日600mg(力価))を超えないこととする。
なお、必要に応じて1回6mg(力価)/kgまで投与できるが、成人での上限用量の1回200mg(力価)1日3回(1日600mg(力価))を超えないこととする。
<上記以外の疾患の場合>
通常、小児にはセフジトレン ピボキシルとして1回3mg(力価)/kgを1日3回食後に経口投与する。
なお、年齢及び症状に応じて適宜増減するが、成人での上限用量の1回200mg(力価)1日3回(1日600mg(力価))を超えないこととする。
なお、年齢及び症状に応じて適宜増減するが、成人での上限用量の1回200mg(力価)1日3回(1日600mg(力価))を超えないこととする。
成人(嚥下困難等により錠剤の使用が困難な場合)
通常、成人にはセフジトレン ピボキシルとして1回100mg(力価)を1日3回食後に経口投与する。
なお、年齢及び症状に応じて適宜増減するが、重症又は効果不十分と思われる場合は、1回200mg(力価)を1日3回食後に経口投与する。
なお、年齢及び症状に応じて適宜増減するが、重症又は効果不十分と思われる場合は、1回200mg(力価)を1日3回食後に経口投与する。
8. 重要な基本的注意
8.1 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
8.2 ショックを起こすおそれがあるので、十分な問診を行うこと。[11.1.1参照]
8.3 肝機能障害があらわれることがあるので、定期的に検査を行うこと。[11.1.5参照]
8.4 急性腎障害等の重篤な腎障害があらわれることがあるので、定期的に検査を行うこと。[11.1.6参照]
8.5 無顆粒球症、溶血性貧血があらわれることがあるので、定期的に検査を行うこと。[11.1.7参照]
8.6 投与期間が長い患者では、臨床検査値異常(AST、ALT上昇、好酸球増多等)の発現率が高くなる傾向がみられるため、定期的に検査を行うなど注意すること。[11.2参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 セフェム系又はペニシリン系抗生物質に対し過敏症の既往歴のある患者(ただし、本剤に対し過敏症の既往歴のある患者には投与しないこと)
9.1.2 本人又は両親、兄弟に気管支喘息、発疹、蕁麻疹等のアレルギー症状を起こしやすい体質を有する患者
9.1.3 経口摂取の不良な患者又は非経口栄養の患者、全身状態の悪い患者
観察を十分に行うこと。ビタミンK欠乏症状があらわれることがある。
9.2 腎機能障害患者
9.2.1 高度の腎障害のある患者
投与間隔をあけて使用すること。血中濃度が持続する。[16.6.1参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。妊娠後期にピボキシル基を有する抗生物質を投与された妊婦と、その出生児において低カルニチン血症の発現が報告されている。[11.1.8参照]
9.7 小児等
9.7.1 低出生体重児、新生児を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.7.2 3歳未満で1回6mg(力価)/kgを1日3回投与した場合、下痢・軟便の発現頻度が高いので、これらの症状が認められた場合には症状に応じて対症療法等の適切な処置を行うこと。肺炎、中耳炎、副鼻腔炎の患者を対象とした1回6mg(力価)/kg1日3回による臨床試験における下痢・軟便の副作用発現率は3歳未満で36.2%(17例/47例)、3歳以上で16.2%(11例/68例)であった。
9.7.3 カルニチンの低下に注意すること。血清カルニチンが低下する先天性代謝異常であることが判明した場合には投与しないこと。小児(特に乳幼児)においてピボキシル基を有する抗生物質の投与により、低カルニチン血症に伴う低血糖があらわれることがある。[11.1.8参照]
9.8 高齢者
次の点に注意して、投与間隔を変更するなどして投与すること。高齢者とそれ以外の成人では副作用に差がみられなかったが、一般に生理機能が低下していることが多い。
・本剤は腎機能低下患者で排泄に遅延が認められているので、血中濃度が高く推移する可能性がある。[16.6.1参照]
・類薬で、ビタミンK欠乏による出血傾向があらわれるとの報告がある。
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
<共通>
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
不快感、口内異常感、喘鳴、眩暈、便意、耳鳴、発汗等の異常が認められた場合には、投与を中止し、適切な処置を行うこと。[8.2参照]
11.1.2 偽膜性大腸炎等の血便を伴う重篤な大腸炎(頻度不明)
腹痛、頻回の下痢があらわれた場合には、直ちに投与を中止し、適切な処置を行うこと。
11.1.3 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、多形紅斑(いずれも頻度不明)
11.1.4 間質性肺炎、PIE症候群(いずれも頻度不明)
発熱、咳嗽、呼吸困難、胸部X線像異常、好酸球増多等を伴う間質性肺炎、PIE症候群等があらわれることがあるので、観察を十分に行い、このような症状があらわれた場合には、投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.5 肝機能障害(頻度不明)
黄疸、AST、ALT、Al-Pの著しい上昇等を伴う肝機能障害があらわれることがある。[8.3参照]
11.1.6 急性腎障害等の重篤な腎障害(頻度不明)[8.4参照]
11.1.7 無顆粒球症、溶血性貧血(いずれも頻度不明)[8.5参照]
<小児>
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 過敏症 | 発疹 | 蕁麻疹、紅斑、そう痒、発熱 | リンパ節腫脹、関節痛 |
| 血液 | 顆粒球減少、好酸球増多注) | 血小板減少 | |
| 肝臓 | AST、ALT、Al-Pの上昇注) | 黄疸 | |
| 腎臓 | BUN上昇、蛋白尿 | 血中クレアチニン上昇 | |
| 消化器 | 下痢、軟便、嘔気、胃不快感、腹痛 | 腹部膨満感、悪心、嘔吐 | |
| 菌交代症 | 口内炎 | カンジダ症 | |
| ビタミン欠乏症 | ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等)、ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) | ||
| その他 | 頭痛、めまい | 浮腫、しびれ |
12. 臨床検査結果に及ぼす影響
12.1 テステープ反応を除くベネディクト試薬、フェーリング試薬による尿糖検査では偽陽性を呈することがあるので注意すること。
12.2 直接クームス試験陽性を呈することがあるので注意すること。
14. 適用上の注意
14.1 薬剤交付時の注意
分包製剤は湿気を避けて保存し、服用時に開封するよう指示すること。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与(顆粒剤注))
腎機能の正常な小児患者に1回3mg/kg、6mg/kgをそれぞれ食後単回経口投与した場合、セフジトレンの血清中濃度・薬物動態パラメータは、図1・表1のとおりであり、用量依存性を示した3)。
図1 腎機能の正常な小児患者のセフジトレンの血清中濃度
| 投与量 | Cmax(μg/mL) | T1/2(hr) | AUC0→∞(μg・hr/mL) |
| ●:3mg/kg(n=19) | 1.45 | 2.25 | 7.16 |
| ○:6mg/kg(n=18) | 2.85 | 1.68 | 11.90 |
16.3 分布
16.4 代謝
16.5 排泄
16.5.1 尿中排泄(顆粒剤注))
腎機能が正常な小児患者に1回3mg/kg、6mg/kgをそれぞれ食後単回経口投与した場合、セフジトレンとしての尿中排泄率(0〜8時間)は、それぞれ約20%、17%であった3)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者(旧錠剤注))
腎機能障害患者及び人工透析導入患者(いずれも成人)に200mgを食後単回経口投与した場合、セフジトレンの血清中濃度・薬物動態パラメータは、図2・表2のとおりであり、いずれの場合も高値で推移し、腎機能の障害の程度に応じたT1/2の遅延が認められた。また、尿中排泄率は腎機能の障害の程度が大きくなるにつれて低下し、排泄の遅延が認められた14)。[9.2.1、9.8参照]
図2 腎機能障害患者におけるセフジトレンの血清中濃度
| 患者条件〔Ccr(mL/min)〕 | 例数 | Tmax(hr) | Cmax(μg/mL) | T1/2(hr) | AUC0→∞(μg・hr/mL) |
| 軽度〔51〜70〕 | 3 | 2 | 2.32 | 1.13 | 10.2 |
| 中等度〔30〜50〕 | 4 | 4 | 2.17 | 2.06 | 16.4 |
| 高度〔<30〕 | 2 | 8 | 3.70 | 5.68 | 53.5 |
| 透析患者※ | 1 | 6 | 4.60 | 5.37 | 50.2 |
注)本剤と旧細粒剤、旧細粒剤と顆粒剤及びメイアクトMS錠と旧錠剤の生物学的同等性が確認されている。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験(顆粒剤注1)の承認時)
小児細菌感染症患者を対象とした臨床試験での有効率は次のとおりであった3)。
(1)皮膚科領域感染症
表在性皮膚感染症(伝染性膿痂疹)、深在性皮膚感染症(蜂巣炎、化膿性爪囲(廓)炎)、リンパ管・リンパ節炎(リンパ管(節)炎)、慢性膿皮症(皮下膿瘍)に対する有効率は93.1%(54/58)であった。
(2)外科領域感染症
肛門周囲膿瘍に対する有効率は100%(1/1)であった。
(3)呼吸器感染症
咽頭・喉頭炎(咽喉頭炎(咽喉膿瘍))、急性気管支炎、扁桃炎(扁桃周囲炎、扁桃周囲膿瘍を含む)、肺炎に対する有効率は97.9%(277/283)であった。
(4)尿路感染症
腎盂腎炎、膀胱炎に対する有効率は94.6%(35/37)であった。
(5)猩紅熱
猩紅熱に対する有効率は100%(36/36)であった。
(6)百日咳
百日咳に対する有効率は100%(11/11)であった。
(7)耳鼻科領域感染症
中耳炎、副鼻腔炎に対する有効率は100%(18/18)であった。
安全性評価対象症例456例中19例(4.17%)に副作用が報告され、その内容は、消化器症状(下痢のみ)17件(3.73%)及びアレルギー症状(発疹、発赤各1件)2件(0.44%)であった。また、臨床検査値の変動は3.60%(10/278)に認められ、その主なものは、好酸球増多1.97%(5/254)等の血液像異常、ALT上昇0.90%(2/222)、AST上昇0.45%(1/222)等の肝機能異常であった。
17.1.2 国内臨床試験(旧細粒剤注1)の効能追加承認時)
歯科・口腔外科領域感染症(歯周組織炎、顎炎)小児患者を対象とした臨床試験での有効率は98.4%(62/63)であった15)。
総投与症例72例中、副作用は水様便1例(1.4%)が報告された。また、臨床検査値の異常変動は好酸球数増多6.9%(4/58)が認められた。
総投与症例72例中、副作用は水様便1例(1.4%)が報告された。また、臨床検査値の異常変動は好酸球数増多6.9%(4/58)が認められた。
17.1.3 国内臨床試験(用法・用量一部変更承認時)
肺炎、中耳炎、副鼻腔炎小児患者を対象とした1回6mg(力価)/kg1日3回投与による臨床試験での有効率及び耐性度別の細菌学的効果は次のとおりであった16)。
| 疾患名 | 有効例数/有効性 評価対象例数 | 有効率(%) |
| 肺炎 | 14/14 | 100 |
| 中耳炎 | 71/79 | 89.9 |
| 副鼻腔炎 | 12/13 | 92.3 |
| 原因菌 | 陰性化株数/株数計 | 消失率(%) | |
| 肺炎球菌注2) | 10/12 | 83.3 | |
| PSSP(ペニシリンG MIC:≦0.06μg/mL)注3) | 6/6 | 100 | |
| PISP(ペニシリンG MIC:0.12〜1μg/mL)注3) | 2/4 | − | |
| PRSP(ペニシリンG MIC:≧2μg/mL)注3) | 2/2 | − | |
| インフルエンザ菌 | 28/32 | 87.5 | |
| アンピシリン感性(MIC:≦1μg/mL) | 12/12 | 100 | |
| アンピシリン中等度耐性(MIC:2μg/mL) | 2/3 | − | |
| アンピシリン耐性(MIC:≧4μg/mL) | 14/17 | 82.4 | |
| モラクセラ(ブランハメラ)・カタラーリス | 4/4 | − | |
| 化膿レンサ球菌 | 4/4 | − | |
安全性評価対象例115例中36例(31.3%)に副作用が認められた。主なものは、下痢・軟便28例(24.3%)であった。また、臨床検査値の異常変動は、検査を実施した安全性評価対象例113例中7例(6.2%)に認められた。主なものは、血小板数増加等であった。
注1)本剤と旧細粒剤及び旧細粒剤と顆粒剤の生物学的同等性が確認されている。
18. 薬効薬理
18.1 作用機序
18.2 抗菌作用
18.2.1 セフジトレン ピボキシルは、吸収時に腸管壁で代謝を受けてセフジトレンとなり、抗菌力を示す。
18.3 実験的感染症に対する治療効果
19. 有効成分に関する理化学的知見
19.1. セフジトレン ピボキシル
20. 取扱い上の注意
防湿のため、ボトル入製剤は調剤後必ず密栓すること。ボトル入製剤を分包した場合は光、湿気を避けて保存すること。
22. 包装
ボトル(乾燥剤入)
100g
分包(乾燥剤入)
0.3g×240包(3連包×80) 0.5g×120包(3連包×40)
23. 主要文献
- 厚生労働省健康局結核感染症課編:抗微生物薬適正使用の手引き
- 藤井良知ほか, Jpn.J.Antibiot., 46 (10), 926-937, (1993) »PubMed
- 藤井良知ほか, Jpn.J.Antibiot., 46 (1), 95-114, (1993) »PubMed
- 高橋 淳ほか, Chemotherapy., 40 (S-2), 434-445, (1992) »DOI
- 馬場駿吉ほか, 耳鼻と臨床, 38 (5), 663-680, (1992) »DOI
- 西園浩文ほか, Chemotherapy., 40 (S-2), 643-650, (1992) »DOI
- 秋山尚範ほか, Chemotherapy., 40 (S-2), 619-623, (1992) »DOI
- 佐々木次郎ほか, Chemotherapy., 40 (S-2), 664-672, (1992) »DOI
- 松元 隆ほか, Chemotherapy., 40 (S-2), 120-130, (1992) »DOI
- 社内資料:ME1207単回投与におけるME1206およびその代謝物の尿中,糞便中排泄率
- 柴 孝也ほか, Chemotherapy., 40 (11), 1310-1319, (1992) »DOI
- 由良二郎ほか, Chemotherapy., 41 (1), 24-40, (1993) »DOI
- 社内資料:ME1207の生体内動態
- 青木信樹ほか, Chemotherapy., 40 (S-2), 371-381, (1992) »DOI
- 金子明寛ほか, 歯科薬物療法, 22 (1), 1-17, (2003) »DOI
- 砂川慶介ほか, 日本化学療法学会雑誌, 60 (4), 478-491, (2012)
- 横田 健ほか, Chemotherapy., 40 (S-2), 7-15, (1992) »DOI
- 西野武志ほか, Chemotherapy., 40 (S-2), 37-50, (1992) »DOI
- 河原條勝己ほか, Chemotherapy., 40 (S-2), 51-58, (1992) »DOI
- 五島瑳智子ほか, Chemotherapy., 40 (S-2), 16-29, (1992) »DOI
- 渡辺邦友ほか, Chemotherapy., 40 (S-2), 30-36, (1992) »DOI
- 田村 淳ほか, Chemotherapy., 40 (S-2), 1-6, (1992) »DOI
- 生方公子ほか, 日本化学療法学会雑誌, 50 (11), 794-804, (2002) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
Meiji Seikaファルマ株式会社
くすり相談室
〒104-8002
東京都中央区京橋2-4-16
電話:フリーダイヤル0120-093-396
03-3273-3539
03-3273-3539
FAX:03-3272-2438
製品情報問い合わせ先
Meiji Seikaファルマ株式会社
くすり相談室
〒104-8002
東京都中央区京橋2-4-16
電話:フリーダイヤル0120-093-396
03-3273-3539
03-3273-3539
FAX:03-3272-2438
26. 製造販売業者等
26.1 製造販売元
Meiji Seikaファルマ株式会社
東京都中央区京橋2-4-16