医薬品情報
| 総称名 | サンドスタチン |
|---|---|
| 一般名 | オクトレオチド酢酸塩 |
| 欧文一般名 | Octreotide Acetate |
| 製剤名 | オクトレオチド酢酸塩注射液 |
| 薬効分類名 | 持続性ソマトスタチンアナログ製剤 |
| 薬効分類番号 | 2499 |
| ATCコード | H01CB02 |
| KEGG DRUG |
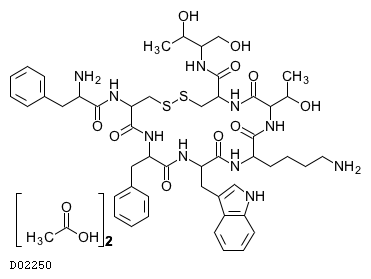
D02250
オクトレオチド酢酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年5月 改訂(第2版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| サンドスタチン皮下注用50μg | Sandostatin for s.c.injection | ノバルティスファーマ | 2499403A1037 | 566円/管 | 劇薬, 処方箋医薬品 |
| サンドスタチン皮下注用100μg | Sandostatin for s.c.injection | ノバルティスファーマ | 2499403A2033 | 963円/管 | 劇薬, 処方箋医薬品 |
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
○下記疾患に伴う諸症状の改善
○下記疾患における成長ホルモン、ソマトメジン-C分泌過剰状態及び諸症状の改善
○進行・再発癌患者の緩和医療における消化管閉塞に伴う消化器症状の改善
○先天性高インスリン血症に伴う低血糖(他剤による治療で効果が不十分な場合)
5. 効能または効果に関連する注意
<下垂体性巨人症>
5.1 脳性巨人症や染色体異常など他の原因による高身長例を鑑別し、下垂体性病変に由来するものであることを十分に確認すること。
<先天性高インスリン血症に伴う低血糖>
5.2 ジアゾキシドによる治療で効果が不十分な場合に本剤の投与を検討すること。
5.3 重症低血糖によって引き起こされる中枢神経症状に対する有効性は認められていない。
6. 用法及び用量
<消化管ホルモン産生腫瘍、先端巨大症・下垂体性巨人症>
通常、成人にはオクトレオチドとして1日量100又は150μgより投与をはじめ、効果が不十分な場合は1日量300μgまで漸増し、2〜3回に分けて皮下投与する。なお、症状により適宜増減する。
<進行・再発癌患者の緩和医療における消化管閉塞に伴う消化器症状>
通常、成人にはオクトレオチドとして1日量300μgを24時間持続皮下投与する。なお、症状により適宜増減する。
<先天性高インスリン血症に伴う低血糖>
通常、オクトレオチドとして1日量5μg/kgを、3〜4回に分けて皮下投与又は24時間持続皮下投与する。なお、患者の状態に応じて適宜増減するが、最大投与量は1日量25μg/kgまでとする。
7. 用法及び用量に関連する注意
<進行・再発癌患者の緩和医療における消化管閉塞に伴う消化器症状>
7.2 本剤を継続投与する際には、患者の病態の観察を十分に行い、7日間毎を目安として投与継続の可否について慎重に検討すること。
<先天性高インスリン血症に伴う低血糖>
7.3 本剤の用量は、患者の低血糖状態の重症度、血糖値及び臨床症状に基づき、最も少ない用量で効果が認められるよう、個別に調整すること。増量の際には観察を十分に行いながら慎重に増量すること。
8. 重要な基本的注意
<効能共通>
8.1 本剤の投与中はインスリン、グルカゴン及び成長ホルモン等互いに拮抗的に調節作用をもつホルモン間のバランスの変化による一過性の低又は高血糖を伴うことがあるので、投与開始時及び低又は高血糖のために投与量を変更する場合は患者を十分に観察すること。[11.2参照]
8.2 胆石の形成又は胆石症の悪化(急性胆嚢炎、胆管炎、膵炎)が報告されているので、本剤の投与前及び投与中は、定期的に(6〜12ヵ月毎に)超音波・X線による胆嚢及び胆管検査を受けることが望ましい。[11.2参照]
8.3 自己投与に際しては、以下の点に注意すること。
・自己投与の適用については、医師がその妥当性を慎重に検討し、十分な教育訓練を実施した後、本剤投与による危険性と対処法について患者及び介護者が理解し、自ら確実に投与できることを確認した上で、医師の管理指導の下で実施すること。
・自己投与の適用後、感染症等の本剤による副作用が疑われる場合や自己投与の継続が困難な状況となる可能性がある場合には、直ちに自己投与を中止させ、医師の管理下で慎重に観察するなど適切な処置を行うこと。また、本剤投与後に副作用の発現が疑われる場合は、医療施設へ連絡するよう患者及び介護者に指導を行うこと。
・使用済みの注射器を再使用しないように患者及び介護者に注意を促し、すべての器具の安全な廃棄方法に関する指導を行うと同時に、使用済みの注射器を廃棄する容器を提供すること。
<先端巨大症・下垂体性巨人症>
8.4 成長ホルモン産生下垂体腺腫は進展することがあり、これに伴い視野狭窄などの重篤な症状を生じることがあるので患者の状態を十分観察すること。腫瘍の進展が認められた場合は、他の治療法への切り替え等適切な処置を行うこと。
8.5 成長ホルモン及びソマトメジン-Cを定期的に測定することが望ましい。
<進行・再発癌患者の緩和医療における消化管閉塞に伴う消化器症状>
8.6 増量投与を行う場合は、低体重、悪液質等の患者の状態に注意し、慎重な監視のもとで投与すること。[7.1参照]
<先天性高インスリン血症に伴う低血糖>
8.7 本剤を長期的に投与する場合は、血糖、尿糖及び尿ケトン値を定期的に検査すること。
8.8 本剤を使用する際には、関連文献(「医療上の必要性の高い未承認薬・適応外薬検討会議 公知申請への該当性に係る報告書:オクトレオチド酢酸塩(先天性高インスリン血症に伴う低血糖)」1)等)を熟読すること。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
<消化管ホルモン産生腫瘍、先端巨大症・下垂体性巨人症、進行・再発癌患者の緩和医療における消化管閉塞に伴う消化器症状>
9.7.1 小児等を対象とした臨床試験は実施していない。
<先天性高インスリン血症に伴う低血糖>
9.7.2 新生児及び乳児において、壊死性腸炎が報告されている。
9.7.3 小児に投与する場合は定期的に身長、体重を測定すること。成長遅延が報告されている。
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意
| シクロスポリン | シクロスポリンの血中濃度が低下することがある。 | 本剤がシクロスポリンの吸収を阻害するため。 |
| インスリン製剤 | 血糖降下作用の増強による低血糖症状、又は減弱による高血糖症状があらわれることがある。併用する場合は、血糖値その他患者の状態を十分に観察しながら投与すること。 | インスリン、グルカゴン及び成長ホルモン等互いに拮抗的に調節作用をもつホルモン間のバランスが変化することがある。 |
| ブロモクリプチン | ブロモクリプチンのAUCが上昇したとの報告がある。 | 機序は不明である。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 アナフィラキシー(頻度不明)
血圧低下、呼吸困難、気管支痙攣等のアナフィラキシーがあらわれることがある。皮疹、そう痒、蕁麻疹、発疹を伴う末梢性の浮腫等があらわれた場合には直ちに投与を中止すること。また、その後の投与は行わないこと。
11.1.2 徐脈(0.1%)
投与直後に重篤な徐脈を起こすことがある。β-遮断剤、カルシウム拮抗剤等の徐脈作用を有する薬剤又は水分や電解質を補正する薬剤を投与している患者において、徐脈が認められた場合、これらの用量を調節すること。
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 内分泌障害 | − | − | − | 甲状腺機能低下症、甲状腺機能障害(甲状腺刺激ホルモン(TSH)減少、総サイロキシン(T4)減少及び遊離T4減少等) |
| 代謝及び栄養障害 | − | − | 耐糖能異常注1)、低血糖注1)、高血糖注1) | 脱水 |
| 神経系障害 | − | − | 頭痛、めまい | − |
| 呼吸器障害 | − | − | 呼吸困難 | |
| 胃腸障害 | 嘔気 | 胃部不快感、下痢、嘔吐 | 便秘、腹痛、食欲不振、白色便、腹部膨満 | 膵炎、鼓腸放屁 |
| 肝胆道系障害 | − | 肝機能異常、AST上昇、ALT上昇、ALP上昇、γ-GTP上昇、胆石注2) | LDH上昇、ビリルビン上昇 | 胆嚢炎 |
| 皮膚及び皮下組織障害 | − | − | 発赤、皮膚そう痒感、脱毛 | − |
| 全身障害 | − | − | 疲労、けん怠感 | − |
| 注射部位 | 疼痛 | − | 発赤、硬結 | 刺激感、刺痛、腫脹、灼熱感 |
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 皮下注射にあたっては、組織、神経等への影響を避けるため、下記の点に注意すること。
・神経走行部位を避けるように注意すること。
・繰返し注射する場合には、例えば左右交互に注射するなど同一部位を避けて行うこと。
・注射針を刺入したとき、激痛を訴えたり、血液の逆流をみた場合は、直ちに針を抜き、部位をかえて注射すること。
・注射部位に疼痛をみることがある。
14.1.2 持続皮下投与時の各種シリンジポンプ等医薬品注入器の具体的な使用方法については、注入機器の使用説明書注3)及びノバルティスファーマ社作成使用手引き注4)の内容を熟知して使用すること。
注3)当該注入機器の製造販売業者作成の添付文書及び取扱い説明書
注4)本剤の注入速度の設定方法、注入液量の調整方法についての解説
14.2 配合変化
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 海外において本剤により消化管ホルモン産生腫瘍の症状が管理されていた患者で症状管理が不可能になり、急激に症状が再発したとの報告がある。
15.1.2 オクトレオチド酢酸塩製剤を反復投与した患者に、抗オクトレオチド抗体が出現することがある。なお、抗体に起因すると考えられる特異的な副作用は認められていない。
15.1.3 本剤により脂肪の吸収が低下する可能性がある。海外において本剤の投与中に糞中の脂肪が増加したとの報告がある。
15.1.4 海外において本剤を投与された患者で、血清ビタミンB12の低下、シリングテストでの異常値がみられたとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 健康成人
国内健康成人にサンドスタチン皮下注用50及び100μgを単回皮下投与し、ラジオイムノアッセイ法により血漿中濃度を測定した。いずれの投与量においても投与後1時間までに最高濃度に達し、消失半減期t1/2は約1.8時間であった。最高薬物濃度Cmaxは2.44ng/mL及び4.80ng/mLであり、投与後8時間までの薬物濃度−時間曲線下面積AUC0-8は6.57ng・h/mL及び12.4ng・h/mLで、Cmax、AUC0−8共に投与量にほぼ比例して増加した。
なお、海外健康成人を対象とした単回静脈内投与(25、50、100、200μg)試験及び単回皮下投与(50、100、200、400μg)試験の成績から皮下投与時のバイオアベイラビリティはほぼ100%と推定された。また海外健康成人に50あるいは200μgを1日3回5日間反復皮下投与した場合、初回投与時と比較し反復投与後で累積は認められなかった4)5)6)7)。
なお、海外健康成人を対象とした単回静脈内投与(25、50、100、200μg)試験及び単回皮下投与(50、100、200、400μg)試験の成績から皮下投与時のバイオアベイラビリティはほぼ100%と推定された。また海外健康成人に50あるいは200μgを1日3回5日間反復皮下投与した場合、初回投与時と比較し反復投与後で累積は認められなかった4)5)6)7)。
国内健康成人にサンドスタチン皮下注用50μg及び100μgを単回皮下投与した後の血漿中濃度推移(平均値±標準偏差、n=16)
| 投与量(μg) | 50 | 100 |
| Cmax(ng/mL) | 2.44±0.63 | 4.80±0.86 |
| Tmax(h) | 0.57±0.24 | 0.68±0.19 |
| t1/2(h) | 1.79±0.19 | 1.77±0.49 |
| AUC※(ng・h/mL) | 6.57±1.52[6.78±1.39] | 12.4±1.3[13.1±1.4] |
16.1.2 先端巨大症・下垂体性巨人症患者
国内において本剤を反復投与されている先端巨大症・下垂体性巨人症患者に、100μgを皮下投与し血清中濃度を測定した場合、Cmaxは3.82ng/mL、AUC0-8は10.9ng・h/mL、t1/2は2.37時間であった8)。
16.1.3 消化管閉塞を伴う進行・再発癌患者
国内の消化管閉塞を伴う進行・再発癌患者に300μg/日の注入速度で6日間持続皮下投与し投与開始から2〜6日目までの血漿中濃度を測定した場合、平均薬物濃度は2.84ng/mLで、1日あたりのAUCは71.8ng・h/mLであった9)。
16.3 分布
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
<消化管ホルモン産生腫瘍>
17.1.1 国内臨床試験
VIP産生腫瘍、カルチノイド症候群の特徴を示すカルチノイド腫瘍、ガストリン産生腫瘍患者15例におけるサンドスタチンの非盲検、非対照試験成績の概要は次のとおりである13)。
(1)VIP産生腫瘍
血中VIP値の低下に伴い、水様性下痢等の症状の改善が認められた。
本疾患4例中2例に有用性が認められた。
本疾患4例中2例に有用性が認められた。
(2)カルチノイド症候群の特徴を示すカルチノイド腫瘍
血中セロトニン値又は5-HIAA値の低下が認められ、顔面潮紅、下痢等の症状の改善が認められた。本疾患3例において有用性が認められた。
(3)ガストリン産生腫瘍
血中ガストリン値の低下、吻合部潰瘍、心窩部痛、全身けん怠感、吐下血等の症状の改善が認められた。本疾患8例中5例において有用性が認められた。
(4)副作用
副作用発現頻度は66.7%(10/15例)であった。主な副作用は、下痢及び注射部位疼痛各20.0%(3/15例)、嘔気及び嘔吐各13.3%(2/15例)であった。
<先端巨大症・下垂体性巨人症>
17.1.2 国内臨床試験
先端巨大症64例、下垂体性巨人症3例、計67例における非盲検、非対照試験の有効率は76.1%(51/67)であった14)。
(1)血中成長ホルモン(GH)に対する効果
67例中18例(26.9%)において、投与終了後血中GH値が正常化した。
また、67例中投与終了時の血中GH値が投与前値に対して50%以下を示したものは49例(73.1%)であった。
また、67例中投与終了時の血中GH値が投与前値に対して50%以下を示したものは49例(73.1%)であった。
(2)血中ソマトメジン-C(SM-C)に対する効果
30例中14例(46.7%)において、血中SM-Cが正常化した。
(3)臨床症状の改善
発汗は33例中17例(51.5%)、頭重感は17例中14例(82.4%)、頭痛は13例中13例(100%)に改善が認められ、また、手足のしびれ、めまい、息切れ等においても改善がみられた。軟部組織の肥厚に対して、手の容積とheel padの厚さにおいて、有意な減少が認められた。
(4)下垂体腫瘍の縮小効果
投与前後でCT検査施行35例中5例(14.3%)、MRI検査施行9例中8例(88.9%)に腫瘍の縮小が認められた。
(5)副作用
副作用発現頻度は47.8%(32/67例)であった。主な副作用は、注射部疼痛31.3%(21/67例)、胃不快感13.4%(9/67例)、嘔気7.5%(5/67例)及び下痢4.5%(3/67例)であった。
<進行・再発癌患者の緩和医療における消化管閉塞に伴う消化器症状>
17.1.3 国内第I/II相試験及び国内第II相試験
消化管閉塞に伴う消化器症状を示す進行・再発癌患者、計35例を対象とした非盲検、非対照試験(第I/II相試験、第II相試験)において、Japan Clinical Oncology Group(JCOG)の悪心・嘔吐のToxicity Scaleを用いて判定した有効率は、44%(11/25:第I/II相試験)及び60%(6/10:第II相試験)であった。
また、これらの試験において、胃管非挿入患者では1日あたりの嘔吐回数が減少し(第I/II相試験:17例の中央値で投与開始前7回から最終観察時2回、第II相試験:4例の中央値で投与開始前4.5回から最終観察時3回)、経鼻的胃管挿入患者では胃管からの消化液排出量が減少した(第I/II相試験:8例の中央値で投与開始前795mLから最終観察時525mL、第II相試験:6例の中央値で投与開始前567.5mLから最終観察時207.5mL)。なお、消化液排出量の減少が著明であった8例(第I/II相試験:4例、第II相試験:4例)では、胃管の抜去及び抜去後の嘔吐の良好なコントロールが可能であった15)16)。なお、本剤300μg/日投与で期待される効果が得られなかった症例に対する増量による効果の発現については、上述の臨床試験(第I/II相試験、第II相試験)において検討されておらず、海外における臨床報告においても明確にはされていない17)18)19)。[7.1参照]
また、これらの試験において、胃管非挿入患者では1日あたりの嘔吐回数が減少し(第I/II相試験:17例の中央値で投与開始前7回から最終観察時2回、第II相試験:4例の中央値で投与開始前4.5回から最終観察時3回)、経鼻的胃管挿入患者では胃管からの消化液排出量が減少した(第I/II相試験:8例の中央値で投与開始前795mLから最終観察時525mL、第II相試験:6例の中央値で投与開始前567.5mLから最終観察時207.5mL)。なお、消化液排出量の減少が著明であった8例(第I/II相試験:4例、第II相試験:4例)では、胃管の抜去及び抜去後の嘔吐の良好なコントロールが可能であった15)16)。なお、本剤300μg/日投与で期待される効果が得られなかった症例に対する増量による効果の発現については、上述の臨床試験(第I/II相試験、第II相試験)において検討されておらず、海外における臨床報告においても明確にはされていない17)18)19)。[7.1参照]
第I/II相試験の副作用発現頻度は8.0%(2/25例)であり、悪心及び不穏各4.0%(1/25例)であった。
第II相試験の副作用発現頻度は15.4%(2/13例)であり、嘔気増悪及び注射部位硬結各7.7%(1/13例)であった。
18. 薬効薬理
18.1 作用機序
18.1.1 本剤はソマトスタチン受容体サブタイプ1〜5(SSTR1〜5)のうちSSTR2に特に強い親和性を示し、SSTR2選択的ソマトスタチンアナログであると考えられた(in vitro)。
18.1.2 本剤は、細胞を用いた検討において、カルシウムイオン流入の阻害作用、cAMP産生の抑制作用を示した(in vitro)。
18.2 薬理作用
19. 有効成分に関する理化学的知見
19.1. オクトレオチド酢酸塩
20. 取扱い上の注意
外箱開封後は遮光して保存すること。
22. 包装
<サンドスタチン皮下注用50μg>
1mL 10管
<サンドスタチン皮下注用100μg>
1mL 10管
23. 主要文献
- 医療上の必要性の高い未承認薬・適応外薬検討会議 公知申請への該当性に係る報告書:オクトレオチド酢酸塩(先天性高インスリン血症に伴う低血糖)
- 花村美帆ほか, 日本病院薬剤師会雑誌, 46 (11), 1501-1504, (2010)
- 社内資料:サンドスタチン皮下注用の配合変化試験
- 社内資料:日本人健康成人における薬物動態
- 社内資料:日本人健康成人における薬物動態
- 社内資料:外国人健康成人における薬物動態パラメータ
- 社内資料:外国人健康成人における薬物動態パラメータ
- 社内資料:日本人先端巨大症患者又は下垂体性巨人症患者における薬物動態
- 社内資料:消化管閉塞を伴う日本人進行・再発癌患者における薬物動態
- 社内資料:ヒトにおける血漿蛋白結合及び血球移行性
- 社内資料:外国人健康成人における尿中排泄率
- 社内資料:胆管挿管ラットにおける放射能及び未変化体の排泄
- 清野 裕ほか, ホルモンと臨床, 36 (6), 581-590, (1988)
- 島津 章ほか, 日本内分泌学会雑誌, 65 (7), 640-652, (1989) »DOI
- Shima,Y.et al., Jpn.J.Clin.Oncol., 38 (5), 354-359, (2008) »PubMed
- 社内資料:進行・再発癌患者を対象とした第II相試験
- Mercadante,S.et al., Palliat Med., 7 (4), 295-299, (1993) »PubMed
- Khoo,D.et al., Eur.J.Cancer, 30A (1), 28-30, (1994) »PubMed
- Mangili,G.et al., Gynecol.Oncol., 61 (3), 345-348, (1996) »PubMed
- 前田征洋ほか, 日本内科学会雑誌, 77 (1), 86-90, (1988) »DOI
- 吉岡光明ほか, 日本内科学会雑誌, 77 (8), 1276-1277, (1988) »DOI
- Kvols,L.K.et al., N.Engl.J.Med., 315 (11), 663-666, (1986) »PubMed
- 福島英生ほか, 日本内分泌学会雑誌, 64 (8), 666-676, (1988) »DOI
- Lamberts,S.W.J.et al., Clin.Endocrinol., 27 (1), 11-23, (1987) »PubMed
- Miyachi,M.et al., Biomed.Res., 8 (Suppl.), 65-70, (1987)
- Aurang,K.et al., J.Pharmacol.Exp.Ther., 281 (1), 245-252, (1997) »PubMed
- Verchere,C.B.et al., Pharmacology, 46 (1), 50-60, (1993) »PubMed
- Misumi,A.et al., Surgery, 103 (4), 450-455, (1988) »PubMed
- Nellgard,P.et al., Scand.J.Gastroenterol., 30 (5), 464-469, (1995) »PubMed
- Anthone,G.J.et al., Surgery, 108 (6), 1136-1142, (1990) »PubMed
- Demura,N.et al., Jpn.Pharmacol.Ther., 38 (9), 817-823, (2010)
- Pless,J.et al., Scand.J.Gastroenterol., 21 (S119), 54-64, (1986)
24. 文献請求先及び問い合わせ先
文献請求先
ノバルティスファーマ株式会社
ノバルティスダイレクト
〒105-6333
東京都港区虎ノ門1-23-1
電話:0120-003-293 受付時間:月〜金 9:00〜17:30(祝祭日及び当社休日を除く)
製品情報問い合わせ先
ノバルティスファーマ株式会社
ノバルティスダイレクト
〒105-6333
東京都港区虎ノ門1-23-1
電話:0120-003-293 受付時間:月〜金 9:00〜17:30(祝祭日及び当社休日を除く)
26. 製造販売業者等
26.1 製造販売
ノバルティスファーマ株式会社
東京都港区虎ノ門1-23-1