医薬品情報
| 総称名 | アボルブ |
|---|---|
| 一般名 | デュタステリド |
| 欧文一般名 | Dutasteride |
| 製剤名 | デュタステリドカプセル |
| 薬効分類名 | 5α還元酵素阻害薬 前立腺肥大症治療薬 |
| 薬効分類番号 | 2499 |
| ATCコード | G04CB02 |
| KEGG DRUG |
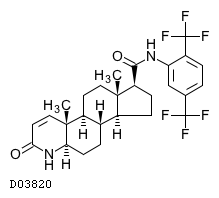
D03820
デュタステリド
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年8月 改訂(第2版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アボルブカプセル0.5mg | Avolve Capsules 0.5mg | グラクソ・スミスクライン | 2499011M1027 | 46円/カプセル | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
前立腺肥大症
5. 効能または効果に関連する注意
6. 用法及び用量
通常、成人にはデュタステリドとして1回0.5mgを1日1回経口投与する。
7. 用法及び用量に関連する注意
投与開始初期に改善が認められる場合もあるが、治療効果を評価するためには、通常6ヵ月間の治療が必要である。
8. 重要な基本的注意
8.2 本剤投与前に直腸診や他の前立腺癌の検査を実施すること。また、本剤投与中においても定期的にこれらの検査を実施すること。
8.3 本剤は、血清前立腺特異抗原(PSA)に影響を与えるので、以下の点に注意すること。
・PSA値は、前立腺癌のスクリーニングにおける重要な指標である。一般に、PSA値が基準値(通常、4.0ng/mL)以上の場合には、更なる評価が必要となり、前立腺生検の実施を考慮に入れる必要がある。なお、本剤投与中の患者で、本剤投与前のPSA値が基準値未満であっても、前立腺癌の診断を除外しないように注意すること。
・本剤は、前立腺癌の存在下であっても、投与6ヵ月後にPSA値を約50%減少させる。したがって、本剤を6ヵ月以上投与している患者のPSA値を評価する際には、測定値を2倍した値を目安として基準値と比較すること。なお、PSA値は、本剤投与中止後6ヵ月以内に本剤投与開始前の値に戻る。
・本剤投与中におけるPSA値の持続的増加に対しては、前立腺癌の発現や本剤の服薬不遵守を考慮に含め、注意して評価すること。
・本剤投与中において、free/total PSA比は一定に維持されるので、前立腺癌のスクリーニングの目的で%free PSAを使用する場合には、測定値の調整は不要である。
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
9.3.1 重度の肝機能障害のある患者
投与しないこと。本剤は主に肝臓で代謝されるため、血中濃度が上昇するおそれがある。[2.4参照]
9.3.2 肝機能障害のある患者(重度の肝機能障害のある患者を除く)
本剤は主に肝臓で代謝される。肝機能障害のある患者に投与した場合の薬物動態は検討されていない。[16.4.1参照]
9.5 妊婦
9.6 授乳婦
9.7 小児等
10. 相互作用
相互作用序文
本剤は、主としてCYP3A4で代謝される。[16.4.1参照]
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| CYP3A4阻害作用を有する薬剤 リトナビル等 [16.7.1参照] | これらの薬剤との併用により本剤の血中濃度が上昇する可能性がある。 | CYP3A4による本剤の代謝が阻害される。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
肝機能障害(1.5%)、黄疸(頻度不明)
AST、ALT、ビリルビンの上昇等を伴う肝機能障害や黄疸があらわれることがある。
11.2 その他の副作用
| 1%以上 | 1%未満 | 頻度不明 | |
| 過敏症 | 蕁麻疹 | アレルギー反応、発疹、そう痒症、限局性浮腫、血管性浮腫 | |
| 精神神経系 | リビドー減退 | 浮動性めまい | 抑うつ気分、味覚異常 |
| 生殖系及び乳房障害 | 勃起不全、乳房障害(女性化乳房、乳頭痛、乳房痛、乳房不快感) | 射精障害 | 精巣痛、精巣腫脹 |
| 皮膚 | 脱毛症(主に体毛脱落)、多毛症 | ||
| 消化器 | 腹部不快感 | 下痢 | |
| その他 | 倦怠感 | 血中CK増加 |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.2 カプセルの内容物が口腔咽頭粘膜を刺激する場合があるので、カプセルは噛んだり開けたりせずに服用させること。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 海外臨床試験において、18〜52歳の健康成人(本剤群:27例、プラセボ群:23例)を対象に、52週間の投与期間及び24週間の投与後追跡期間を通して、本剤0.5mg/日の精液特性に対する影響を評価した。投与52週目における総精子数、精液量及び精子運動率の投与前値からの平均減少率(プラセボ群の投与前値からの変化で調整)は、それぞれ23、26及び18%であり、精子濃度及び精子形態への影響は認められなかった。本剤群における総精子数の投与前値からの平均減少率は、24週間の追跡期間後においても23%のままであった。しかしながら、いずれの評価時期においても、全ての精液パラメータの平均値は正常範囲内であり、事前に規定した臨床的に重要な変動(30%)には至らなかった。また、本剤群の2例において、投与52週目に投与前値から90%を超える精子数の減少が認められたが、追跡24週目には軽快した。本剤の精液特性に及ぼす影響が、個々の患者の受胎能に対しどのような臨床的意義をもつかは不明である。
15.1.2 市販後において、本剤を投与された患者で男性乳癌が報告されている。デュタステリドと男性乳癌の発現との関連性は不明である。なお、2〜4年間の海外臨床試験(4325例)において3例の乳癌が報告された。このうち、デュタステリドが投与された症例では2例(曝露期間10週間、11ヵ月)、プラセボのみが投与された症例では1例報告されている。国内臨床試験での報告はない。
15.1.3 白人を主体とした50〜75歳の男性8231例(生検により前立腺癌が陰性かつPSA値2.5〜10.0ng/mL)を対象とした4年間の国際共同試験(日本人57例を含む)において、Modified Gleason Score注)8〜10の前立腺癌の発現率がプラセボ群(0.5%)に対し本剤群(1.0%)において高かった(相対リスク2.06[95%信頼区間:1.13-3.75])との報告がある1)2)3)。
注)組織学的悪性度の指標
15.2 非臨床試験に基づく情報
15.2.1 アカゲザルの器官形成期にデュタステリドを2010ng/匹/日まで静脈内投与した結果、2010ng/匹/日群(本剤を服用した男性の精液5mLを介して100%吸収されると仮定した場合に、体重50kgの女性が曝露される推定最大曝露量の186倍に相当する)の雌胎児1例に、本薬投与との関連性は不明であるが、卵巣・卵管の不均衡発達が認められた。
15.2.2 ラットのがん原性試験において、高用量(臨床用量における曝露量の約141倍)投与時に精巣間細胞腫の増加がみられた。しかしながら、精巣間細胞腫及び過形成の発現に起因するラットの内分泌機構のヒトへの外挿性が低いことから、ヒトに精巣間細胞腫を発現させる危険性は低いと考えられている。なお、マウスのがん原性試験においては、デュタステリドに関連すると考えられる腫瘍の発生は認められなかった。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人に本剤1〜20mg注)を単回経口投与した時、投与後2.0〜2.3時間に最高血漿中薬物濃度(Cmax)に達し、みかけの分布容積は232〜298Lであった。Cmaxは投与量に依存して増加し、終末相の消失半減期(t1/2)は89〜174時間であり、消失は非線形であった。
16.1.2 反復投与
前立腺肥大症患者に本剤0.05〜2.5mg注)を1日1回6ヵ月間反復経口投与した時、0.5mgではおよそ投与5ヵ月で定常状態に達し、6ヵ月での血清中薬物濃度は44.82±17.91ng/mLであった。0.5mg投与の定常状態におけるt1/2は3.4±1.2週間であり、消失は非線形であった。
図1 反復経口投与後の血清中デュタステリド濃度の推移(平均値+SD)
(0.05mgの投与終了後は定量下限未満)
16.2 吸収
16.2.1 食事の影響
健康成人に本剤2.5mg注)を食後単回経口投与した時、薬物動態パラメータに若干の変化を認め、AUC0-∞は空腹時投与の2573から2197ng・hr/mLに減少した。なお、この変化は臨床上影響を与えるものではない。
16.2.2 生物学的利用率
健康成人に本剤0.5mgを単回経口投与した時、生物学的利用率は59%であった(外国人データ)。
16.3 分布
16.3.1 蛋白結合率
In vitro試験において、デュタステリド(2000ng/mL)のヒト血清蛋白結合率は99.8%と高く、血清アルブミン、α1-酸性糖蛋白、コルチコステロイド結合グロブリン及び性ホルモン結合グロブリンに対する結合率は、それぞれ99.0%、96.6%、89.2%及び87.6%であった。また、これらの蛋白に対する結合率は20〜2000ng/mLの範囲で線形であった(限外ろ過法)。
16.3.2 精液移行
健康成人に本剤0.5mgを反復経口投与した時、精液中/血清中薬物濃度比は平均11.5%であった(外国人データ)。
16.4 代謝
16.4.1 主な代謝酵素
16.4.2 代謝酵素阻害
In vitro試験において、デュタステリドはCYP1A2、2C9及び2D6活性を阻害しなかったが、CYP2C19及び3A4活性を阻害し、IC50は50μMであった。
16.4.3 代謝酵素誘導
In vitro試験において、デュタステリドはPXR活性化によるCYP3A4誘導能を示さなかった。
16.4.4 主代謝物
前立腺肥大症患者に本剤0.5mgを1日1回反復経口投与した時、主代謝物として1,2-二水素化体、4'-水酸化体、6-水酸化体が確認された。
16.5 排泄
16.5.1 単回投与
健康成人に本剤1〜20mg注)を単回経口投与した時、投与後48時間以内の尿中に未変化体は検出されなかった。
16.5.2 反復投与
健康成人に本剤0.5mgを1日1回6ヵ月以上反復経口投与した時、糞中に約5%の未変化体が排泄され、関連物質(未変化体+代謝物)として約42%が回収された。尿中への未変化体の排泄は0.1%未満であり、関連物質の排泄も微量であった(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 高齢者
24〜87歳の健康成人に本剤5mg注)を単回経口投与した時、50〜69歳及び70歳以上の年齢群のt1/2は49歳以下の年齢群に比べて延長し、AUC0-∞は約20%増加した。なお、この変化は臨床上影響を与えるものではない(外国人データ)。
16.7 薬物相互作用
16.7.1 CYP3A4阻害作用を有する薬剤
(1)In vitro試験において、デュタステリドの酸化的代謝はCYP3A4阻害作用を有するケトコナゾールによって阻害された。[10.2参照]
(2)CYP3A4阻害薬と本剤の薬物相互作用試験は実施されていないが、臨床試験で血漿中薬物濃度が測定された患者データの母集団薬物動態解析の結果、ベラパミル塩酸塩又はジルチアゼム塩酸塩との併用により本剤のクリアランスが低下した(外国人データ)。[10.2参照]
16.7.2 その他の薬剤
本剤0.5mgあるいは5mg注)と、コレスチラミン、ワルファリン、ジゴキシン、タムスロシン塩酸塩、テラゾシン塩酸塩との併用において薬物相互作用は認められなかった(外国人データ)。
注)本剤の承認用量は1日1回0.5mgである。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第II相試験
前立腺体積30mL以上の前立腺肥大症患者を対象とした二重盲検比較試験(1日1回24週間経口投与)4)において、用量依存的な前立腺体積の減少が認められた。本剤0.5mgはプラセボに比し、前立腺体積を有意に減少させ、I-PSS(国際前立腺症状スコア)及び最大尿流率を有意に改善した。
| プラセボ(70例) | 0.05mg注)(67例) | 0.5mg(70例) | 2.5mg注)(67例) | ||
| 投与前 | 平均値(SD) | 45.7(20.26) | 44.4(14.22) | 45.4(15.20) | 41.0(13.61) |
| 24週後 | 平均値(SD) | 42.1(21.26) | 37.9(14.72) | 34.6(14.66) | 30.7(11.85) |
| 変化率(%) | −8.7 | −15.5 | −25.3 | −25.6 | |
| p値 | − | 0.021 | <0.001 | <0.001 | |
副作用発現頻度は、本剤0.05mgで6%(4/70例)、本剤0.5mgで15%(11/71例)及び本剤2.5mgで13%(9/69例)であった。主な副作用は、本剤0.05mgで勃起不全3%(2/70例)、本剤0.5mgでリビドー減退4%(3/71例)、勃起不全3%(2/71例)及び射精障害3%(2/71例)、本剤2.5mgで勃起不全4%(3/69例)及びリビドー減退1%(1/69例)であった。[5.参照]
17.1.2 国内第III相試験
前立腺体積30mL以上の前立腺肥大症患者を対象とした二重盲検比較試験(1日1回52週間経口投与)5)において、本剤0.5mgはプラセボに比し、I-PSS及び最大尿流率を有意に改善し、前立腺体積を有意に減少させた。
| 評価項目\投与群 | プラセボ(181例) | 0.5mg(184例) | p値 | ||
| I-PSS(点) | 投与前 | 平均値(SD) | 16.0(6.01) | 16.6(6.56) | |
| 52週後 | 平均値(SD) | 12.4(6.32) | 11.1(6.82) | ||
| 変化量 | −3.7 | −5.3 | 0.003 | ||
| 最大尿流率(mL/sec) | 投与前 | 平均値(SD) | 11.2(4.41) | 11.2(4.13) | |
| 52週後 | 平均値(SD) | 11.9(4.82) | 13.4(5.75) | ||
| 変化量 | 0.7 | 2.2 | <0.001 | ||
| 前立腺体積(mL) | 投与前 | 平均値(SD) | 49.4(17.16) | 50.2(19.79) | |
| 52週後 | 平均値(SD) | 44.7(17.36) | 35.1(19.04) | ||
| 変化率(%) | −10.8 | −33.8 | <0.001 | ||
図1 I-PSSのベースラインからの変化量の推移
(変化量は線形モデルによる調整済み平均値)
図2 最大尿流率のベースラインからの変化量の推移
(変化量は線形モデルによる調整済み平均値)
図3 前立腺体積のベースラインからの変化率の推移
(変化率は線形モデルによる調整済み平均値)
副作用発現頻度は、本剤0.5mgで6%(12/193例)であった。主な副作用は、勃起不全2%(4/193例)、浮動性めまい1%(2/193例)及びリビドー減退1%(2/193例)であった。[5.参照]
注)本剤の承認用量は1日1回0.5mgである。
18. 薬効薬理
18.1 作用機序
デュタステリドは、テストステロンをジヒドロテストステロンへ変換する1型及び2型5α還元酵素を阻害する。ジヒドロテストステロンは前立腺肥大に関与する主なアンドロゲンである。
18.2 In vitro及び動物における成績
18.2.1 5α還元酵素阻害作用
In vitroにおいて、ヒト1型及び2型5α還元酵素を阻害した6)。また、去勢ラットにおいて、外因性に投与したテストステロンの前立腺におけるジヒドロテストステロンへの変換を阻害した。
18.2.2 前立腺組織中のジヒドロテストステロン濃度低下作用
ラットに反復投与することにより、前立腺組織中ジヒドロテストステロン濃度を低下させた。
18.2.3 前立腺縮小作用及び肥大抑制作用
ラットに反復投与することにより、前立腺を縮小させた7)。また、去勢ラットに反復投与することにより、テストステロン誘発前立腺肥大を抑制した。
18.3 ヒトにおける成績
18.3.1 血清中のジヒドロテストステロン濃度低下作用
前立腺肥大症患者に本剤0.05〜2.5mg注)を1日1回反復経口投与した時、血清中ジヒドロテストステロン濃度は投与2週までに速やかに低下した。反応は用量依存的であり、投与6ヵ月の0.5mgによる減少は89.7%と2.5mgと同程度で最大であった。
18.3.2 前立腺組織中のジヒドロテストステロン濃度低下作用
前立腺肥大症患者に本剤0.5mgを1日1回反復経口投与した時、投与3ヵ月の前立腺組織中ジヒドロテストステロン濃度はプラセボ投与と比較して93%減少した(外国人データ)。
注)本剤の承認用量は1日1回0.5mgである。
19. 有効成分に関する理化学的知見
19.1. デュタステリド
20. 取扱い上の注意
光及び湿気を避けるため、PTP包装のまま保存すること。
22. 包装
30カプセル[10カプセル(PTP)×3]
90カプセル[10カプセル(PTP)×9]
23. 主要文献
- Andriole GL,et al., N Engl J Med., 362, 1192-1202, (2010) »PubMed
- Theoret MR,et al., N Engl J Med., 365, 97-99, (2011) »PubMed
- Akaza H,et al., Jpn J Clin Oncol., 41, 417-423, (2011) »PubMed
- 塚本泰司ほか, 泌尿紀要, 55, 209-214, (2009)
- Tsukamoto T,et al., Int J Urol., 16, 745-750, (2009) »PubMed
- Tian G,et al., Biochemistry., 34, 13453-13459, (1995) »PubMed
- Bramson HN,et al., J Pharmacol Exp Ther., 282, 1496-1502, (1997) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
グラクソ・スミスクライン株式会社
メディカル・インフォメーション
東京都港区赤坂1-8-1
電話:0120-561-007(9:00〜17:45/土日祝日及び当社休業日を除く)
製品情報問い合わせ先
グラクソ・スミスクライン株式会社
メディカル・インフォメーション
東京都港区赤坂1-8-1
電話:0120-561-007(9:00〜17:45/土日祝日及び当社休業日を除く)
25. 保険給付上の注意
25.1 本製剤の効能又は効果は、「前立腺肥大症」であること。
25.2 本製剤が「男性における男性型脱毛症」の治療目的で処方された場合には、保険給付の対象としないこととする。
26. 製造販売業者等
26.1 製造販売元
グラクソ・スミスクライン株式会社
東京都港区赤坂1-8-1