医薬品情報
| 総称名 | シムビコート |
|---|---|
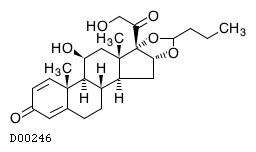
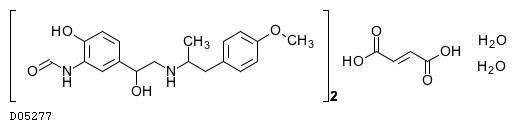
| 一般名 | ブデソニド ホルモテロールフマル酸塩水和物 |
| 欧文一般名 | Budesonide Formoterol Fumarate Hydrate |
| 製剤名 | ブデソニド/ホルモテロールフマル酸塩水和物吸入剤 |
| 薬効分類名 | ドライパウダー吸入式喘息・COPD治療配合剤 |
| 薬効分類番号 | 2290 |
| ATCコード | R03AK07 |
| KEGG DRUG |
D09595
ブデソニド・ホルモテロールフマル酸塩水和物
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年1月 改訂(第2版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| シムビコートタービュヘイラー30吸入 | Symbicort Turbuhaler 30 doses | アストラゼネカ | 2290801G1029 | 1242.2円/キット | 処方箋医薬品注) |
| シムビコートタービュヘイラー60吸入 | Symbicort Turbuhaler 60 doses | アストラゼネカ | 2290801G2025 | 2042.3円/キット | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 有効な抗菌剤の存在しない感染症、深在性真菌症の患者[ステロイドの作用により症状を増悪するおそれがある。]
2.2 本剤の成分に対して過敏症(接触性皮膚炎を含む)の既往歴のある患者
4. 効能または効果
○気管支喘息(吸入ステロイド剤及び長時間作動型吸入β2刺激剤の併用が必要な場合)
5. 効能または効果に関連する注意
<気管支喘息>
5.1 本剤の投与開始前には、患者の喘息症状を比較的安定な状態にしておくこと。特に、喘息発作重積状態又は喘息の急激な悪化状態のときには原則として本剤は使用しないこと。
<慢性閉塞性肺疾患(慢性気管支炎・肺気腫)の諸症状の緩解>
5.2 本剤は増悪時の急性期治療を目的として使用する薬剤ではない。
6. 用法及び用量
<気管支喘息>
通常、成人には、維持療法として1回1吸入(ブデソニドとして160μg、ホルモテロールフマル酸塩水和物として4.5μg)を1日2回吸入投与する。なお、症状に応じて増減するが、維持療法としての1日の最高量は1回4吸入1日2回(合計8吸入:ブデソニドとして1280μg、ホルモテロールフマル酸塩水和物として36μg)までとする。
維持療法として1回1吸入あるいは2吸入を1日2回投与している患者は、発作発現時に本剤の頓用吸入を追加で行うことができる。本剤を維持療法に加えて頓用吸入する場合は、発作発現時に1吸入する。数分経過しても発作が持続する場合には、さらに追加で1吸入する。必要に応じてこれを繰り返すが、1回の発作発現につき、最大6吸入までとする。
維持療法と頓用吸入を合計した本剤の1日の最高量は、通常8吸入までとするが、一時的に1日合計12吸入(ブデソニドとして1920μg、ホルモテロールフマル酸塩水和物として54μg)まで増量可能である。
維持療法と頓用吸入を合計した本剤の1日の最高量は、通常8吸入までとするが、一時的に1日合計12吸入(ブデソニドとして1920μg、ホルモテロールフマル酸塩水和物として54μg)まで増量可能である。
(参考)
| 維持療法として用いる場合 | 維持療法に加えて頓用吸入としても使用する場合 (維持療法として1回1吸入あるいは2吸入を1日2回投与している患者で可能) | ||
| 用法・用量 | 発作発現時の頓用吸入としての用法・用量 | 1回の発作発現における吸入可能回数 | 1日最高量 |
| 通常1回1吸入1日2回、症状に応じ1回4吸入1日2回まで。 | 1吸入行い、数分経過しても発作が持続する場合、さらに1吸入する。必要に応じてこれを繰り返す。 | 6吸入まで。 | 通常合計8吸入まで、一時的に合計12吸入まで注)。 |
<慢性閉塞性肺疾患(慢性気管支炎・肺気腫)の諸症状の緩解>
通常、成人には、1回2吸入(ブデソニドとして320μg、ホルモテロールフマル酸塩水和物として9μg)を1日2回吸入投与する。
7. 用法及び用量に関連する注意
<気管支喘息>
7.1 症状の緩解がみられた場合は、治療上必要最小限の用量を投与し、必要に応じ吸入ステロイド剤への切り替えも考慮すること。
7.2 β刺激剤の薬理学的作用による症状(動悸、頻脈、不整脈、振戦、頭痛及び筋痙攣等)の発現等により本剤を治療上必要な用量まで増量できない場合は、他の治療法を考慮すること。
[本剤を維持療法として使用する場合]
7.3 喘息患者を対象とした国内臨床試験における本剤の1日最高量(1回4吸入1日2回(1,280/36μg/日))の使用経験は少ないため、最高用量(1回4吸入1日2回)の投与は慎重に行うこと。
[本剤を維持療法に加えて頓用吸入としても使用する場合]
7.4 本剤の頓用吸入は維持療法としての使用に追加して行うこと。本剤は頓用吸入のみに使用しないこと。
7.5 維持療法としての吸入に引き続き頓用吸入を行う場合は、維持療法と頓用吸入の合計で最大6吸入までとすること。
7.6 維持療法として1回2吸入1日2回を超える用量を投与している場合は、発作発現時に本剤を頓用吸入で使用しないこと(1回2吸入1日2回を超える用量を投与している時に本剤を発作治療薬として頓用吸入した臨床経験がない)。
7.7 喘息患者を対象とした国際共同臨床試験(日本人患者を含む)において、本剤の通常1日最高量である合計8吸入超の使用経験、及び発作発現時に1回6吸入した使用経験は少ないため、1日最高量の投与は慎重に行うこと。
8. 重要な基本的注意
<効能共通>
8.1 本剤の維持療法としての定期吸入は気管支喘息あるいは慢性閉塞性肺疾患の長期管理を目的としており、毎日規則正しく使用すること。
8.2 喘息患者及び慢性閉塞性肺疾患患者において、感染を伴う症状の増悪がみられた場合には、ステロイド療法の強化と感染症の治療を考慮すること。
8.3 本剤の投与を突然中止すると喘息の急激な悪化を起こすことがあるので、投与を中止する場合には患者の喘息症状を観察しながら徐々に減量すること。なお、慢性閉塞性肺疾患患者においても、投与中止により症状が悪化するおそれがあるので、観察を十分に行うこと。
8.4 全身性ステロイド剤と比較して可能性は低いが、吸入ステロイド剤を長期間投与する場合には、副腎皮質機能低下等の全身作用が発現する可能性がある。特に本剤の高用量を長期間投与する場合には、定期的に検査を行うことが望ましい。また、異常が認められた場合には、患者の症状を観察しながら適切な処置を行うこと。
8.5 全身性ステロイド剤の減量は本剤吸入開始後症状の安定をみて徐々に行うこと。減量にあたっては一般のステロイド剤の減量法に準ずること。
8.6 全身性ステロイド剤の減量並びに離脱に伴って、鼻炎、湿疹、蕁麻疹、眩暈、動悸、倦怠感、顔のほてり、結膜炎等の症状が発現・増悪することがあるので、このような症状があらわれた場合には適切な処置を行うこと。
8.7 過度に本剤の使用を続けた場合、不整脈、場合により心停止を起こすおそれがあるので、用法・用量を超えて投与しないよう注意すること。また、患者に対し、本剤の過度の使用による危険性について理解させ、用法・用量を超えて使用しないよう注意を与えること。[13.1参照]
<気管支喘息>
8.8 以下の事項に注意すること。また患者に注意を与えること。
・本剤を維持療法として定期吸入する場合は、本剤の投与期間中に発現する発作に対しては、発作治療薬として短時間作動型吸入β2刺激剤等の他の適切な薬剤を使用すること。
・本剤を維持療法に加えて頓用吸入としても使用する場合は、発作に対しては、原則として他の発作治療薬は用いず、本剤を使用すること。
8.9 発作治療薬(本剤の頓用吸入を含む)の使用量が増加したり、効果が十分でなくなってきた場合には、喘息の管理が十分でないことが考えられるので、可及的速やかに医療機関を受診し治療を求めるように患者に注意を与えると共に、そのような状態がみられた場合には、生命を脅かす可能性があるので、本剤の維持用量の増量、あるいは全身性ステロイド剤等の他の適切な薬剤の追加を考慮すること。併用薬剤は症状の軽減に合わせて徐々に減量すること。
8.10 本剤を維持療法に加えて頓用吸入としても使用し、1日使用量が合計8吸入を超える場合には、医療機関を受診するよう患者に注意を与えること。またこのような患者では、喘息の状態を再度評価し、患者が受けている喘息維持治療の内容についても検討を行うこと。
8.11 喘息患者において、本剤を含む吸入ステロイド剤投与後に、潜在していた基礎疾患である好酸球性多発血管炎性肉芽腫症にみられる好酸球増多症がまれにあらわれることがある。この症状は通常、全身性ステロイド剤の減量並びに離脱に伴って発現しており、本剤との直接的な因果関係は確立されていない。本剤の投与期間中は、好酸球数の推移や、他の好酸球性多発血管炎性肉芽腫症の症状(しびれ、発熱、関節痛、肺の浸潤等の血管炎症状等)に注意すること。
<慢性閉塞性肺疾患(慢性気管支炎・肺気腫)の諸症状の緩解>
8.12 本剤の投与期間中に発現する慢性閉塞性肺疾患の急性増悪に対しては、医療機関を受診するよう患者に注意を与えること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 結核性疾患の患者
ステロイドの作用により症状を増悪するおそれがある。
9.1.2 感染症(有効な抗菌剤の存在しない感染症、深在性真菌症を除く)の患者
ステロイドの作用により症状を増悪するおそれがある。
9.1.3 甲状腺機能亢進症の患者
甲状腺機能亢進症の症状を悪化させるおそれがある。
9.1.4 高血圧の患者
血圧を上昇させるおそれがある。
9.1.5 心疾患のある患者
β1作用により症状を増悪させるおそれがある。
9.1.6 糖尿病の患者
グリコーゲン分解作用及びステロイドの作用により症状を増悪させるおそれがある。
9.1.7 低カリウム血症の患者
Na+/K+ ATPaseを活性化し細胞外カリウムを細胞内へ移動させることにより低カリウム血症を増悪させるおそれがある。
9.1.8 長期又は大量の全身性ステロイド療法を受けている患者
全身性ステロイド剤の減量中並びに離脱後も副腎皮質機能検査を行い、外傷、手術、重症感染症等の侵襲には十分に注意を払うこと。また、必要があれば一時的に全身性ステロイド剤の増量を行うこと。これらの患者では副腎皮質機能不全となっていることが考えられる。
9.1.9 喘息悪化により気管支粘液の分泌が著しい患者
全身性ステロイド剤等の併用を考慮すること。
9.1.10 低酸素血症の患者
血清カリウム値をモニターすることが望ましい。低酸素血症は血清カリウム値の低下が心リズムに及ぼす作用を増強することがある。[11.1.2参照]
9.3 肝機能障害患者
9.3.1 重度な肝機能障害のある患者
本剤の成分であるブデソニド及びホルモテロールはいずれも主に肝臓で代謝されるため血中濃度が上昇する可能性がある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。ラットを用いた器官形成期毒性試験では、ブデソニド/ホルモテロールフマル酸塩水和物として12/0.66μg/kg以上を吸入投与したときに、着床後胚損失率の増加、及び催奇形性作用が認められたことが報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
ブデソニドはヒト乳汁に移行するが、乳児の血液中には検出されないことが報告されている。ホルモテロールのヒト乳汁への移行は不明であるが、ラット乳汁への移行が報告されている。
9.7 小児等
小児等に対する臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能が低下している。
10. 相互作用
相互作用序文
ブデソニドは主として肝代謝酵素CYP3A4で代謝される。
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| CYP3A4阻害剤 イトラコナゾール等 [16.7.2参照] | 副腎皮質ステロイド剤を全身投与した場合と同様の症状があらわれる可能性がある。 | CYP3A4による代謝が阻害されることにより、ブデソニドの血中濃度が上昇する可能性がある。 |
| カテコールアミン アドレナリン イソプレナリン等 | 不整脈、場合によっては心停止を起こすおそれがあるので、副作用の発現に注意し、異常が認められた場合には減量又は投与を中止するなど適切な処置を行うこと。 | 併用により、アドレナリン作動性神経刺激の増大が起きる。 そのため、不整脈を起こすことがある。 |
| キサンチン誘導体 テオフィリン アミノフィリン等 [11.1.2参照] | 低カリウム血症による不整脈を起こすおそれがある。血清カリウム値のモニターを行うことが望ましい。 | キサンチン誘導体はアドレナリン作動性神経刺激を増大させるため、血清カリウム値の低下を増強することがある。 |
| 全身性ステロイド剤 プレドニゾロン ベタメタゾン等 [11.1.2参照] | 低カリウム血症による不整脈を起こすおそれがある。血清カリウム値のモニターを行うことが望ましい。 | 全身性ステロイド剤及び利尿剤は尿細管でのカリウム排泄促進作用があるため、血清カリウム値の低下が増強することが考えられる。 |
| 利尿剤 フロセミド等 [11.1.2参照] | 低カリウム血症による不整脈を起こすおそれがある。血清カリウム値のモニターを行うことが望ましい。 | 全身性ステロイド剤及び利尿剤は尿細管でのカリウム排泄促進作用があるため、血清カリウム値の低下が増強することが考えられる。 |
| β遮断剤 アテノロール等 | ホルモテロールの作用を減弱する可能性がある。 | β受容体において競合的に拮抗する。 |
| QT間隔延長を起こすことが知られている薬剤 抗不整脈剤 三環系抗うつ剤等 | QT間隔が延長され心室性不整脈等のリスクが増大するおそれがある。 | いずれもQT間隔を延長させる可能性がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 アナフィラキシー(頻度不明)
アナフィラキシー(呼吸困難、気管支攣縮、全身潮紅、血管浮腫、蕁麻疹等)があらわれることがある。
11.1.2 重篤な血清カリウム値の低下(0.1〜1%未満)
11.2 その他の副作用
| 1〜5%未満 | 0.1〜1%未満 | 0.1%未満 | 頻度不明 | |
| 過敏症 | 発疹、蕁麻疹、接触性皮膚炎、血管浮腫等の過敏症状 | |||
| 口腔・呼吸器 | 嗄声 | 咽喉頭の刺激感、口腔カンジダ症、咳嗽、感染、肺炎 | 味覚異常、気管支痙攣注) | |
| 消化器 | 悪心 | |||
| 精神神経系 | 頭痛、振戦、神経過敏 | 情緒不安、めまい、睡眠障害 | 激越、抑うつ、行動障害 | |
| 循環器 | 動悸、不整脈(心房細動、上室性頻脈、期外収縮等)、頻脈、血圧上昇 | 狭心症 | ||
| 筋・骨格系 | 筋痙攣 | |||
| 内分泌 | 高血糖 | |||
| その他 | 皮膚挫傷 |
13. 過量投与
13.1 症状
ブデソニドの過量投与により副腎皮質系機能が低下することがある。ホルモテロールフマル酸塩水和物の過量投与により、動悸、頻脈、不整脈、振戦、頭痛及び筋痙攣等、β刺激剤の薬理学的作用による全身作用が発現する可能性がある。また、重篤な症状として、血圧低下、代謝性アシドーシス、低カリウム血症、高血糖、心室性不整脈あるいは心停止等が発現する可能性がある。[8.7参照]
13.2 処置
副腎皮質系機能の低下がみられた場合には患者の症状を観察しながら徐々に減量するなど適切な処置を行うこと。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 吸入前
本剤の投与にあたって、吸入器の操作法、吸入法等を十分に説明すること。
(1)患者に本剤を交付する際には、包装中に添付している患者用説明文書を渡し、使用方法を指導すること。
(2)初めて本剤を投与する患者には、本剤が十分に気道に到達するよう吸入方法をよく説明したうえ、吸入の訓練をさせること。
14.1.2 吸入時
本剤は口腔内への吸入投与のみに使用すること。
14.1.3 吸入後
口腔カンジダ症又は嗄声の予防のため、本剤吸入後に、うがいを実施するよう患者を指導すること。ただし、うがいが困難な患者には、うがいではなく口腔内をすすぐよう指導すること。
14.1.4 保管時
(1)使用後は必ずキャップ(カバー)を閉めて保管すること。
(2)マウスピースの外側を週に1〜2回乾燥した布で清拭すること(水洗いはしないこと)。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 外国における疫学調査で、吸入ステロイド剤投与によりまれに白内障が発現するとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男性(14例)に本剤4吸入(ブデソニド:640μg、ホルモテロールフマル酸塩水和物:18μg)を単回吸入投与したとき、ブデソニド及びホルモテロールはいずれも速やかに最高血漿中濃度(Cmax)に達した。消失半減期(t1/2)はブデソニドで約3時間、ホルモテロールで約6時間であった1)。
図1 単回吸入投与後の血漿中ブデソニド濃度(14例の平均値±標準偏差)
| ブデソニド(μg) | Cmax(nmol/L) | Tmax(min) | AUC0-∞(nmol・h/L) | t1/2(h) |
| 640 | 10.3±2.37 | 5.36±1.34 | 14.0±1.93 | 3.09±0.49 |
図2 単回吸入投与後の血漿中ホルモテロール濃度(14例の平均値±標準偏差)
| ホルモテロールフマル酸塩水和物(μg) | Cmax(pmol/L) | Tmax(min) | AUC0-∞(pmol・h/L) | t1/2(h) |
| 18 | 175±56.4 | 5.00±0.00 | 329±81.0 | 6.14±2.66 |
16.1.2 反復投与
健康成人男性(11〜12例)に本剤2吸入(ブデソニド:320μg、ホルモテロールフマル酸塩水和物:9μg)または4吸入(ブデソニド:640μg、ホルモテロールフマル酸塩水和物:18μg)を1日2回7日間反復投与したとき、ブデソニド及びホルモテロールはそれぞれ投与後10分以内、投与後5分にCmaxに達した。t1/2はブデソニドで約3.5時間、ホルモテロールで約5〜7時間であった。ブデソニド及びホルモテロールのCmax及び血漿中濃度−時間曲線下面積(AUC)は投与量にほぼ比例して増加した。ブデソニド及びホルモテロールともに反復投与による薬物動態の変化は認められなかった1)。
16.3 分布
16.4 代謝
ブデソニド
ホルモテロール
16.5 排泄
健康成人に3H標識ブデソニド100μgを静脈内投与したとき、投与後96時間までに投与量の57%が尿中に、34%が糞中に排泄された6)(外国人データ)。
健康成人に3H標識ホルモテロール37μgを経口投与後直ちに3H標識ホルモテロール16μgを静脈内持続注入(30分)したとき、投与後168時間までに投与放射能の62%が尿中に、24%が糞中に排泄された8)(外国人データ)。
16.7 薬物相互作用
17. 臨床成績
17.1 有効性及び安全性に関する試験
<気管支喘息>
17.1.1 国内第III相試験
テオフィリン徐放製剤と吸入ステロイド剤を併用中の成人気管支喘息患者346例を対象とした無作為化二重盲検実薬対照並行群間比較試験において、本剤(ブデソニド/ホルモテロールフマル酸塩水和物)1回1吸入1日2回、又は対照薬(ブデソニドとテオフィリン徐放製剤の併用)1日2回を8週間投与した結果は、下表のとおりであった13)。
| 投与群 | 症例数 | 投与前からの変化量a) | 群間差b)95%信頼区間 |
| 本剤(ブデソニド/ホルモテロールフマル酸塩水和物) | 176 | 15.2±31.2 | 8.76(2.64,14.88) |
| 対照(ブデソニド+テオフィリン徐放製剤) | 170 | 6.5±26.2 |
副作用発現頻度は、本剤群で8.0%(14/176例)であった。主な副作用は、筋痙縮2.3%(4/176例)、頭痛及び喘息 各1.1%(2/176例)であった。
17.1.2 国内長期投与試験
成人気管支喘息患者138例を対象とした長期投与試験において、本剤1回1吸入、2吸入または4吸入1日2回を52週間投与したとき、肺機能に関連した評価項目の投与前からの推移は下図の通りであった(図1)14)。なお、本試験では、組み入れ時のステロイドの用量に応じて本剤1吸入または2吸入1日2回で投与開始し、投与開始2週以降は症状に応じて4吸入1日2回まで適宜増減した。
図1 朝のピークフロー値の推移(平均値±標準誤差)
副作用発現頻度は、本剤群で31.9%(44/138例)であった。主な副作用は、発声障害11.6%(16/138例)、動悸5.1%(7/138例)、筋痙縮3.6%(5/138例)、咽喉頭疼痛2.9%(4/138例)であった。
17.1.3 国際共同第III相試験
成人気管支喘息患者2,091例(日本人患者400例を含む)を対象とした無作為化二重盲検実薬対照並行群間比較試験において、本剤1回1吸入1日2回を維持療法として定期吸入することに加えて、発作発現時(咳嗽、喘鳴、胸苦しさ、息切れ等の喘息症状)に本剤または対照薬(テルブタリン硫酸塩の吸入剤注1))を頓用吸入する治療法を52週間行った。本剤を維持療法として定期吸入することに加えて発作発現時に頓用吸入する治療法により、初回の重症急性増悪までの期間が有意に延長し(p=0.0007、ログランク検定)、初回の重症急性増悪のリスクは約30%低下した(図2)。また対照群と比較して重症急性増悪回数は少なく(0.214回/人・年 対 0.307回/人・年)、重症急性増悪を発現した患者の割合についても小さかった(16.2% 対 22.0%)15)
図2 初回の重症急性増悪までの期間
副作用発現頻度は、本剤を維持療法として定期吸入することに加えて発作発現時に頓用吸入する治療法群で3.9%(41/1049例)であった。主な副作用は、口腔カンジダ症及び動悸 各0.5%(5/1049例)、発声障害及び細菌性上気道感染 各0.3%(3/1049例)であった。
17.1.4 海外第III相試験
外国人の成人及び思春期気管支喘息患者3,394例を対象とした12ヵ月間の無作為化二重盲検実薬対照並行群間比較試験において、本剤を維持療法として定期吸入(1吸入1日2回)することに加えて発作発現時(咳嗽、喘鳴、胸苦しさ、息切れ等の喘息症状)に頓用吸入する治療法により、対照群(本剤1吸入1日2回の定期吸入に加えて発作発現時にホルモテロール注2)を頓用吸入)と比較して、初回の重症急性増悪までの期間が有意に延長し(p=0.0048、ログランク検定)、初回の重症急性増悪のリスクは27%低下した。また、対照群と比較して、重症急性増悪回数は少なかった(0.19回/人・年 対 0.29回/人・年)16)。
有害事象発現頻度は、本剤を維持療法として定期吸入することに加えて発作発現時に頓用吸入する治療法群で50.2%(556/1107例)であった。主な有害事象は、鼻咽頭炎10.1%(112/1107例)、咽頭炎5.8%(64/1107例)及び上気道感染5.2%(58/1107例)であった。
17.1.5 海外第III相試験
外国人の成人及び思春期気管支喘息患者3,335例を対象とした6ヵ月間の無作為化二重盲検実薬対照並行群間比較試験において、本剤を維持療法として定期吸入(1吸入1日2回)することに加えて発作発現時(咳嗽、喘鳴、胸苦しさ、息切れ等の喘息症状)に頓用吸入する治療法により、対照群(サルメテロール/フルチカゾンプロピオン酸エステル配合剤100/500μg/日の定期吸入に加えて発作発現時にテルブタリン硫酸塩注1)を頓用吸入)と比較して、初回の重症急性増悪までの期間が有意に延長し(p=0.0034、ログランク検定)、初回の重症急性増悪のリスクは33%低下した。また、対照群と比較して、重症急性増悪回数は少なかった(0.12回/人・6ヵ月 対 0.19回/人・6ヵ月)17)。
有害事象発現頻度は、本剤を維持療法として定期吸入することに加えて発作発現時に頓用吸入する治療法群で41.4%(457/1103例)であった。主な有害事象は、上気道感染5.5%(61/1103例)、咽頭炎5.2%(57/1103例)及び鼻咽頭炎4.3%(47/1103例)であった。
17.1.6 海外第III相試験
外国人の成人及び思春期気管支喘息患者2,309例を対象とした26週間の無作為化二重盲検実薬対照並行群間比較試験において、本剤を維持療法として定期吸入(2吸入1日2回投与)することに加えて発作発現時(咳嗽、喘鳴、胸苦しさ、息切れ等の喘息症状)に頓用吸入する治療法により、対照群(サルメテロール/フルチカゾンプロピオン酸エステル配合剤100/1,000μg/日を維持療法として定期的に吸入し、発作発現時にテルブタリン硫酸塩注1)を頓用吸入)と比較して重症急性増悪回数は少なかった(0.12回/人・6ヵ月 対 0.16回/人・6ヵ月)が、主要評価項目である初回の重症急性増悪までの期間に関する対比較において有意差は認められなかった(p=0.12、国を層としたCoxの比例ハザードモデル)18)。
有害事象発現頻度は、本剤を維持療法として定期吸入することに加えて発作発現時に頓用吸入する治療法群で39.2%(451/1151例)であった。主な有害事象は、上気道感染5.6%(64/1151例)、鼻咽頭炎4.7%(54/1151例)及び頭痛3.2%(37/1151例)であった。
注1)テルブタリン硫酸塩の吸入剤は本邦未承認
注2)ホルモテロールの吸入剤は気管支喘息に対して本邦未承認
<慢性閉塞性肺疾患(慢性気管支炎・肺気腫)>
17.1.7 国際共同第III相試験
慢性閉塞性肺疾患患者1,293例(日本人患者312例を含む)を対象とした12週間の国際共同無作為化二重盲検実薬対照並行群間比較試験19)において、本剤2吸入1日2回投与により、ホルモテロールフマル酸塩水和物に比して肺機能が有意に改善した(表2)。
| 本剤群 | ホルモテロール群 | 本剤群のホルモテロール群に対する比[95%信頼区間] p値b) | |||||
| 例数 | 幾何平均値(CV%) | 中央値(範囲) | 例数 | 幾何平均値(CV%) | 中央値(範囲) | ||
| ベースライン(L) | 635 | 0.971(38.254) | 0.980(0.33-2.53) | 657 | 0.945(37.963) | 0.950(0.31-2.61) | |
| 全投与期間の平均a)(L) | 619 | 1.021(41.361) | 1.033(0.35-3.29) | 635 | 0.968(38.628) | 0.967(0.32-2.58) | − |
| ベースラインに対する比(%) | 618 | 104.6(18.7) | 102.6(37.4-311.1) | 635 | 101.5(16.6) | 100.7(35.1-218.5) | 1.032[1.013,1.052] (p=0.0011) |
更に本剤投与によりホルモテロールに比して増悪回数が減少し(本剤93件、ホルモテロール151件)、増悪を発現した患者の割合についても小さく(本剤11.9%<76/363例>、ホルモテロール16.9%<111/657例>)、初回増悪までの期間が延長した。
副作用発現頻度は、本剤群で4.2%(27/636例)であった。主な副作用は、発声障害1.6%(10/636例)、慢性閉塞性肺疾患及び食道カンジダ症 各0.5%(3/636例)、肺炎0.3%(2/636例)であった。
17.1.8 国内長期投与試験
慢性閉塞性肺疾患患者260例を対象とした長期投与試験20)において、本剤2吸入1日2回を52週間投与したとき、投与前からのFEV1の改善が維持された。
副作用発現頻度は、本剤群で25.4%(33/130例)であった。主な副作用は、肺炎及び発声障害 各3.8%(5/130例)、慢性閉塞性肺疾患、口腔カンジダ症及び食道カンジダ症 各2.3%(3/130例)であった。
17.1.9 海外第III相試験
外国人の慢性閉塞性肺疾患患者1,022例を対象とした12ヵ月の無作為化二重盲検並行群間比較試験において、本剤2吸入1日2回投与はプラセボ、ブデソニド注3)あるいはホルモテロールに比して肺機能を有意に改善した(表3)21)。また本剤投与により初回の重度増悪までの期間がプラセボ、ホルモテロールあるいはブデソニド注3)に比して有意に延長した(表4)。
有害事象発現頻度は、本剤群で62%(157/254例)であった。主な有害事象は、慢性閉塞性気道疾患19%(49/254例)及び呼吸器感染14%(36/254例)であった。
| 例数 | ベースライン(L)a) | 全投与期間中の平均(L)a),b) | ベースラインに対する調整済み比(%)c) | 本剤群の各群に対する比[95%信頼区間](%)c) | p値c) | |
| 本剤群 | 234 | 1.11(0.3-3.1) | 1.10(0.4-2.8) | 98.96 | − | − |
| プラセボ群 | 214 | 1.14(0.4-3.3) | 0.98(0.4-3.2) | 86.74 | 114.09[110.45,117.84] | <0.001 |
| ブデソニド群 | 223 | 1.13(0.3-3.3) | 1.00(0.4-2.8) | 88.88 | 111.34[107.82,114.97] | <0.001 |
| ホルモテロール群 | 213 | 1.18(0.4-2.7) | 1.09(0.4-3.0) | 93.93 | 105.36[101.99,108.84] | 0.002 |
| 中央値(日) | 本剤群の各群に対するハザード比a)[95%信頼区間] | p値b) | |
| 本剤群 | 254 | − | − |
| プラセボ群 | 96 | 0.715[0.562,0.910] | 0.017 |
| ブデソニド群 | 178 | 0.773[0.611,0.980] | 0.037 |
| ホルモテロール群 | 154 | 0.705[0.558,0.891] | 0.002 |
17.1.10 海外第III相試験
外国人の慢性閉塞性肺疾患患者812例を対象とした12ヵ月の無作為化二重盲検並行群間比較試験において、本剤2吸入1日2回投与はプラセボあるいはブデソニド注3)に比して肺機能を有意に改善した(表5)22)。また本剤投与により重度増悪回数がプラセボあるいはホルモテロールに比して有意に減少した(表6)。
有害事象発現頻度は、本剤群で65%(136/208例)であった。主な有害事象は、慢性閉塞性気道疾患17%(35/208例)及び呼吸器感染12%(24/208例)であった。
| 例数 | ベースライン(L)a) | 全投与期間中の平均(L)a),b) | ベースラインに対する調整済み比(%)c) | 本剤群の各群に対する比[95%信頼区間](%)c) | p値c) | |
| 本剤群 | 201 | 0.96(0.4-2.0) | 1.08(0.4-2.9) | 111.52 | − | − |
| プラセボ群 | 185 | 0.98(0.4-2.8) | 0.95(0.4-2.3) | 97.03 | 114.94[110.96,119.06] | <0.001 |
| ブデソニド群 | 182 | 0.98(0.4-2.3) | 1.01(0.5-2.4) | 102.14 | 109.18[105.38,113.12] | <0.001 |
| ホルモテロール群 | 191 | 1.00(0.4-2.7) | 1.10(0.4-3.2) | 110.15 | 101.25[97.76,104.86] | 0.487 |
| 例数 | 平均回数a)(/人・年) | 本剤群の各群に対する比[95%信頼区間]a) | p値a),b) | |
| 本剤群 | 204 | 1.42 | − | − |
| プラセボ群 | 201 | 1.87 | 0.758[0.586,0.981] | 0.035 |
| ブデソニド群 | 192 | 1.59 | 0.889[0.682,1.159] | 0.385 |
| ホルモテロール群 | 199 | 1.84 | 0.771[0.599,0.992] | 0.043 |
注3)ブデソニド吸入剤は慢性閉塞性肺疾患に対して本邦未承認
18. 薬効薬理
18.1 作用機序
18.2 抗炎症作用
ブデソニド
18.3 気道過敏反応抑制作用
18.4 気管支拡張作用
ホルモテロールフマル酸塩水和物
18.5 GM-CSF産生の抑制作用
シムビコート(ブデソニド+ホルモテロールフマル酸塩水和物)
In vitroのヒト気管支上皮細胞において、ブデソニドとホルモテロールの同時添加によって、TNF-α刺激GM-CSF産生を単独添加よりも強力に抑制した37)。
18.6 気管支保護作用及び肺浮腫抑制作用
シムビコート(ブデソニド+ホルモテロールフマル酸塩水和物)
ラットアレルギーモデルの気管内にブデソニドとホルモテロールを併用投与時、メタコリン誘発気道収縮及び肺浮腫を相乗的に抑制した(各抑制率(%)は、ブデソニド、ホルモテロール、併用の順に、気道収縮:29.1、12.9、73.2、肺浮腫:25.9、15.7、45.3)38)。
19. 有効成分に関する理化学的知見
19.1. ブデソニド
19.2. ホルモテロールフマル酸塩水和物
22. 包装
<シムビコートタービュヘイラー30吸入>
[1本、乾燥剤入り]
<シムビコートタービュヘイラー60吸入>
[1本、乾燥剤入り]
[10本、乾燥剤入り]
23. 主要文献
- 深瀬広幸 他, アレルギー・免疫, 16 (10), 1586-602, (2009)
- 社内資料:ブデソニドのin vitro血漿蛋白結合, (1995)
- 社内資料:ホルモテロールフマル酸塩のin vitro血漿蛋白結合(843-RD-0354)(2009年10月16日承認、CTD2.7.2.2)
- 宮本昭正 他, アレルギーの領域, 4 (S-1), 18-25, (1997)
- 社内資料:ホルモテロール吸入投与時の肺内到達率(SD-037-0602)(2009年10月16日承認、CTD2.7.2.2)
- 社内資料:ブデソニドのヒトにおける代謝排泄, (1984)
- Jonsson G,et al., Drug Metab Dispos., 23, 137-42, (1995) »PubMed
- Rosenborg J,et al., Drug Metab Dispos., 27, 1104-16, (1999) »PubMed
- 社内資料:ホルモテロールのシトクロムP450阻害作用の検討(843-RD-0395)(2009年10月16日承認、CTD2.7.2.2)
- 社内資料:シムビコートと各単剤の血漿中濃度の比較(SD-039-0259)(2009年10月16日承認、CTD2.7.1.2)
- Seidegard J., Clin Pharmacol Ther., 68, 13-7, (2000) »PubMed »DOI
- Raaska K,et al., Clin Pharmacol Ther., 72, 362-9, (2002) »PubMed »DOI
- 大田 健 他, アレルギー・免疫, 17 (4), 624-38, (2010)
- 足立 満, アレルギー・免疫, 17 (2), 266-82, (2010)
- Atienza T,et al., Respirology., 18 (2), 354-63, (2013) »PubMed »DOI
- Rabe KF,et al., Lancet., 368, 744-53, (2006) »PubMed »DOI
- Kuna P,et al., Int J Clin Pract., 61, 725-36, (2007) »PubMed »DOI
- Bousquet J,et al., Respir Med., 101, 2437-46, (2007) »PubMed »DOI
- 社内資料:シムビコートの慢性閉塞性肺疾患患者における国際共同第III相比較試験(2012年8月10日承認、CTD2.7.3.3)
- 社内資料:シムビコートの日本人慢性閉塞性肺疾患患者における第III相長期投与試験(2012年8月10日承認、CTD2.7.3.3)
- Calverley PM,et al., Eur Respir J., 22, 912-9, (2003) »PubMed »DOI
- Szafranski W,et al., Eur Respir J., 21, 74-81, (2003) »PubMed »DOI
- Brattsand R,et al., Clin Ther., 25 (Suppl C), C28, (2003) »PubMed »DOI
- Edsbacker S,et al., Annals of Allergy Asthma&Immunology., 88 (6), 609-16, (2002)
- Ullman A,et al., Allergy., 47, 384-7, (1992) »PubMed »DOI
- Barnes PJ., Eur Respir J., 19, 182-91, (2002) »PubMed »DOI
- Roth M,et al., The Lancet., 360, 1293-9, (2002)
- Linden M,et al., Pulm Pharmacol., 7, 43-7, (1994) »PubMed »DOI
- Woolley MJ,et al., J Appl Physiol., 77, 1303-8, (1994) »PubMed »DOI
- 社内資料:呼吸困難症SD系ラットにおける卵白アルブミン誘発気道/肺過敏反応及び炎症細胞に対する作用, (1995)
- Svensjo E,et al., Prog Resp Res., 19, 173-80, (1985)
- Brattsand R,et al., Amsterdam,Excerpta Medica.Proceeding from a Symposium in Basel., 145-53, (1984)
- O’Riordan TG,et al., J Appl Physiol., 85 (3), 1086-91, (1998) »PubMed »DOI
- Abraham WM,et al., Bull Eur Physiopathol Respir., 22, 387-92, (1986) »PubMed
- Ida H., Arzneimittelforschung., 26 (7), 1337-40, (1976) »PubMed
- Selroos O.et al., Pulm Pharmacol Ther., 15, 175-83, (2002)
- Korn SH,et al., Eur Respir J., 17, 1070-7, (2001) »PubMed »DOI
- 社内資料:アレルギーラットモデルの気道過敏性及び炎症に及ぼす影響(2009年10月16日承認、CTD2.6.2.2)
24. 文献請求先及び問い合わせ先
文献請求先
アストラゼネカ株式会社
メディカルインフォメーションセンター
〒530-0011
大阪市北区大深町3番1号
電話:0120-189-115
製品情報問い合わせ先
アストラゼネカ株式会社
メディカルインフォメーションセンター
〒530-0011
大阪市北区大深町3番1号
電話:0120-189-115
26. 製造販売業者等
26.1 製造販売元
アストラゼネカ株式会社
大阪市北区大深町3番1号
その他の説明
参考
本剤のブデソニド用量は、容器(タービュヘイラー)から放出される薬剤量として表記しており、パルミコートタービュヘイラーのブデソニド用量は容器(タービュヘイラー)内で量り取られる薬剤量として表記している。
両薬剤の用量対応は、以下のとおりである。
両薬剤の用量対応は、以下のとおりである。
| ブデソニドの用量 | ||
| シムビコートタービュヘイラー 容器から放出される量 (delivered dose) | パルミコート200μgタービュヘイラー 容器内で量り取られる量 (metered dose) | |
| 1回吸入 | 160μg | 200μg |
| 2回吸入 | 320μg | 400μg |
| 4回吸入 | 640μg | 800μg |
| 8回吸入 | 1280μg | 1600μg |