医薬品情報
| 総称名 | アマリール |
|---|---|
| 一般名 | グリメピリド |
| 欧文一般名 | Glimepiride |
| 薬効分類名 | スルホニルウレア系経口血糖降下剤 |
| 薬効分類番号 | 3961 |
| ATCコード | A10BB12 |
| KEGG DRUG |
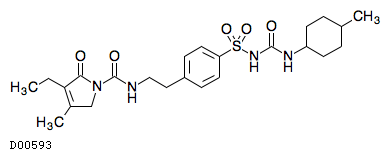
D00593
グリメピリド
|
| KEGG DGROUP |
DG01734
スルホニル尿素薬 (SU薬)
DG02044
血糖降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年3月 改訂(第2版)

|
1.警告 2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アマリール0.5mg錠 | Amaryl Tablets | サノフィ | 3961008F3023 | 10.8円/錠 | 劇薬, 処方箋医薬品 |
| アマリール1mg錠 | Amaryl Tablets | サノフィ | 3961008F1020 | 10.8円/錠 | 劇薬, 処方箋医薬品 |
| アマリール3mg錠 | Amaryl Tablets | サノフィ | 3961008F2027 | 16.6円/錠 | 劇薬, 処方箋医薬品 |
1. 警告
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
2型糖尿病(ただし、食事療法・運動療法のみで十分な効果が得られない場合に限る。)
6. 用法及び用量
通常、グリメピリドとして1日0.5〜1mgより開始し、1日1〜2回朝または朝夕、食前または食後に経口投与する。
維持量は通常1日1〜4mgで、必要に応じて適宜増減する。なお、1日最高投与量は6mgまでとする。
維持量は通常1日1〜4mgで、必要に応じて適宜増減する。なお、1日最高投与量は6mgまでとする。
8. 重要な基本的注意
8.2 投与する場合には、少量より開始し、血糖、尿糖を定期的に検査し、薬剤の効果を確かめ、効果が不十分な場合には、速やかに他の治療法への切り替えを行うこと。
8.3 重篤かつ遷延性の低血糖を起こすことがあるので、高所作業、自動車の運転等に従事している患者に投与するときには注意すること。[11.1.1参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 低血糖を起こすおそれのある以下の患者又は状態
9.2 腎機能障害患者
9.3 肝機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。スルホニルウレア系薬剤は胎盤を通過することが報告されており、新生児の低血糖、巨大児が認められている。また、本剤の動物実験(ラット、ウサギ)で催奇形性作用が報告されている。[2.5参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。授乳を継続する場合、児の低血糖の症状について観察を十分に行うこと。本剤のヒト母乳への移行性及び乳汁産生への影響は不明である。動物実験(ラット)において、母乳への移行が認められている。また、他のスルホニルウレア系薬剤で母乳へ移行することが報告されている。
9.7 小児等
9.7.2 低出生体重児、新生児、乳児、幼児又は9歳未満の小児を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.8 高齢者
少量から投与を開始し定期的に検査を行うなど慎重に投与すること。生理機能が低下していることが多く、低血糖があらわれやすい。[11.1.1参照]
10. 相互作用
相互作用序文
本剤は、主に肝代謝酵素CYP2C9により代謝される。
薬物代謝酵素用語
CYP2C9
10.2 併用注意
| 糖尿病用薬 インスリン製剤 ビグアナイド系薬剤 チアゾリジン系薬剤 α-グルコシダーゼ阻害剤 DPP-4阻害薬 GLP-1受容体作動薬 SGLT2阻害剤 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 血糖降下作用が増強される。 |
| プロベネシド | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 腎排泄抑制により血糖降下作用が増強される。 |
| クマリン系薬剤 ワルファリンカリウム | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 肝代謝抑制により血糖降下作用が増強される。 |
| サリチル酸剤 アスピリン サザピリン 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 血中蛋白との結合抑制、サリチル酸剤の血糖降下作用により血糖降下作用が増強される。 |
| プロピオン酸系消炎剤 ナプロキセン ロキソプロフェンナトリウム水和物 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 血中蛋白との結合抑制により、これらの消炎剤は蛋白結合率が高いので、血中に本剤の遊離型が増加して血糖降下作用が増強するおそれがある。 |
| アリール酢酸系消炎剤 アンフェナクナトリウム水和物 ナブメトン 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 血中蛋白との結合抑制により、これらの消炎剤は蛋白結合率が高いので、血中に本剤の遊離型が増加して血糖降下作用が増強するおそれがある。 |
| オキシカム系消炎剤 ロルノキシカム 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 血中蛋白との結合抑制により、これらの消炎剤は蛋白結合率が高いので、血中に本剤の遊離型が増加して血糖降下作用が増強するおそれがある。 |
| β-遮断剤 プロプラノロール アテノロール ピンドロール 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 糖新生抑制、アドレナリンによる低血糖からの回復抑制、低血糖に対する交感神経症状抑制により血糖降下作用が増強される。 |
| モノアミン酸化酵素阻害剤 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | インスリン分泌促進、糖新生抑制により血糖降下作用が増強される。 |
| クラリスロマイシン | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 機序不明 左記薬剤が他のスルホニルウレア系薬剤の血中濃度を上昇させたとの報告がある。 |
| サルファ剤 スルファメトキサゾール 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 血中蛋白との結合抑制、肝代謝抑制、腎排泄抑制により血糖降下作用が増強される。 |
| クロラムフェニコール | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 肝代謝抑制により血糖降下作用が増強される。 |
| テトラサイクリン系抗生物質 テトラサイクリン塩酸塩 ミノサイクリン塩酸塩 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | インスリン感受性促進により血糖降下作用が増強される。 |
| シプロフロキサシン レボフロキサシン水和物 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 機序不明 |
| フィブラート系薬剤 クロフィブラート ベザフィブラート 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 血中蛋白との結合抑制、肝代謝抑制、腎排泄抑制により血糖降下作用が増強される。 |
| アゾール系抗真菌剤 ミコナゾール フルコナゾール 等 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | 肝代謝抑制(CYP2C9阻害)、血中蛋白との結合抑制により血糖降下作用が増強される。 |
| シベンゾリンコハク酸塩 ジソピラミド ピルメノール塩酸塩水和物 | 低血糖症状が起こることがある。 血糖値その他患者の状態を十分観察し、必要に応じて本剤又は併用薬剤の投与量を調節するなど慎重に投与すること。特にβ-遮断剤と併用する場合にはプロプラノロール等の非選択性薬剤は避けることが望ましい。 | インスリン分泌促進によると考えられる血糖降下作用の増強のおそれがある。 |
| アドレナリン | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 末梢でのブドウ糖の取り込み抑制、肝臓での糖新生促進により血糖降下作用が減弱される。 |
| 副腎皮質ホルモン コルチゾン酢酸エステル ヒドロコルチゾン 等 | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 肝臓での糖新生促進、末梢組織でのインスリン感受性低下により血糖降下作用が減弱される。 |
| 甲状腺ホルモン レボチロキシンナトリウム水和物 乾燥甲状腺 等 | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 腸管でのブドウ糖吸収亢進、グルカゴンの分泌促進、カテコールアミンの作用増強、肝臓での糖新生促進により血糖降下作用が減弱される。 |
| 卵胞ホルモン エストラジオール安息香酸エステル エストリオール 等 | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 コルチゾール分泌変化、組織での糖利用変化、成長ホルモンの過剰産生、肝機能の変化等によると考えられる血糖降下作用の減弱のおそれがある。 |
| 利尿剤 トリクロルメチアジド フロセミド 等 | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン分泌の抑制、末梢でのインスリン感受性の低下により血糖降下作用が減弱される。 |
| ピラジナミド | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 血糖値のコントロールが難しいとの報告がある。 |
| イソニアジド | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 糖質代謝の障害による血糖値上昇及び耐糖能異常により血糖降下作用が減弱される。 |
| リファンピシン | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 肝代謝促進(CYP誘導)により血糖降下作用が減弱される。 |
| ニコチン酸 | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 肝臓でのブドウ糖の同化抑制により血糖降下作用が減弱される。 |
| フェノチアジン系薬剤 クロルプロマジン フルフェナジン 等 | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン遊離抑制、副腎からのアドレナリン遊離により血糖降下作用が減弱される。 |
| フェニトイン | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | インスリンの分泌阻害により血糖降下作用が減弱される。 |
| ブセレリン酢酸塩 | 高血糖症状(嘔気・嘔吐、脱水、呼気のアセトン臭等)が起こることがある。 血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 ブセレリン酢酸塩投与により、耐糖能が悪化したという報告がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 低血糖(4.08%)
低血糖(初期症状:脱力感、高度の空腹感、発汗等)があらわれることがある。なお、徐々に進行する低血糖では、精神障害、意識障害等が主である場合があるので注意すること。
また、本剤の投与により低血糖症状(脱力感、高度の空腹感、発汗、動悸、振戦、頭痛、知覚異常、不安、興奮、神経過敏、集中力低下、精神障害、意識障害、痙攣等)が認められた場合には糖質を含む食品を摂取するなど適切な処置を行うこと。ただし、α-グルコシダーゼ阻害剤との併用により低血糖症状が認められた場合にはブドウ糖を投与すること。
また、低血糖は投与中止後、臨床的にいったん回復したと思われる場合でも数日間は再発することがある。[1.、2.2、2.4、8.1、8.3、9.1.1、9.2.1、9.2.2、9.3.1、9.3.2、9.7.1、9.8、13.1参照]
また、本剤の投与により低血糖症状(脱力感、高度の空腹感、発汗、動悸、振戦、頭痛、知覚異常、不安、興奮、神経過敏、集中力低下、精神障害、意識障害、痙攣等)が認められた場合には糖質を含む食品を摂取するなど適切な処置を行うこと。ただし、α-グルコシダーゼ阻害剤との併用により低血糖症状が認められた場合にはブドウ糖を投与すること。
また、低血糖は投与中止後、臨床的にいったん回復したと思われる場合でも数日間は再発することがある。[1.、2.2、2.4、8.1、8.3、9.1.1、9.2.1、9.2.2、9.3.1、9.3.2、9.7.1、9.8、13.1参照]
11.1.2 汎血球減少、無顆粒球症、溶血性貧血、血小板減少(いずれも頻度不明)
11.1.3 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、Al-Pの上昇等を伴う肝機能障害、黄疸があらわれることがある。
11.1.4 再生不良性貧血(頻度不明)
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 血液 | 白血球減少、貧血 | |
| 肝臓 | AST上昇、ALT上昇、Al-P上昇、LDH上昇、γ-GTP上昇 | |
| 腎臓 | BUN上昇 | |
| 消化器 | 嘔気、嘔吐、心窩部痛、下痢、腹部膨満感 | 便秘、腹痛 |
| 過敏症 | 発疹、そう痒感等 | 光線過敏症 |
| 精神神経系 | めまい | 頭痛 |
| その他 | 血清カリウム上昇・ナトリウム低下等の電解質異常 | 味覚異常、CK上昇、浮腫、倦怠感、脱毛、一過性視力障害 |
13. 過量投与
13.1 症状
低血糖が起こることがある。[11.1.1参照]
13.2 処置
13.2.1 飲食が可能な場合
ブドウ糖(5〜15g)又は10〜30gの砂糖の入った吸収の良いジュース、キャンディなどを摂取させる。
13.2.2 意識障害がある場合
ブドウ糖液(50%20mL)を静注し、必要に応じて5%ブドウ糖液点滴により血糖値の維持を図る。
13.2.3 その他
血糖上昇ホルモンとしてのグルカゴン投与もよい。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 スルホニルウレア系薬剤(トルブタミド1日1.5g)を長期間継続使用した場合、食事療法単独の場合と比較して心臓・血管系障害による死亡率が有意に高かったとの報告がある。
15.1.2 インスリン又は経口血糖降下剤の投与中にアンジオテンシン変換酵素阻害剤を投与することにより、低血糖が起こりやすいとの報告がある。
15.2 非臨床試験に基づく情報
イヌを用いた慢性毒性試験において、最高用量の320mg/kg投与群の雌雄各1例に白内障を認めた。ウシの水晶体を用いたin vitro試験とラットを用いた検討結果では、白内障を発症させる作用や発症増強作用の可能性は認められなかった。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男子6例に本剤1mgを朝食直前に単回経口投与したときのグリメピリドの血清中濃度推移、及び薬物動態学的パラメータを示す1)。
| Tmax | Cmax(平均±SD) | 半減期 |
| 1.33時間 | 103.5±29.1ng/mL | 1.47時間 |
16.1.2 反復投与
インスリン非依存型糖尿病患者9例に本剤0.5mgもしくは1mgを1日1回7日間朝食前に連続投与したとき、初回及び最終回投与時のグリメピリドの薬物動態学的パラメータに差は認められなかった2)。
16.1.3 2型糖尿病患者(小児及び成人)における薬物動態
国内の小児2型糖尿病患者及び成人2型糖尿病患者[解析対象集団136例(小児31例及び成人105例)、血清中濃度517点]を対象に、0.5〜6mg/日の用量で、一定用量を2週間以上投与した任意の時点で母集団薬物動態解析を行った。
その結果、グリメピリドの消失プロファイルは1-コンパートメントモデルによくフィットした。共変量の検討を行った結果、最終モデルに反映される影響因子はなかった。最終モデルから得られた母集団のパラメータはCL/Fが1.56L/h、Vss/Fが6.84Lであった。母集団モデルを用いて推定したパラメータを以下に示す。小児及び成人患者の推定パラメータは同様の値であった。[9.7.1参照]
その結果、グリメピリドの消失プロファイルは1-コンパートメントモデルによくフィットした。共変量の検討を行った結果、最終モデルに反映される影響因子はなかった。最終モデルから得られた母集団のパラメータはCL/Fが1.56L/h、Vss/Fが6.84Lであった。母集団モデルを用いて推定したパラメータを以下に示す。小児及び成人患者の推定パラメータは同様の値であった。[9.7.1参照]
| 2型糖尿病患者 | CL/F(L/h) (平均±SD) | Vss/F(L) (平均±SD) | t1/2(h) (平均±SD) |
| 小児(9〜16歳) | 1.79±0.77 | 6.84±0.09 | 3.15±1.38 |
| 成人(17歳以上) | 1.64±0.59 | 6.83±0.11 | 3.30±1.60 |
16.2 吸収
外国人12例に本剤1mgをクロスオーバー法にて単回経口投与及び静脈内投与した時、それぞれのAUCの比から得られたバイオアベイラビリティーはほぼ100%であり、消化管からの吸収は良好であると考えられた3)。
16.4 代謝
16.4.1 代謝酵素
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第3相プラセボ対照二重盲検比較試験
食事療法のみにて治療中で、HbA1c(JDS値)が7.0%以上の成人NIDDM患者(±0.5%以内の変動で安定)を対象に、本剤1〜4mg/日又はプラセボを12週間経口投与した結果、改善率(HbA1c(JDS値)が1.0%以上低下した症例)は67.6%(25/37例)であった。また、HbA1c(JDS値)は本剤投与群で8.26%から6.94%に低下し、プラセボ投与群で8.24%から8.40%に上昇した。
副作用発現割合は、本剤投与群で27.0%(10/37例)、プラセボ投与群で20.0%(8/40例)であり、本剤投与群での主な副作用は、γ-GTP増加(3例)及びALT増加(2例)であった7)。
副作用発現割合は、本剤投与群で27.0%(10/37例)、プラセボ投与群で20.0%(8/40例)であり、本剤投与群での主な副作用は、γ-GTP増加(3例)及びALT増加(2例)であった7)。
17.1.2 国内第3相二重盲検比較試験
グリベンクラミド7.5mg/日以上の投与を受けているにもかかわらず、HbA1c(JDS値)が8.0%以上のNIDDM患者(±0.5%以内の変動で安定)を対象に、本剤4〜6mg/日を用量漸増法にて28週間経口投与した結果、改善率(HbA1c(JDS値)が1.0%以上低下した症例)は7.6%(12/158例)であった。また、HbA1c(JDS値)は9.66%から9.93%と0.27%上昇した。副作用発現割合は、本剤投与群で19.6%(31/158例)であり、主な副作用は、LDH増加(7例)、γ-GTP増加(6例)、AST増加(5例)、ALT増加(4例)であった8)。
17.2 製造販売後調査等
17.2.1 国内小児製造販売後臨床試験
食事療法・運動療法にて治療中の小児2型糖尿病患者(9〜16歳)35例を対象に、本剤0.5〜6mg/日を用量漸増法にて12〜28週間経口投与した非盲検非対照試験において、投与開始時から最終観察時のHbA1c(JDS値)は、試験前本剤未治療の小児患者(10例)では8.24%から7.61%へ、試験前に本剤2mg/日以下で治療していた小児患者(25例)では8.27%から7.94%へ低下の傾向が認められた。
なお、服薬不良又は維持用量の投与期間不足の症例が5例(未治療3例、既治療2例)含まれていた。投与終了時の維持用量は0.5mg/日4例、1mg/日13例、2mg/日6例、4mg/日6例、6mg/日6例であった(ITTpopulation)。副作用発現割合は、11.4%(4/35例)で、低血糖(3例)及び蛋白尿(1例)であった。[9.7.1参照]
なお、服薬不良又は維持用量の投与期間不足の症例が5例(未治療3例、既治療2例)含まれていた。投与終了時の維持用量は0.5mg/日4例、1mg/日13例、2mg/日6例、4mg/日6例、6mg/日6例であった(ITTpopulation)。副作用発現割合は、11.4%(4/35例)で、低血糖(3例)及び蛋白尿(1例)であった。[9.7.1参照]
18. 薬効薬理
18.1 作用機序
本剤は主に膵β細胞の刺激による内因性インスリン分泌の促進(膵作用)により、血糖降下作用を発現するものと考えられる。また、in vitro試験において糖輸送担体の活性化等の関与が示されている。
18.2 薬理作用
18.2.1 血糖降下作用及びインスリン分泌作用
健康成人男子9例に本剤1mgを朝食直前に単回投与した時、プラセボ投与時と比べ、朝食後の血中グルコース濃度は本剤投与時において有意に低下した。
この時の血清中インスリン濃度のCmaxは、プラセボ投与時と比べ本剤投与時では有意差は認められなかったが、朝食後4時間までのAUCはプラセボ投与時と比べ有意に増加した9)。
ウサギ、ラット、イヌを用いた経口投与試験において、本剤の血糖降下作用は投与1時間後から認められた。
グリベンクラミドとの比較では同等もしくはそれ以上の血糖降下作用を示した10)。
ラットβ細胞腫を用いたin vitro試験で、β細胞上のSU剤レセプターに対してグリメピリドはグリベンクラミドに比して1/5の結合親和性を示した11)。
この時の血清中インスリン濃度のCmaxは、プラセボ投与時と比べ本剤投与時では有意差は認められなかったが、朝食後4時間までのAUCはプラセボ投与時と比べ有意に増加した9)。
ウサギ、ラット、イヌを用いた経口投与試験において、本剤の血糖降下作用は投与1時間後から認められた。
グリベンクラミドとの比較では同等もしくはそれ以上の血糖降下作用を示した10)。
ラットβ細胞腫を用いたin vitro試験で、β細胞上のSU剤レセプターに対してグリメピリドはグリベンクラミドに比して1/5の結合親和性を示した11)。
18.2.2 インスリン作用の増強
19. 有効成分に関する理化学的知見
19.1. グリメピリド
22. 包装
<アマリール0.5mg錠>
100錠[10錠(PTP)×10]
500錠[10錠(PTP)×50]
700錠[14錠(PTP)×50]
<アマリール1mg錠>
100錠[10錠(PTP)×10]
500錠[10錠(PTP)×50]
500錠(瓶、バラ)
700錠[14錠(PTP)×50]
1000錠[10錠(PTP)×100]
<アマリール3mg錠>
100錠[10錠(PTP)×10]
500錠[10錠(PTP)×50]
700錠[14錠(PTP)×50]
23. 主要文献
- 中島光好 他, 臨床医薬, 9 (3), 503-22, (1993)
- 加来浩平 他, 臨床医薬, 9 (4), 795-807, (1993)
- Badian M,et al., Drug Metabol Drug Interact., 11, 331-9, (1994) »PubMed
- Niemi M,et al., Clin Pharmacol Ther., 72, 326-32, (2002) »PubMed
- Yamazaki H,et al., Arzneim-Forsch/Drug Res., 43, 1317-21, (1993)
- Eckert H G,et al., 基礎と臨床, 27 (5), 1493-524, (1993)
- 豊田隆謙 他, 臨床医薬, 13 (17), 4457-78, (1997)
- 兼子俊男 他, 臨床医薬, 13 (17), 4479-511, (1997)
- 中島光好 他, 臨床医薬, 9 (3), 535-48, (1993)
- Geisen K, Arzneim-Forsch/Drug Res., 38, 1120-30, (1988)
- 社内資料:ラットβ細胞腫を用いたSU剤レセプターへの結合親和性(1999年9月22日承認、申請資料概要ホ.I. 2.(1)3))
- 久保田昌詞 他, 糖尿病, 38 (6), 447-53, (1995) »DOI
- 久保田昌詞 他, 糖尿病, 35 (Suppl.1), 204, (1992)
- Muler G,et al., Diabetes Res Clin Pract., 28 (Suppl), S115-37, (1995)
- Muler G,et al., Diabetes, 42, 1852-67, (1993)
24. 文献請求先及び問い合わせ先
文献請求先
サノフィ株式会社
くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
製品情報問い合わせ先
サノフィ株式会社
くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
26. 製造販売業者等
26.1 製造販売元
サノフィ株式会社
〒163-1488
東京都新宿区西新宿三丁目20番2号