医薬品情報
| 総称名 | ラジカット |
|---|---|
| 一般名 | エダラボン |
| 欧文一般名 | Edaravone |
| 薬効分類名 | フリーラジカルスカベンジャー |
| 薬効分類番号 | 1190 |
| ATCコード | N07XX14 |
| KEGG DRUG |
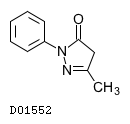
D01552
エダラボン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年4月 改訂(第5版 D16)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ラジカット点滴静注バッグ30mg | RADICUT BAG for I.V.Infusion | 田辺ファーマ | 1190401G1026 | 1731円/キット | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
○脳梗塞急性期に伴う神経症候、日常生活動作障害、機能障害の改善
○筋萎縮性側索硬化症(ALS)における機能障害の進行抑制
5. 効能または効果に関連する注意
<筋萎縮性側索硬化症(ALS)>
6. 用法及び用量
<脳梗塞急性期に伴う神経症候、日常生活動作障害、機能障害の改善>
通常、成人に1回1袋(エダラボンとして30mg)を、30分かけて1日朝夕2回の点滴静注を行う。
発症後24時間以内に投与を開始し、投与期間は14日以内とする。
<筋萎縮性側索硬化症(ALS)における機能障害の進行抑制>
通常、成人に1回2袋(エダラボンとして60mg)を、60分かけて1日1回点滴静注を行う。
通常、本剤投与期と休薬期を組み合わせた28日間を1クールとし、これを繰り返す。第1クールは14日間連日投与する投与期の後14日間休薬し、第2クール以降は14日間のうち10日間投与する投与期の後14日間休薬する。
8. 重要な基本的注意
<効能共通>
8.1 本剤の投与は、本剤に関する十分な知識及び適応疾患の治療経験を持つ医師との連携のもとで行うこと。
8.2 投与に際しては、患者又はそれに代わり得る適切な者に対して、本剤の副作用等について十分な説明を行うこと。
8.3 急性腎障害又は腎機能障害の増悪、重篤な肝障害、播種性血管内凝固症候群(DIC)があらわれ、致命的な経過をたどることがある。これらの症例では、腎機能障害、肝機能障害、血液障害等を同時に発現する重篤な症例が報告されている。
8.3.1 検査値の急激な悪化は、投与開始初期に発現することが多いので、投与前又は投与開始後速やかにBUN、クレアチニン、AST、ALT、LDH、CK、赤血球、血小板等の腎機能検査、肝機能検査及び血液検査を実施すること。本剤投与中も、腎機能検査、肝機能検査及び血液検査を頻回に実施し、投与後も継続して十分な観察を行うこと。[9.1.1-9.1.3、9.2.1、9.2.2、9.3、11.1.1-11.1.4、11.1.6、16.6.2、16.6.3参照]
8.3.2 筋萎縮性側索硬化症(ALS)患者では、病勢進展に伴う筋萎縮により血清クレアチニン値の低下を認める可能性があるため、一時点の血清クレアチニン値を基準値と比較するのではなく、血清クレアチニン値の推移を確認し、悪化傾向の有無を確認すること。また、BUN値は体内水分量等により変動するため、一時点のBUN値を基準値と比較するのではなく、BUN値の推移を確認し、悪化傾向の有無を確認すること。[2.1参照]
8.3.3 筋萎縮のある患者では、投与開始前及び投与中定期的に、血清クレアチニン値・BUN値の測定に加えて、血清シスタチンCによる推定糸球体ろ過量の算出や、蓄尿によるクレアチニンクリアランスの算出等、筋肉量による影響を受けにくい腎機能評価を実施すること。[2.1参照]
<脳梗塞急性期に伴う神経症候、日常生活動作障害、機能障害の改善>
8.4 症状に応じてより短期間で投与を終了することも考慮すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
<効能共通>
9.1.1 脱水のある患者
9.1.2 感染症のある患者
9.1.3 心疾患のある患者
<脳梗塞急性期に伴う神経症候、日常生活動作障害、機能障害の改善>
9.1.4 高度な意識障害(Japan Coma Scale 100以上:刺激しても覚醒しない)のある患者
投与に際してはリスクとベネフィットを十分考慮すること。致命的な経過をたどる例が多く報告されている。[11.1.1参照]
9.2 腎機能障害患者
9.2.1 重篤な腎機能障害のある患者
9.2.2 腎機能障害のある患者(重篤な腎機能障害のある患者を除く)
9.3 肝機能障害患者
9.5 妊婦
投与しないことが望ましい。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)において本剤の乳汁移行が認められている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
副作用があらわれた場合は投与を中止し、適切な処置を行うこと。一般に高齢者では生理機能が低下しており、致命的な経過をたどる例が多く報告されている。
10. 相互作用
10.2 併用注意
| 抗生物質 (セファゾリンナトリウム、セフォチアム塩酸塩、ピペラシリンナトリウム等) [8.3.4参照] | 腎機能障害が増悪するおそれがあるので、併用する場合には頻回に腎機能検査を実施するなど観察を十分に行うこと。 | 機序は不明であるが、本剤は主として腎臓から排泄されるため、腎排泄型の抗生物質との併用により、腎臓への負担が増強する可能性が考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 急性腎障害(0.26%)、ネフローゼ症候群(0.02%)
11.1.2 劇症肝炎(頻度不明)、肝機能障害(0.24%)、黄疸(頻度不明)
劇症肝炎等の重篤な肝炎、AST、ALT、ALP、γ-GTP、LDH、ビリルビン等の著しい上昇を伴う肝機能障害、黄疸があらわれることがある。[8.3.1参照]
11.1.3 血小板減少(0.08%)、顆粒球減少(頻度不明)[8.3.1参照]
11.1.4 播種性血管内凝固症候群(DIC)(0.08%)
播種性血管内凝固症候群を疑う血液所見や症状があらわれた場合には、投与を中止し、適切な処置を行うこと。[8.3.1参照]
11.1.5 急性肺障害(頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常を伴う急性肺障害があらわれることがあるので、患者の状態を十分に観察し、このような症状があらわれた場合には、投与を中止し、副腎皮質ホルモン剤投与等の適切な処置を行うこと。
11.1.6 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇が認められた場合には、投与を中止し、適切な処置を行うこと。[8.3.1参照]
11.1.7 ショック、アナフィラキシー(いずれも頻度不明)
ショック、アナフィラキシー(蕁麻疹、血圧低下、呼吸困難等)があらわれることがある。
注)発現頻度は、製造販売後調査の結果を含む。
11.2 その他の副作用
| 5%以上 | 0.1〜5%未満 | 頻度不明 | |
| 過敏症 | 発疹、腫脹、紅斑(多形滲出性紅斑等) | 発赤、膨疹、そう痒感 | |
| 血液 | 赤血球減少、白血球増多、白血球減少、ヘマトクリット値減少、ヘモグロビン減少、血小板増加、血小板減少 | ||
| 注射部位 | 注射部発疹、注射部発赤腫脹 | ||
| 肝臓 | ALT上昇 | 総ビリルビン値上昇、AST上昇、LDH上昇、ALP上昇、γ-GTP上昇、ビリルビン尿 | ウロビリノーゲン陽性 |
| 腎臓 | BUN上昇、血清尿酸上昇、血清尿酸低下、蛋白尿、血尿 | 多尿、クレアチニン上昇 | |
| 消化器 | 嘔気 | 嘔吐 | |
| その他 | 発熱、血清コレステロール上昇、血清コレステロール低下、トリグリセライド上昇、血清総蛋白減少、CK上昇、CK低下、血清カリウム低下、尿中ブドウ糖陽性、熱感、血圧上昇、血清カルシウム低下 | 血清カリウム上昇、頭痛 |
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 抗痙攣薬の注射液(ジアゼパム、フェニトインナトリウム等)と混合しないこと。白濁することがある。
14.1.2 カンレノ酸カリウムと混合しないこと。白濁することがある。
14.2 薬剤投与時の注意
14.2.1 高カロリー輸液、アミノ酸製剤との混合又は同一経路からの点滴はしないこと。混合すると、その後エダラボンの濃度低下を来すことがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 本剤投与中あるいは投与後に、脳塞栓の再発又は脳内出血が認められたとの報告がある。
15.1.2 本剤は添加剤として亜硫酸塩を含有している。喘息患者では非喘息患者よりも亜硫酸塩に対する過敏症が多く認められるとの報告がある。
15.2 非臨床試験に基づく情報
24時間持続静注によるイヌ28日間投与毒性試験において、60mg/kg/日以上の用量で、イヌ39週間反復経口投与毒性試験において、100mg/kg/日以上の用量で、四肢動作の限定、歩行異常等の症状及び病理組織検査における末梢神経及び脊髄(背索)の神経線維変性が観察されたとの報告がある。
16. 薬物動態
16.1 血中濃度
健康成人男子5例に本剤を体重1kg当たり0.5mg、30分かけて1日2回2日間反復点滴静脈内投与したときの血漿中未変化体濃度の推移及び初回投与時の血漿中未変化体濃度推移から求めたパラメータは次のとおりである。蓄積性は認められなかった1)。
| 薬物動態パラメータ | 健康成人男子(5例) |
| Cmax(ng/mL) | 888±171 |
| t1/2α(h) | 0.27±0.11 |
| t1/2β(h) | 2.27±0.80 |
16.3 分布
16.3.1 蛋白結合率
エダラボン(5μM及び10μM)のヒト血清蛋白及びヒト血清アルブミンに対する結合率は、92%及び89〜91%であった2)(in vitro)。
16.4 代謝
健康成人男子及び健康高齢者における本剤の主要代謝部位は肝臓と推定され、血漿中における主代謝物は硫酸抱合体であり、グルクロン酸抱合体も検出された。一方、尿中においては主代謝物はグルクロン酸抱合体であり、硫酸抱合体も認められた1)。
16.5 排泄
健康成人男子及び健康高齢者に本剤を1日2回2日間反復点滴静脈内投与(0.5mg/kg/30分×2回/日)したとき、各回投与12時間までに尿中に未変化体として0.7〜0.9%、代謝物として71.0〜79.9%が排泄された1)。
16.6 特定の背景を有する患者
16.6.1 高齢者
65歳以上の健康高齢者5例に本剤を体重1kg当たり0.5mg、30分かけて1日2回2日間反復点滴静脈内投与したときの血漿中未変化体濃度の推移及び初回投与時の血漿中未変化体濃度推移から求めたパラメータは次のとおりである。血漿中未変化体濃度は健康成人男子とほぼ同様に消失し、蓄積性は認められなかった1)。
| 薬物動態パラメータ | 健康高齢者(5例) |
| Cmax(ng/mL) | 1041±106 |
| t1/2α(h) | 0.17±0.03 |
| t1/2β(h) | 1.84±0.17 |
注)本剤の脳梗塞急性期で承認された1回用量は30mg、筋萎縮性側索硬化症(ALS)で承認された1回用量は60mgである。
16.6.2 腎機能障害者
軽度腎機能障害者(6例)、中等度腎機能障害者(8例)又は腎機能正常者(8例)にエダラボン30mgを60分かけて単回点滴静脈内投与したときの血漿中未変化体濃度の推移から求めたパラメータは次のとおりである3)。腎機能障害の程度に伴い、t1/2の平均値は延長する傾向が認められた。腎機能正常者に対するCmax、AUC0-∞の幾何平均値の比(90%信頼区間)はそれぞれ軽度腎機能障害患者で1.150(0.967-1.366)、1.202(0.991-1.457)、中等度腎機能障害者で1.247(1.063-1.463)、1.294(1.083-1.547)であった。[8.3.1、9.2.2参照]
| 薬物動態パラメータ | 軽度腎機能障害 | 中等度腎機能障害 | 腎機能正常 |
| Cmax(ng/mL) | 545.4±92.59 | 593.2±115.4 | 475.9±95.32 |
| AUC0-∞(ng・h/mL) | 771.0±153.6 | 826.4±149.4 | 644.9±153.1 |
| t1/2(h) | 5.38±6.04 | 7.31±5.83 | 2.87±0.38 |
注)ALSで承認された1回用量は60mgである。
軽度:eGFRが60〜89mL/分/1.73m2、中等度:eGFRが30〜59mL/分/1.73m2、正常:eGFR≧90mL/分/1.73m2
16.6.3 肝機能障害者
(1)重度肝機能障害者(6例)又は肝機能正常者(6例)にエダラボン30mgを60分かけて単回点滴静脈内投与したときの血漿中未変化体濃度の推移から求めたパラメータは次のとおりである4)。Cmax及びAUC0-∞の幾何平均値の比(90%信頼区間)はそれぞれ1.203(0.819-1.766)及び1.190(0.835-1.696)であった。[8.3.1、9.3参照]
| 薬物動態パラメータ | 重度肝機能障害 | 肝機能正常 |
| Cmax(ng/mL) | 347.6±146.8 | 280.3±101.0 |
| AUC0-∞(ng・h/mL) | 497.0±183.8 | 416.3±165.0 |
| t1/2(h) | 3.88±1.12 | 9.51±6.62 |
注)ALSで承認された1回用量は60mgである。
重度:Child-Pugh分類C
(2)軽度肝機能障害者(8例)、中等度肝機能障害者(6例)又は肝機能正常者(8例)にエダラボン30mgを60分かけて単回点滴静脈内投与したときの血漿中未変化体濃度の推移から求めたパラメータは次のとおりである4)。肝機能正常者に対するCmax、AUC0-∞の幾何平均値の比(90%信頼区間)はそれぞれ軽度肝機能障害患者で1.203(0.992-1.458)、1.065(0.860-1.320)、中等度肝機能障害者で1.235(1.003-1.521)、1.142(0.906-1.440)であった。[8.3.1、9.3参照]
| 薬物動態パラメータ | 軽度肝機能障害 | 中等度肝機能障害 | 肝機能正常 |
| Cmax(ng/mL) | 538.1±182.3 | 533.4±88.57 | 429.0±44.36 |
| AUC0-∞(ng・h/mL) | 727.6±262.0 | 751.5±148.3 | 654.3±107.2 |
| t1/2(h) | 3.14±0.58 | 4.37±1.90 | 4.70±6.92 |
注)ALSで承認された1回用量は60mgである。
軽度:Child-Pugh分類A、中等度:Child-Pugh分類B
17. 臨床成績
17.1 有効性及び安全性に関する試験
<脳梗塞急性期>
17.1.1 国内第III相試験
発症後72時間以内の脳梗塞急性期患者※1を対象に本剤30mg又はプラセボを1日2回14日間投与した、プラセボ対照の二重盲検群間比較試験において、本剤群は神経症候、日常生活動作障害の改善を示した。最終全般改善度における改善率の差は32.8%(95%信頼区間:20.3〜45.3%)であり、順位和検定で本剤群とプラセボ群の間に有意な差が認められた。この内、発症後24時間以内に投与を開始した患者においては、最終全般改善度における改善率の差は48.2%(95%信頼区間:26.6〜69.7%)であった。全症例及び発症後24時間で層別した最終全般改善度(改善以上)は表1のとおりである。
| 本剤群 | プラセボ群 | |
| 全症例 発症後72時間以内に投与を開始 | 64.8%(81例/125例) | 32.0%(40例/125例) |
| 発症後24時間以内に投与を開始 | 73.8%(31例/42例) | 25.6%(10例/39例) |
また、全症例における3ヵ月以内の退院日(入院中の場合は3ヵ月後)に評価した機能予後(modified Rankin Scale)に関し、本剤群とプラセボ群の間に順位和検定で有意な差が認められ、「全く症状なし」の率において本剤群がプラセボ群を上回った(本剤群:22.3%(27例/121例)、プラセボ群:10.0%(12例/120例))。この内、発症後24時間以内に投与を開始した患者において、「全く症状なし」の率は本剤群:34.1%(14例/41例)、プラセボ群:2.9%(1例/35例)であった。
副作用発現頻度は本剤群で7.2%(9/125例)及びプラセボ群で11.2%(14/125例)であった。本剤群の主な副作用は、発疹1.6%(2/125例)、肝機能障害3.2%(4/125例)であった7)。
なお、両群とも基礎治療として濃グリセリン・果糖を原則併用している。
副作用発現頻度は本剤群で7.2%(9/125例)及びプラセボ群で11.2%(14/125例)であった。本剤群の主な副作用は、発疹1.6%(2/125例)、肝機能障害3.2%(4/125例)であった7)。
なお、両群とも基礎治療として濃グリセリン・果糖を原則併用している。
17.1.2 国内臨床試験
※1 ラジカット注30mg開発時の臨床試験は主として発症後72時間以内の脳梗塞急性期患者を対象に実施された。この全症例を対象にした解析において有効性が認められたが、層別解析の結果、発症後24時間以内に投与を開始した症例において効果がより顕著であったため、承認された用法及び用量においては「発症後24時間以内に投与を開始」と設定された。
注)ラジカット注30mgの承認された用法及び用量の抜粋
発症後24時間以内に投与を開始し、投与期間は14日以内とする。
<筋萎縮性側索硬化症(ALS)>
本剤投与による生存期間への影響を確認する試験は実施されていない。
17.1.3 国内第III相試験(プラセボ対照二重盲検比較試験:検証的試験2回目)
ALS患者(El Escorial改訂Airlie House診断基準の「Definite」又は「Probable」に該当し、ALS重症度分類1度又は2度、努力性肺活量(%FVC)が80%以上及び罹病期間が2年以内)を対象に、本剤60mg又はプラセボを6クール※2点滴静注した結果、主要評価項目である改訂ALS機能評価尺度(ALSFRS-R)の変化量は表2のとおりであり、投与群間で統計学的に有意な差が認められた。
副作用発現頻度は本剤群で2.9%(2/69例)及びプラセボ群で7.4%(5/68例)であった。本剤群の副作用の内訳は、腹部不快感、湿疹及び肝機能検査異常いずれも1.4%(1/69例)であった10)。[5.1参照]
副作用発現頻度は本剤群で2.9%(2/69例)及びプラセボ群で7.4%(5/68例)であった。本剤群の副作用の内訳は、腹部不快感、湿疹及び肝機能検査異常いずれも1.4%(1/69例)であった10)。[5.1参照]
| 投与群 | 評価例数a) | ALSFRS-Rスコアb) | 変化量d)e) | プラセボ群との比較e) | ||
| 第1クール投与開始前 | 最終評価時c) | 群間差[95%信頼区間] | p値 | |||
| プラセボ群 | 66 | 41.9±2.2 | 35.0±5.6 | −7.50±0.66 | 2.49[0.99,3.98] | 0.0013 |
| 本剤群 | 68 | 41.9±2.5 | 37.5±5.3 | −5.01±0.64 | ||
17.1.4 国内第III相試験(プラセボ対照二重盲検比較試験:検証的試験1回目)
ALS患者(El Escorial改訂Airlie House診断基準の「Definite」、「Probable」又は「Probable-laboratory-supported」に該当し、ALS重症度分類1度又は2度、%FVCが70%以上及び罹病期間が3年以内)を対象に、本剤60mg又はプラセボを6クール※2点滴静注した結果、主要評価項目であるALSFRS-Rの変化量は表3のとおりであり、投与群間で統計学的に有意な差は認められなかった。
副作用発現頻度は本剤群で13.7%(14/102例)及びプラセボ群で19.2%(20/104例)であった。本剤群の主な副作用は尿中ブドウ糖陽性2.0%(2/102例)であった11)。[5.1参照]
副作用発現頻度は本剤群で13.7%(14/102例)及びプラセボ群で19.2%(20/104例)であった。本剤群の主な副作用は尿中ブドウ糖陽性2.0%(2/102例)であった11)。[5.1参照]
| 投与群 | 評価例数a) | ALSFRS-Rスコアb) | 変化量d)e) | プラセボ群との比較e) | ||
| 第1クール投与開始前 | 最終評価時c) | 群間差[95%信頼区間] | p値 | |||
| プラセボ群 | 99 | 41.1±2.9 | 35.1±7.4 | −6.35±0.84 | 0.65[−0.90,2.19] | 0.4108 |
| 本剤群 | 100 | 40.5±3.5 | 35.3±7.1 | −5.70±0.85 | ||
17.1.5 国内第III相試験(プラセボ対照二重盲検比較試験)
ALS重症度分類3度のALS患者を対象に、本剤60mg又はプラセボを6クール※2点滴静注した結果、主要評価項目であるALSFRS-Rの変化量は表4のとおりであり、投与群間で統計学的に有意な差は認められなかった。
副作用発現頻度は本剤群で23.1%(3/13例)及びプラセボ群で8.3%(1/12例)であった。本剤群の副作用の内訳は、筋力低下、冷感及び発疹いずれも7.7%(1/13例)であった12)。[5.1参照]
副作用発現頻度は本剤群で23.1%(3/13例)及びプラセボ群で8.3%(1/12例)であった。本剤群の副作用の内訳は、筋力低下、冷感及び発疹いずれも7.7%(1/13例)であった12)。[5.1参照]
| 投与群 | 評価例数a) | ALSFRS-Rスコアb) | 変化量d)e) | プラセボ群との比較e) | ||
| 第1クール投与開始前 | 最終評価時c) | 群間差[95%信頼区間] | p値 | |||
| プラセボ群 | 12 | 34.6±3.3 | 29.2±4.9 | −6.00±1.83 | −0.52[−5.62,4.58] | 0.8347 |
| 本剤群 | 13 | 32.5±5.5 | 26.6±9.9 | −6.52±1.78 | ||
※2 1日1回14日間の連日投与とそれに続く14日間の休薬期間を第1クールとし、第1クール終了後に、14日間のうち1日1回計10日間の投与とそれに続く14日間の休薬期間から成るクールを5回繰り返した(第2〜6クール)。
18. 薬効薬理
18.1 作用機序
ヒドロキシルラジカル(・OH)等のフリーラジカルが虚血に伴う脳血管障害の主要な1因子であることは数多く報告されており、虚血ないし虚血−再開通時にはアラキドン酸代謝系の異常亢進等によりフリーラジカルの産生が増加する。このフリーラジカルは細胞膜脂質の不飽和脂肪酸を過酸化することにより細胞膜傷害ひいては脳機能障害を引き起こす。
また、筋萎縮性側索硬化症(ALS)の発症並びに病勢進展は原因不明であるが、フリーラジカルによる酸化ストレスが関与している可能性が示唆されている。本剤は、フリーラジカルを消去し脂質過酸化を抑制する作用により、脳細胞(血管内皮細胞・神経細胞)の酸化的傷害を抑制する。
すなわち、脳梗塞急性期に対しては、脳浮腫、脳梗塞、神経症候、遅発性神経細胞死などの虚血性脳血管障害の発現及び進展(増悪)を抑制することにより脳保護作用を示す。筋萎縮性側索硬化症(ALS)に対しても、神経細胞の酸化的傷害を抑制することで病勢進展の抑制を示す。
また、筋萎縮性側索硬化症(ALS)の発症並びに病勢進展は原因不明であるが、フリーラジカルによる酸化ストレスが関与している可能性が示唆されている。本剤は、フリーラジカルを消去し脂質過酸化を抑制する作用により、脳細胞(血管内皮細胞・神経細胞)の酸化的傷害を抑制する。
すなわち、脳梗塞急性期に対しては、脳浮腫、脳梗塞、神経症候、遅発性神経細胞死などの虚血性脳血管障害の発現及び進展(増悪)を抑制することにより脳保護作用を示す。筋萎縮性側索硬化症(ALS)に対しても、神経細胞の酸化的傷害を抑制することで病勢進展の抑制を示す。
18.2 脳梗塞急性期に対する作用
18.2.1 脳神経保護作用
NAA(N-acetyl aspartate)は特異的生存神経細胞マーカーであり、脳梗塞発症直後より減少し24時間以降傷害組織ではほとんど観察されなくなるとされる。脳梗塞急性期患者に本剤を投与し、1H-MRS(magnetic resonance spectroscopy)により測定したところ、梗塞巣中心部のNAAは、第28病日においてコントロール群に比し有意に保持されていた8)。
18.2.2 梗塞周辺領域血流量低下に対する抑制作用
脳梗塞急性期患者8例に本剤を投与し、133Xe-SPECT(シングルフォトン断層法)により局所脳血流量を測定したところ、機能予後(modified Rankin Scale)の良好例5例では、梗塞周辺領域の局所脳血流量低下に対して抑制作用が認められた9)。
18.3 脳虚血モデルに対する脳保護作用
18.3.1 脳浮腫及び脳梗塞抑制作用、神経症候軽減作用
18.3.2 遅発性神経細胞死抑制作用
前脳虚血再開通モデル(ラット)において、再開通直後の静脈内投与(3mg/kg)は、遅発性神経細胞死を抑制した14)。
18.4 フリーラジカル消去作用
18.4.1 フリーラジカル消去作用及び脂質過酸化抑制作用
18.4.2 脳虚血モデルに対するフリーラジカル消去作用
18.4.3 フリーラジカルによる血管内皮細胞傷害に対する抑制作用
1μMから15-HPETE(hydroperoxyeicosatetraenoic acid)による培養血管内皮細胞傷害を抑制した21)(in vitro)。
18.5 筋萎縮性側索硬化症(ALS)の病態に関連した試験
家族性ALSの原因遺伝子とされる変異型スーパーオキシドジスムターゼ(SOD)を導入したトランスジェニックラットに対し、エダラボン3mg/kg/hを1時間かけて静脈内投与(2日間投与し2日間休薬を繰り返す用法)し、ラットの正向反射消失時まで投与したとき、四肢の運動機能を総合的に評価する傾斜板の角度について、雌で有意な低下抑制作用が認められた22)。
19. 有効成分に関する理化学的知見
19.1. エダラボン
20. 取扱い上の注意
20.1 製品の安定性を保持するため脱酸素剤を封入しているので、プラスチックバッグの外包装は使用直前まで開封しないこと。また、開封後は速やかに使用すること。
20.2 外包装内に挿入している酸素検知剤の色が、ピンク以外になっている場合は使用しないこと。
20.3 外箱開封後は遮光して保存すること。
21. 承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
100mL×10袋(脱酸素剤入り)
23. 主要文献
- 横田愼一,他, 臨床薬理, 28 (3), 693-702, (1997) »DOI
- 山本美奈子,他, 薬理と治療, 25 (Suppl.7), 1755-1763, (1997)
- Nakamaru Y,et al., Clin Ther., 42 (9), 1699-1714, (2020), (2020 Sep) »PubMed
- Nakamaru Y,et al., Clin Ther., 42 (8), 1467-1482.e4, (2020), (2020 Aug) »PubMed
- 大友英一,他, Ther Res., 19 (4), 1311-1332, (1998)
- MCI-186脳梗塞急性期研究会:医学のあゆみ, 185 (11), 841-863, (1998)
- Otomo E,et al., Cerebrovasc Dis., 15 (3), 222-229, (2003)
- Houkin K,et al., J Stroke Cerebrovasc Dis., 7 (5), 315-322, (1998) »PubMed
- 三森研自,他, Ther Res., 19 (4), 1333-1345, (1998)
- 田辺ファーマ(株):検証的試験2回目(社内資料)(2015年6月26日承認、CTD2.7.6.1)
- Abe K,et al., Amyotroph Lateral Scler Frontotemporal Degener., 15 (7-8), 610-617, (2014) »PubMed
- 田辺ファーマ(株):ALS重症度分類3度の患者を対象とした探索的試験(社内資料)(2015年6月26日承認、CTD2.7.6.4)
- Mizuno A,et al., Gen Pharmacol., 30 (4), 575-578, (1998) »PubMed
- Yamamoto T,et al., Brain Res., 762 (1-2), 240-242, (1997) »PubMed
- Abe K,et al., Stroke., 19 (4), 480-485, (1988) »PubMed
- 高松康雄,他, 薬理と治療, 25 (Suppl.7), 1785-1791, (1997)
- Kawai H,et al., J Pharmacol Exp Ther., 281 (2), 921-927, (1997) »PubMed
- Nishi H,et al., Stroke., 20 (9), 1236-1240, (1989) »PubMed
- 渡辺俊明,他, 薬理と治療, 25 (Suppl.7), 1691-1698, (1997)
- Yamamoto Y,et al., Redox Rep., 2 (5), 333-338, (1996) »PubMed
- Watanabe T,et al., Prostaglandins Leukot Essent Fatty Acids., 33 (1), 81-87, (1988) »PubMed
- 田辺ファーマ(株):Effects of MCI-186 in superoxide dismutase(SOD)transgenic rats(amyotrophic lateral sclerosis model)(社内資料)(2015年6月26日承認、CTD2.6.2.2.3)
24. 文献請求先及び問い合わせ先
文献請求先
製品情報問い合わせ先
26. 製造販売業者等
26.1 製造販売元
田辺ファーマ株式会社
大阪市中央区道修町3-2-10
26.2 プロモーション提携
塩野義製薬株式会社
大阪市中央区道修町3丁目1番8号