医薬品情報
| 総称名 | アズロキサ |
|---|---|
| 一般名 | エグアレンナトリウム水和物 |
| 欧文一般名 | Egualen Sodium Hydrate |
| 製剤名 | エグアレンナトリウム水和物製剤 |
| 薬効分類名 | 胃潰瘍治療剤 |
| 薬効分類番号 | 2323 |
| KEGG DRUG |
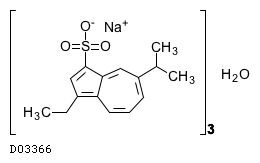
D03366
エグアレンナトリウム水和物
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年4月 改訂(第1版)

|
4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アズロキサ錠15mg | AZULOXA Tablets 15mg | 寿製薬 | 2323002F1025 | 25円/錠 | 処方箋医薬品注) |
| アズロキサ顆粒2.5% | AZULOXA Granules 2.5% | 寿製薬 | 2323002D1032 | 31円/g | 処方箋医薬品注) |
4. 効能または効果
胃潰瘍におけるH2受容体拮抗薬との併用療法
6. 用法及び用量
<アズロキサ錠15mg>
通常、成人にはH2受容体拮抗薬に併用して、1回1錠(エグアレンナトリウム水和物として15mg)を1日2回(朝食後及び就寝前)経口投与する。
<アズロキサ顆粒2.5%>
通常、成人にはH2受容体拮抗薬に併用して、1回0.6g(エグアレンナトリウム水和物として15mg)を1日2回(朝食後及び就寝前)経口投与する。
8. 重要な基本的注意
本剤と併用するH2受容体拮抗薬の用法及び用量、禁忌、重大な副作用等を必ず確認する。
9. 特定の背景を有する患者に関する注意
9.2 腎機能障害患者
9.2.1 腎機能低下のある患者
本剤は大部分が未変化体のまま尿中に排出されるので、血中濃度が持続する可能性がある。[16.5参照]
9.5 妊婦
9.5.1 妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.5.2 ラットの器官形成期に、エグアレンナトリウム水和物として600mg/kg/日を経口投与した群で、出生児の雌の回転棒パス率の亢進が報告されている。
9.5.3 ラットの周産期に、エグアレンナトリウム水和物として10mg/kg/日以上を経口投与した群で、出生児の雌の活動スコアの上昇が報告されている。
9.6 授乳婦
9.6.1 治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.6.2 ラットの授乳期に、エグアレンナトリウム水和物として10mg/kg/日以上を経口投与した群で、出生児の雌の活動スコアの上昇が報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に腎機能が低下していることが多く、本剤は主として腎臓から排泄されるため、高い血中濃度が持続するおそれがある。[16.5参照]
11. 副作用
11.2 その他の副作用
| 0.1〜5%未満 | |
| 肝臓 | 総ビリルビン値、ALT、AST、γ-GTP、Al-Pの上昇 |
| その他 | 口渇感、口唇乾燥感 |
14. 適用上の注意
14.1 薬剤交付時の注意
<錠>
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することがある。
14.2 薬剤投与時の注意
動物(ラット)実験において、餌摂取後の潰瘍部位への付着量が絶食の場合より減少するとの報告があるので、満腹時の服用はなるべく避けること。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 本剤の投与により尿が青味を帯びることがある。
15.2 非臨床試験に基づく情報
15.2.1 イヌに長期間大量に経口投与したところ、尿量と摂水量の増加、BUNとクレアチニン値の上昇、尿細管の再生と拡張が認められている。
16. 薬物動態
16.1 血中濃度
16.1.1 健康成人(生物学的同等性試験)
健康成人男子16名にアズロキサ錠15mg 1錠又はアズロキサ顆粒2.5% 0.6gを単回経口投与した場合、投与後約4.5時間に最高血漿中濃度に達した。血中消失半減期は、約8時間である1)。
16.1.2 生物学的同等性試験
アズロキサ錠15mg(1錠)とアズロキサ顆粒2.5%(0.6g)(いずれもエグアレンナトリウム水和物として15mg)を、2剤2期のクロスオーバー法により健康成人男子に絶食時単回経口投与してLC-MS/MS法にて血漿中エグアレンナトリウム濃度を測定し、得られた薬物動態パラメータ(AUCt、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された1)。
アズロキサ錠15mg、アズロキサ顆粒2.5%単回経口投与時のエグアレンナトリウムの血漿中濃度推移
| AUCt(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | t1/2(hr) | |
| アズロキサ錠15mg | 10744.1±2060.0 | 1272.0±223.8 | 4.4±1.0 | 7.8±0.6 |
| アズロキサ顆粒2.5% 0.6g | 11710.9±2603.9 | 1417.7±307.0 | 4.3±0.7 | 7.9±0.9 |
血漿中濃度並びにAUCt、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験
投与前のステージが崎田・三輪の分類によるA1、A2ステージで、深さが中程度以上、大きさが中程度(10mm)以上の胃潰瘍患者を対象にした本剤とシメチジンとの8週間の併用投与の臨床試験166例において、最終内視鏡治癒率(8週間の投薬が完了する前に治癒又は投与中止となった症例を含む治癒率)は併用群で87.1%(61/70例)、シメチジン単独群64.9%(48/74例)であった。8週内視鏡治癒率は、併用群で87.9%(58/66例)、単独群で67.6%(46/68例)であった。また、有用性評価における「有用」以上の率は併用群91.7%(66/72例)、シメチジン単独群78.4%(58/74例)であった。いずれも、併用により有意に高い値を示した4)。
内視鏡治癒率
18. 薬効薬理
18.1 作用機序
18.1.1 胃粘膜損傷形成抑制作用
18.1.2 潰瘍治癒促進作用
18.1.3 pHに依存しない胃粘膜の被覆保護作用
18.1.4 血管新生作用
18.1.5 胃酸分泌抑制剤との相乗作用
ラットの急性潰瘍モデルである幽門結紮アスピリン胃損傷並びに慢性潰瘍モデルである酢酸潰瘍において、胃酸分泌抑制剤との相乗作用を示す13)。
18.1.6 創傷治癒促進作用
ハムスターにおいて、酢酸塗布及び熱ゴテ接触により誘発した損傷の治癒を促進する14)。
18.1.7 ペプシン活性抑制作用
基質阻害型の抗ペプシン作用を示す15)(in vitro)。
18.1.8 胃粘膜血管保護作用
ラットにおいて、エタノール投与による胃粘膜血管損傷を抑制する16)。
18.1.9 内因性プロスタグランジンを介さない細胞保護作用
ラットの胃粘膜プロスタグランジンE2量に対しては影響を及ぼさず、内因性プロスタグランジンを介さない保護作用を示す16)。
18.1.10 胃粘膜増殖帯保護作用
ラットにおいて、エタノール投与による胃粘膜増殖帯の損傷を抑制し、粘膜の修復を促進する17)。
18.1.11 トロンボキサンA2(TXA2)拮抗作用
18.1.12 ヒスタミン遊離抑制作用
胃及び腹腔肥満細胞並びに感作肺切片からのヒスタミン遊離を抑制する(in vitro)。
18.1.13 膜安定化作用
細胞膜リン脂質二重層の膜を安定化する(in vitro)。
19. 有効成分に関する理化学的知見
19.1. エグアレンナトリウム水和物
20. 取扱い上の注意
<製剤共通>
20.1 多少の色調幅はあるが、成分等に影響はない。
<錠>
20.2 アルミピロー包装開封後は、湿気を避けて保存すること。
<顆粒>
20.3 外箱開封後は、湿気を避けて遮光して保存すること。
22. 包装
<アズロキサ錠15mg>
100錠[10錠(PTP)×10]
<アズロキサ顆粒2.5%>
140包[0.6g(分包)×4×7×5]
23. 主要文献
- 社内資料:アズロキサ錠15mgの生物学的同等性試験
- 海老原昭夫ほか, 臨床医薬, 6 (6), 1163-1177, (1990)
- 海老原昭夫ほか, 臨床医薬, 6 (6), 1139-1161, (1990)
- 三好秋馬ほか, 薬理と治療, 27 (5), 853-868, (1999)
- 岡部進ほか, 日薬理誌, 88, 467-476, (1986) »PubMed
- 社内資料:ラットの各種実験急性胃損傷に対するエグアレンナトリウム水和物の効果
- 若林修一ほか, 日薬理誌, 97, 105-113, (1991) »PubMed
- 社内資料:給餌制限下におけるエグアレンナトリウム水和物の酢酸潰瘍治癒促進効果
- 佐藤正雄ほか, 薬物動態, 5 (6), 845-851, (1990) »DOI
- 社内資料:ラットにおけるエグアレンナトリウム水和物の胃粘膜保護作用
- 小出典子ほか, Ulcer Research., 25 (2), 225-228, (1998)
- 若林修一ほか, Ulcer Research., 25 (2), 229-232, (1998)
- 社内資料:ラットにおけるエグアレンナトリウム水和物の胃酸分泌抑制剤との併用効果
- 社内資料:ハムスターにおけるエグアレンナトリウム水和物の創傷治癒促進作用
- 社内資料:エグアレンナトリウム水和物のペプシン活性抑制作用
- Rogers C,et al., Dig.Dis.Sci., 33 (3), 324-329, (1988) »PubMed
- 望月誠一郎ほか, Jpn.J.Pharmacol., 55 (Suppl.I), 551, (1991)
- 望月誠一郎ほか, International Congress of New Drug Development., PD8, (1991)
- 望月誠一郎ほか, Scand.J.Gastroenterol., 24 (Suppl.162), 194-197, (1989)
24. 文献請求先及び問い合わせ先
文献請求先
寿製薬株式会社
くすり相談窓口
〒389-0697
長野県埴科郡坂城町大字上五明字東川原198
電話:0120-996-156
FAX:0268-82-2215
製品情報問い合わせ先
寿製薬株式会社
くすり相談窓口
〒389-0697
長野県埴科郡坂城町大字上五明字東川原198
電話:0120-996-156
FAX:0268-82-2215
26. 製造販売業者等
26.1 製造販売元
寿製薬株式会社
長野県埴科郡坂城町大字上五明字東川原198