医薬品情報
| 総称名 | ベタメタゾン吉草酸エステル |
|---|---|
| 一般名 | ベタメタゾン吉草酸エステル |
| 欧文一般名 | Betamethasone Valerate |
| 製剤名 | ベタメタゾン吉草酸エステルクリーム |
| 薬効分類名 | 皮膚外用合成副腎皮質ホルモン剤 |
| 薬効分類番号 | 2646 |
| ATCコード | C05AA05 D07AC01 D07XC01 S02BA07 S03BA03 |
| KEGG DRUG |
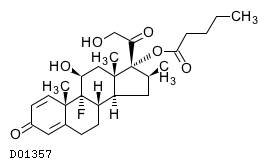
D01357
ベタメタゾン吉草酸エステル
|
| KEGG DGROUP |
DG00095
ベタメタゾン
DG01955
副腎皮質ステロイド
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年4月 改訂(第2版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ベタメタゾン吉草酸エステルクリーム0.12%「YD」 (後発品) | BETAMETHASONE VALERATE CREAM | 陽進堂ホールディングス | 2646701N2178 | 6.3円/g |
2. 禁忌
次の患者には投与しないこと
2.1 細菌・真菌・スピロヘータ・ウイルス皮膚感染症及び動物性皮膚疾患(疥癬、けじらみ等)[これらの疾患が増悪するおそれがある。]
2.2 本剤の成分に対し過敏症の既往歴のある患者
2.3 鼓膜に穿孔のある湿疹性外耳道炎[穿孔部位の治癒の遅延及び感染のおそれがある。]
2.4 潰瘍(ベーチェット病は除く)、第2度深在性以上の熱傷・凍傷[皮膚の再生が抑制され、治癒が遅延するおそれがある。]
4. 効能または効果
○湿疹・皮膚炎群(進行性指掌角皮症、女子顔面黒皮症、ビダール苔癬、放射線皮膚炎、日光皮膚炎を含む)
○皮膚そう痒症
○痒疹群(じん麻疹様苔癬、ストロフルス、固定じん麻疹を含む)
○虫さされ
○乾癬
○扁平苔癬
○光沢苔癬
○紅斑症(多形滲出性紅斑、結節性紅斑、ダリエ遠心性環状紅斑)
○紅皮症(悪性リンパ腫による紅皮症を含む)
○薬疹・中毒疹、円形脱毛症(悪性を含む)
○熱傷(瘢痕、ケロイドを含む)
○凍瘡
○天疱瘡群
○ジューリング疱疹状皮膚炎(類天疱瘡を含む)
○痔核
○鼓室形成手術・内耳開窓術・中耳根治手術の術創
5. 効能または効果に関連する注意
皮膚感染を伴う湿疹・皮膚炎には使用しないことを原則とするが、やむを得ず使用する必要がある場合には、あらかじめ適切な抗菌剤(全身適用)、抗真菌剤による治療を行うか、又はこれらとの併用を考慮すること。
6. 用法及び用量
通常1日1〜数回適量を患部に塗布する。
なお、症状により適宜増減する。
なお、症状により適宜増減する。
8. 重要な基本的注意
8.2 本剤の使用により症状の改善がみられない場合又は症状の悪化をみる場合は、使用を中止すること。
8.3 症状改善後は、できるだけ速やかに使用を中止すること。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性に対しては大量又は長期にわたる広範囲の使用を避けること。[8.1参照]
9.7 小児等
9.8 高齢者
大量又は長期にわたる広範囲の密封法(ODT)等の使用に際しては特に注意すること。一般に副作用があらわれやすい。[8.1参照]
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 眼圧亢進、緑内障、後嚢白内障(頻度不明)
11.2 その他の副作用
| 0.1〜5%未満注1) | 頻度不明 | |
| 過敏症 | 皮膚の刺激感、接触性皮膚炎、発疹 | |
| 眼 | 中心性漿液性網脈絡膜症 | |
| 皮膚の感染症注2) | 細菌感染症(伝染性膿痂疹、毛嚢炎・せつ等)、真菌症(カンジダ症、白癬等)、ウイルス感染症 | |
| その他の皮膚症状注3) | 魚鱗癬様皮膚変化、紫斑、多毛、色素脱失 | ステロイドざ瘡(尋常性ざ瘡に似るが、白色の面皰が多発する傾向)、ステロイド酒さ・口囲皮膚炎(口囲、顔面全体に紅斑、丘疹、毛細血管拡張、痂皮、鱗屑)、ステロイド皮膚(皮膚萎縮、毛細血管拡張) |
| 下垂体・副腎皮質系 | 下垂体・副腎皮質系機能の抑制注4) |
14. 適用上の注意
14.1 薬剤交付時の注意
患者に対し以下の点に注意するよう指導すること。
14.1.1 使用時
化粧下、ひげそり後等に使用することのないよう注意すること。
14.1.2 使用部位
眼科用として使用しないこと。
16. 薬物動態
16.2 吸収
正常なヒト腋窩皮膚に0.15% 3H-標識ベタメタゾン吉草酸エステルクリームを30分、1時間、2時間、4時間、8時間密封法(ODT)により塗布後、薬剤を除去し、オートラジオグラフ法により経表皮吸収及び経皮膚付属器官吸収を検討した結果、共に吸収が良好であった3)。
| 部位\密封(ODT)時間 | 30分 | 1時間 | 2時間 | 4時間 | 8時間 |
| 角質層 | − | + | + | − | + |
| マルピギー層 | − | + | + | ++ | + |
| 毛嚢壁(外側) | + | + | ++ | ++ | ++ |
| 毛嚢壁(内側) | − | + | + | ++ | ++ |
| 皮脂腺 | ? | + | + | ++ | ++ |
| アポクリン腺細胞 | + | + | + | ++ | ++ |
| アポクリン腺腔 | − | − | − | ++ | − |
16.5 排泄
乾癬患者2例及び天疱瘡患者1例に0.1% 3H-標識ベタメタゾン吉草酸エステル軟膏を密封法(ODT)により塗布した場合、7日間の尿中回収率は塗布量の2.0〜18.5%であった4)(外国人データ)。
| 疾患名 | 塗布面積 | 1日塗布量(ODT)注) | 塗布日数 | 7日間の尿中回収率(合計) |
| 乾癬 | 体表の50% | 20mg | 1日間 | 2.0% |
| 乾癬 | 体表の50% | 25mg | 2日間 | 8.7% |
| 天疱瘡 | 体表の20% | 10mg | 3日間 | 18.5% |
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験
0.064%ベタメタゾンジプロピオン酸エステル軟膏・クリーム承認時の二重盲検比較試験において0.12%ベタメタゾン吉草酸エステル軟膏・クリームを対象薬として使用した。0.12%ベタメタゾン吉草酸エステルクリームの有効性評価対象例は137例であり、有効率は82.5%(113例)であった5)。
| 疾患名 | 使用方法 | 使用期間 | 有効例数/有効性評価対象例数 | 有効率 (%) |
| 湿疹・皮膚炎群(苔癬化型) | 2〜3回/日 単純塗布 | 2週間 | 42/47 | 89.4 |
| 乾癬 | 2〜3回/日 単純塗布 | 2週間 | 28/44 | 63.6 |
| 1回/日 密封法(ODT) | 2週間 | 43/46 | 93.5 |
18. 薬効薬理
18.1 作用機序
ステロイドは細胞質に存在する熱ショック蛋白質、抑制蛋白質と複合体を形成したステロイド受容体に結合後核内に移行し、ステロイド反応性の遺伝子を活性化させ、その薬理作用を発揮すると考えられている。また、血管内皮細胞やリンパ球等の細胞膜の障害を抑制するような膜の安定性に関与する作用や、フォスフォリパーゼA2と呼ばれる細胞膜リン脂質からロイコトリエンやプロスタグランジンなど種々の炎症惹起物質を誘導する重要な酵素の機能を抑える作用も知られている。
その作用機序としては、単量体のステロイドとその受容体が複合体を形成することで、NFκBやAP-1と呼ばれるサイトカイン産生の誘導や細胞接着分子の発現等を調節している細胞内転写因子の機能を抑制することで、2量体の受容体と結合した場合、リポコルチン等の誘導を介して、炎症を制御すると考えられている。免疫抑制作用に関しては、リンパ球に対する直接的な機能抑制、アポトーシスの誘導によると考えられている6)。
その作用機序としては、単量体のステロイドとその受容体が複合体を形成することで、NFκBやAP-1と呼ばれるサイトカイン産生の誘導や細胞接着分子の発現等を調節している細胞内転写因子の機能を抑制することで、2量体の受容体と結合した場合、リポコルチン等の誘導を介して、炎症を制御すると考えられている。免疫抑制作用に関しては、リンパ球に対する直接的な機能抑制、アポトーシスの誘導によると考えられている6)。
18.2 薬理作用
18.2.1 皮膚血管収縮試験
ベタメタゾン吉草酸エステルは健康成人20例における皮膚血管収縮試験において、フルオシノロンアセトニドに比べて3.6倍の皮膚血管収縮能を示した7)(外国人データ)。
18.3 生物学的同等性試験
18.3.1 急性炎症抑制作用
ベタメタゾン吉草酸エステルクリーム0.12%「YD」、リンデロン-Vクリーム0.12%を塗布したラットを用いて、カラゲニン足浮腫試験を行い、浮腫率を比較した結果、コントロール群に比較し、両製剤とも有意な浮腫抑制作用が認められた。また、両製剤間の効果に有意差は認められず、両製剤の生物学的同等性が確認された8)。
また、ベタメタゾン吉草酸エステルクリーム0.12%「YD」、リンデロン-Vクリーム0.12%を塗布したラットを用いて、ヒスタミン誘発背部皮膚血管透過性を測定した結果、コントロール群に比較し、両製剤とも有意な透過抑制作用が認められた。また、両製剤間の効果に有意差は認められず、両製剤の生物学的同等性が確認された8)。
18.3.2 慢性炎症抑制作用
背部皮下にコットンペレットを埋め込んだラットを用い、埋め込み部分にベタメタゾン吉草酸エステルクリーム0.12%「YD」、リンデロン-Vクリーム0.12%を連続7日間塗布した。発生した肉芽腫重量を比較した結果、コントロール群に比較し、両製剤とも有意な肉芽増殖抑制作用が認められた。また、両製剤間の効果に有意差は認められず、両製剤の生物学的同等性が確認された8)。
また、右後肢足にアジュバントを注射したラットを用い、投与箇所にベタメタゾン吉草酸エステルクリーム0.12%「YD」、リンデロン-Vクリーム0.12%を1日1回7日間塗布し、浮腫改善率を比較した結果、コントロール群に比較し、両製剤とも有意な浮腫抑制作用が認められ、また、両製剤間の効果に有意差は認められず、両製剤の生物学的同等性が確認された8)。
19. 有効成分に関する理化学的知見
19.1. ベタメタゾン吉草酸エステル
20. 取扱い上の注意
遮光して保存すること。
22. 包装
10g(チューブ)×10本
10g(チューブ)×50本
500g(プラスチック容器)
23. 主要文献
- Vermeer,B.J.et al., Dermatologica., 149, 299-304, (1974) »PubMed
- Zugerman,C.et al., Arch.Dermatol., 112, 1326, (1976) »PubMed
- 久木田淳 他, 西日本皮膚科, 33, 129-137, (1971) »DOI
- Butler,J.et al., Br.J.Dermatol., 78, 665-668, (1966) »PubMed
- 安田利顕 他, 臨床評価, 2, 271-297, (1974)
- 片山一朗, アレルギー, 55, 1279-1283, (2006) »DOI
- McKenzie,A.W.et al., Arch.Dermatol., 89, 741-746, (1964) »PubMed
- 社内資料:生物学的同等性試験
24. 文献請求先及び問い合わせ先
文献請求先
陽進堂ホールディングス株式会社
お客様相談室
富山県富山市婦中町萩島3697番地の8
電話:0120-647-734
製品情報問い合わせ先
陽進堂ホールディングス株式会社
お客様相談室
富山県富山市婦中町萩島3697番地の8
電話:0120-647-734
26. 製造販売業者等
26.1 製造販売元
陽進堂ホールディングス株式会社
富山県富山市婦中町萩島3697番地の8