医薬品情報
| 総称名 | ナジフロキサシン |
|---|---|
| 一般名 | ナジフロキサシン |
| 欧文一般名 | Nadifloxacin |
| 製剤名 | ナジフロキサシンローション |
| 薬効分類名 | ニューキノロン系外用抗菌剤 |
| 薬効分類番号 | 2639 |
| ATCコード | D10AF05 |
| KEGG DRUG |
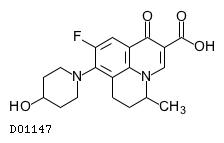
D01147
ナジフロキサシン
|
| KEGG DGROUP |
DG01549
ニューキノロン系抗生物質
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年9月 改訂(第2版)

|
4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ナジフロキサシンローション1%「トーワ」 (後発品) | NADIFLOXACIN LOTION 1%"TOWA" | 東和薬品 | 2639700Q1063 | 17円/mL | 処方箋医薬品注) |
4. 効能または効果
6. 用法及び用量
本品の適量を1日2回、洗顔後、患部に塗布する。
7. 用法及び用量に関連する注意
4週間で効果の認められない場合は使用を中止すること。また、炎症性皮疹が消失した場合には継続使用しないこと。
8. 重要な基本的注意
本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の適用にとどめること。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.7 小児等
低出生体重児、新生児、乳児又は幼児を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
11. 副作用
11.2 その他の副作用
| 1%以上 | 頻度不明 | |
| 皮膚 | 刺激感(10.6%) | そう痒感、発赤、潮紅、丘疹、顔面の熱感、接触皮膚炎、皮膚乾燥、ほてり感 |
14. 適用上の注意
14.1 薬剤投与時の注意
皮膚のみに使用し、眼科用として角膜、結膜には使用しないこと。
誤って眼に入った場合は速やかに水でよく洗い流すこと。
誤って眼に入った場合は速やかに水でよく洗い流すこと。
15. その他の注意
16. 薬物動態
16.1 血中濃度
16.1.1 単回塗布
健康成人男性6例の背部にナジフロキサシンローション1%10mLを単回塗布した時の血漿中濃度は各個体間で塗布後4時間から48時間までに最高血漿中濃度を示すなどバラツキが認められ、最高血漿中濃度は0.58〜2.12ng/mLであった。6)
16.1.2 反復塗布
健康成人男性6例の背部にナジフロキサシンローション1%5mLを1日2回、7日間反復塗布した時の血漿中濃度は3日目以降ほぼ一定となり、最終塗布後の血漿中濃度は塗布後6時間に最高値1.79ng/mLを示し、以後半減期66.1時間で減少した。6)
16.3 分布
ヒト血漿蛋白結合率は、75〜81%であった(in vitro、限外ろ過法、0.05〜5μg/mL)。7)
16.5 排泄
健康成人男性6例の背部にナジフロキサシンローション1%10mLを単回塗布した時の塗布後48時間までの尿中排泄率は0.031%であった。また、ナジフロキサシンローション1%5mLを1日2回、7日間反復塗布した時の最終塗布後の尿中排泄率は0.003%であった。6)
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内一般臨床試験
多発性炎症性皮疹を有する尋常性ざ瘡〔ざ瘡(化膿性炎症を伴うもの)〕患者172例を対象にナジフロキサシンローション1%を1日2回朝・夕、洗顔後、患部に4週間塗布した一般臨床試験における有効率(有効以上)は、84.4%(135/160例)であり、炎症性皮疹の減少及び炎症程度の改善が認められた。また、塗布前後で実施した細菌学的検査の結果、ナジフロキサシンローション1%に対する耐性化は認められなかった。副作用発現頻度は170例中18例(10.6%)であり、副作用は全例とも塗布時の刺激感であった。8)
17.3 その他
17.3.1 第I相試験(皮膚刺激性)
本邦パッチテスト研究班の基準に基づき、健康成人30例で上背部傍脊椎側の無傷皮膚表面にナジフロキサシンローション1%及び基剤を用いたクローズドパッチテスト並びに光パッチテストを実施した結果、ナジフロキサシンローション1%の皮膚刺激性の弱いこと、また、光過敏反応を示さないことが確認された。9)
18. 薬効薬理
18.1 作用機序
細菌のDNAジャイレースに作用し、DNA複製を阻害することにより殺菌的に作用する。10)
18.2 抗菌スペクトラム
ナジフロキサシンはアクネ菌及び表皮ブドウ球菌を含む、好気性グラム陽性菌、陰性菌及び嫌気性菌に対し、強い抗菌力と広い抗菌スペクトラムを有し、その作用は殺菌的である。
ナジフロキサシンはMRSA(メチシリン耐性黄色ブドウ球菌)に対し、MSSA(メチシリン感受性黄色ブドウ球菌)と同様の強い抗菌力を示し、また、キノロン耐性MRSAに対しても良好な抗菌力を示し、既存のニューキノロン剤との間に交叉耐性はほとんど認められなかった(in vitro)。11)
ナジフロキサシンはMRSA(メチシリン耐性黄色ブドウ球菌)に対し、MSSA(メチシリン感受性黄色ブドウ球菌)と同様の強い抗菌力を示し、また、キノロン耐性MRSAに対しても良好な抗菌力を示し、既存のニューキノロン剤との間に交叉耐性はほとんど認められなかった(in vitro)。11)
18.3 動物モデルにおける抗菌活性
ナジフロキサシンローション1%はアクネ菌及び表皮ブドウ球菌を用いた実験的マウス皮膚感染症モデルに対し、ローション基剤よりも優れた治療効果を示した。また、ナジフロキサシンクリーム1%との生物学的同等性が確認された。12)
18.4 耐性
継代培養による耐性獲得試験において、既存のニューキノロン系の合成抗菌剤に比べ、耐性が獲得されにくいことが認められた。また、自然耐性菌の出現頻度は、10−8以下と低率であった(in vitro)。11)
18.5 薬力学的試験
19. 有効成分に関する理化学的知見
19.1. ナジフロキサシン
20. 取扱い上の注意
20.1 他の容器に移す場合には、遮光すること。
20.2 火気を避けて保存すること。
22. 包装
20mL×10本[ボトル]
23. 主要文献
- 上出良一, 皮膚科の臨床, 34 (9 特32), 1369-1377, (1992)
- 青儀 巧 ほか, 医薬品研究, 21 (4), 626-635, (1990)
- Takahashi,N.et al., Arzneim-Forsh/Drug Res., 44 (II(11)), 1265-1268, (1994)
- 前川健郎 ほか, 変異原性試験, 2 (3), 154-161, (1993)
- Shimada,H.et al., Arzneim-Forsh/Drug Res., 42 (I(3a)), 378-385, (1992)
- 由良明彦 ほか, 薬理と治療, 26 (4), 577-587, (1998)
- 小池正己 ほか, 医薬品研究, 21 (5), 998-1021, (1990)
- 原田昭太郎 ほか, 西日本皮膚科, 60 (3), 364-371, (1998) »DOI
- 早川律子 ほか, 皮膚, 40 (2), 165-171, (1998) »DOI
- 田中千賀子 ほか, NEW薬理学 改訂第7版, 567, (2017), (南江堂)
- 河端繁勝 ほか, Chemotherapy., 37 (9), 1160-1178, (1989) »DOI
- 山田博明 ほか, 医薬品研究, 31 (8), 525-528, (2000)
- 社内資料:薬力学的試験(マウス:Staphylococcus aureus)
- 社内資料:薬力学的試験(マウス:Staphylococcus epidermidis)
- 社内資料:薬力学的試験(マウス:Propionibacterium acnes)
24. 文献請求先及び問い合わせ先
文献請求先
東和薬品株式会社
学術部DIセンター
〒570-0081
大阪府守口市日吉町2丁目5番15号
電話:0120-108-932
FAX:06-7177-7379
製品情報問い合わせ先
東和薬品株式会社
学術部DIセンター
〒570-0081
大阪府守口市日吉町2丁目5番15号
電話:0120-108-932
FAX:06-7177-7379
26. 製造販売業者等
26.1 製造販売元
東和薬品株式会社
大阪府門真市新橋町2番11号