医薬品情報
| 総称名 | ブロモクリプチン |
|---|---|
| 一般名 | ブロモクリプチンメシル酸塩 |
| 欧文一般名 | Bromocriptine Mesilate |
| 製剤名 | ブロモクリプチンメシル酸塩錠 |
| 薬効分類名 | 持続性ドパミン作動薬 |
| 薬効分類番号 | 1169 |
| ATCコード | G02CB01 N04BC01 |
| KEGG DRUG |
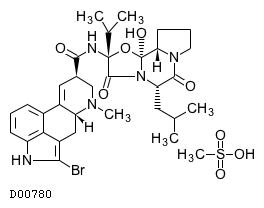
D00780
ブロモクリプチンメシル酸塩
|
| KEGG DGROUP |
DG01967
抗パーキンソン病薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年11月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ブロモクリプチン錠2.5mg「F」 (後発品) | BROMOCRIPTINE tablets | 富士製薬工業 | 1169005F1278 | 10.8円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
5. 効能または効果に関連する注意
末端肥大症(先端巨大症)、下垂体性巨人症、高プロラクチン血性下垂体腺腫の診断・治療については、国内外のガイドライン等の最新の情報を参考にすること。
6. 用法及び用量
<末端肥大症、下垂体性巨人症>
通常、ブロモクリプチンとして1日2.5mg〜7.5mgを2〜3回に分けて食直後に経口投与する。
なお、年令・症状に応じ適宜増減する。
なお、年令・症状に応じ適宜増減する。
<乳汁漏出症、産褥性乳汁分泌抑制、高プロラクチン血性排卵障害、高プロラクチン血性下垂体腺腫(外科的処置を必要としない場合に限る)>
通常、ブロモクリプチンとして1日1回2.5mgを夕食直後に経口投与し、効果をみながら1日5.0〜7.5mgまで漸増し、2〜3回に分けて食直後に経口投与する。
なお、年令・症状に応じ適宜増減する。
なお、年令・症状に応じ適宜増減する。
<パーキンソン症候群>
通常、ブロモクリプチンとして1日1回1.25mg又は2.5mgを朝食直後に経口投与から始め、1又は2週毎に1日量として2.5mgずつ増量し、維持量(標準1日15.0〜22.5mg)を定める。
1日量はブロモクリプチンとして5.0mgの場合は朝食及び夕食直後に、7.5mg以上の場合は毎食直後に分けて経口投与する。
なお、年令・症状により適宜増減する。
1日量はブロモクリプチンとして5.0mgの場合は朝食及び夕食直後に、7.5mg以上の場合は毎食直後に分けて経口投与する。
なお、年令・症状により適宜増減する。
8. 重要な基本的注意
<効能共通>
8.2 本剤投与は、少量から開始し、血圧、血液学的検査等の観察を十分に行い慎重に維持量まで増量すること。
8.3 レボドパ又はドパミン受容体作動薬の投与により、病的賭博(個人的生活の崩壊等の社会的に不利な結果を招くにもかかわらず、持続的にギャンブルを繰り返す状態)、病的性欲亢進、強迫性購買、暴食等の衝動制御障害が報告されているので、このような症状が発現した場合には、減量又は投与を中止するなど適切な処置を行うこと。また、患者及び家族等にこのような衝動制御障害の症状について説明すること。
8.4 本剤の減量、中止が必要な場合は、漸減すること。急激な減量又は中止により、悪性症候群を誘発することがある。また、ドパミン受容体作動薬の急激な減量又は中止により、薬剤離脱症候群(無感情、不安、うつ、疲労感、発汗、疼痛などの症状を特徴とする)があらわれることがある。[11.1.2参照]
<乳汁漏出症、高プロラクチン血性排卵障害>
8.5 投与開始前に、トルコ鞍の検査を行うこと。
<高プロラクチン産生下垂体腺腫>
8.6 トルコ鞍外に進展する高プロラクチン産生下垂体腺腫の患者において、本剤投与により腺腫の著明な縮小がみられた場合、それに伴い髄液鼻漏があらわれることがあるので、このような場合には、減量又は中止するなど適切な処置を行うこと。[9.1.2参照]
8.7 視野障害のみられる高プロラクチン産生下垂体腺腫の患者において、本剤投与により腺腫の縮小がみられ、一旦、視野障害が改善した後、トルコ鞍の空洞化により視交叉部が鞍内に陥入することによって、再び視野障害があらわれることがあらわれたとの報告がある。異常が認められた場合には、減量又は中止するなど適切な処置を行うこと。[9.1.2参照]
<産褥性乳汁分泌抑制>
8.8 死産や母親のHTLV-1又はHIV感染等の医学的に必要な患者にのみ投与すること。氷罨法等により乳汁分泌抑制が可能である場合には投与しないこと。
8.9 場合により氷罨法等の補助的方法を併用すること。
8.10 分娩後、呼吸、脈拍、血圧等が安定した後、投与すること。また、投与中(特に投与初日)は観察を十分に行い、血圧上昇、頭痛、中枢神経症状等があらわれた場合には、直ちに投与を中止すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 下垂体腫瘍がトルコ鞍外に進展し、視力障害等の著明な末端肥大症(先端巨大症)及び下垂体性巨人症の患者
この様な患者では手術療法が第一選択となる。
9.1.2 下垂体腫瘍がトルコ鞍外に進展し、視力障害等の著明な高プロラクチン血性下垂体腺腫の患者
9.1.3 消化性潰瘍、又はその既往歴のある患者
胃・十二指腸潰瘍の悪化がみられたとの報告がある。[11.1.7参照]
9.1.4 レイノー病の患者
レイノー症状の悪化がみられたとの報告がある。
9.1.5 精神病、又はその既往歴のある患者
精神症状の悪化がみられたとの報告がある。
9.1.6 重篤な心血管障害、又はその既往歴のある患者
外国において心臓発作、脳血管障害等があらわれたとの報告がある。[11.1.8参照]
9.2 腎機能障害患者
9.2.1 腎疾患、又はその既往歴のある患者
急激な血圧低下があらわれた場合、腎血流量が低下するおそれがある。
9.3 肝機能障害患者
9.3.1 肝障害、又はその既往歴のある患者
本剤は主として肝臓で代謝される。また、肝機能障害が報告されている。
9.4 生殖能を有する者
9.4.1 本剤を長期連用する場合には、プロラクチン分泌が抑制され、婦人科的異常が起こる可能性があるので、定期的に一般的な婦人科検査を実施すること。[15.2参照]
9.4.2 妊娠を望まない患者には避妊の方法を指導すること。
9.4.3 妊娠希望の患者に本剤投与中は、妊娠を早期に発見するため定期的に妊娠反応等の検査を実施すること。[9.5.1参照]
9.5 妊婦
9.5.2 高プロラクチン血性排卵障害で本剤の投与中に妊娠が確認された場合は、直ちに投与を中止すること。なお、下垂体腺腫のある患者では妊娠中に下垂体腺腫の拡大が起こることがあるので、本剤中止後も観察を十分に行い、腺腫の拡大を示す症状(頭痛、視野狭窄等)に注意すること。[9.5.1参照]
9.6 授乳婦
授乳を望む母親には本剤を投与しないこと。本剤は乳汁分泌を抑制する。乳汁過多症の褥婦14例に本剤2.5mg/日を分娩後5日目より3日間連続投与した結果、投与後6、7、8日目に採取した乳汁中ブロモクリプチン濃度は検出限界(0.2ng/mL)以下であった1)。
9.7 小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
10. 相互作用
相互作用序文
本剤は、肝代謝酵素CYP3A4で代謝され、またこれを阻害するので、本酵素の活性に影響を及ぼす薬剤と併用する場合には注意して投与すること。
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| 交感神経刺激剤 アドレナリン等 麦角アルカロイド エルゴメトリン メチルエルゴメトリン エルゴタミン ジヒドロエルゴタミン | 血圧上昇、頭痛、痙攣等があらわれるおそれがある。特に産褥性乳汁分泌の抑制に投与する際には分娩後、呼吸、脈拍、血圧等が安定した後、用量に注意して投与すること。 | 機序は明確ではないが、本剤はこれらの薬剤の血管収縮作用、血圧上昇作用等に影響を及ぼすと考えられる。 |
| 降圧作用を有する薬剤 | 降圧作用が強くあらわれることがある。服用開始初期には特に注意すること。 | 本剤は末梢交感神経終末のノルアドレナリン遊離を抑制する。 |
| アルコール | 胃腸系の副作用やアルコール不耐性を起こすことがある。 | 相互に作用が増強されるため。 |
| フェノチアジン系薬剤 クロルプロマジン等 ブチロフェノン系薬剤 ハロペリドール スピペロン等 イミノジベンジル系薬剤 カルピプラミン等 非定型抗精神病剤 ペロスピロン ブロナンセリン等 メトクロプラミド ドンペリドン | 相互に作用を減弱することがある。 | 本剤はドパミン作動薬であり、これらの薬剤とドパミン受容体において競合的に拮抗する。 |
| 抗パーキンソン剤 レボドパ チオキサンテン系薬剤等 | 精神神経系の副作用が増強されることがある。 | 相互に作用が増強されるため。 |
| シクロスポリン タクロリムス | これらの薬剤の血中濃度が上昇することがある。 | CYP3Aに対する競合的阻害によりこれらの薬剤の代謝が阻害される。 |
| マクロライド系抗生物質 エリスロマイシン ジョサマイシン等 HIVプロテアーゼ阻害剤 リトナビル サキナビル等 アゾール系抗真菌剤 イトラコナゾール等 | 本剤の作用が増強されるおそれがある。 | CYP3Aに対する競合的阻害により本剤の代謝が阻害される。 |
| オクトレオチド | 本剤のAUCが上昇したとの報告がある。 | 機序は不明である。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、急激な血圧低下、起立性低血圧(いずれも頻度不明)
急激な血圧低下、起立性低血圧により悪心・嘔吐、顔面蒼白、冷汗、失神等のショック症状を起した場合には、投与を中止し、昇圧等の処置を行うこと。[8.1参照]
11.1.2 悪性症候群(頻度不明)
発熱、意識障害、無動緘黙、強度の筋強剛、嚥下困難、頻脈、血圧の変動、発汗、血清CKの上昇等があらわれることがある。このような症状があらわれた場合には、投与開始初期の場合は中止し、また、継続投与中の用量変更・中止時の場合は一旦もとの投与量に戻した後慎重に漸減し、体冷却、水分補給等の全身管理とともに適切な処置を行うこと。[8.4参照]
11.1.3 胸膜炎、心膜炎、胸膜線維症、肺線維症(いずれも頻度不明)
胸水、心膜液、胸膜炎、心膜炎、胸膜線維症、肺線維症があらわれることがあるので、胸痛、呼吸器症状等があらわれた場合には、速やかに胸部X線検査を実施し、異常が認められた場合には、投与を中止し、適切な処置を行うこと。特に、高用量を長期間投与した患者では発現リスクが増大するおそれがある。
11.1.4 心臓弁膜症(頻度不明)
心雑音の発現又は増悪等があらわれた場合には、速やかに胸部X線検査、心エコー検査等を実施すること。心臓弁尖肥厚、心臓弁可動制限及びこれらに伴う狭窄等の心臓弁膜の病変が認められた場合には投与を中止し、適切な処置を行うこと。特に、高用量を長期間投与した患者では発現リスクが増大するおそれがある。[2.4参照]
11.1.5 後腹膜線維症(頻度不明)
背部痛、下肢浮腫、腎機能障害等があらわれた場合には、投与を中止し、適切な処置を行うこと。特に、高用量を長期間投与した患者では発現リスクが増大するおそれがある。
11.1.6 幻覚・妄想、せん妄、錯乱(いずれも頻度不明)
11.1.7 胃腸出血、胃・十二指腸潰瘍(いずれも頻度不明)[9.1.3参照]
11.1.9 突発的睡眠(頻度不明)
前兆のない突発的睡眠があらわれることがある。[8.1参照]
発現頻度は使用成績調査を含む
11.2 その他の副作用
| 5%以上 | 0.1%〜5%未満 | 0.1%未満 | 頻度不明 | |
| 過敏症 | − | 発疹 | − | − |
| 精神神経系 | − | 興奮、不安感、不眠、頭痛、ジスキネジア、口渇、鼻閉 | 気力低下状態、衝動制御障害(病的賭博、病的性欲亢進)、耳鳴 | 傾眠、錯感覚 |
| 眼 | − | 視覚異常 | 霧視 | − |
| 肝臓 | − | AST、ALTの上昇 | ALPの上昇 | − |
| 循環器 | − | めまい、立ちくらみ、動悸、血圧低下、起立性低血圧、胸部不快感、浮腫 | 顔面潮紅 | 夜間に脚の痙攣及び寒冷による可逆性の指趾の蒼白、頻脈、徐脈、不整脈 |
| 消化器 | 悪心 | 嘔吐、便秘、食欲不振、胃痛・腹痛、胃部不快感、胸やけ、腹部膨満感、下痢 | 口内乾燥 | − |
| 泌尿器 | − | − | 尿失禁 | − |
| その他 | − | 貧血、けん怠感 | 頭髪の脱毛、帯下の増加、しびれ感、呼吸困難、疲労 | 薬剤離脱症候群注)(無感情、不安、うつ、疲労感、発汗、疼痛など) |
13. 過量投与
13.1 症状
悪心、嘔吐、めまい、低血圧、起立性低血圧、頻脈、傾眠、嗜眠、昏睡、幻覚、発熱等。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.2 非臨床試験に基づく情報
16. 薬物動態
16.1 血中濃度
16.1.1 生物学的同等性試験(動物)
ブロモクリプチン錠2.5mg「F」とパーロデル錠2.5mgをそれぞれ3錠(ブロモクリプチンとして7.5mg)日本白色種雄性家兎に単回経口投与して血清中ブロモクリプチン濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について統計解析を行った結果、両剤の生物学的同等性が確認された3)。
| AUC0-inf(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | t1/2(hr) |
| 509.95±173.76 | 48.38±15.24 | 1.88±0.50 | 5.33±1.29 |
17. 臨床成績
17.1 有効性及び安全性に関する試験
<産褥性乳汁分泌抑制>
17.1.1 国内臨床試験
分娩又は流・早産後に乳汁分泌の抑制を希望する女性99例を対象として、ブロモクリプチンメシル酸塩錠5mg/日を14日間投与し、二重盲検法により、乳汁分泌、乳房緊満感及び血中プロラクチンの抑制効果をプラセボと比較した結果、ブロモクリプチンメシル酸塩錠の有用性が確認された。
副作用発現率は、ブロモクリプチン群で53例中12例(22.6%)25件、プラセボ群46例中6例(13.0%)10件であった。主な副作用は、ブロモクリプチン群で便秘8件(32%)、めまい、ふらつき7件(28.0%)、嘔気4件(16.0%)、嘔吐2件(8.0%)等、プラセボ群でめまい、ふらつき3件(30.0%)、嘔気2件(20.0%)、便秘2件(20.0%)、全身倦怠感2件(20.0%)等であった4)。
副作用発現率は、ブロモクリプチン群で53例中12例(22.6%)25件、プラセボ群46例中6例(13.0%)10件であった。主な副作用は、ブロモクリプチン群で便秘8件(32%)、めまい、ふらつき7件(28.0%)、嘔気4件(16.0%)、嘔吐2件(8.0%)等、プラセボ群でめまい、ふらつき3件(30.0%)、嘔気2件(20.0%)、便秘2件(20.0%)、全身倦怠感2件(20.0%)等であった4)。
<乳汁漏出症、高プロラクチン血性排卵障害及び下垂体腺腫>
17.1.2 国内一般臨床試験
Chiari-Frommel症候群、Argonz-del Castillo症候群、下垂体腺腫等の乳汁漏出・排卵障害の女性253例を対象として、ブロモクリプチンメシル酸塩錠5〜7.5mg/日を投与した一般臨床試験における結果、乳汁漏出症患者216例における乳漏停止は53.7%(116/216)、乳漏減少は34.3%(74/216)、計88%に改善が認められた。副作用発現率は、216例中143例(66.2%)であった。主な副作用は、嘔気122例(56.5%)、嘔吐49例(22.7%)、めまい・ふらつき51例(23.6%)、全身倦怠感35例(16.2%)、頭重感26例(12.0%)であった5)。
高プロラクチン血性排卵障害患者221例の無排卵症例における排卵率は76.7%(165/215)、不妊症例における妊娠率は45.3%(78/172)であった。
高プロラクチン血性下垂体腺腫患者50例において、乳汁漏出に対する有効率76.7%(33/43)、排卵率54.0%(27/50)及び妊娠率43.2%(16/37)であった。
副作用発現率は、221例中142例(64.3%)であった。主な副作用は、嘔気120例(47.4%)、嘔吐52例(20.6%)、めまい・ふらつき50例(19.8%)、全身倦怠感31例(12.3%)、便秘39例(15.4%)であった6)。
高プロラクチン血性排卵障害患者221例の無排卵症例における排卵率は76.7%(165/215)、不妊症例における妊娠率は45.3%(78/172)であった。
高プロラクチン血性下垂体腺腫患者50例において、乳汁漏出に対する有効率76.7%(33/43)、排卵率54.0%(27/50)及び妊娠率43.2%(16/37)であった。
副作用発現率は、221例中142例(64.3%)であった。主な副作用は、嘔気120例(47.4%)、嘔吐52例(20.6%)、めまい・ふらつき50例(19.8%)、全身倦怠感31例(12.3%)、便秘39例(15.4%)であった6)。
<末端肥大症(先端巨大症)、下垂体性巨人症>
17.1.3 国内一般臨床試験
末端肥大症(先端巨大症)及び下垂体性巨人症の患者152例中99例を対象として、ブロモクリプチンメシル酸塩錠1日1回2.5mgを初回量とし、維持量7.5mg/日を基準として長期投与した。ブロモクリプチンメシル酸塩錠投与により血中成長ホルモンの低下とともに発汗、糖尿病症状、頭痛・頭重感、手足のしびれ感、軟部組織の縮小並びに顔貌及び高血圧症状の改善がみられた。
副作用発現率は、152例中51例(34.0%)であった。主な副作用は、便秘14例(9.2%)、吐き気・嘔吐12例(7.9%)、悪心10例(6.6%)、上腹部不快感8例(5.3%)、血圧低下傾向6例(4.0%)、頭痛・頭重感6例(4.0%)等であった7)。
副作用発現率は、152例中51例(34.0%)であった。主な副作用は、便秘14例(9.2%)、吐き気・嘔吐12例(7.9%)、悪心10例(6.6%)、上腹部不快感8例(5.3%)、血圧低下傾向6例(4.0%)、頭痛・頭重感6例(4.0%)等であった7)。
18. 薬効薬理
18.1 作用機序
ブロモクリプチンメシル酸塩錠は持続的なドパミン受容体作動効果を有し、内分泌系に対しては下垂体前葉からのプロラクチン分泌を特異的に抑制し、末端肥大症(先端巨大症)患者において異常に上昇した成長ホルモン分泌を抑制する。また、中枢神経系に対しては黒質線条体のドパミン受容体に作用して抗パーキンソン作用を示す。
18.2 内分泌系に対する作用
18.2.1 乳汁分泌抑制作用
18.2.2 ゴナドトロピン分泌に及ぼす影響
高プロラクチン血性排卵障害婦人において、ブロモクリプチンメシル酸塩錠の投与により血中プロラクチン値の低下に伴って、エストロゲンによるLH放出の回復がみられる9)。
18.2.3 成長ホルモン分泌抑制作用
18.3 中枢神経系に対する作用
18.3.1 常同行動の誘発作用
ラットにおいて嗅ぎ込み及びなめ等の常同行動を誘発するが、この作用はレボドパに比して持続する11)。
18.3.2 回旋運動誘発作用
黒質線条体片側破壊ラット(Ungerstedtモデル)において破壊側とは反対側への回旋運動を誘発する11)。
18.3.3 レセルピンに対する拮抗作用
レセルピンにより誘発されるアキネジア、α固縮及びカタレプシーを抑制する(マウス、ラット)11)。
18.3.4 抗振戦作用
片側性脳損傷サルにみられる振戦を抑制する12)。
18.3.5 ドパミン代謝回転率に及ぼす影響
脳内DOPAC含量を減少し、ドパミン代謝回転率を減少させる(ラット)13)。
19. 有効成分に関する理化学的知見
19.1. ブロモクリプチンメシル酸塩
20. 取扱い上の注意
外箱開封後は遮光し、湿気を避けて保存すること。
22. 包装
100錠[10錠(PTP)×10]
23. 主要文献
- Peters, F., et al., Acta endocr., 109, 463-466, (1985) »PubMed
- Griffith, R. W., Brit. Med. J., 2, 1605, (1977) »PubMed
- 社内資料:生物学的同等性試験に関する資料
- 倉智敬一ほか, 産科と婦人科, 48 (3), 359-367, (1981)
- 倉智敬一ほか, 産科と婦人科, 48 (2), 241-248, (1981)
- 倉智敬一ほか, 産科と婦人科, 48 (1), 117-124, (1981)
- 鎮目和夫ほか, ホルモンと臨床, 25 (12), 1349-1353, (1977) »PubMed
- del Pozo, E., et al., J. Clin. Endocrinol., Metab. (35), 768-771, (1972)
- Aono, T., et al., Acta endocr.(Kbh)., 91, 591-600, (1979)
- Liuzzi, A., et al., J. Clin. Endocrinol., Metab. (38), 910-912, (1974)
- Johnson, A. M., et al., Br. J. Pharmacol., 56, 59-68, (1976) »PubMed
- Goldstein, M., et al., Pharmacology., 16 (Suppl.1), 143-149, (1978)
- Burki, H. R., et al., Psychopharmacology., 57, 227-237, (1978) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
製品情報問い合わせ先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
26. 製造販売業者等
26.1 製造販売元
富士製薬工業株式会社
富山県富山市水橋辻ヶ堂1515番地