医薬品情報
| 総称名 | アデノシン |
|---|---|
| 一般名 | アデノシン |
| 欧文一般名 | Adenosine |
| 製剤名 | アデノシン注 |
| 薬効分類名 | 心臓疾患診断補助剤 |
| 薬効分類番号 | 7990 |
| ATCコード | C01EB10 |
| KEGG DRUG |
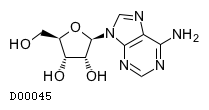
D00045
アデノシン
|
| KEGG DGROUP |
DG00243
アデノシン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年10月 改訂(第2版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アデノシン負荷用静注60mgシリンジ「FRI」 (後発品) | ADENOSINE Injection Syringe FRI | PDRファーマ | 7990402G1021 | 4806円/筒 | 処方箋医薬品注) |
1. 警告
1.1 本剤投与により下記の副作用等が発現するおそれがあるので、蘇生処置ができる準備をしておくこと。負荷試験中(本剤投与開始から心筋シンチグラフィ施行終了時まで)は血圧及び心電図の継続した監視を行い、注意深く患者を観察すること。また、検査の継続が困難と判断した場合には検査を中断し、本剤投与中であれば直ちに投与を中止すること。
1.1.1 致死的心停止、心室頻拍、心室細動、非致死性心筋梗塞を発現することがある。特に不安定狭心症患者では、その危険性が増大するおそれがあるので、薬物治療によっても安定化しない不安定狭心症の患者には投与しないこと。[2.1,9.1.1参照]
1.1.3 過度の血圧低下を起こすことがある。特に交感神経機能異常、狭窄性心臓弁疾患、心膜炎や心膜滲出、脳血流不全を伴う狭窄性頸動脈疾患、未処置の循環血液量減少等の患者では症状が増悪するおそれがある。[9.1.5参照]
1.1.4 呼吸困難が発現することがある。特に慢性閉塞性肺疾患(肺気腫、慢性気管支炎等)のある患者ではその危険性が増大するおそれがあり、負荷試験後の回復期間も含め、注意深く観察すること。[9.1.6参照]
1.2 喘息等の気管支攣縮性肺疾患のある患者、その既往のある患者あるいはその疑いのある患者に本剤が投与された場合、呼吸停止を含む重篤な呼吸障害を発症することがあるので、これらの疾患に関する病歴調査を必ず行い、疑わしい場合は本剤を投与しないこと。[2.7参照]
2. 禁忌
次の患者には投与しないこと
2.2 II度又はIII度房室ブロックのある患者(人工ペースメーカーが装着されている患者を除く)[症状が増悪するおそれがある。][1.1.2参照]
2.3 洞不全症候群又は症候性の著しい洞性徐脈のある患者(人工ペースメーカーが装着されている患者を除く)[刺激伝導抑制作用により、症状が増悪するおそれがある。]
2.4 QT延長症候群の患者[刺激伝導抑制作用により、徐脈が発現した場合、Torsade de pointesを惹起させるおそれがある。]
2.5 高度な低血圧のある患者[末梢血管拡張作用により、症状が増悪するおそれがある。]
2.6 代償不全状態にある心不全の患者[陰性変力作用により心不全の急性増悪を来すおそれがある。]
2.7 喘息等の気管支攣縮性肺疾患のある患者、その既往のある患者あるいはその疑いのある患者[呼吸停止を含む重篤な呼吸障害を発症することがある][1.2参照]
2.8 アデノシンに対し過敏症の既往歴のある患者
4. 効能または効果
十分に運動負荷をかけられない患者において心筋血流シンチグラフィによる心臓疾患の診断を行う場合の負荷誘導
5. 効能または効果に関連する注意
5.1 本剤の国内承認前の臨床試験成績は201Tlを使用した成績である。
5.2 本剤の使用は心筋シンチグラフィ施行時に限ること。
6. 用法及び用量
1分間当たりアデノシンとして120μg/kgを6分間持続静脈内投与する(アデノシン総投与量0.72mg/kg)。
7. 用法及び用量に関連する注意
7.1 シリンジポンプにより持続静脈内投与すること。また、本剤が体内に急速に注入されることを防ぐために、原則として本剤及び放射性診断薬は別々の投与経路を確保すること。
7.2 本剤の持続静脈内投与開始3分後に放射性診断薬を静脈内投与する。本剤の持続静脈内投与は放射性診断薬投与時も継続し、合計6分間行うこと。
7.3 本剤を急速に静脈内投与するとII度又はIII度房室ブロック、徐脈及び血圧低下等の発現が増強するおそれがあるので、投与時間を遵守すること。
8. 重要な基本的注意
8.1 本剤投与前に患者の病歴を確認し、薬剤負荷心筋シンチグラフィの実施可否について判断するとともに、検査実施中に何らかの異常を認めた場合には速やかに訴えるように患者に指導すること。
8.2 本剤投与開始から心筋シンチグラフィ施行終了時まで、血圧、心拍数、心電図及び自他覚所見等の観察を注意深く行うこと。また、負荷を行う検査室には除細動器を含めた救急備品を準備すること。[11.1.1-11.1.6参照]
8.3 胸痛、房室ブロック、不整脈等が出現し、検査の継続が困難と判断した場合には検査を中断し、本剤投与中であれば直ちに投与を中止すること。必要に応じてアミノフィリン水和物静脈内投与、硝酸剤舌下投与等の処置を行うこと。[11.1.3参照]
8.4 本剤の末梢血管拡張作用により過度の血圧低下を発現することがあるので、検査の継続が困難と判断した場合には検査を中断し、本剤投与中であれば直ちに投与を中止すること。承認前の国内臨床試験では収縮期血圧80mmHg未満の患者は対象から除外とした。また、国内臨床試験で120μg/kg/minを投与された症例のうち36.3%(120/331例)で20mmHg以上の収縮期血圧の低下を認めた。[11.1.2参照]
8.5 本剤投与により血圧(収縮期及び拡張期)が上昇することがあるので、本剤投与開始から投与終了まで注意深く血圧を監視すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 心筋梗塞急性期の患者
本剤の刺激伝導抑制作用及び陰性変力作用により、症状の悪化又は不整脈を発現するおそれがある。
9.1.3 I度房室ブロックや脚ブロックのある患者
伝導障害をさらに悪化させるおそれがある。[1.1.2参照]
9.1.4 心房細動や心房粗動のある患者及び副伝導路のある患者
状態が増悪するおそれがある。
9.1.5 交感神経機能異常、狭窄性心臓弁疾患、心膜炎や心膜滲出、脳血流不全を伴う狭窄性頸動脈疾患、未処置の循環血液量減少の患者
過度の血圧低下を来すおそれがある。[1.1.3参照]
9.1.6 慢性閉塞性肺疾患(肺気腫、慢性気管支炎等)の患者[1.1.4参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、本剤の負荷心筋シンチグラフィによる診断の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
本剤投与開始から心筋シンチグラフィ施行終了時まで注意深く心電図及び血圧を監視すること。海外において加齢とともに房室ブロック、血圧低下、不整脈、ST-T変化の発現率が漸増することが報告されている。
10. 相互作用
10.1 併用禁忌
| ジピリダモール ペルサンチン [2.9参照] | 完全房室ブロック、心停止等が発現することがある。ジピリダモールの投与を受けた患者に本剤を投与する場合には少なくとも12時間の間隔をおくこと。もし完全房室ブロック、心停止等の症状が現れた場合は本剤の投与を中止すること。 | ジピリダモールは体内でのアデノシンの血球、血管内皮や各臓器での取り込みを抑制し、血中アデノシン濃度を増大させることによりアデノシンの作用を増強する。 |
| メチルキサンチン類 無水カフェイン・カフェイン水和物 テオフィリン(テオドール) アミノフィリン水和物(ネオフィリン) カフェインを含む飲食物 コーヒー、紅茶、日本茶、コーラ、チョコレート等 [2.9,8.6参照] | メチルキサンチン類によりアデノシンによる冠血流速度の増加及び冠血管抵抗の減少を抑制し、虚血診断に影響を及ぼすことがある。本剤を投与する場合は12時間以上の間隔をあけること。 | メチルキサンチン類はアデノシン受容体に拮抗するため、アデノシンの作用を減弱させる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 心停止(頻度不明)、心室頻拍(頻度不明)、心室細動(頻度不明)、心筋梗塞(頻度不明)[8.2参照]
11.1.3 洞房ブロック(頻度不明)、完全房室ブロック(頻度不明)
11.1.4 呼吸障害(頻度不明)
呼吸停止に至る重篤な呼吸障害が認められることがある。重篤な呼吸障害が発現した場合は直ちに本剤の投与を中止すること。[8.2参照]
11.1.5 肺浮腫(頻度不明)
重篤な肺浮腫が発現した場合は直ちに本剤の投与を中止すること。[8.2参照]
11.1.6 脳血管障害(頻度不明)
脳血管障害の発現が疑われた場合は、直ちに本剤の投与を中止すること。[8.2参照]
11.1.7 アナフィラキシー(頻度不明)
アナフィラキシーショックに至った例も報告されている。
11.2 その他の副作用
| 5%以上 | 0.5〜5%未満 | 0.5%未満 | 頻度不明 | |
| 循環器 | 胸痛・胸部不快感・心窩部不快感(36.9%)、血圧低下、ST-T変化、房室ブロック | 胸部・心窩部圧迫感、頻脈、心室性期外収縮、上室性期外収縮、動悸、血圧上昇、QT延長 | 洞停止、心房細動、洞房ブロック、脚ブロック、冠動脈攣縮、徐脈、QRS幅拡大 | |
| 呼吸器 | 息切れ・呼吸困難 | 頻呼吸 | 鼻炎、気管支痙攣、咳 | |
| 過敏症 | 皮疹 | 紅斑 | ||
| 精神神経系 | めまい、あくび | 不安・神経過敏、異常感覚、振戦、傾眠、意識消失 | ||
| 消化器 | 口渇、腹痛、腹部不快感、嘔気・嘔吐 | 歯痛 | 嚥下困難、胃腸不快感 | |
| 血液 | 赤血球減少、血小板減少、ヘモグロビン減少、ヘマトクリット値低下 | 白血球増加、白血球減少、血小板増加 | ||
| 肝臓 | ALT上昇 | ALP上昇、総ビリルビン上昇 | ||
| 腎臓 | BUN上昇、クレアチニン上昇 | |||
| 全身 | 熱感(16.7%)、頭痛・頭重感 | 潮紅、喉・首・顎の不快感、倦怠感、異常感 | 背部痛、発汗・冷汗 | 無力症、背部不快感、上肢不快感、下肢不快感、気分不良 |
| その他 | 眼のかすみ、鼻腔・口内異常感覚、総コレステロール上昇、総コレステロール減少、CK上昇 | 弱視、眼痛、耳痛、味覚倒錯 |
13. 過量投与
13.1 症状
アデノシンの半減期は10秒未満であることから、本剤の投与を終了あるいは中止すれば速やかに回復することが考えられるが、本邦及び米国において、僅かながら遅延性あるいは持続性の症状発現も認められている。
13.2 処置
アデノシン受容体拮抗作用のあるアミノフィリン水和物を静脈内投与する。
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 薬剤負荷開始とともに本剤が確実に静脈内に注入されるように、予め本剤を投与経路(チューブ内)に充填しておくこと。
14.1.2 体重あたりの投与速度換算表は次のとおりである。
| 体重(kg) | 投与速度(mL/min) |
| 40 | 1.6 |
| 50 | 2.0 |
| 60 | 2.4 |
| 70 | 2.8 |
| 80 | 3.2 |
14.1.3 本シリンジの使用にあたっては、適合するシリンジポンプを使用すること。
14.1.4 シリンジが破損するおそれがあるため、強い衝撃を避けること。
14.1.5 外袋は使用直前まで開封しないこと。
14.1.6 薬液が漏れている場合や、薬液に着色や混濁等の異常が認められた場合には使用しないこと。
14.1.7 シリンジに破損等の異常が認められるときは使用しないこと。
14.1.8 シリンジ先端のキャップを外した後、シリンジ先端部に触れないこと。
14.1.9 外筒を強く握らないこと。[液漏れする可能性がある。]
14.1.10 シリンジポンプにセットする前に、十分注意して外筒内のエアーを抜き取った後、シリンジ先端に、注入ラインの接合部をしっかりと装着・ロックすること。[不十分な場合、接合部位のはずれ、接合部位からの液漏れや注入ライン内へのエアー混入が起こることがある。]
14.1.11 シリンジポンプの送り機構(スライダー)のフックに確実にセットすること。[正しくセットされていない場合、サイフォニング(自然落下による急速注入)や逆流が起こるおそれがある。]
14.1.12 シリンジポンプにセットした後、患者に静脈針を穿刺する前には、使用するシリンジポンプの指定する方法に従い、必ずプライミング(注入経路のエアー抜き等)を行うこと。
14.1.13 シリンジポンプと注入ライン先端(投与部位)の落差はできるだけ小さくすること。[高低差によるサイフォニング現象により、薬液の急速注入が起こることがある。また、落差と接合部の装着・ロックが不十分であることが重なると注入ライン内へのエアー混入が助長される可能性がある。]
14.1.14 投与中は注入ラインの破損、接合部の緩み及び薬液漏れ等について定期的に確認すること。
14.2 薬剤投与後の注意
14.2.1 開封後の使用は1回限りとし、使用後の残液は容器とともに速やかに廃棄すること。
14.2.2 シリンジの再滅菌・再使用はしないこと。
16. 薬物動態
16.1 血中濃度
健康成人男性23例にアデノシン60〜140μg/kg/min注)を6分間持続静脈内投与したとき、いずれの用量でもアデノシン投与群の血漿中アデノシン濃度は生理食塩液投与群と差は認められなかった。アデノシンの細胞への取り込み及び代謝が非常に速いため、静脈血中の内因性アデノシン濃度には殆ど影響を及ぼさなかったものと推察された。
アデノシンをヒト血液に加えたときの血液及び血漿からの消失半減期はそれぞれ10秒1)及び1秒前後2)と、非常に早く消失することが報告されている(in vitro)。アデノシンの代謝物のうち、血漿中ヒポキサンチン濃度は投与中僅かに上昇したが、血漿中キサンチン及び尿酸濃度には投与中も影響は認められなかった3)。
アデノシンをヒト血液に加えたときの血液及び血漿からの消失半減期はそれぞれ10秒1)及び1秒前後2)と、非常に早く消失することが報告されている(in vitro)。アデノシンの代謝物のうち、血漿中ヒポキサンチン濃度は投与中僅かに上昇したが、血漿中キサンチン及び尿酸濃度には投与中も影響は認められなかった3)。
16.4 代謝
健康成人男性23例にアデノシン60〜140μg/kg/min注)を6分間持続静脈内投与したとき、血漿中にはアデノシン及びその代謝物であるヒポキサンチン、キサンチン及び尿酸が検出されたが、イノシンについてはほとんどの例で検出限界以下であった3)。
16.5 排泄
健康成人男性23例にアデノシン60〜140μg/kg/min注)を6分間持続静脈内投与したとき、アデノシン、イノシン、ヒポキサンチン、キサンチン及び尿酸の尿中排泄量は、投与前及び生理食塩液投与群と比べて差がなく、アデノシン投与による影響は認められなかった3)。
注)本剤の承認用量はアデノシン120μg/kg/minである。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
アデノシン120μg/kg/minの6分間持続静脈内投与による負荷201Tl心筋シンチグラフィと運動負荷201Tl心筋シンチグラフィとの虚血診断一致率を検討した37例における非盲検試験の臨床成績は次表のとおりであり、虚血診断の一致率は97.3%(36/37例)であった4)。なお、臨床試験で使用した核種は201Tlを使用した成績である。
| アデノシン負荷\運動負荷 | 虚血あり | 虚血なし | 合計(例) |
| 虚血あり | 6 | 1 | 7 |
| 虚血なし | 0 | 30 | 30 |
| 合計(例) | 6 | 31 | 37 |
副作用の発現頻度は44.7%(17/38例)であり、主な副作用は血圧低下及び顔のほてり7.9%(3/38例)であった。
18. 薬効薬理
18.1 作用機序
18.2 冠動脈血流量増加作用
麻酔犬においてアデノシンは、用量依存的に冠動脈血流量を増加させた7)。
18.3 冠動脈拡張作用
麻酔犬においてアデノシンは、心外膜側、心内膜側ともに冠動脈を用量依存的に拡張させたが、その作用はより細い冠動脈ほど顕著であった8)。
18.4 冠動脈狭窄下での心筋組織血流量に対する作用
左冠動脈回旋枝を狭窄した麻酔犬において、アデノシンは、狭窄血管支配領域の心筋組織血流量をほとんど変化させなかったが、正常血管である左冠動脈前下行枝支配領域の心筋組織血流量を著明に増加させ、正常領域と狭窄血管支配領域との間で心筋組織血流量に有意な差を生じさせた9)。
19. 有効成分に関する理化学的知見
19.1. アデノシン
20. 取扱い上の注意
低温下(0℃付近)では結晶が析出することがあるので、このような場合には体温付近まで加温し、溶解した後に使用すること。
22. 包装
20mLシリンジ×5本
23. 主要文献
- Klabunde RE., Eur J Pharmacol., 93 (1-2), 21-26, (1983) »PubMed
- Moser GH,et al., Am J Physiol., 256, C799-C806, (1989)
- Uematsu T,et al., Br J Clin Pharmacol., 50 (2), 177-181, (2000) »PubMed
- 西村重敬ほか, 核医学, 41 (2), 143-154, (2004) »PubMed
- Berne R M, Circ Res., 47 (6), 807-813, (1980) »PubMed
- Belardinelli L,et al., Prog Cardiovasc Dis., 32 (1), 73-97, (1989) »PubMed
- 日高寿範ほか, Pharma Medica., 21 (11), 161-167, (2003)
- 矢田豊隆ほか, 臨床と研究, 80 (8), 1555-1566, (2003)
- 高木弘光ほか, Pharma Medica., 21 (12), 121-128, (2003)
24. 文献請求先及び問い合わせ先
文献請求先
PDRファーマ株式会社
製品情報センター
〒104-0031
東京都中央区京橋2-14-1 兼松ビルディング
電話:0120-383-624
製品情報問い合わせ先
PDRファーマ株式会社
製品情報センター
〒104-0031
東京都中央区京橋2-14-1 兼松ビルディング
電話:0120-383-624
26. 製造販売業者等
26.1 製造販売元
PDRファーマ株式会社
東京都中央区京橋2-14-1 兼松ビルディング