医薬品情報
| 総称名 | ワンクリノン |
|---|---|
| 一般名 | プロゲステロン |
| 欧文一般名 | Progesterone |
| 製剤名 | プロゲステロン |
| 薬効分類名 | 黄体ホルモン製剤 |
| 薬効分類番号 | 2477 |
| ATCコード | G03DA04 |
| KEGG DRUG |
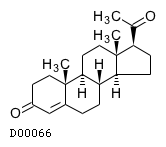
D00066
プロゲステロン
|
| KEGG DGROUP |
DG02004
プロゲステロン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年1月 改訂(第3版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ワンクリノン腟用ゲル90mg | OneCrinone vaginal gel 90mg | メルクバイオファーマ | 2477700H4020 | 1042.3円/管 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
生殖補助医療における黄体補充
6. 用法及び用量
プロゲステロンとして1回90mgを1日1回、採卵日(又はホルモン補充周期下での凍結胚移植ではエストロゲン投与により子宮内膜が十分な厚さになった時点)から最長10週間(又は妊娠12週まで)腟内に投与する。
8. 重要な基本的注意
8.1 傾眠状態や浮動性めまいを引き起こすことがあるので、自動車の運転等、危険を伴う機械の操作に従事する際には注意するよう患者に十分説明すること。
8.2 投与の中止により、不安、気分変化、発作感受性の増大を引き起こす可能性があるので、投与中止の際には注意するよう患者に十分説明すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 てんかん又はその既往歴のある患者
病態が悪化するおそれがある。
9.1.2 うつ病又はその既往歴がある患者
注意深く観察し、症状の悪化を認めた場合は投与を中止するなど注意すること。病態が悪化するおそれがある。
9.1.3 片頭痛、喘息又はその既往歴のある患者
病態が悪化するおそれがある。
9.1.4 心機能障害のある患者
体液貯留を引き起こすおそれがある。
9.1.5 糖尿病の患者
糖尿病が悪化するおそれがある。
9.2 腎機能障害患者
体液貯留を引き起こすおそれがある。
9.3 肝機能障害患者
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒト母乳中へ移行することがある。
10. 相互作用
10.2 併用注意
| 他の腟剤 | 本剤の作用が増強又は減弱する可能性がある。 | 本剤からのプロゲステロン放出及び吸収を変化させる可能性がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 血栓性障害(頻度不明)
心筋梗塞、脳血管障害、動脈又は静脈の血栓塞栓症(静脈血栓塞栓症又は肺塞栓症)、血栓性静脈炎、網膜血栓症があらわれたとの報告がある。[2.6参照]
11.1.2 アナフィラキシーショック(頻度不明)
11.2 その他の副作用
| 1〜5%未満 | 1%未満 | 頻度不明 | |
| 全身症状 | アレルギー | ||
| 精神神経系 | 頭痛、傾眠、浮動性めまい、疲労、神経過敏、攻撃的反応、もの忘れ、うつ病 | ||
| 消化器 | 腹痛 | 便秘、下痢、軟便 | 悪心、嘔吐、腹部膨満感 |
| 皮膚及び皮下組織 | ばら色粃糠 | 過敏症 | |
| 生殖系及び乳房 | 腟出血 | 外陰部炎、不正子宮出血 | 会陰痛、乳房圧痛、乳房痛、性交困難、性器モニリア症、陰部そう痒症、腟乾燥、腟分泌物、月経中間期出血(小出血)、腟刺激感、腹部疝痛 |
| 泌尿器 | 膀胱炎 | 夜間頻尿、尿路感染 | |
| 筋骨格系 | 関節痛 | ||
| 投与部位 | 疼痛、外陰腟不快感、外陰腟紅斑、外陰腟そう痒症、外陰腟腫脹 | ||
| その他 | 腟内異物 | 尿中ケトン体陽性、切迫流産、妊娠時出血 | リビドー減退 |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 本剤は腟に適用する製剤のため、内服させないこと。
14.1.2 本剤の基材の残渣が腟内に蓄積することがある。
14.1.3 本剤を投与するときは、次の手順にて腟内に直接投与すること。
(1)密封包装を破り、アプリケータを取り出す。このときはまだ、ねじ切りタブはそのままにしておく。
(2)親指と人差し指で、バルブ部分の両横にあるシーム線に沿ってアプリケータを持つ。3〜4回強く振り(温度計のように)、内容物がアプリケータの細い方に集まるようにする。
(3)アプリケータのバルブの平たい部分を持ち、細い方の端にあるねじ切りタブをねじ切り(引っぱって切らないこと)、捨てる。ねじ切り時にバルブ部分を押さないようにする(挿入前にジェルの一部が飛び出してしまう場合があるため)。
(4)座った状態、中腰の状態、又は仰向けに寝て膝を曲げた状態で腟にアプリケータを挿入する。
(5)アプリケータのバルブ部分を押してジェルを腟内に挿入する。その後アプリケータを取り出し、ゴミとして捨てる。アプリケータ内に少量のジェルが残るが、その状態で適切な一定量が挿入されているため問題はない。
15. その他の注意
15.1 臨床使用に基づく情報
本剤との関連性は不明であるが、海外では1999年以降、口唇/口蓋裂、心臓疾患、発育性股関節形成不全、尿道下裂、臍帯ヘルニア等の先天奇形が自発報告されている。また、海外臨床試験2試験において、妊娠例26例中1例に臍帯ヘルニアが、新生児47例中1例に口蓋裂がそれぞれ報告されている。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
16.3 分布
血中プロゲステロンの大部分は血漿蛋白(95〜98%)と結合し、主にアルブミン及びコルチゾール結合グロブリンと結合する2)。
16.4 代謝
プロゲステロンは主に肝臓でプレグナンジオール及びプレグナノロンに代謝され、さらにグルクロン酸及び硫酸抱合体に代謝される2)。
16.5 排泄
プロゲステロン代謝物は尿中及び糞中などに排泄される。プロゲステロンを非経口投与したときの主排泄経路は尿中(約50%)である。また、糞中排泄は約10%である3)。
注)本剤の承認された用量は、プロゲステロンとして1回90mgを1日1回である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
体外受精−胚移植を受ける日本人女性149例を対象に、採卵日から本剤90mgを1日1回腟内に12週間投与した。胚移植例における臨床的妊娠率は28.5%(35/123例)であった4)。
なお、149症例中15症例(10.1%)に副作用(臨床検査値の異常を含む)が発現した。主な副作用は、腟出血4例(2.7%)、腹痛、腟内異物各2例(1.3%)であった。
なお、149症例中15症例(10.1%)に副作用(臨床検査値の異常を含む)が発現した。主な副作用は、腟出血4例(2.7%)、腹痛、腟内異物各2例(1.3%)であった。
18. 薬効薬理
18.1 作用機序
19. 有効成分に関する理化学的知見
19.1. プロゲステロン
22. 包装
ポリエチレン製アプリケータ×7本
23. 主要文献
- 社内資料:第I相試験(平成28年7月4日承認、CTD2.7.2.2.1.1、2.7.6.2.2)
- Pfeifer SM,et al., Reproductive Endocrinology,Surgery,and Technology.LWW., 493-504, (1996)
- 熊谷 洋, 臨床薬理学大系, 12, 79-116, (1966), (東京:中山書店)
- 社内資料:第III相試験(平成28年7月4日承認、CTD2.7.6.2.7.8)
- Neumann F, Postgrad Med J., 54 (suppl 2), 11-24, (1978)
- Rothchild I, Progesterone and Progestins.Raven Press., 219-29, (1983)
- Halasz M,et al., J Reprod Immunol., 97 (1), 43-50, (2013) »PubMed
- 社内資料:非臨床薬理試験(平成28年7月4日承認、CTD2.4.2.3)
24. 文献請求先及び問い合わせ先
文献請求先
メルクバイオファーマ株式会社
メディカル・インフォメーション
東京都港区麻布台一丁目3番1号
電話:0120-870-088
製品情報問い合わせ先
メルクバイオファーマ株式会社
メディカル・インフォメーション
東京都港区麻布台一丁目3番1号
電話:0120-870-088
26. 製造販売業者等
26.1 製造販売元
メルクバイオファーマ株式会社
東京都港区麻布台一丁目3番1号