医薬品情報
| 総称名 | メコバラミン |
|---|---|
| 一般名 | メコバラミン |
| 欧文一般名 | Mecobalamin |
| 薬効分類名 | 末梢性神経障害治療剤 |
| 薬効分類番号 | 3136 |
| ATCコード | B03BA05 |
| KEGG DRUG |
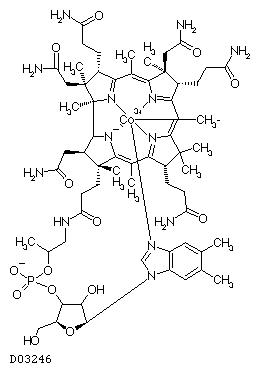
D03246
メコバラミン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年9月 改訂(第2版)

|
4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| メコバラミン錠250μg「JG」 (後発品) | 日本ジェネリック | 3136004F1093 | 6.1円/錠 | ||
| メコバラミン錠500μg「JG」 (後発品) | 日本ジェネリック | 3136004F2243 | 6.1円/錠 |
4. 効能または効果
末梢性神経障害
6. 用法及び用量
<メコバラミン錠250μg「JG」>
通常、成人は1日6錠(メコバラミンとして1日1,500μg)を3回に分けて経口投与する。
ただし、年令及び症状により適宜増減する。
ただし、年令及び症状により適宜増減する。
<メコバラミン錠500μg「JG」>
通常、成人は1日3錠(メコバラミンとして1日1,500μg)を3回に分けて経口投与する。
ただし、年令及び症状により適宜増減する。
ただし、年令及び症状により適宜増減する。
8. 重要な基本的注意
本剤投与で効果が認められない場合、月余にわたって漫然と使用すべきでない。
9. 特定の背景を有する患者に関する注意
9.7 小児等
小児等を対象とした臨床試験は実施していない。
11. 副作用
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | |
| 消化器 | 食欲不振、悪心・嘔吐、下痢 | |
| 過敏症 | 発疹 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.2 非臨床試験に基づく情報
水銀及びその化合物を取り扱う職業従事者に長期にわたって大量に投与することは避けることが望ましい。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男子にメコバラミン120μg、1,500μg注)を絶食下単回経口投与した場合、いずれの投与量においても投与後約3時間で最高血中濃度に達し、濃度依存による吸収が観察された。半減期、血清中総ビタミンB12(以下B12)濃度の投与12時間までの増加分及びΔAUC120を下表に示し、血清中総B12濃度の推移を下図に示した。
尿中総B12排泄量は投与後8時間までに投与後24時間排泄量の40〜90%が排泄された1)。
尿中総B12排泄量は投与後8時間までに投与後24時間排泄量の40〜90%が排泄された1)。
注)本剤の承認された用法及び用量は「通常、成人はメコバラミンとして1日1,500μgを3回に分けて経口投与する。」である。
血清中総B12濃度の増加分
| 投与量 | tmax(hour) | Cmax(pg/mL) | ΔCmax(pg/mL) | ΔCmax%(%) | ΔAUC120※1(pg・hr/mL) | t1/2※2(hour) |
| 120μg | 2.8±0.2 | 743±47 | 37±15 | 5.1±2.1 | 168±58 | 算出不能 |
| 1,500μg | 3.6±0.5 | 972±55 | 255±51 | 36.0±7.9 | 2033±510 | 12.5 |
16.1.2 反復投与
健康成人男子に1,500μgを12週間反復経口投与し、投与中止後4週間の血清中総B12量の変動率を検討した。投与4週間で投与前値の約2倍に達し、以後も漸増し、12週後には約2.8倍を示した。投与中止4週後でも投与前値の約1.8倍を示した2)。
16.8 その他
<メコバラミン錠250μg「JG」>
メコバラミン錠250μg「JG」は、「経口固形製剤の処方変更の生物学的同等性試験ガイドライン(平成24年2月29日 薬食審査発0229第10号 別紙3)」に基づき、処方変更前製剤[ヒトを対象とした生物学的同等性試験により同等性が確認されている。]を標準製剤とした溶出試験の結果、溶出挙動は同等と判定され、生物学的に同等とみなされた3)。
<メコバラミン錠500μg「JG」>
メコバラミン錠500μg「JG」は、「経口固形製剤の処方変更の生物学的同等性試験ガイドライン(平成24年2月29日 薬食審査発0229第10号 別紙3)」に基づき、処方変更前製剤[ヒトを対象とした生物学的同等性試験により同等性が確認されている。]を標準製剤とした溶出試験の結果、溶出挙動は同等と判定され、生物学的に同等とみなされた4)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験(用量比較試験)
末梢性神経障害に対して、メコバラミンとして1日1,500μg及び1日120μg(低用量群)を3回に分けて4週間反復経口投与し、二重盲検比較試験を行った。慢性期及び固定期の症例に対して、メコバラミンの改善率は改善以上で1,500μgが17.6%(6/34)、120μgが9.7%(3/31)、やや改善以上で1,500μgが64.7%(22/34)、120μgが41.9%(13/31)であり、1,500μg/日投与の有用性が認められた5)。
17.1.2 国内臨床試験(コバマミド及びプラセボ対照比較試験)
末梢神経障害に対してメコバラミン1日1,500μg、コバマミド1日1,500μg及びプラセボを4週間反復経口投与し、二重盲検比較試験を行った。全般改善度は中等度改善以上で、メコバラミン投与群38.6%(17/44)、コバマミド投与群22.2%(10/45)、プラセボ投与群26.7%(12/45)であり、メコバラミンの有用性が認められた6)。
17.1.3 末梢神経障害に対する臨床効果
末梢神経障害による症状(しびれ、疼痛、知覚鈍麻等)を訴えた患者を対象に、本剤をメコバラミンとして1日1,500μg3分割投与し、臨床成績を評価したところ、有効率は65.8%(54/82)であった7)。
18. 薬効薬理
18.1 作用機序
18.2 神経細胞内小器官へよく移行し、核酸・蛋白合成を促進
18.3 軸索内輸送、軸索再生の促進
18.4 髄鞘形成(リン脂質合成)の促進
18.5 シナプス伝達の遅延、神経伝達物質の減少を回復
19. 有効成分に関する理化学的知見
19.1. メコバラミン
20. 取扱い上の注意
PTP包装はアルミピロー包装開封後、バラ包装はボトル開栓後、湿気を避けて遮光して保存すること。
22. 包装
<メコバラミン錠250μg「JG」>
100錠[10錠(PTP)×10、乾燥剤入り]
<メコバラミン錠500μg「JG」>
100錠[10錠(PTP)×10、乾燥剤入り]
1000錠[10錠(PTP)×100、乾燥剤入り]
500錠[プラスチック容器、バラ、乾燥剤入り]
23. 主要文献
- 田中信夫 他, 新薬と臨牀, 35 (1), 67-74, (1986)
- 田中信夫 他, ビタミン, 55 (3), 155-161, (1981) »DOI
- 社内資料:生物学的同等性試験(錠250μg)
- 社内資料:生物学的同等性試験(錠500μg)
- 亀山正邦 他, 臨床評価, 1 (1), 71-76, (1972)
- 亀山正邦 他, 臨牀と研究, 49 (7), 1963-1966, (1972)
- 社内資料:臨床試験
- 第十八改正日本薬局方解説書, C5618-C5623, (2021), (廣川書店)
- グッドマン・ギルマン薬理書(第13版), 1248-1253, (2022), (廣川書店)
- 稲田雅美 他, 神経系とメチルB12(協和企画通信), 23-29, (1981)
- 中沢恒幸 他, ビタミン, 42 (3), 193-197, (1970) »DOI
- 中沢恒幸 他, ビタミン, 42 (5), 275-279, (1970) »DOI
- 竹中敏文 他, Prog.Med., 2 (10), 1759-1762, (1982)
- 大西晃生 他, 臨床薬理, 18 (2), 387-392, (1987) »DOI
- Watanabe,T.et al., J.Neurol.Sci., 122 (2), 140-143, (1994) »PubMed
- 斉藤豊和 他, 神経系とメチルB12(協和企画通信), 75-86, (1981)
- Yamazaki,K.et al., Neurosci.Lett., 170 (1), 195-197, (1994) »PubMed
- 八木橋操六 他, 臨床薬理, 19 (2), 437-443, (1988) »DOI
- 中沢恒幸 他, 神経系とメチルB12(協和企画通信), 54-60, (1981)
- 米沢猛 他, 神経系とメチルB12(協和企画通信), 49-53, (1981)
- 渋谷統寿, 神経系とメチルB12(協和企画通信), 134-140, (1981)
- Sasaki,H.et al., Pharmacol.Biochem.Behav., 43 (2), 635-639, (1992) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
共創未来ファーマ株式会社
お客様相談室
〒155-8655
東京都世田谷区代沢4-43-11
電話:050-3383-3846
製品情報問い合わせ先
共創未来ファーマ株式会社
お客様相談室
〒155-8655
東京都世田谷区代沢4-43-11
電話:050-3383-3846
26. 製造販売業者等
26.1 製造販売元
日本ジェネリック株式会社
東京都港区芝五丁目33番11号
26.2 販売元
共創未来ファーマ株式会社
東京都品川区広町1-4-4