医薬品情報
| 総称名 | エレトリプタン |
|---|---|
| 一般名 | エレトリプタン臭化水素酸塩 |
| 欧文一般名 | Eletriptan Hydrobromide |
| 製剤名 | エレトリプタン臭化水素酸塩錠 |
| 薬効分類名 | 5-HT1B/1D受容体作動型片頭痛治療剤 |
| 薬効分類番号 | 2160 |
| ATCコード | N02CC06 |
| KEGG DRUG |
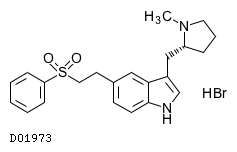
D01973
エレトリプタン臭化水素酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年3月 改訂(第2版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| エレトリプタン錠20mg「日新」 (後発品) | Eletriptan Tablets 20mg"NISSIN" | 日新製薬-山形 | 2160005F1099 | 146.9円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 心筋梗塞の既往歴のある患者、虚血性心疾患又はその症状・兆候のある患者、異型狭心症(冠動脈攣縮)のある患者[不整脈、狭心症、心筋梗塞を含む重篤な虚血性心疾患様症状があらわれることがある。]
2.3 脳血管障害や一過性脳虚血発作の既往のある患者[脳血管障害や一過性脳虚血性発作があらわれることがある。]
2.4 末梢血管障害を有する患者[症状を悪化させる可能性が考えられる。]
2.5 コントロールされていない高血圧症の患者[一過性の血圧上昇を引き起こすことがある。]
2.7 エルゴタミン、エルゴタミン誘導体含有製剤、他の5-HT1B/1D受容体作動薬、HIVプロテアーゼ阻害薬(リトナビル)、あるいはニルマトレルビル・リトナビルを投与中の患者[10.1参照]
4. 効能または効果
片頭痛
5. 効能または効果に関連する注意
5.1 本剤は国際頭痛学会による片頭痛診断基準1)により「前兆のない片頭痛」あるいは「前兆のある片頭痛」と確定診断が行われた場合にのみ投与すること。特に次のような患者は、くも膜下出血等の脳血管障害や他の原因による頭痛の可能性があるので、本剤投与前に問診、診察、検査を十分に行い、頭痛の原因を確認してから投与すること。
・今までに片頭痛と診断が確定したことのない患者
・片頭痛と診断されたことはあるが、片頭痛に通常見られる症状や経過とは異なった頭痛及び随伴症状のある患者
5.2 家族性片麻痺性片頭痛、孤発性片麻痺性片頭痛、脳底型片頭痛あるいは眼筋麻痺性片頭痛の患者には投与しないこと。
6. 用法及び用量
通常、成人にはエレトリプタンとして1回20mgを片頭痛の頭痛発現時に経口投与する。
なお、効果が不十分な場合には、追加投与をすることができるが、前回の投与から2時間以上あけること。
また、20mgの経口投与で効果が不十分であった場合には、次回片頭痛発現時から40mgを経口投与することができる。
ただし、1日の総投与量を40mg以内とする。
なお、効果が不十分な場合には、追加投与をすることができるが、前回の投与から2時間以上あけること。
また、20mgの経口投与で効果が不十分であった場合には、次回片頭痛発現時から40mgを経口投与することができる。
ただし、1日の総投与量を40mg以内とする。
7. 用法及び用量に関連する注意
7.1 本剤は頭痛発現時にのみ使用し、予防的には使用しないこと。
7.2 本剤投与により全く効果が認められない場合は、その発作に対して追加投与をしないこと。このような場合は、再検査の上、頭痛の原因を確認すること。
8. 重要な基本的注意
8.1 心血管系の疾患が認められない患者においても、重篤な心疾患が極めてまれに発生することがある。このような場合は以後の投与を中止し、適切な処置を行うこと。
8.2 片頭痛あるいは本剤投与により眠気を催すことがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械操作に従事させないよう十分注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 虚血性心疾患の可能性のある患者
例えば、以下のような患者では不整脈、狭心症、心筋梗塞を含む重篤な虚血性心疾患様症状があらわれるおそれがある。[11.1.2参照]
・虚血性心疾患を疑わせる重篤な不整脈のある患者
・閉経後の女性
・40歳以上の男性
・冠動脈疾患の危険因子を有する患者
9.1.2 ウォルフ・パーキンソン・ホワイト症候群(WPW症候群)又は他の心臓副伝導路と関連した不整脈のある患者
WPW症候群の典型的症状である重篤な発作性頻脈が発現したとの報告がある。[11.1.4参照]
9.1.3 脳血管障害の可能性のある患者
脳血管障害があらわれるおそれがある。
9.1.4 てんかんあるいは痙攣を起こしやすい器質的脳疾患のある患者
てんかん様発作がおこるおそれがある。[11.1.3参照]
9.1.5 コントロールされている高血圧症患者
一過性の血圧上昇や末梢血管抵抗の上昇を引き起こすことがある。
9.3 肝機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
授乳しないことが望ましい。本剤は投与後24時間までにヒト母乳中に約0.02%の移行が認められている2)(外国人データ)。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
血圧の上昇は、若年者よりも高齢者で大きいので慎重に投与すること。高齢者と若年者における収縮期血圧の最大上昇の差は10.19mmHg、拡張期血圧の最大上昇の差は2.59mmHgであった3)(外国人データ)。
10. 相互作用
相互作用序文
本剤は、主として肝代謝酵素チトクロームP450 3A4により代謝される。[16.4.1参照]
薬物代謝酵素用語
CYP3A4
10.1 併用禁忌
| エルゴタミン エルゴタミン酒石酸塩・無水カフェイン・イソプロピルアンチピリン(クリアミン) エルゴタミン誘導体含有製剤 ジヒドロエルゴタミンメシル酸塩(ジヒデルゴット) エルゴメトリンマレイン酸塩(エルゴメトリンF) メチルエルゴメトリンマレイン酸塩(メテルギン) [2.7参照] | 血圧上昇又は血管攣縮が増強されるおそれがある。 本剤投与後にエルゴタミンあるいはエルゴタミン誘導体含有製剤を投与する場合、もしくはその逆の場合は、それぞれ24時間以上の間隔をあけて投与すること。 | 5-HT1B/1D受容体作動薬との薬理的相加作用により、相互に作用(血管収縮作用)を増強させる。 |
| 5-HT1B/1D受容体作動薬 スマトリプタンコハク酸塩(イミグラン) ゾルミトリプタン(ゾーミッグ) リザトリプタン安息香酸塩(マクサルト) ナラトリプタン塩酸塩(アマージ) [2.7参照] | 血圧上昇又は血管攣縮が増強されるおそれがある。 本剤投与後に他の5-HT1B/1D受容体作動型の片頭痛薬を投与する場合、もしくはその逆の場合は、それぞれ24時間以内に投与しないこと。 | 併用により相互に作用を増強させる。 |
| HIVプロテアーゼ阻害剤 リトナビル(ノービア) [2.7参照] | 本剤の代謝が阻害され血中濃度が上昇するおそれがある。 | 本剤は、主として肝代謝酵素チトクロームP450 3A4により代謝され、代謝酵素阻害薬によりクリアランスが減少する。 |
| ニルマトレルビル・リトナビル(パキロビッド) [2.7参照] | 本剤の代謝が阻害され血中濃度が上昇するおそれがある。 | 本剤は、主として肝代謝酵素チトクロームP450 3A4により代謝され、代謝酵素阻害薬によりクリアランスが減少する。 |
10.2 併用注意
| マクロライド系抗生物質 エリスロマイシン、 ジョサマイシン、クラリスロマイシン [16.7.1参照] | エリスロマイシンとの併用により、本剤の最高血漿中濃度(Cmax)は2倍、血漿中濃度−時間曲線下面積(AUC)は4倍に増大し、軽度に血圧が上昇した。 | 本剤は、主として肝代謝酵素チトクロームP450 3A4により代謝され、代謝酵素阻害薬によりクリアランスが減少する。 |
| 抗真菌剤 イトラコナゾール | イトラコナゾールとの併用により、本剤のCmax、AUCが増大し、血圧が上昇するおそれがある。 | 本剤は、主として肝代謝酵素チトクロームP450 3A4により代謝され、代謝酵素阻害薬によりクリアランスが減少する。 |
| カルシウム拮抗剤 ベラパミル [16.7.2参照] | ベラパミルとの併用により、本剤のCmax、AUCが増大した。 | 本剤は、主として肝代謝酵素チトクロームP450 3A4により代謝され、代謝酵素阻害薬によりクリアランスが減少する。 |
| 飲食物 グレープフルーツジュース | 本剤の作用が増強するおそれがある。 | 本剤は、主として肝代謝酵素チトクロームP450 3A4により代謝され、代謝酵素阻害薬によりクリアランスが減少する。 |
| エンシトレルビル フマル酸 | 本剤の血中濃度が上昇し、作用が増強するおそれがある。 | エンシトレルビル フマル酸のチトクロームP450 3Aに対する阻害作用により、本剤の代謝が阻害されることが考えられる。 |
| 副腎皮質ホルモン剤 デキサメタゾン 抗てんかん剤 カルバマゼピン 抗結核薬 リファンピシン | 本剤の代謝が促進され血中濃度が低下するおそれがある。 | 酵素誘導剤により本剤の代謝が促進されるおそれがある。 |
| 飲食物 セイヨウオトギリソウ(St.John's Wort、セント・ジョーンズ・ワート)含有食品 | 本剤の代謝が促進され血中濃度が低下するおそれがある。 | セイヨウオトギリソウにより本剤の代謝が促進されるおそれがある。 |
| 選択的セロトニン再取り込み阻害薬 フルボキサミンマレイン酸塩 パロキセチン塩酸塩水和物 セルトラリン塩酸塩 セロトニン・ノルアドレナリン再取り込み阻害薬 ミルナシプラン塩酸塩 デュロキセチン塩酸塩 | セロトニン症候群(不安、焦燥、興奮、頻脈、発熱、反射亢進、協調運動障害、下痢等)があらわれることがある。 | セロトニンの再取り込みを阻害し、セロトニン濃度を上昇させる。よって本剤との併用により、セロトニン作用が増強する可能性が考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 アナフィラキシーショック(頻度不明)、アナフィラキシー(頻度不明)
11.1.2 虚血性心疾患様症状(頻度不明)
11.1.3 てんかん様発作(頻度不明)[9.1.4参照]
11.1.4 頻脈(WPW症候群における)(頻度不明)
WPW症候群の典型的症状である重篤な発作性頻脈の報告がある。[9.1.2参照]
11.1.5 薬剤の使用過多による頭痛(頻度不明)[8.3参照]
11.2 その他の副作用
| 1%以上a) | 1%未満a) | 頻度不明 | |
| 神経系 | 浮動性めまい、傾眠・眠気、異常感覚、頭痛 | 感覚減退、回転性めまい、筋緊張亢進 | |
| 心・血管系 | 熱感 | 潮紅 | 動悸、頻脈、血圧上昇 |
| 消化器系 | 嘔気、口内乾燥 | 消化不良、腹痛 | 嘔吐 |
| 皮膚 | 発疹、そう痒症、蕁麻疹、血管浮腫 | ||
| その他 | 疲労、咽喉絞扼感b) | 多汗、胸部絞扼感b)、無力症、悪寒、咽喉頭疼痛、疼痛、背部痛 | 胸痛b)、倦怠感、筋痛、胸部圧迫感b)、筋無力症 |
13. 過量投与
13.1 処置
本剤の消失半減期は約4時間であり、少なくとも20時間、あるいは症状・徴候が持続する限り患者をモニターすること。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
16.1.1 生物学的同等性試験
エレトリプタン錠20mg「日新」とレルパックス錠20mgを、クロスオーバー法によりそれぞれ1錠(エレトリプタンとして20mg)健康成人男子に絶食時単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両製剤の生物学的同等性が確認された4)。
| 判定パラメータ | 参考パラメータ | |||
| AUC0-24(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | |
| エレトリプタン錠20mg「日新」 | 203.66±124.79 | 38.71±18.66 | 1.1±0.5 | 4.5±0.6 |
| レルパックス錠20mg | 208.88±112.50 | 41.24±19.56 | 0.9±0.4 | 4.4±0.7 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.4 代謝
16.6 特定の背景を有する患者
16.6.1 肝機能障害患者
16.7 薬物相互作用
16.7.1 健康成人18例にエリスロマイシン500mg又はプラセボを反復経口投与し、投与7日目にエレトリプタン80mg注)を単回経口投与した時、エリスロマイシン併用群ではプラセボ併用群と比較してエレトリプタンのCmaxは約2倍、AUCが約4倍に増大し、T1/2は4.6時間から7.1時間に延長した。同時に軽度の血圧上昇が認められた7)(外国人データ)。[10.2参照]
16.7.2 健康成人18例にベラパミル240mg又はプラセボを反復経口投与し、投与6日目にエレトリプタン80mg注)を単回経口投与した時、ベラパミル併用群ではプラセボ併用群と比較してエレトリプタンのCmaxは2.2倍、AUCが2.7倍に増大し、T1/2は4.5時間から4.9時間となり、その差は小さかった。臨床的に問題となる血圧への影響は認められなかった8)(外国人データ)。[10.2参照]
注:エレトリプタンの日本での承認用量は1回20mg又は40mgであり、1日の総投与量は40mg以内である。
18. 薬効薬理
18.1 作用機序
エレトリプタンは5-HT1B/1D受容体選択的作動薬である。5-HT1B/1D受容体選択的作動薬は頭蓋内血管の収縮を引き起こす9)。
19. 有効成分に関する理化学的知見
19.1. エレトリプタン臭化水素酸塩
22. 包装
10錠[10錠(PTP)×1]
10錠[10錠(患者さん用パッケージ入りPTP)×1]
23. 主要文献
- International Headache Society 2018, Cephalalgia., 38 (1), 1-211, (2018)
- 母乳中排泄(レルパックス錠:2002年4月11日承認、申請資料概要ヘ.3.1.3)
- 健康成人における薬物動態(性差、高齢者)(レルパックス錠:2002年4月11日承認、申請資料概要ヘ.3.1.6、ト.1.3.1)
- 社内資料:生物学的同等性試験
- 代謝に関与するチトクロムP450(レルパックス錠:2002年4月11日承認、申請資料概要ヘ.3.4.1)
- 肝機能障害患者における薬物動態(レルパックス錠:2002年4月11日承認、申請資料概要ヘ.3.3.1)
- エリスロマイシン併用時の薬物動態(レルパックス錠:2002年4月11日承認、申請資料概要ヘ.3.4.7、ト.1.3.2)
- ベラパミル併用時の薬物動態(レルパックス錠:2002年4月11日承認、申請資料概要ヘ.3.4.7、ト.1.3.2)
- Brunton,L.L.et al., グッドマン・ギルマン薬理書 第12版上巻(たか折修二ほか監訳), 430, (2013), (東京:廣川書店)
24. 文献請求先及び問い合わせ先
文献請求先
日新製薬株式会社
安全管理部
〒994-0069
山形県天童市清池東二丁目3番1号
電話:023-655-2131
FAX:023-655-3419
Email:d-info@yg-nissin.co.jp
製品情報問い合わせ先
日新製薬株式会社
安全管理部
〒994-0069
山形県天童市清池東二丁目3番1号
電話:023-655-2131
FAX:023-655-3419
Email:d-info@yg-nissin.co.jp
26. 製造販売業者等
26.1 製造販売元
日新製薬株式会社
山形県天童市清池東二丁目3番1号