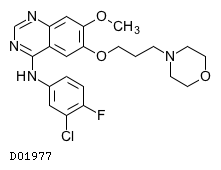
医薬品情報
| 総称名 | ゲフィチニブ |
|---|---|
| 一般名 | ゲフィチニブ |
| 欧文一般名 | Gefitinib |
| 製剤名 | ゲフィチニブ錠 |
| 薬効分類名 | 抗悪性腫瘍剤 上皮成長因子受容体(EGFR)チロシンキナーゼ阻害剤 |
| 薬効分類番号 | 4291 |
| ATCコード | L01EB01 |
| KEGG DRUG |
D01977
ゲフィチニブ
|
| KEGG DGROUP |
DG03162
EGFR阻害薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年6月 改訂(第3版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ゲフィチニブ錠250mg「JG」 (後発品) | 日本ジェネリック | 4291013F1043 | 1135.1円/錠 | 劇薬, 処方箋医薬品注) |
1. 警告
1.1 本剤による治療を開始するにあたり、患者に本剤の有効性・安全性、息切れ等の副作用の初期症状、非小細胞肺癌の治療法、致命的となる症例があること等について十分に説明し、同意を得た上で投与すること。[8.2参照]
1.2 本剤の投与により急性肺障害、間質性肺炎があらわれることがあるので、胸部X線検査等を行うなど観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。また、急性肺障害や間質性肺炎が本剤の投与初期に発生し、致死的な転帰をたどる例が多いため、少なくとも投与開始後4週間は入院またはそれに準ずる管理の下で、間質性肺炎等の重篤な副作用発現に関する観察を十分に行うこと。[8.1、9.1.1、11.1.1参照]
1.3 特発性肺線維症、間質性肺炎、じん肺症、放射線肺炎、薬剤性肺炎の合併は、本剤投与中に発現した急性肺障害、間質性肺炎発症後の転帰において、死亡につながる重要な危険因子である。このため、本剤による治療を開始するにあたり、特発性肺線維症、間質性肺炎、じん肺症、放射線肺炎、薬剤性肺炎の合併の有無を確認し、これらの合併症を有する患者に使用する場合には特に注意すること。[9.1.1、17.2参照]
1.4 急性肺障害、間質性肺炎による致死的な転帰をたどる例は全身状態の良悪にかかわらず報告されているが、特に全身状態の悪い患者ほど、その発現率及び死亡率が上昇する傾向がある。本剤の投与に際しては患者の状態を慎重に観察するなど、十分に注意すること。[9.1.2、17.2参照]
1.5 本剤は、肺癌化学療法に十分な経験をもつ医師が使用するとともに、投与に際しては緊急時に十分に措置できる医療機関で行うこと。
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌
5. 効能または効果に関連する注意
5.1 EGFR遺伝子変異検査を実施すること。EGFR遺伝子変異不明例の扱い等を含めて、本剤を投与する際は、日本肺癌学会の「肺癌診療ガイドライン」等の最新の情報を参考に行うこと。
5.2 本剤の術後補助療法における有効性及び安全性は確立していない。
5.3 「17.臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で適応患者の選択を行うこと。
6. 用法及び用量
通常、成人にはゲフィチニブとして250mgを1日1回、経口投与する。
7. 用法及び用量に関連する注意
7.1 日本人高齢者において無酸症が多いことが報告されているので、食後投与が望ましい。[9.1.3参照]
8. 重要な基本的注意
8.1 急性肺障害、間質性肺炎等の重篤な副作用が起こることがあり、致命的な経過をたどることがあるので、本剤の投与にあたっては、臨床症状(呼吸状態、咳及び発熱等の有無)を十分に観察し、定期的に胸部X線検査を行うこと。また、必要に応じて胸部CT検査、動脈血酸素分圧(PaO2)、肺胞気動脈血酸素分圧較差(A-aDO2)、肺拡散能力(DLco)などの検査を行うこと。[1.2、9.1.1、11.1.1参照]
8.2 本剤を投与するにあたっては、本剤の副作用について患者に十分に説明するとともに、臨床症状(息切れ、呼吸困難、咳及び発熱等の有無)を十分に観察し、これらが発現した場合には、速やかに医療機関を受診するように患者を指導すること。[1.1参照]
8.4 皮膚の副作用があらわれた場合には、患者の状態に応じて休薬あるいは対症療法を施すなど適切な処置を行うこと。
8.5 臨床試験において無力症が報告されているので、本剤投与中の患者には自動車の運転等危険を伴う機械を操作する際には注意するよう指導すること。
8.6 非臨床試験において本剤によるQT延長の可能性が示唆されていることから、必要に応じて心電図検査を実施すること。[15.2.1参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 急性肺障害、特発性肺線維症、間質性肺炎、じん肺症、放射線肺炎、薬剤性肺炎またはこれらの疾患の既往歴のある患者
9.1.2 全身状態の悪い患者
9.1.3 無酸症など著しい低胃酸状態が持続している患者
9.3 肝機能障害患者
9.4 生殖能を有する者
本剤投与中の女性には妊娠を避けるよう指導すること。[9.5参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。やむを得ず投与する場合は、本剤投与によるリスクについて患者に十分説明すること。
動物実験で胎児重量の減少(ウサギ)、生存出生児数の減少(ラット)及び出生児の早期死亡(ラット)が認められている。[9.4参照]
動物実験で胎児重量の減少(ウサギ)、生存出生児数の減少(ラット)及び出生児の早期死亡(ラット)が認められている。[9.4参照]
9.6 授乳婦
授乳しないことが望ましい。動物実験(ラット)で乳汁中へ移行することが認められている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に高齢者では生理機能が低下していることが多い。
なお、本剤の臨床試験成績から、65歳以上と65歳未満で血漿中濃度及び副作用発現率並びにその程度に差はみられていない。
なお、本剤の臨床試験成績から、65歳以上と65歳未満で血漿中濃度及び副作用発現率並びにその程度に差はみられていない。
10. 相互作用
相互作用序文
in vitro試験において、本薬は薬物代謝酵素チトクロームP450(CYP3A4)で代謝されることが示唆されているので、本酵素の活性に影響を及ぼす薬剤と併用する場合には、注意して投与すること。CYP3A4活性を阻害する薬剤との併用により、本剤の代謝が阻害され、本剤の血中濃度が上昇する可能性がある。また、CYP3A4誘導剤との併用により、本剤の代謝が促進され血中濃度が低下する可能性がある。[10.2、16.4、16.7.1、16.7.2参照]
一方、本薬はin vitro試験においてCYP2D6を阻害することが示唆されているので、CYP2D6により代謝される他の薬剤の血中濃度を増加させる可能性がある(本剤とメトプロロールの併用では、メトプロロールのAUCは平均で35%増加した)。
一方、本薬はin vitro試験においてCYP2D6を阻害することが示唆されているので、CYP2D6により代謝される他の薬剤の血中濃度を増加させる可能性がある(本剤とメトプロロールの併用では、メトプロロールのAUCは平均で35%増加した)。
薬物代謝酵素用語
CYP3A4
薬物代謝酵素用語
CYP2D6
10.2 併用注意
| CYP3A4誘導剤 フェニトイン、 カルバマゼピン、 リファンピシン、 バルビツール酸系薬物、 セイヨウオトギリソウ (St. John's Wort、セント・ジョーンズ・ワート)含有食品等 [16.7.1参照] | 本剤の血中濃度が低下し、作用が減弱するおそれがある。 | 本剤の代謝には主にCYP3A4が関与しているため、左記薬剤のようなCYP3A4誘導剤との併用で、本剤の代謝が亢進し血中濃度が低下する可能性がある。 |
| CYP3A4阻害剤 アゾール系抗真菌剤(イトラコナゾール等)、 マクロライド系抗生物質(エリスロマイシン等)、 リトナビル、ジルチアゼム塩酸塩、ベラパミル塩酸塩等 グレープフルーツジュース [16.7.2参照] | 本剤の血中濃度が増加し、副作用の発現頻度及び重症度が増加するおそれがある。 | 本剤の代謝には主にCYP3A4が関与しているため、左記のようなCYP3A4阻害剤等との併用で、本剤の代謝が阻害され血中濃度が増加する可能性がある。 |
| プロトンポンプ阻害剤 オメプラゾール等 H2-受容体拮抗剤 ラニチジン塩酸塩等 [9.1.3、16.7.3参照] | 著しい低胃酸状態が持続することにより、本剤の血中濃度が低下するおそれがある。 | 本剤の溶解性がpHに依存することから、胃内pHが持続的に上昇した条件下において、本剤の吸収が低下し、作用が減弱するおそれがある。 |
| ワルファリン | INR上昇や出血があらわれたとの報告がある。本剤とワルファリンを併用する場合には、定期的にプロトロンビン時間又はINRのモニターを行うこと。 | 機序は不明。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 急性肺障害、間質性肺炎(1〜10%未満)
11.1.2 重度の下痢(1%未満)
下痢があらわれた場合には、患者の状態に応じて休薬あるいは対症療法を施すなど、速やかに適切な処置を行うこと。
11.1.3 脱水(1%未満)
下痢、嘔気、嘔吐又は食欲不振に伴う脱水があらわれることがある。なお、脱水により腎不全に至った症例も報告されていることから、必要に応じて電解質や腎機能検査を行うこと。
11.1.4 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、多形紅斑(1%未満)
11.1.5 肝炎(頻度不明)、肝機能障害(10%以上)、黄疸(頻度不明)、肝不全(頻度不明)
11.1.6 血尿(1%未満)、出血性膀胱炎(1%未満)
11.1.7 急性膵炎(頻度不明)
腹痛、血清アミラーゼ値の上昇等が認められた場合には投与を中止し、適切な処置を行うこと。
11.1.8 消化管穿孔(頻度不明)、消化管潰瘍(1%未満)、消化管出血(1%未満)
異常が認められた場合には、内視鏡、腹部X線、CT等の必要な検査を行い、本剤の投与を中止するなど、適切な処置を行うこと。
11.2 その他の副作用
| 10%以上 | 1〜10%未満 | 1%未満 | 頻度不明 | |
| 全身 | 無力症、倦怠感 | 疲労 | ||
| 皮膚 | 発疹、そう痒症、皮膚乾燥、皮膚亀裂、ざ瘡等の皮膚症状 | 爪の障害 | 脱毛、皮下出血 | 皮膚血管炎、手掌・足底発赤知覚不全症候群 |
| 眼注1) | 結膜炎、眼瞼炎、角膜炎、角膜びらん注2)、眼乾燥注3) | |||
| 消化器 | 下痢 | 嘔気、嘔吐、食欲不振、口内炎 | 口内乾燥注3) | |
| 血液 | 白血球減少、血小板減少 | |||
| 肝臓 | 肝機能障害(AST上昇、ALT上昇等) | |||
| 過敏症 | じん麻疹 | 血管浮腫 | ||
| その他 | 鼻出血、クレアチニン上昇、蛋白尿、発熱 | INR上昇注4)、出血注4) |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 海外で実施された化学療法歴のない進行非小細胞肺癌患者を対象とした2つの臨床試験において、本剤とビノレルビンとの併用により、重症の好中球減少や発熱性好中球減少がみられ、臨床試験が中止された。また、日本においても、本剤とビノレルビンとの併用で重篤な好中球減少、白血球減少、血小板減少が報告されている。
15.1.2 国内で実施した「非小細胞肺癌患者におけるゲフィチニブ投与及び非投与での急性肺障害・間質性肺炎の相対リスク及び危険因子を検討するためのコホート内ケースコントロールスタディ」(V-15-33)2)において、本剤の急性肺障害・間質性肺炎発症の化学療法に対する相対リスクは、治療法間の患者背景の偏りを調整したオッズ比(調整オッズ比)で3.23(95%信頼区間:1.94-5.40)であった。
15.1.3 国内で実施した1又は2レジメンの化学療法治療歴を有する、進行/転移性(IIIB期/IV期)又は術後再発の非小細胞肺癌患者490例を対象に本剤(250mg/日投与)とドセタキセル(60mg/m2投与)の生存期間を比較する第III相製造販売後臨床試験(V-15-32)3)において、全生存期間の中央値は、イレッサ群で11.5ヵ月、ドセタキセル群で14.0ヵ月であり(ハザード比:1.12、95.24%信頼区間:0.89-1.40)、全生存期間における本剤のドセタキセルに対する非劣性は示されなかった。
本剤投与群で安全性評価対象症例244例中233例(95.5%)に副作用が認められ、主な副作用は、発疹158例(64.8%)、下痢113例(46.3%)、皮膚乾燥84例(34.4%)等であった。なお、急性肺障害・間質性肺炎は13例(5.3%)で、そのうち死亡例は3例であった。
本剤投与群で安全性評価対象症例244例中233例(95.5%)に副作用が認められ、主な副作用は、発疹158例(64.8%)、下痢113例(46.3%)、皮膚乾燥84例(34.4%)等であった。なお、急性肺障害・間質性肺炎は13例(5.3%)で、そのうち死亡例は3例であった。
15.1.4 海外で実施された1〜2レジメンの化学療法歴のある再発又は進行非小細胞肺癌患者を対象とした無作為化プラセボ対照二重盲検第III相比較臨床試験(ISEL)4)において、腫瘍縮小効果では統計学的に有意差が認められたが、対象患者全体(HR=0.89,p=0.09,中央値5.6ヵ月 vs 5.1ヵ月)、腺癌患者群(HR=0.84,p=0.09,中央値6.3ヵ月 vs 5.4ヵ月)で生存期間の延長に統計学的な有意差は認められなかった。
15.2 非臨床試験に基づく情報
15.2.1 非臨床の一般薬理試験において、本薬が心電図検査でQT間隔の延長を示す可能性のあることが以下のように示唆されている。イヌプルキンエ線維を用いた刺激伝達試験(in vitro系)において、本薬は濃度依存的に再分極時間を延長させた。またhERG(ヒト電位依存性カリウムチャンネルのαサブユニットをコードする遺伝子)を発現させたヒト胚腎細胞を用いたin vitro試験において、本薬は遅延整流性カリウム電流を濃度依存的に阻害し、心筋の再分極阻害を示唆する結果が得られた。さらにイヌのテレメトリー試験では心電図には統計学的に有意な変化は認められなかったが、個体別にQTc間隔の投与前値と投与後2時間の値を検討した結果、5mg/kg投与群の6例中1例、50mg/kg投与群の6例中2例に10%を超えるQTc間隔の延長が認められた。[8.6参照]
15.2.2 イヌを用いた反復投与毒性試験の心電図検査では、回復性のあるPR間隔の延長及びII度の房室ブロックが単発的かつ少数例に認められた。
15.2.3 ラット及びイヌを用いた反復投与毒性試験では、投与量及び投与期間に依存すると考えられる角膜における異常(半透明化、混濁及び角膜上皮の萎縮等)がみられた。これらのうち、角膜混濁はイヌにおいてのみ認められたものの、回復試験終了時においても正常には回復しなかった。また、ラット角膜創傷モデルにおいて、創傷治癒を遅延させるものの、創傷治癒を完全には妨げないという以下の報告もある5)。(溶媒対照群では創傷誘発後84時間までに完全治癒したのに対し、本薬投与群(40及び80mg/kg/日)では、創傷誘発後108または136時間後に治癒したが、創傷誘発後84時間以降は、溶媒対照群及び本薬投与群において、角膜上皮の損傷面積に統計学的な有意差は認められなかった。)
15.2.4 ラット及びイヌを用いた反復投与毒性試験では、皮膚(痂皮形成等)、腎臓(腎乳頭壊死等)及び卵巣(黄体数減少等)における所見が認められた。これらの所見は、本薬のEGFRチロシンキナーゼ阻害作用に起因した所見と考えられる。
15.2.5 2年間がん原性試験において、ラットの高用量(10mg/kg/日)投与群で有意な肝細胞腺腫(雌雄)と腸間膜リンパ節血管肉腫(雌)の発生増加が認められた。また、マウスの高用量(90mg/kg/日、125mg/kg/日を22週目から減量)投与群(雌)で有意な肝細胞腺腫の発生増加が認められた。
16. 薬物動態
16.1 血中濃度
16.1.1 単回及び反復経口投与時の血中濃度
日本人固形癌患者(n=6)にゲフィチニブ225mg注)を単回経口投与したとき、ゲフィチニブの吸収は緩徐で、最高血漿中濃度到達時間は概ね4時間であり、患者間で変動(3〜12時間)がみられた。終末相における消失半減期は約30時間であった。
ゲフィチニブ225mg注)を単回経口投与したときの単回及び反復投与時の薬物動態パラメータは以下の通りである6)7)。
ゲフィチニブ225mg注)を単回経口投与したときの単回及び反復投与時の薬物動態パラメータは以下の通りである6)7)。
| Cmax (ng/mL) | Tmaxa) (hr) | AUC0→∞ (ng・hr/mL) | t1/2 (hr) | |
| 単回 | 188±120 | 4.0(3.0〜12.0) | 4968±2125 | 30.1±4.6 |
| 反復 | 384±194 | 5.0(3.0〜7.0) | 16660±10630 | 41.3±9.9 |
16.1.2 反復経口投与におけるトラフ濃度
16.1.3 日本人及び欧米人患者の薬物動態
16.1.4 生物学的同等性試験
ゲフィチニブ錠250mg「JG」とイレッサ錠250を、クロスオーバー法によりそれぞれ1錠(ゲフィチニブとして250mg)健康成人男性に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された11)。
| 判定パラメータ | 参考パラメータ | |||
| AUC0-144 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
| ゲフィチニブ錠250mg「JG」 | 5682.9±1501.0 | 209.17±59.96 | 5.1±1.5 | 31.0±5.7 |
| イレッサ錠250 | 5478.3±1638.6 | 205.58±67.14 | 5.4±1.7 | 30.5±5.4 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.2.1 バイオアベイラビリティ
欧米人固形癌患者(n=17)における絶対バイオアベイラビリティは59%であった12)。
16.2.2 食事の影響
欧米人健康志願者(n=25)において、ゲフィチニブを食後投与したときAUC及びCmaxがそれぞれ37%及び32%増加したが、臨床上特に問題となる変化ではなかった13)。
16.3 分布
16.4 代謝
ヒト血漿中には、ゲフィチニブのO-脱メチル体、O,N-脱アルキル体、酸化脱フッ素体及びその他5種の代謝物が認められた。血漿中の主代謝物はO-脱メチル体であり、その濃度には大きな個体間変動がみられたが、未変化体と同程度の血漿中濃度を示した。O,N-脱アルキル体及び酸化脱フッ素体の血漿中濃度は未変化体の約3%以下であった。その他の代謝物はほとんど定量できなかった。
未変化体からO-脱メチル体への代謝にはCYP2D6が関与し、その他の代謝経路では主にCYP3A4が関与する。ヒト肝ミクロソームを用いたin vitro試験においてO-脱メチル体の生成量は僅かであり、CYP3A4阻害剤の共存下でO-脱メチル体を除く代謝物の生成量は明らかに減少した8)15)。
以上のことから、肝臓がゲフィチニブの代謝クリアランスにおいて重要な役割を果たしているものと推察される。
未変化体からO-脱メチル体への代謝にはCYP2D6が関与し、その他の代謝経路では主にCYP3A4が関与する。ヒト肝ミクロソームを用いたin vitro試験においてO-脱メチル体の生成量は僅かであり、CYP3A4阻害剤の共存下でO-脱メチル体を除く代謝物の生成量は明らかに減少した8)15)。
以上のことから、肝臓がゲフィチニブの代謝クリアランスにおいて重要な役割を果たしているものと推察される。
16.5 排泄
16.7 薬物相互作用
16.7.1 リファンピシン
16.7.2 イトラコナゾール
16.7.3 ラニチジン
注)本剤の承認用量は250mg/日である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第I相臨床試験
各種固形癌患者を対象にゲフィチニブ50〜700mg/日注)の用量で多施設共同非無作為化非盲検国内第I相臨床試験6)が行われ、適格例31例(非小細胞肺癌は23例)のうち5例にPR(非小細胞肺癌)、7例にNC(非小細胞肺癌、結腸・直腸癌、頭頸部癌、乳癌)が認められた。5例のPRはいずれも225mg/日注)よりも上の用量で認められた。
17.1.2 国際共同第II相臨床試験(IDEAL-1)
ゲフィチニブ単独投与による日本人及び外国人の進行非小細胞肺癌患者(化学療法による既治療例)を対象とし、ゲフィチニブ250及び500mg/日注)の有効性及び安全性を検討した無作為化二重盲検並行群間第II相国際共同臨床試験20)が実施されている。2001年5月時点までの集計(ゲフィチニブ250mg/日投与群)において、奏効率は18.4%(19/103)であり、そのうち、日本人における奏効率は27.5%(14/51)、外国人における奏効率は9.6%(5/52)であった。治療期間a)は日本人で平均105.7日、外国人で平均64.9日であった。
| 日本人 | 外国人 | 合計 | |
| 奏効率b) | 27.5% (14/51) | 9.6% (5/52) | 18.4% (19/103) |
| 病勢コントロール率c) | 70.6% (36/51) | 38.5% (20/52) | 54.4% (56/103) |
| 症状改善率d) | 48.5% (16/33) | 32.4% (11/34) | 40.3% (27/67) |
| 病勢進行までの期間;中央値 (95%信頼区間;下限〜上限) | 114日 (86日〜128日) | 57日 (55日〜66日) | 83日 (61日〜86日) |
ゲフィチニブ250mg/日が投与された103例中88例(85.4%)において副作用が認められた。主な副作用は、発疹48例(46.6%)、下痢41例(39.8%)、そう痒症31例(30.1%)、皮膚乾燥28例(27.2%)、嘔気、ALT増加、ざ瘡各13例(12.6%)等であった。
17.1.3 外国第II相臨床試験(IDEAL-2)
米国におけるゲフィチニブ単独投与による進行非小細胞肺癌患者(2回以上の化学療法による既治療例)を対象とし、ゲフィチニブ250及び500mg/日注)の有効性及び安全性を検討した無作為化二重盲検並行群間第II相臨床試験21)の結果、2001年8月時点までの集計において、ゲフィチニブ250mg/日群の奏効率は11.8%(12/102)であった。治療期間a)は平均72.6日であった。
| 奏効率b) | 11.8%(12/102) |
| 病勢コントロール率c) | 42.2%(43/102) |
| 症状改善率d) | 43.1%(44/102) |
| 病勢進行までの期間;中央値 (95%信頼区間;下限〜上限) | 59日(56日〜86日) |
ゲフィチニブ250mg/日が投与された102例中74例(72.5%)において副作用が認められた。主な副作用は、下痢49例(48.0%)、発疹44例(43.1%)、ざ瘡25例(24.5%)、皮膚乾燥、嘔気各13例(12.7%)等であった。
17.1.4 アジア国際共同第III相臨床試験(IPASS)
日本を含むアジアで実施した無作為化非盲検並行群間比較試験22)では、軽度の喫煙歴を有する又は非喫煙であり、かつ組織型が腺癌である、化学療法未治療の進行・再発非小細胞肺癌患者1217例(うち日本人233例)を対象に、ゲフィチニブ(250mg/日)と、カルボプラチンとパクリタキセルの併用化学療法が比較された。
主要評価項目である無増悪生存期間及び副次評価項目である全生存期間の結果は下表及び下図の通りである。
なお、本試験は無増悪生存期間における非劣性検証を主要目的として実施された。
主要評価項目である無増悪生存期間及び副次評価項目である全生存期間の結果は下表及び下図の通りである。
なお、本試験は無増悪生存期間における非劣性検証を主要目的として実施された。
| 全集団 | ゲフィチニブ群 (例数) | カルボプラチン+パクリタキセル群 (例数) | ハザード比a) | 95%信頼区間 |
| 無増悪生存期間 | 5.7ヵ月(中央値) (n=609) | 5.8ヵ月(中央値) (n=608) | 0.741 | 0.651-0.845b) |
| 全生存期間 | 18.8ヵ月(中央値) (n=609) | 17.4ヵ月(中央値) (n=608) | 0.901 | 0.793-1.023 |
図1 全集団における主要評価項目(無増悪生存期間)のKaplan-Meier曲線
ゲフィチニブ投与群で安全性評価対象症例607例中538例(88.6%)に副作用が認められ、主な副作用は、発疹・ざ瘡394例(64.9%)、下痢254例(41.8%)、皮膚乾燥143例(23.6%)等であった。なお、急性肺障害・間質性肺炎は8例(1.3%)で、そのうち死亡例は3例であった。(効能・効果の一部変更承認時)
また、EGFR遺伝子変異(Exon18〜21の変異が検討された)の有無による部分集団解析の結果は、下表及び下図の通りである。
また、EGFR遺伝子変異(Exon18〜21の変異が検討された)の有無による部分集団解析の結果は、下表及び下図の通りである。
| 評価項目 (EGFR遺伝子変異) | ゲフィチニブ群 (例数) | カルボプラチン+パクリタキセル群 (例数) | ハザード比a) | 95%信頼区間 |
| 無増悪生存期間 (陽性) | 9.5ヵ月(中央値) (n=132) | 6.3ヵ月(中央値) (n=129) | 0.482 | 0.362-0.642 |
| 無増悪生存期間 (陰性) | 1.5ヵ月(中央値) (n=91) | 5.5ヵ月(中央値) (n=85) | 2.853 | 2.048-3.975 |
| 全生存期間 (陽性) | 21.6ヵ月(中央値) (n=132) | 21.9ヵ月(中央値) (n=129) | 1.002 | 0.756-1.328 |
| 全生存期間 (陰性) | 11.2ヵ月(中央値) (n=91) | 12.7ヵ月(中央値) (n=85) | 1.181 | 0.857-1.628 |
図2 EGFR遺伝子変異別の無増悪生存期間のKaplan-Meier曲線
17.2 製造販売後調査等
国内で実施した特別調査「イレッサ錠250プロスペクティブ調査」1)における多変量解析の結果、喫煙歴有、全身状態の悪い患者、ゲフィチニブ投与時の間質性肺炎の合併、化学療法歴有が急性肺障害、間質性肺炎の発現因子として報告されている。また、全身状態の悪い患者、男性が予後不良因子(転帰死亡)として報告されている。
安全性評価対象症例3,322例中1,867例(56.2%)に副作用が認められ、主な副作用は、発疹568例(17.1%)、肝機能異常369例(11.1%)、下痢367例(11.1%)、急性肺障害・間質性肺炎は193例(5.8%)等であった。急性肺障害・間質性肺炎193例のうち、75例が死亡し、安全性評価対象症例数3,322例中の死亡率は2.3%、急性肺障害・間質性肺炎発現症例数193例中の死亡率は38.9%であった。(2004年8月報告時)[1.3、1.4、9.1.1、9.1.2参照]
安全性評価対象症例3,322例中1,867例(56.2%)に副作用が認められ、主な副作用は、発疹568例(17.1%)、肝機能異常369例(11.1%)、下痢367例(11.1%)、急性肺障害・間質性肺炎は193例(5.8%)等であった。急性肺障害・間質性肺炎193例のうち、75例が死亡し、安全性評価対象症例数3,322例中の死亡率は2.3%、急性肺障害・間質性肺炎発現症例数193例中の死亡率は38.9%であった。(2004年8月報告時)[1.3、1.4、9.1.1、9.1.2参照]
注)本剤の承認用量は250mg/日である。
18. 薬効薬理
18.1 作用機序
18.2 抗腫瘍効果
18.2.1 in vitro試験
ゲフィチニブは口腔扁平上皮癌株KBのEGF刺激による増殖を阻害した(IC50:0.054μmol/L)23)。ゲフィチニブはEGFRチロシンキナーゼを選択的に阻害し(EGFRチロシンキナーゼに対するIC50は0.027μmol/Lであり、ErbB2、KDR、Flt-1、Raf、MEK-1及びERK-2に対する阻害作用はその100分の1以下)、腫瘍細胞の増殖能を低下させる23)。
また、DNA断片化24)及び組織形態学的観察25)26)に基づき、ゲフィチニブがアポトーシスを誘導するとの報告がある。さらに、血管内皮増殖因子(VEGF)の産生抑制を介して腫瘍内の血管新生を阻害することも報告されている27)。さらにゲフィチニブは野生型EGFRよりも変異型EGFRに対してより低濃度で阻害作用を示し28)、アポトーシスを誘導することにより29)、悪性腫瘍の増殖抑制あるいは退縮を引き起こすことが報告されている。
また、DNA断片化24)及び組織形態学的観察25)26)に基づき、ゲフィチニブがアポトーシスを誘導するとの報告がある。さらに、血管内皮増殖因子(VEGF)の産生抑制を介して腫瘍内の血管新生を阻害することも報告されている27)。さらにゲフィチニブは野生型EGFRよりも変異型EGFRに対してより低濃度で阻害作用を示し28)、アポトーシスを誘導することにより29)、悪性腫瘍の増殖抑制あるいは退縮を引き起こすことが報告されている。
18.2.2 in vivo試験
ヒト腫瘍ヌードマウス移植系において、ゲフィチニブは12.5〜200mg/kg/日の用量で非小細胞肺癌株A549、ヒト前立腺癌株Du145、ヒト外陰部腫瘍株A431、大腸癌株CR10、HCT15、HT29、LoVo、口腔扁平上皮癌株KB、卵巣癌株HX62に対して腫瘍増殖抑制作用を示した23)。
18.3 代謝物
ヒトの主代謝物O-脱メチル体のEGF刺激下での細胞増殖に対する阻害作用はゲフィチニブの約14分の1であり、本代謝物の臨床効果への寄与は小さいと思われる30)。
19. 有効成分に関する理化学的知見
19.1. ゲフィチニブ
22. 包装
14錠[14錠(PTP)×1]
23. 主要文献
- 吉田茂, 医薬ジャーナル, 41 (2), 772-789, (2005)
- Kudoh, S. et al., Am. J. Respir. Crit. Care Med., 177 (12), 1348-1357, (2008) »PubMed
- 平成20年度第2回薬事・食品衛生審議会医薬品等安全対策部会安全対策調査会 資料3, (2008)
- Thatcher, N. et al., Lancet., 366, 1527-1537, (2005) »PubMed
- Nakamura, Y. et al., Exp. Eye Res., 72 (5), 511-517, (2001) »PubMed
- Nakagawa, K. et al., Ann. Oncol., 14 (6), 922-930, (2003) »PubMed
- 日本人固形癌患者にゲフィチニブを単回及び1日1回14日間反復投与したときの薬物動態(イレッサ錠:2002年7月5日承認、申請資料概要 ヘ.3.2.2)
- 第十八改正 日本薬局方解説書, C1945-C1951, (2021), (廣川書店)
- 日本人及び欧米人非小細胞肺癌患者に1日1回継続経口投与したときのポピュレーションファーマコキネティクス(イレッサ錠:2002年7月5日承認、申請資料概要 ヘ.3.2.3)
- Ranson, M. et al., J. Clin. Oncol., 20 (9), 2240-2250, (2002) »PubMed
- 社内資料:生物学的同等性試験
- 250mg単回経口投与時の薬物動態・バイオアベイラビリティ(イレッサ錠:2002年7月5日承認、申請資料概要 ヘ.3.4)
- 体内動態に及ぼす食事及び胃内pHの影響(イレッサ錠:2002年7月5日承認、申請資料概要 ヘ.3.5)
- 血漿蛋白結合率及び結合蛋白の同定(イレッサ錠:2002年7月5日承認、申請資料概要 ヘ.2.2.3.1)
- 代謝(イレッサ錠:2002年7月5日承認、申請資料概要 へ.2.3)
- 欧米人健康志願者に14C-ゲフィチニブを投与したときの体内動態(イレッサ錠:2002年7月5日承認、申請資料概要 ヘ.3.6)
- ラットにおける胆汁中排泄率(イレッサ錠:2002年7月5日承認、申請資料概要 ヘ.2.4.2)
- リファンピシンとの併用(イレッサ錠:2002年7月5日承認、申請資料概要 へ.3.7.1)
- イトラコナゾールとの併用(イレッサ錠:2002年7月5日承認、申請資料概要 へ.3.7.2)
- Fukuoka, M. et al., J. Clin. Oncol., 21 (12), 2237-2246, (2003) »PubMed
- Kris, M.G. et al., JAMA., 290 (16), 2149-2158, (2003) »PubMed
- Mok, T.S. et al., N. Engl. J. Med., 361 (10), 947-957, (2009) »PubMed
- Wakeling, A.E. et al., Cancer Res., 62 (20), 5749-5754, (2002) »PubMed
- Ciardiello, F. et al., Clin. Cancer Res., 6 (5), 2053-2063, (2000) »PubMed
- Chan, K.C. et al., Cancer Res., 62 (1), 122-128, (2002) »PubMed
- Albanell, J. et al., J. Clin. Oncol., 20 (1), 110-124, (2002) »PubMed
- Ciardiello, F. et al., Clin. Cancer Res., 7 (5), 1459-1465, (2001) »PubMed
- Lynch, T.J. et al., N. Engl. J. Med., 350 (21), 2129-2139, (2004) »PubMed
- Sordella, R. et al., Science., 305, 1163-1167, (2004) »PubMed
- 代謝物の薬理作用(イレッサ錠:2002年7月5日承認、申請資料概要 ホ.1.3)
24. 文献請求先及び問い合わせ先
文献請求先
日本ジェネリック株式会社
お客さま相談室
〒108-0014
東京都港区芝五丁目33番11号
電話:0120-893-170
FAX:0120-893-172
製品情報問い合わせ先
日本ジェネリック株式会社
お客さま相談室
〒108-0014
東京都港区芝五丁目33番11号
電話:0120-893-170
FAX:0120-893-172
26. 製造販売業者等
26.1 製造販売元
日本ジェネリック株式会社
東京都港区芝五丁目33番11号