医薬品情報
| 総称名 | ツートラム |
|---|---|
| 一般名 | トラマドール塩酸塩 |
| 欧文一般名 | Tramadol Hydrochloride |
| 製剤名 | 1日2回投与型トラマドール塩酸塩徐放錠 |
| 薬効分類名 | 慢性疼痛・がん疼痛 持続性鎮痛剤 |
| 薬効分類番号 | 1149 |
| ATCコード | N02AX02 |
| KEGG DRUG |
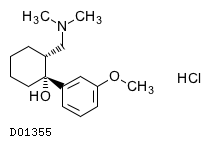
D01355
トラマドール塩酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年5月 改訂(第7版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ツートラム錠25mg | Twotram tab.25mg | 日本臓器製薬 | 1149038G5025 | 28.7円/錠 | 劇薬, 処方箋医薬品 |
| ツートラム錠50mg | Twotram tab.50mg | 日本臓器製薬 | 1149038G2026 | 47.4円/錠 | 劇薬, 処方箋医薬品 |
| ツートラム錠100mg | Twotram tab.100mg | 日本臓器製薬 | 1149038G3022 | 83.7円/錠 | 劇薬, 処方箋医薬品 |
| ツートラム錠150mg | Twotram tab.150mg | 日本臓器製薬 | 1149038G4029 | 115.2円/錠 | 劇薬, 処方箋医薬品 |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
非オピオイド鎮痛剤で治療困難な下記における鎮痛
慢性疼痛
疼痛を伴う各種がん
5. 効能または効果に関連する注意
慢性疼痛患者においては、原因となる器質的病変、心理的・社会的要因、依存リスクを含めた包括的な診断を行い、本剤の投与の適否を慎重に判断すること。
6. 用法及び用量
通常、成人にはトラマドール塩酸塩として1日100〜300mgを2回に分けて経口投与する。なお、症状に応じて適宜増減する。ただし1回200mg、1日400mgを超えないこととする。
7. 用法及び用量に関連する注意
ツートラム錠25mg
<製剤共通>
7.1 初回投与量
本剤を初めて投与する場合は、1回50mgから開始することが望ましい。なお、他のトラマドール塩酸塩経口剤から切り替える場合は、その経口剤の1日投与量、鎮痛効果及び副作用を考慮して、本剤の初回投与量を設定すること。
7.2 投与間隔
本剤の投与は1日2回とし、朝、夕に服用することが望ましい。
7.3 増量及び減量
本剤投与開始後に患者の状態を観察し、適切な鎮痛効果が得られ副作用が最小となるよう用量調整を行うこと。増量・減量の目安は、1回50mg、1日100mgずつ行うことが望ましい。
7.4 がん疼痛患者における疼痛増強時の臨時追加投与(レスキュー薬)
本剤服用中に疼痛が増強した場合や鎮痛効果が得られている患者で突出痛が発現した場合は、直ちにトラマドール塩酸塩即放性製剤の臨時追加投与を行って鎮痛を図ること。臨時追加投与の1回投与量は、定時投与中の本剤の1日量の1/8〜1/4を経口投与すること。ただし、トラマドール塩酸塩としての1日総投与量は400mgを超えないこと。
7.5 投与の継続
慢性疼痛患者において、本剤の投与開始後4週間を経過してもなお期待する効果が得られない場合は、他の適切な治療への変更を検討すること。また、定期的に症状及び効果を確認し、投与の継続の必要性について検討すること。
7.6 投与の中止
7.6.1 本剤の投与を必要としなくなった場合は、退薬症候の発現を防ぐために徐々に減量すること。
7.6.2 がん疼痛患者において、本剤の1日の定時投与量が300mgで鎮痛効果が不十分となった場合、本剤の投与を中止し、モルヒネ等の強オピオイド鎮痛剤への変更を考慮すること。その場合には、定時投与量の1/5の用量の経口モルヒネを初回投与量の目安とすることが望ましい。また、経口モルヒネ以外の強オピオイド鎮痛剤に変更する場合は、経口モルヒネとの換算で投与量を求めることが望ましい。
7.7 高齢者への投与
75歳以上の高齢者では、本剤の血中濃度が高い状態で持続し、作用及び副作用が増強するおそれがあるので、1日300mgを超えないことが望ましい。[16.6.1参照]
<25mg錠>
7.8 25mg錠の投与
原則として、25mg錠は1回1錠のみで使用しないこと。本剤の通常用量は、1日100〜300mgである。
ツートラム錠50mg
<製剤共通>
7.1 初回投与量
本剤を初めて投与する場合は、1回50mgから開始することが望ましい。なお、他のトラマドール塩酸塩経口剤から切り替える場合は、その経口剤の1日投与量、鎮痛効果及び副作用を考慮して、本剤の初回投与量を設定すること。
7.2 投与間隔
本剤の投与は1日2回とし、朝、夕に服用することが望ましい。
7.3 増量及び減量
本剤投与開始後に患者の状態を観察し、適切な鎮痛効果が得られ副作用が最小となるよう用量調整を行うこと。増量・減量の目安は、1回50mg、1日100mgずつ行うことが望ましい。
7.4 がん疼痛患者における疼痛増強時の臨時追加投与(レスキュー薬)
本剤服用中に疼痛が増強した場合や鎮痛効果が得られている患者で突出痛が発現した場合は、直ちにトラマドール塩酸塩即放性製剤の臨時追加投与を行って鎮痛を図ること。臨時追加投与の1回投与量は、定時投与中の本剤の1日量の1/8〜1/4を経口投与すること。ただし、トラマドール塩酸塩としての1日総投与量は400mgを超えないこと。
7.5 投与の継続
慢性疼痛患者において、本剤の投与開始後4週間を経過してもなお期待する効果が得られない場合は、他の適切な治療への変更を検討すること。また、定期的に症状及び効果を確認し、投与の継続の必要性について検討すること。
7.6 投与の中止
7.6.1 本剤の投与を必要としなくなった場合は、退薬症候の発現を防ぐために徐々に減量すること。
7.6.2 がん疼痛患者において、本剤の1日の定時投与量が300mgで鎮痛効果が不十分となった場合、本剤の投与を中止し、モルヒネ等の強オピオイド鎮痛剤への変更を考慮すること。その場合には、定時投与量の1/5の用量の経口モルヒネを初回投与量の目安とすることが望ましい。また、経口モルヒネ以外の強オピオイド鎮痛剤に変更する場合は、経口モルヒネとの換算で投与量を求めることが望ましい。
7.7 高齢者への投与
75歳以上の高齢者では、本剤の血中濃度が高い状態で持続し、作用及び副作用が増強するおそれがあるので、1日300mgを超えないことが望ましい。[16.6.1参照]
ツートラム錠100mg
<製剤共通>
7.1 初回投与量
本剤を初めて投与する場合は、1回50mgから開始することが望ましい。なお、他のトラマドール塩酸塩経口剤から切り替える場合は、その経口剤の1日投与量、鎮痛効果及び副作用を考慮して、本剤の初回投与量を設定すること。
7.2 投与間隔
本剤の投与は1日2回とし、朝、夕に服用することが望ましい。
7.3 増量及び減量
本剤投与開始後に患者の状態を観察し、適切な鎮痛効果が得られ副作用が最小となるよう用量調整を行うこと。増量・減量の目安は、1回50mg、1日100mgずつ行うことが望ましい。
7.4 がん疼痛患者における疼痛増強時の臨時追加投与(レスキュー薬)
本剤服用中に疼痛が増強した場合や鎮痛効果が得られている患者で突出痛が発現した場合は、直ちにトラマドール塩酸塩即放性製剤の臨時追加投与を行って鎮痛を図ること。臨時追加投与の1回投与量は、定時投与中の本剤の1日量の1/8〜1/4を経口投与すること。ただし、トラマドール塩酸塩としての1日総投与量は400mgを超えないこと。
7.5 投与の継続
慢性疼痛患者において、本剤の投与開始後4週間を経過してもなお期待する効果が得られない場合は、他の適切な治療への変更を検討すること。また、定期的に症状及び効果を確認し、投与の継続の必要性について検討すること。
7.6 投与の中止
7.6.1 本剤の投与を必要としなくなった場合は、退薬症候の発現を防ぐために徐々に減量すること。
7.6.2 がん疼痛患者において、本剤の1日の定時投与量が300mgで鎮痛効果が不十分となった場合、本剤の投与を中止し、モルヒネ等の強オピオイド鎮痛剤への変更を考慮すること。その場合には、定時投与量の1/5の用量の経口モルヒネを初回投与量の目安とすることが望ましい。また、経口モルヒネ以外の強オピオイド鎮痛剤に変更する場合は、経口モルヒネとの換算で投与量を求めることが望ましい。
7.7 高齢者への投与
75歳以上の高齢者では、本剤の血中濃度が高い状態で持続し、作用及び副作用が増強するおそれがあるので、1日300mgを超えないことが望ましい。[16.6.1参照]
ツートラム錠150mg
<製剤共通>
7.1 初回投与量
本剤を初めて投与する場合は、1回50mgから開始することが望ましい。なお、他のトラマドール塩酸塩経口剤から切り替える場合は、その経口剤の1日投与量、鎮痛効果及び副作用を考慮して、本剤の初回投与量を設定すること。
7.2 投与間隔
本剤の投与は1日2回とし、朝、夕に服用することが望ましい。
7.3 増量及び減量
本剤投与開始後に患者の状態を観察し、適切な鎮痛効果が得られ副作用が最小となるよう用量調整を行うこと。増量・減量の目安は、1回50mg、1日100mgずつ行うことが望ましい。
7.4 がん疼痛患者における疼痛増強時の臨時追加投与(レスキュー薬)
本剤服用中に疼痛が増強した場合や鎮痛効果が得られている患者で突出痛が発現した場合は、直ちにトラマドール塩酸塩即放性製剤の臨時追加投与を行って鎮痛を図ること。臨時追加投与の1回投与量は、定時投与中の本剤の1日量の1/8〜1/4を経口投与すること。ただし、トラマドール塩酸塩としての1日総投与量は400mgを超えないこと。
7.5 投与の継続
慢性疼痛患者において、本剤の投与開始後4週間を経過してもなお期待する効果が得られない場合は、他の適切な治療への変更を検討すること。また、定期的に症状及び効果を確認し、投与の継続の必要性について検討すること。
7.6 投与の中止
7.6.1 本剤の投与を必要としなくなった場合は、退薬症候の発現を防ぐために徐々に減量すること。
7.6.2 がん疼痛患者において、本剤の1日の定時投与量が300mgで鎮痛効果が不十分となった場合、本剤の投与を中止し、モルヒネ等の強オピオイド鎮痛剤への変更を考慮すること。その場合には、定時投与量の1/5の用量の経口モルヒネを初回投与量の目安とすることが望ましい。また、経口モルヒネ以外の強オピオイド鎮痛剤に変更する場合は、経口モルヒネとの換算で投与量を求めることが望ましい。
7.7 高齢者への投与
75歳以上の高齢者では、本剤の血中濃度が高い状態で持続し、作用及び副作用が増強するおそれがあるので、1日300mgを超えないことが望ましい。[16.6.1参照]
8. 重要な基本的注意
8.1 連用により薬物依存を生じることがあるので、観察を十分に行い、慎重に投与すること。[11.1.4参照]
8.2 本剤を投与した際に、悪心、嘔吐、便秘等の症状があらわれることがある。悪心・嘔吐に対する対策として制吐剤の併用を、便秘に対する対策として下剤の併用を考慮し、本剤投与時の副作用の発現に十分注意すること。
8.3 眠気、めまい、意識消失が起こることがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械の操作に従事させないよう注意すること。なお、意識消失により自動車事故に至った例も報告されている。
8.4 鎮痛剤による治療は原因療法ではなく、対症療法であることに留意すること。
8.5 本剤は徐放性製剤であることから、急激な血中濃度の上昇による重篤な副作用の発現を避けるため、服用に際して割ったり、砕いたり又はかみ砕いたりしないように指示すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 18歳未満の肥満、閉塞性睡眠時無呼吸症候群又は重篤な肺疾患を有する患者
投与しないこと。重篤な呼吸抑制のリスクが増加するおそれがある。
9.1.2 てんかんのある患者、痙攣発作を起こしやすい患者又は痙攣発作の既往歴のある患者(治療により十分な管理がされていないてんかん患者を除く)
本剤投与中は観察を十分に行うこと。痙攣発作を誘発することがある。[2.6参照]
9.1.3 薬物乱用又は薬物依存傾向のある患者
厳重な医師の管理下に、短期間に限って投与すること。依存性を生じやすい。
9.1.4 呼吸抑制状態にある患者
呼吸抑制を増強するおそれがある。
9.1.5 脳に器質的障害のある患者
呼吸抑制や頭蓋内圧の上昇を来すおそれがある。
9.1.6 オピオイド鎮痛剤に対し過敏症の既往歴のある患者(本剤の成分に対し過敏症の既往歴のある患者を除く)[2.2参照]
9.1.7 ショック状態にある患者
循環不全や呼吸抑制を増強するおそれがある。
9.2 腎機能障害患者
9.2.1 高度な腎機能障害のある患者
投与しないこと。高い血中濃度が持続し、作用及び副作用が増強するおそれがある。[2.7参照]
9.2.2 腎機能障害のある患者(高度な腎機能障害のある患者を除く)
高い血中濃度が持続するおそれがある。
9.3 肝機能障害患者
9.3.1 高度な肝機能障害のある患者
投与しないこと。高い血中濃度が持続し、作用及び副作用が増強するおそれがある。[2.7参照]
9.3.2 肝機能障害のある患者(高度な肝機能障害のある患者を除く)
高い血中濃度が持続するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。胎盤を通過し、退薬症候が新生児に起こる可能性がある。なお、動物実験で、器官形成、骨化及び出生児の生存に影響を及ぼすことが報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。静脈内投与(国内未承認)の場合、0.1%が乳汁中に移行することが知られている。
9.7 小児等
9.7.1 12歳未満の小児
投与しないこと。海外において、12歳未満の小児で死亡を含む重篤な呼吸抑制のリスクが高いとの報告がある。[2.1参照]
9.7.2 12歳以上の小児
12歳以上の小児に対する有効性及び安全性を指標とした臨床試験は実施していない。
9.7.3 肥満、閉塞性睡眠時無呼吸症候群又は重篤な肺疾患を有する小児
投与しないこと。重篤な呼吸抑制のリスクが増加するおそれがある。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。生理機能が低下していることが多く、代謝・排泄が遅延し副作用があらわれやすい。
10. 相互作用
相互作用序文
本剤は主にCYP2D6及びCYP3A4により代謝される。
薬物代謝酵素用語
CYP2D6
薬物代謝酵素用語
CYP3A4
10.1 併用禁忌
| モノアミン酸化酵素阻害剤 セレギリン塩酸塩 エフピー ラサギリンメシル酸塩 アジレクト サフィナミドメシル酸塩 エクフィナ [2.4参照] | 外国において、セロトニン症候群(錯乱、激越、発熱、発汗、運動失調、反射異常亢進、ミオクローヌス、下痢等)を含む中枢神経系(攻撃的行動、固縮、痙攣、昏睡、頭痛)、呼吸器系(呼吸抑制)及び心血管系(低血圧、高血圧)の重篤な副作用が報告されている。モノアミン酸化酵素阻害剤を投与中の患者又は投与中止後14日以内の患者には投与しないこと。また、本剤投与中止後にモノアミン酸化酵素阻害剤の投与を開始する場合には、2〜3日間の間隔をあけることが望ましい。 | 相加的に作用が増強され、また中枢神経のセロトニンが蓄積すると考えられる。 |
| ナルメフェン塩酸塩水和物 セリンクロ [2.5参照] | 離脱症状を起こすおそれがある。本剤の鎮痛作用を減弱させるため、効果を得るために必要な用量が通常用量より多くなり、呼吸抑制等の中枢神経抑制症状が発現するおそれがある。ナルメフェンを投与中の患者又は投与中止後1週間以内の患者には投与しないこと。 | ナルメフェンのμオピオイド受容体拮抗作用により、本剤に対して競合的に阻害する。 |
10.2 併用注意
| オピオイド鎮痛剤 中枢神経抑制剤 フェノチアジン系薬剤、催眠鎮静剤等 | 痙攣閾値の低下や呼吸抑制の増強を来すおそれがある。 | 本剤と相加的に作用が増強されると考えられる。 |
| 三環系抗うつ剤 セロトニン作用薬 選択的セロトニン再取り込み阻害剤(SSRI)等 | セロトニン症候群(錯乱、激越、発熱、発汗、運動失調、反射異常亢進、ミオクローヌス、下痢等)があらわれるおそれがある。 また、痙攣発作の危険性を増大させるおそれがある。 | 相加的に作用が増強され、また、中枢神経のセロトニンが蓄積すると考えられる。 |
| リネゾリド | セロトニン症候群(錯乱、激越、発熱、発汗、運動失調、反射異常亢進、ミオクローヌス、下痢等)があらわれるおそれがある。 また、痙攣発作の危険性を増大させるおそれがある。 | リネゾリドの非選択的、可逆的モノアミン酸化酵素阻害作用により、相加的に作用が増強され、また、中枢神経のセロトニンが蓄積すると考えられる。 |
| メチルチオニニウム塩化物水和物(メチレンブルー) | セロトニン症候群(錯乱、激越、発熱、発汗、運動失調、反射異常亢進、ミオクローヌス、下痢等)があらわれるおそれがある。 | メチルチオニニウム塩化物水和物のモノアミン酸化酵素阻害作用によりセロトニン作用が増強される。 |
| アルコール | 呼吸抑制が生じるおそれがある。 | 本剤と相加的に作用が増強されると考えられる。 |
| カルバマゼピン | 同時あるいは前投与で本剤の鎮痛効果を下げ作用時間を短縮させる可能性がある。 | 本剤の代謝酵素が誘導される。 |
| キニジン | 相互に作用が増強するおそれがある。 | 機序不明 |
| ジゴキシン | 外国において、ジゴキシン中毒が発現したとの報告がある。 | 機序不明 |
| オンダンセトロン塩酸塩水和物 | 本剤の鎮痛作用を減弱させるおそれがある。 | 本剤の中枢におけるセロトニン作用が抑制されると考えられる。 |
| ブプレノルフィン ペンタゾシン等 | 本剤の鎮痛作用を減弱させるおそれがある。また、退薬症候を起こすおそれがある。 | 本剤が作用するμ-オピオイド受容体の部分アゴニストである。 |
| クマリン系抗凝血剤 ワルファリン | 出血を伴うプロトロンビン時間の延長、斑状出血等の抗凝血作用への影響がみられたとの報告がある。 | 機序不明 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(頻度不明)
呼吸困難、気管支痙攣、喘鳴、血管神経性浮腫等があらわれることがある。
11.1.2 呼吸抑制(頻度不明)
11.1.3 痙攣(頻度不明)
11.1.4 依存性(頻度不明)
長期使用時に、耐性、精神的依存及び身体的依存が生じることがある。本剤の中止又は減量時において、激越、不安、神経過敏、不眠症、運動過多、振戦、胃腸症状、パニック発作、幻覚、錯感覚、耳鳴等の退薬症候が生じることがある。[8.1参照]
11.1.5 意識消失(頻度不明)
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 消化器 | 悪心(41.6%) 便秘(38.1%) 嘔吐(15.3%) 食欲減退 | 腹部不快感 | 消化不良、胃炎、腹部膨満感、下痢、胃食道逆流性疾患、上腹部痛、口内炎、出血性胃炎、口唇炎、口角口唇炎 | 口の錯感覚、胃腸音異常、口内乾燥、腹痛、おくび、イレウス |
| 精神神経系 | 傾眠(20.3%) 浮動性めまい(10.3%) | 頭痛 | 回転性めまい、振戦、不眠症、耳鳴、味覚不全、感覚鈍麻、頭部不快感、片頭痛、体位性めまい、錯感覚、譫妄、不安 | 睡眠障害、健忘、幻覚、鎮静、悪夢、落ち着きのなさ、活動性低下、異常行動、無感情、不快気分、不随意性筋収縮、記憶障害、ジスキネジー、眼振、疲労、気分変動、うつ病、頭重感、激越、抑うつ気分、両手のしびれ感、ふらつき感、不快感、協調運動異常、失神、錯乱、精神運動亢進、錯覚、言語障害 |
| 呼吸器 | 呼吸困難、口腔咽頭痛、咽喉乾燥、口腔咽頭不快感、発声障害 | |||
| 循環器 | 動悸、高血圧、ほてり | 不整脈、蒼白、胸内苦悶、頻脈、徐脈、血圧上昇、血圧低下、起立性低血圧 | ||
| 血液凝固系 | 好中球数増加 | ヘマトクリット減少、血小板減少、好酸球増加・減少、リンパ球減少、ヘモグロビン減少、赤血球減少、白血球増加 | ||
| 肝臓 | 肝機能異常、ALT増加、AST増加、LDH増加 | Al-P増加、ビリルビン増加 | ||
| 皮膚 | そう痒症、多汗症 | 湿疹、発疹、薬疹、冷汗、蕁麻疹、寝汗 | ||
| 腎臓及び尿路系 | 排尿困難 | 尿中血陽性、尿中ブドウ糖陽性、膀胱炎、頻尿、尿閉、血中クレアチニン増加、尿量減少 | 尿蛋白陽性、BUN増加、夜間頻尿 | |
| 代謝異常 | 血中尿酸増加、脱水 | トリグリセリド増加 | ||
| その他 | 口渇(6.9%) | 倦怠感、CK増加 | 末梢性浮腫、異常感、胸部不快感、体重減少 | 熱感、視力障害、背部痛、疼痛、霧視、散瞳、無力症、関節痛、四肢痛、筋骨格硬直、易刺激性、悪寒、発熱、冷感、視調節障害、心電図QT延長、浮腫、転倒 |
13. 過量投与
13.1 症状
中毒による典型的な症状は、縮瞳、嘔吐、心血管虚脱、昏睡に至る意識障害、痙攣、呼吸停止に至る呼吸抑制等が報告されている。
13.2 処置
緊急処置として、気道を確保し、症状に応じた呼吸管理と循環の管理を行うこと。本剤摂取後2時間以内の場合、胃内容物の吸引、胃洗浄あるいは活性炭投与等の処置が有効である。また、呼吸抑制に対してはナロキソンの投与、痙攣に対してはジアゼパムの静脈内投与を行うこと(ナロキソンは動物実験で痙攣を増悪させるとの報告があるので注意すること)。本剤は透析によってはほとんど除去されず、急性中毒に対して、解毒のための血液透析、あるいは血液濾過のみの治療は不適切である。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 本剤の投与にあたっては、具体的な服用方法、服用時の注意点、保管方法等を十分に説明し、本剤の目的以外への使用をしないように指導するとともに、本剤を子供の手の届かないところに保管するよう指導すること。
14.1.2 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.3 有効成分放出後の基剤(抜け殻)が糞便中に排泄されることがある。
15. その他の注意
15.1 臨床使用に基づく情報
遺伝的にCYP2D6の活性が過剰であることが判明している患者(Ultra-rapid Metabolizer)では、トラマドールの活性代謝物の血中濃度が上昇し、呼吸抑制等の副作用が発現しやすくなるおそれがある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男性7例にトラマドール塩酸塩徐放錠をそれぞれ50mg、100mg、200mg、400mg注1)絶食下に単回投与した時、トラマドール及び活性代謝物O-デメチルトラマドール(M1)のCmax及びAUC0-infにおいて、用量比例性が認められた。1)2)
注1)本剤の承認用量における1回投与量は最大200mgである。
健康成人男性22〜24例を対象とし、トラマドール塩酸塩徐放錠をそれぞれ25mg×2錠、50mg、100mg、150mgで絶食下に単回投与した時、トラマドール及びM1のCmax及びAUC0-tが用量に依存して増加した。3)
| トラマドール | ||||
| \ | 本剤 | |||
| 25mg×2錠 | 50mg | 100mg | 150mg | |
| Cmax(ng/mL) | 116.2±25.0 | 114.0±23.4 | 207.5±36.0 | 325.5±51.9 |
| tmax(h) | 1.36±0.93 | 1.04±0.54 | 1.28±0.65 | 1.51±0.64 |
| t1/2(h) | 8.463±1.219 | 8.598±1.096 | 7.853±1.128 | 7.596±1.202 |
| AUC0-t(ng・h/mL) | 1319.6±449.8 | 1265.6±384.4 | 2301.1±625.2 | 4101.5±978.8 |
トラマドール
| M1 | ||||
| \ | 本剤 | |||
| 25mg×2錠 | 50mg | 100mg | 150mg | |
| Cmax(ng/mL) | 28.33±10.21 | 26.68±10.28 | 54.12±15.57 | 69.79±22.82 |
| tmax(h) | 1.56±0.98 | 1.38±0.66 | 1.63±0.80 | 2.57±1.24 |
| t1/2(h) | 10.738±1.861 | 11.658±3.933 | 9.727±1.771 | 8.898±1.327 |
| AUC0-t(ng・h/mL) | 432.54±106.83 | 420.41±130.97 | 822.17±161.98 | 1201.37±277.44 |
M1
16.1.2 反復投与
健康成人男性6〜7例にトラマドール塩酸塩徐放錠をそれぞれ1回50mg、100mgを1日2回7日間反復投与した時、トラマドール及び活性代謝物M1共に投与後約24時間までに定常状態に達し、Cmax及びAUC0-12は投与1日目の約2倍であった。2)
16.2 吸収
16.2.1 食事の影響
健康成人男性18〜20例にトラマドール塩酸塩徐放錠をそれぞれ50mg、100mg、150mg絶食下又は高脂肪食後に単回投与した時、いずれの製剤も絶食投与と高脂肪食後投与のトラマドールのCmax及びAUC0-tにおいて、食事の影響は認められなかった。また、食後投与でtmaxが約1時間延長した。4)
16.3 分布
14C-トラマドール塩酸塩を雄性ラットに2mg/kgの用量で単回経口投与した結果、投与後0.5時間でほぼ全身に放射能分布がみられ、肝臓、腎臓及び膵臓では血漿中放射能濃度と比較して高い分布を示した。その後、血漿と同様に各組織中から速やかに消失し、放射能濃度は投与後24時間で最高値の10%以下に低下した。14C-トラマドール塩酸塩を妊娠ラットに単回経口投与した結果、放射能は胎盤を通過して胎児に分布した。胎児中放射能濃度は母体の血液中濃度と同程度で、胎児中からの消失は母体の血液中放射能と同様に速やかであった。
ヒト血漿タンパク質との結合率(in vitro)は、25〜2000ng/mLの濃度範囲で25〜30%であった。5)
ヒト血漿タンパク質との結合率(in vitro)は、25〜2000ng/mLの濃度範囲で25〜30%であった。5)
16.4 代謝
トラマドールの主な代謝経路は、N-脱メチル化又はO-脱メチル化(第I相反応)とO-脱メチル化代謝物の抱合化である。
活性代謝物O-デメチルトラマドール(M1)などのO-脱メチル化はCYP2D6、N-脱メチル化はCYP3A4が主に関与している。6)
活性代謝物O-デメチルトラマドール(M1)などのO-脱メチル化はCYP2D6、N-脱メチル化はCYP3A4が主に関与している。6)
16.5 排泄
16.6 特定の背景を有する患者
17. 臨床成績
17.1 有効性及び安全性に関する試験
<慢性疼痛>
17.1.1 変形性膝関節症に対する国内第III相試験
変形性膝関節症と診断され、非ステロイド性消炎鎮痛剤(NSAIDs)の経口投与により十分な鎮痛効果が得られない慢性疼痛患者を対象とし、非盲検下で1〜4週間かけて1日2回、100〜300mg/日の範囲で適宜漸増した後、二重盲検期への移行基準注2)を満たした患者159例を、本剤群78例又はプラセボ群81例にランダム割付けし4週間投与した。二重盲検期開始時から治験薬の鎮痛効果が不十分となる注3)までの期間について、log-rank検定で比較した結果、有意差が認められ(p=0.042)、本剤群のプラセボ群に対する優越性が検証された。
累積継続率
副作用の発現率は80.2%(199/248例)であった。10%以上発現した副作用は、悪心44.4%(110/248例)、便秘40.7%(101/248例)、傾眠21.4%(53/248例)、嘔吐17.7%(44/248例)であった。8)
17.1.2 帯状疱疹後神経痛に対する国内第III相試験
帯状疱疹後神経痛と診断され、鎮痛補助剤や非オピオイド鎮痛剤の経口投与により十分な鎮痛効果が得られない慢性疼痛患者を対象とし、非盲検下で1〜5週間かけて1日2回、100〜400mg/日の範囲で適宜漸増した後、二重盲検期への移行基準注2)を満たした患者171例を、本剤群83例又はプラセボ群88例にランダム割付けし4週間投与した。二重盲検期開始時から、治験薬の鎮痛効果が不十分となる注3)までの期間について、log-rank検定で比較した結果、有意差が認められ(p=0.0005)、プラセボ群に対する本剤群の優越性が検証された。
累積継続率
副作用発現率は、70.7%(176/249例)であった。10%以上発現した副作用は、便秘43.0%(107/249例)、悪心33.3%(83/249例)、傾眠18.5%(46/249例)、浮動性めまい10.8%(27/249例)であった。9)
注2)二重盲検期への移行基準
・非盲検期(固定期)の服薬率が70%以上である。
・二重盲検期開始前3日間の平均NRS値が非盲検期開始前3日間の平均NRS値より2以上改善している。
・二重盲検期開始前3日間のNRS値の最大値と最小値の差が2以内である。
注3)鎮痛効果が不十分となる基準
・二重盲検期におけるNRS値が二重盲検期開始時の前3日間の平均NRS値と比較して、2以上悪化した日が2日連続した場合。
・二重盲検期に、被験者が鎮痛効果不十分を理由に治験薬の投与中止を申し出た場合。
17.1.3 慢性疼痛に対する長期投与試験
腰痛症、変形性膝関節症、関節リウマチ、脊柱管狭窄症、帯状疱疹後神経痛、有痛性糖尿病性神経障害、線維筋痛症、複合性局所疼痛症候群のいずれかによる慢性疼痛を有し、鎮痛補助剤や非オピオイド鎮痛剤の経口投与により十分な鎮痛効果が得られない患者174例を対象とし、本剤を1日2回、100〜400mg/日の範囲で8週間適宜増減して最長52週間(12ヶ月)投与した。
0〜10の11段階で評価するNRS値(過去24時間の最大疼痛)の平均値の推移は、用量調節期を通じて経時的に低下し、継続投与期の32週目まで低下し続け、以降は改善状態が維持された。NRS値(過去24時間の最大疼痛)の変化量の平均値(標準偏差)は、用量調節期終了時で−2.77(1.77)であり、継続投与期では、−3.20〜−3.83で維持された。また、NRS値(過去24時間の最も長く続いた痛み)の平均値の推移も、NRS値(過去24時間の最大疼痛)の平均値の推移と同様の傾向を示した。
0〜10の11段階で評価するNRS値(過去24時間の最大疼痛)の平均値の推移は、用量調節期を通じて経時的に低下し、継続投与期の32週目まで低下し続け、以降は改善状態が維持された。NRS値(過去24時間の最大疼痛)の変化量の平均値(標準偏差)は、用量調節期終了時で−2.77(1.77)であり、継続投与期では、−3.20〜−3.83で維持された。また、NRS値(過去24時間の最も長く続いた痛み)の平均値の推移も、NRS値(過去24時間の最大疼痛)の平均値の推移と同様の傾向を示した。
| 原疾患別の最終評価時における各NRS値のベースラインからの変化量 | |||
| 原疾患 | 例数 | 過去24時間の最大疼痛 | 過去24時間の最も長く続いた痛み |
| 腰痛症 | 29例 | −3.13±2.03 | −2.88±2.07 |
| 変形性膝関節症 | 29例 | −2.56±2.09 | −2.27±1.97 |
| 関節リウマチ | 10例 | −2.91±2.45 | −2.26±2.23 |
| 脊柱管狭窄症 | 25例 | −2.76±2.41 | −2.38±2.02 |
| 帯状疱疹後神経痛 | 19例 | −2.84±2.32 | −2.04±1.83 |
| 有痛性糖尿病性神経障害 | 17例 | −3.64±2.37 | −3.39±2.31 |
| 線維筋痛症 | 30例 | −4.70±1.98 | −4.06±1.89 |
| 複合性局所疼痛症候群 | 11例 | −1.95±1.59 | −1.85±1.49 |
| 合計 | 170例 | −3.18±2.26 | −2.77±2.08 |
NRS値の推移
副作用発現率は88.5%(154/174例)であった。10%以上発現した副作用は、悪心が52.9%(92/174例)、便秘が36.8%(64/174例)、傾眠が24.1%(42/174例)、嘔吐が20.1%(35/174例)、浮動性めまいが10.9%(19/174例)であった。10)
<がん疼痛>
17.1.4 がん疼痛に対する国内第III相試験
オピオイド鎮痛剤未投与かつ非オピオイド鎮痛剤投与中で、安静時のVAS値(痛みの程度)が25mm以上のがん疼痛患者244例を対象としたランダム化二重盲検比較試験を実施した。本剤を1日2回、100mg/日又は対照薬(トラマドール塩酸塩即放性製剤)を1日4回、100mg/日にて投与開始し、いずれも300mg/日までの範囲で適宜増減しながら14日間投与した。主要評価項目である安静時の投与開始時と投与終了時のVAS値の変化量を指標として検討した結果、本剤群の対照群に対する非劣性が検証された。
| 投与群 | 本剤群 | 対照群 |
| 例数 | 124例 | 120例 |
| 投与開始前3日間のVAS平均値(mm)a) | 48.26±16.19 | 47.24±14.87 |
| 投与終了前3日間のVAS平均値(mm)a) | 25.98±22.45 | 28.39±20.62 |
| VAS平均値の変化量(mm)a) | −22.28±22.50 | −18.86±18.82 |
| VAS平均値の変化量の調整済み平均(mm)b) | −22.07 | −19.08 |
| VAS平均値の変化量の調整済み平均の群間差(mm)b)(95%信頼区間) | −2.99(−7.96〜1.99c)) | |
安静時の痛みの変化量
副作用発現率は、58.7%(74/126例)であった。10%以上発現した副作用は、悪心27.8%(35/126例)、便秘19.8%(25/126例)、嘔吐16.7%(21/126例)、傾眠14.3%(18/126例)であった。11)
18. 薬効薬理
18.1 作用機序
トラマドール塩酸塩及び肝臓で生成される活性代謝物M1は、モルヒネと同じ作用機序のμ-オピオイド受容体に対する作用に加えて、抗うつ作用様のセロトニン及びノルアドレナリンの再取込み阻害による下行性疼痛抑制系の活性化作用を有しており、これら二つの作用によって鎮痛効果を発揮すると考えられる。
18.2 オピオイド受容体結合に対する作用
オピオイド受容体(μ、δ及びκ)に対する親和性をラットの脳標本を用いて検討した結果、トラマドール塩酸塩はδ及びκ-オピオイド受容体に対しても親和性を有したが、μ-オピオイド受容体に対する親和性が最も高かった。活性代謝物M1のラットμ-オピオイド受容体に対する結合親和性は、トラマドール塩酸塩より高かった。(in vitro)12)
18.3 ノルアドレナリン及びセロトニンの再取込みに対する作用
ラットの脳標本を用いてシナプトソームへのノルアドレナリン及びセロトニンの再取込み阻害活性を検討した結果、トラマドール塩酸塩はノルアドレナリン及びセロトニンの再取込みを阻害した。M1の再取り込み阻害作用はトラマドール塩酸塩と比べて弱かった。(in vitro)12)
18.4 侵害受容性疼痛に対する抑制作用
18.4.1 マウスを用いた酢酸ライジング法
18.4.2 ラットを用いたテイルフリック法
テイルフリック法による侵害刺激実験において、トラマドール塩酸塩及びM1は脊髄クモ膜下腔内投与で鎮痛効果を示したが、M1の鎮痛効果はトラマドール塩酸塩よりも強かった。セロトニン2型受容体拮抗薬リタンセリンはトラマドール塩酸塩の脊髄クモ膜下腔内投与による鎮痛効果に対して拮抗したが、M1の脊髄クモ膜下腔内投与による鎮痛効果には拮抗しなかった。15)
18.5 各種疼痛モデルに対する鎮痛効果
19. 有効成分に関する理化学的知見
19.1. トラマドール塩酸塩
20. 取扱い上の注意
PTPシート又は容器開封後は、高温高湿を避けて保存すること。
22. 包装
ツートラム錠25mg
PTP包装
100錠(10錠×10)
ツートラム錠50mg
PTP包装
100錠(10錠×10)
ツートラム錠100mg
PTP包装
100錠(10錠×10)
ツートラム錠150mg
PTP包装
100錠(10錠×10)
23. 主要文献
- 社内資料:ツートラム錠の第I相単回投与試験
- 社内資料:ツートラム錠の第I相単回投与追加試験並びに反復投与試験
- 社内資料:ツートラム錠の生物学的同等性試験
- 社内資料:ツートラム錠の食事影響試験
- 社内資料:ツートラム錠の薬物動態試験
- Grond S,et al., Clin Pharmacokinet., 43 (13), 879-923, (2004) »PubMed
- 社内資料:変形性膝関節症の高齢患者を対象としたツートラム錠の第II相薬物動態及び最大耐量探索試験
- 社内資料:変形性膝関節症に対するツートラム錠の第III相臨床試験
- 社内資料:帯状疱疹後神経痛に対するツートラム錠の第III相臨床試験
- 社内資料:非がん性慢性疼痛に対するツートラム錠の長期投与試験
- 社内資料:がん疼痛に対するツートラム錠の第III相臨床試験
- 社内資料:in vitroにおける鎮痛作用機序の検討
- 社内資料:酢酸ライジング法を用いた鎮痛作用機序の検討−μオピオイド受容体−
- 社内資料:酢酸ライジング法を用いた鎮痛作用機序の検討−ノルアドレナリンとセロトニン受容体−
- 社内資料:ラットのtail flick試験を用いた鎮痛作用機序の検討−セロトニン受容体−
- 社内資料:ラット変形性関節症モデルにおける薬効薬理試験
- 社内資料:ラットアジュバント関節炎モデルにおける薬効薬理試験
- 社内資料:Chungモデルラットにおける薬効薬理試験
24. 文献請求先及び問い合わせ先
文献請求先
日本臓器製薬株式会社
くすりの相談窓口 受付時間 9:00〜17:00 土・日・祝日を除く
〒541-0046
大阪市中央区平野町4丁目2番3号
電話:フリーダイヤル 0120-630-093
06-6233-6085
06-6233-6085
FAX:06-6233-6087
製品情報問い合わせ先
日本臓器製薬株式会社
くすりの相談窓口 受付時間 9:00〜17:00 土・日・祝日を除く
〒541-0046
大阪市中央区平野町4丁目2番3号
電話:フリーダイヤル 0120-630-093
06-6233-6085
06-6233-6085
FAX:06-6233-6087
26. 製造販売業者等
26.1 製造販売元
日本臓器製薬株式会社
大阪市中央区平野町4丁目2番3号