医薬品情報
| 総称名 | クロモグリク酸Na |
|---|---|
| 一般名 | クロモグリク酸ナトリウム |
| 欧文一般名 | Sodium Cromoglicate |
| 製剤名 | クロモグリク酸ナトリウム点眼液 |
| 薬効分類名 | アレルギー性結膜炎治療剤 |
| 薬効分類番号 | 1319 |
| ATCコード | S01GX01 |
| KEGG DRUG |
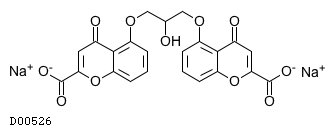
D00526
クロモグリク酸ナトリウム
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年2月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 15.その他の注意 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| クロモグリク酸Na点眼液2%「センジュ」 (後発品) | CROMOGLICATE Na OPHTHALMIC SOLUTION 2% | 千寿製薬 | 1319717Q1421 | 187.8円/瓶 |
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
アレルギー性結膜炎、春季カタル
6. 用法及び用量
1回1〜2滴、1日4回(朝、昼、夕方及び就寝前)点眼
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。動物実験(ウサギ、マウス)で母体に毒性があらわれる大量の注射により胎児毒性(胎児吸収、体重減少等)の報告がある。
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 アナフィラキシー(0.1%未満注))
呼吸困難、血管浮腫、蕁麻疹等があらわれることがある。
注)発現頻度は製造販売後調査を含む
11.2 その他の副作用
| 0.1〜5%未満注) | 0.1%未満注) | |
| 眼 | 点眼時一過性の眼刺激感、結膜充血、眼瞼炎 | 結膜炎 |
14. 適用上の注意
14.1 薬剤交付時の注意
患者に対し以下の点に注意するよう指導すること。
<アレルギー性結膜炎>
・本剤に含まれているベンザルコニウム塩化物はソフトコンタクトレンズに吸着されることがあるので、ソフトコンタクトレンズを装用している場合には、点眼前にレンズを外し、点眼後少なくとも5〜10分間の間隔をあけて再装用すること。
<効能共通>
・薬液汚染防止のため、点眼のとき、容器の先端が直接目に触れないように注意すること。
・患眼を開瞼して結膜嚢内に点眼し、1〜5分間閉瞼して涙嚢部を圧迫させた後、開瞼すること。
・点眼のとき、液が眼瞼皮膚等についた場合には、すぐにふき取ること。
・他の点眼剤を併用する場合には、少なくとも5分以上間隔をあけてから点眼すること。
15. その他の注意
15.1 臨床使用に基づく情報
本剤の保存剤であるベンザルコニウム塩化物による過敏症が知られている。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験
春季カタル及びアレルギー性結膜炎患者135名を対象に、1週間の対照観察期間の後に2%クロモグリク酸ナトリウム点眼液又はプラセボ点眼液を両眼に1回1〜2滴、1日4回、4週間点眼する二重遮蔽比較試験を実施した。試験薬投与2週後及び4週後に対照観察期間と比較した結果、2%クロモグリク酸ナトリウム点眼液群の全般改善度(改善以上)は、2週後40.6%(26/64例)、4週後55.5%(30/54例)であり、プラセボ点眼液群の2週後14.9%(10/67例)、4週後32.8%(22/67例)に比べ有意な改善が認められた(p<0.01;U検定)。疾患別全般改善度(投与4週後)は下表のとおりであり、2%クロモグリク酸ナトリウム点眼液群はプラセボ点眼液群に比べ有意な改善が認められた1)。
| 診断名 | 試験薬 | 改善以上/判定例数 | 全般改善度(%)(改善以上) | U検定 |
| 春季カタル | 2%クロモグリク酸ナトリウム点眼液 | 9/19 | 47.4 | p<0.05 |
| プラセボ点眼液 | 3/20 | 15.0 | ||
| アレルギー性結膜炎 | 2%クロモグリク酸ナトリウム点眼液 | 21/35 | 60.0 | p<0.01 |
| プラセボ点眼液 | 19/47 | 40.4 |
2%クロモグリク酸ナトリウム点眼液の副作用は69例中3例(4.3%)に認められ、しみる2.9%(2例)、痛み1.4%(1例)であった。
18. 薬効薬理
18.1 作用機序
18.2 抗原眼誘発反応に対する防御効果
アレルギー性結膜炎患者における抗原眼誘発反応に対して防御効果を示した4)。
18.3 結膜組織内ヒスタミン濃度の低下作用
アレルギー性結膜炎における結膜組織内ヒスタミン濃度の低下作用を示した5)。
18.4 生物学的同等性試験
ラットの片眼にcompound48/80溶液を点眼し、結膜炎を惹起すると同時にEvans'blue溶液を静脈内投与した。30分後に結膜を含む眼瞼を切り出し、色素を抽出して色素漏出量を測定し、結膜炎の指標とした。本剤あるいはインタール点眼液2%は結膜炎惹起の30、60及び120分前に点眼した。その結果、両製剤間における色素漏出量の平均値の差の90%信頼性区間は−0.481μg〜0.699μgであり、インタール点眼液2%の平均値に対する割合が−10%〜14%と許容範囲を±20%と設定するとき、両剤の生物学的同等性が確認された6)。
| 色素漏出量(μg) | |
| 本剤 | 4.93±0.24 |
| インタール点眼液2% | 5.04±0.25 |
19. 有効成分に関する理化学的知見
19.1. クロモグリク酸ナトリウム
20. 取扱い上の注意
開栓後1ヵ月経過した場合は、残液を使用しないこと。
22. 包装
プラスチック点眼容器 5mL×10
23. 主要文献
- 内田幸男 他, 眼科臨床医報, 75, 725-746, (1981)
- Cox JSG, Disodium Cromoglycate in Allergic Airways Disease.In:Pepys J,Frankland AW,editors., 13-25, (1970), (London:Butterworths)
- Kay AB,et al., J Allergy Clin Immunol, 80, 1-8, (1987) »PubMed
- 三国郁夫, 臨床眼科, 34, 1551-1557, (1980)
- Hennawi MM, The Mast Cell.In:Pepys J,Edwards AM,editors., 486-492, (1979), (London:Pitman Medical)
- 社内資料:生物学的同等性試験
24. 文献請求先及び問い合わせ先
文献請求先
千寿製薬株式会社
カスタマーサポート室 受付時間 9:00〜17:30(土、日、祝日を除く)
〒541-0048
大阪市中央区瓦町三丁目1番9号
電話:0120-069-618
FAX:06-6201-0577
製品情報問い合わせ先
千寿製薬株式会社
カスタマーサポート室 受付時間 9:00〜17:30(土、日、祝日を除く)
〒541-0048
大阪市中央区瓦町三丁目1番9号
電話:0120-069-618
FAX:06-6201-0577
26. 製造販売業者等
26.1 製造販売元
千寿製薬株式会社
大阪市中央区瓦町三丁目1番9号
26.2 販売
武田薬品工業株式会社
大阪市中央区道修町四丁目1番1号