医薬品情報
| 総称名 | スクラルファート |
|---|---|
| 一般名 | スクラルファート水和物 |
| 欧文一般名 | Sucralfate Hydrate |
| 製剤名 | スクラルファート水和物液 |
| 薬効分類名 | 胃炎・消化性潰瘍治療剤 |
| 薬効分類番号 | 2329 |
| ATCコード | A02BX02 |
| KEGG DRUG |
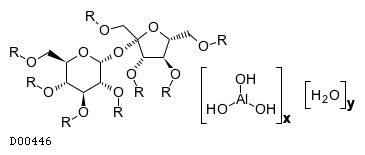
D00446
スクラルファート水和物
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年2月 改訂(第2版)

|
2.禁忌 4.効能または効果 6.用法及び用量 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 15.その他の注意 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| スクラルファート内用液10%「NIG」 (後発品) | Sucralfate Oral Solution | 日医工岐阜工場 | 2329008S1130 | 1.5円/mL |
2. 禁忌
次の患者には投与しないこと
透析療法を受けている患者[9.2.1参照]
4. 効能または効果
6. 用法及び用量
通常、成人1回10mLを1日3回経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 リン酸塩の欠乏している患者
アルミニウムは消化管内でリン酸塩と結合し、その吸収を阻害する。
9.2 腎機能障害患者
9.2.1 透析療法を受けている患者
投与しないこと。長期投与によりアルミニウム脳症、アルミニウム骨症、貧血等があらわれることがある。[2.参照]
9.2.2 腎障害のある患者
長期投与によりアルミニウム脳症、アルミニウム骨症、貧血等があらわれるおそれがあるので、定期的に血中アルミニウム、リン、カルシウム、アルカリフォスファターゼ等の測定を行うこと。
9.5 妊婦
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
用量に注意すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意
| クエン酸製剤 クエン酸カリウム、クエン酸ナトリウム水和物 等 | 血中アルミニウム濃度が上昇することがあるので、同時に服用させないなど注意すること。 | キレートを形成し、アルミニウムの吸収が促進されると考えられる。 |
| 血清カリウム抑制イオン交換樹脂 ポリスチレンスルホン酸カルシウム、ポリスチレンスルホン酸ナトリウム | 血清カリウム抑制イオン交換樹脂の効果が減弱するおそれがある。 | アルミニウムイオンと非選択的に交換すると考えられる。 |
| ニューキノロン系抗菌剤 ノルフロキサシン、塩酸シプロフロキサシン 等 | 同時に服用することにより、これら併用薬剤の吸収を遅延又は阻害するおそれがある。この相互作用は併用薬を本剤の2時間以上前に服用することにより、弱まるとの報告がある。 | アルミニウムイオンと併用薬剤が不溶性のキレートを形成し、消化管からの吸収を遅延又は阻害する。 |
| ジギタリス製剤 ジゴキシン 等 フェニトイン テトラサイクリン系抗生物質 スルピリド 等 | 同時に服用することにより、これら併用薬剤の吸収を遅延又は阻害するおそれがある。この作用は薬剤の服用時間をずらすことにより、弱まるとの報告がある。 | 本剤が併用薬剤を吸着し、消化管からの吸収を遅延又は阻害する。 |
| 甲状腺ホルモン剤 レボチロキシンナトリウム水和物 等 | 同時に服用することにより、これら併用薬剤の吸収を遅延又は阻害することがある。これらの作用は薬剤の服用時間をずらすことにより、弱まると考えられる。 | 消化管内で本剤と吸着することにより、これらの薬剤の吸収が阻害される。 |
| 胆汁酸製剤 ウルソデオキシコール酸、ケノデオキシコール酸 | 同時に服用することにより、これら併用薬剤の吸収を遅延又は阻害することがある。これらの作用は薬剤の服用時間をずらすことにより、弱まると考えられる。 | 消化管内で本剤と吸着することにより、これらの薬剤の吸収が阻害される。 |
| テオフィリン徐放性製剤 | 同時に服用することにより、テオフィリン徐放性製剤のAUCが低下するおそれがある。 | 本剤がテオフィリン徐放性製剤の吸収を阻害するとの報告がある。 |
| キニジン 等 | 制酸剤(乾燥水酸化アルミニウムゲル等)の投与により、併用薬剤の排泄が遅延することが知られている。 | 制酸剤による尿のpH上昇による。 |
11. 副作用
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 消化器 | 便秘、嘔気 | 口渇、悪心等 |
| 皮膚 | 発疹、蕁麻疹等 | |
| 過敏症 | アナフィラキシー反応 |
15. その他の注意
15.1 臨床使用に基づく情報
経管栄養処置を受けている成人患者、低出生体重児及び新生児発育不全において、胃石・食道結石がみられたとの報告があるので、観察を十分に行い、これらが疑われた場合には本剤の投与を中止し、適切な処置を行うこと。
17. 臨床成績
17.1 有効性及び安全性に関する試験
国内のべ58施設、250例で実施した胃潰瘍1)、十二指腸潰瘍2)及び急性胃炎・慢性胃炎の急性増悪期3)の一般臨床試験成績は次の通りである。
| 対象 | 胃潰瘍 | 十二指腸潰瘍 | 急性胃炎・慢性胃炎の急性増悪期 |
| 施設数・総症例数 | 23施設・75例 | 16施設・70例 | 19施設・105例 |
| 自他覚症状改善例数 中等度改善以上(%) | 62/62例 (100) | 60/62例 (96.8) | 86/92例 (93.5) |
| 内視鏡改善例数 治癒a)又は中等度改善以上b)(%) | 50/64例 (78.1)a) | 46/63例 (73.0)a) | 78/92例 (84.8)b) |
| 有効例数 有効以上(%) | 59/64例 (92.2) | 56/63例 (88.9) | 79/93例 (84.9) |
18. 薬効薬理
18.1 作用機序
ラット酢酸胃潰瘍及び十二指腸潰瘍実験において経口投与した14C-スクラルファート水和物は、正常胃粘膜部位に比較して胃及び十二指腸潰瘍部位に選択的に結合し、かつ保護層を形成することによって治癒を促進させた4)。同様に、エタノール及びアスピリン胃炎ラットにおいても14C-スクラルファート水和物の胃炎病巣への選択的結合・付着が確かめられた5)。消化性潰瘍及び胃炎患者に本剤を経口投与した際にも、本剤が潰瘍部位ないし胃炎病巣へ強固に結合していることが確認されており、本剤は炎症部位ないし潰瘍底の白苔中の蛋白成分と強力に結合し、保護層を形成することによって胃液の消化力から病変部を化学的に保護し、治癒を促進するものと考えられる6)7)8)。
18.2 胃液ペプシン活性抑制作用
18.3 制酸作用
18.4 再生粘膜の発育促進及び血管増生
18.5 抗潰瘍及び潰瘍治癒効果
18.6 胃炎モデルへの効果
19. 有効成分に関する理化学的知見
19.1. スクラルファート水和物
22. 包装
10mL分包×210
23. 主要文献
- 松尾 裕,他, Prog.Med., 14 (7), 1977-1983, (1994)
- 松尾 裕,他, Prog.Med., 14 (7), 1984-1990, (1994)
- 松尾 裕,他, Prog.Med., 14 (7), 1991-1998, (1994)
- Nagashima,R.et al., Arzneim.Forsch.,Drug Res., 30 (1 S-I), 84-88, (1980)
- 日野原好和,他, 薬理と治療, 10 (5), 2493-2498, (1982)
- Nakazawa,S.et al., Dig.Dis.Sci., 26 (4), 297-300, (1981) »PubMed
- 石森 章,他, 医学と薬学, 9 (1), 25-31, (1983)
- Sasaki,H.et al., Scand.J.Gastroenterol., 18 (S-83), 13-14, (1983)
- 行方正也,他, 薬学雑誌, 87 (4), 376-380, (1967) »DOI
- 行方正也,他, 薬学雑誌, 87 (7), 778-780, (1967) »DOI
- 行方正也,他, 薬学雑誌, 87 (8), 889-893, (1967) »DOI
- 清水正洋,他, 基礎と臨床, 2 (5), 365-373, (1968)
- 川崎久徳, 日本消化器病学会雑誌, 67 (11), 940-951, (1970) »DOI
- 清水正洋,他, 基礎と臨床, 2 (5), 383-391, (1968)
- 三好秋馬,他, 内科宝函, 15 (12), 419-425, (1968)
- 平野武明,他, 基礎と臨床, 8 (4), 1075-1079, (1974)
- Okabe,S.et al., Dig.Dis.Sci., 28 (11), 1034-1042, (1983) »PubMed
- 松尾 裕,他, 医学のあゆみ, 74 (13), 681-685, (1970)
- 星野英一,他, 薬理と治療, 10 (5), 2479-2486, (1982)
- 岸本真也,他, 内科宝函, 33 (4), 107-113, (1986)
24. 文献請求先及び問い合わせ先
文献請求先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
製品情報問い合わせ先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
26. 製造販売業者等
26.1 製造販売元
日医工岐阜工場株式会社
富山市総曲輪1丁目6番21
26.2 販売元
日医工株式会社
富山市総曲輪1丁目6番21