医薬品情報
| 総称名 | ジエノゲスト |
|---|---|
| 一般名 | ジエノゲスト |
| 欧文一般名 | Dienogest |
| 製剤名 | ジエノゲスト |
| 薬効分類名 | 月経困難症治療剤 |
| 薬効分類番号 | 2499 |
| ATCコード | G03DB08 |
| KEGG DRUG |
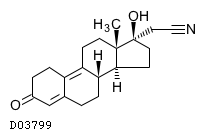
D03799
ジエノゲスト
|
| KEGG DGROUP |
DG02004
プロゲステロン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年10月 改訂(第4版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ジエノゲスト錠0.5mg「モチダ」 (後発品) | Dienogest Tablets 0.5mg MOCHIDA | 持田製薬販売 | 2499010F3034 | 38.7円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
月経困難症
6. 用法及び用量
通常、成人にはジエノゲストとして1日1mgを2回に分け、月経周期2〜5日目より経口投与する。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
8.1 本剤の投与に際しては、器質的疾患を伴う患者では、器質的疾患の類似疾患(悪性腫瘍等)との鑑別に留意し、投与中に腫瘤が増大したり、臨床症状の改善がみられない場合は投与を中止すること。[2.1参照]
8.2 卵巣チョコレート嚢胞は、頻度は低いものの自然経過において悪性化を示唆する報告があるので、定期的に画像診断や腫瘍マーカー等の検査を行い、患者の状態に十分注意すること。
8.3 本剤投与中は経過を十分に観察し、期待する効果が得られない場合には漫然と投与を継続せず、他の適切な治療を考慮すること。
8.4 本剤投与後に不正子宮出血があらわれ、重度の貧血に至ることがある。不正子宮出血の程度には個人差があり、投与中に出血が持続する場合や一度に大量の出血が生じる場合もあるので、以下の点に注意すること。[2.4、11.1.1参照]
・患者にはあらかじめ十分に説明し、出血量が多く持続日数が長い場合や一度に大量の不正子宮出血が認められた場合には、医師へ相談するよう指導すること。
・貧血のある患者では、必要に応じて本剤投与前に貧血の治療を行うこと。
・不正子宮出血が認められた場合には必要に応じて血液検査を実施し、患者の状態を十分に観察すること。異常が認められた場合には鉄剤の投与又は本剤の投与中止、輸血等の適切な処置を行うこと。
・子宮内膜症患者を対象としたディナゲスト錠1mg注)の国内臨床試験において、子宮腺筋症又は子宮筋腫を合併する患者での貧血の発現率は、合併しない患者と比較して高い傾向が認められている。
注)ディナゲスト錠1mgの効能又は効果は、「子宮内膜症」及び「子宮腺筋症に伴う疼痛の改善」である。
8.5 本剤を長期投与する場合には以下の点に注意すること。
・不正子宮出血が持続的に認められている患者は、類似疾患(悪性腫瘍等)に起因する出血との鑑別に留意し、定期的に画像診断等を行うなど、患者の状態に十分注意すること。また、必要に応じ細胞診等の病理学的検査の実施を考慮すること。
・本剤の1年を超える投与における有効性及び安全性は確立していないので、1年を超える投与は治療上必要と判断される場合にのみ行い、定期的に臨床検査(血液検査、骨塩量検査等)等を行うなど、患者の状態に十分注意すること。
8.6 本剤の投与により更年期障害様のうつ症状を起こすことが報告されているので、本剤の使用に際しては患者の状態等を十分に観察すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 子宮筋腫のある患者
不正子宮出血が増悪し、まれに大量出血を起こすおそれがある。
9.1.2 うつ病又はうつ状態の患者並びにそれらの既往歴のある患者
更年期障害様のうつ症状があらわれるおそれがある。
9.1.3 最大骨塩量に達していない患者
9.3 肝機能障害患者
代謝能の低下により、本剤の作用が増強することがある。重度の肝機能障害患者は臨床試験では除外されている。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。動物実験(ラット、ウサギ)において、受胎阻害、胚死亡率の増加及び流産等が認められている。[2.2、7.参照]
9.6 授乳婦
授乳しないことが望ましい。動物実験(ラット)において、乳汁中に移行することが報告されている。
9.7 小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。[9.1.3参照]
10. 相互作用
相互作用序文
本剤は主にCYP3A4で代謝される。[16.4参照]
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| CYP3A4阻害剤 エリスロマイシン クラリスロマイシン アゾール系抗真菌剤 イトラコナゾール フルコナゾール 等 [16.7.1参照] | 本剤の血中濃度が上昇するおそれがある。(本剤とクラリスロマイシンの併用により、本剤のCmax及びAUCはそれぞれ単独投与時の20%及び86%増加した。) | これらの薬剤が本剤の薬物代謝酵素であるCYP3A4を阻害することによると考えられる。 |
| CYP3A4誘導剤 リファンピシン フェニトイン フェノバルビタール カルバマゼピン 等 | 本剤の血中濃度が低下することにより本剤の有効性が減弱するおそれがある。 | これらの薬剤が本剤の薬物代謝酵素であるCYP3A4を誘導することによると考えられる。 |
| 卵胞ホルモン含有製剤 エストラジオール誘導体 エストリオール誘導体 結合型エストロゲン製剤 等 | 本剤の効果が減弱する可能性がある。 | エストロゲン依存性の疾患については、卵胞ホルモン含有製剤の投与により本剤の治療効果が減弱する可能性がある。 |
| 黄体ホルモン含有製剤 プロゲステロン製剤 メドロキシプロゲステロン酢酸エステル製剤 ノルエチステロン製剤 ジドロゲステロン製剤 等 | プロゲステロン作用が増強する可能性がある。 | ともにプロゲステロン受容体に対するアゴニスト活性を示すことから、プロゲステロン作用が相加的に増強する可能性がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 重篤な不正子宮出血(頻度不明)、重度の貧血(頻度不明)
11.1.2 アナフィラキシー(頻度不明)
アナフィラキシー(呼吸困難、血管浮腫、蕁麻疹、そう痒感等)があらわれることがあるので、このような症状があらわれた場合には投与を中止し、適切な処置を行うこと。
11.2 その他の副作用
| 3%以上 | 3%未満 | 頻度不明 | |
| 低エストロゲン症状 | 頭痛 | ほてり、めまい、不眠、動悸 | 不安、抑うつ、発汗 |
| 子宮 | 不正子宮出血(93.8%) | 腹痛 | |
| 乳房 | 乳房緊満感 | 乳房痛 | 乳汁分泌 |
| 皮膚 | 外陰部かぶれ・かゆみ注) | ざ瘡、脱毛 | 皮膚乾燥 |
| 精神神経系 | 傾眠 | いらいら感、しびれ感 | 片頭痛 |
| 過敏症 | 発疹等 | そう痒感 | |
| 肝臓 | AST・ALT・γ-GTP・ビリルビン上昇等の肝機能検査値異常 | ||
| 消化器 | 悪心、腹痛、便秘、胃部不快感、下痢、口内炎 | 腹部膨満感、嘔吐 | |
| 血液 | 貧血、白血球減少 | ||
| 筋骨格系 | 関節痛 | 背部痛、肩こり、骨塩量低下 | |
| その他 | 倦怠感 | 浮腫、耳鳴、体重増加 | 疲労、発熱、血糖値上昇、コレステロール上昇 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人女性にジエノゲスト0.5mg、1mg、2mgを絶食単回経口投与注)したときのジエノゲストの薬物動態パラメータは以下のとおりであり、血漿中濃度は、投与後0.9〜1.3時間で最高血漿中濃度に達した。Cmax及びAUC0-∞は用量に依存して増大し、半減期は6.65〜7.66時間であった2)。
| 投与量 | Cmax(ng/mL) | tmax(hr) | t1/2α(hr) | t1/2β(hr) | AUC0-∞(ng・hr/mL) |
| 0.5mg | 17.5±2.2 | 0.9±0.2 | 0.749±0.201 | 7.06±1.00 | 154.9±34.2 |
| 1mg | 34.7±3.1 | 1.3±0.6 | 0.772±0.364 | 6.65±1.49 | 320.4±56.7 |
| 2mg | 76.1±14.6 | 1.2±0.4 | 0.580±0.209 | 7.66±1.22 | 695.1±114.2 |
16.1.2 反復投与
健康成人女性にジエノゲスト0.5mg、1mg、2mgを1日2回12時間毎に11回(6日間)反復経口投与注)したところ、血漿中濃度は投与回数に従い徐々に上昇し、いずれの用量においても投与回数6回でほぼ定常状態に達した3)4)。ジエノゲスト0.5mgを1日2回反復経口投与したときのジエノゲストの薬物動態パラメータは以下のとおりである3)。
| 投与回数 | Cmax(ng/mL) | tmax(hr) | t1/2β(hr) | AUCa)(ng・hr/mL) |
| 1回目 | 12.4±0.4 | 2.3±1.0 | 8.82±1.48 | 166.5±39.5 |
| 11回目 | 22.3±4.9 | 2.3±0.5 | 9.97±3.21 | 187.4±47.2 |
16.2 吸収
16.2.1 食事の影響
16.2.2 生物学的利用率
健康成人男性20例にジエノゲスト2mgを絶食単回経口投与(錠剤)及び静脈内投与注)したとき、生物学的利用率は90.55%であった5)(外国人データ)。
16.3 分布
16.4 代謝
16.5 排泄
健康成人女性6例にジエノゲスト2mgを絶食単回経口投与注)した場合、尿中に未変化体は検出されず、尿中の代謝物として主に水酸化体及びグルクロン酸抱合体が排泄された2)。
16.7 薬物相互作用
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
月経困難症患者94例(平均32.8歳、21〜47歳)を対象としたランダム化プラセボ対照二重盲検比較試験(ジエノゲスト1mg/日、12週間投与)では、「子宮体部の最大径が10cm以上又は子宮筋層最大厚4cm以上の患者」及び「ヘモグロビン値8.0g/dL未満の患者」を除外し、「ヘモグロビン値8.0g/dL以上11.0g/dL未満の患者」はジエノゲスト投与前に貧血に対する治療を実施し、ヘモグロビン値11.0g/dL以上に改善した症例のみを登録した。
有効性の評価には、疼痛の程度及び鎮痛剤の使用状況を指標とした月経困難症スコア13)を用いた。その結果、「投与12週時の月経困難症スコアのベースラインからの変化量(LOCF)」において、ジエノゲスト1mg/日群のプラセボ群に対する優越性が示された。
副作用発現頻度は、93.6%(44/47例)であった。主な副作用は、不正子宮出血93.6%(44/47例)であった14)。[2.4参照]
有効性の評価には、疼痛の程度及び鎮痛剤の使用状況を指標とした月経困難症スコア13)を用いた。その結果、「投与12週時の月経困難症スコアのベースラインからの変化量(LOCF)」において、ジエノゲスト1mg/日群のプラセボ群に対する優越性が示された。
副作用発現頻度は、93.6%(44/47例)であった。主な副作用は、不正子宮出血93.6%(44/47例)であった14)。[2.4参照]
| 項目 | 程度 | 内容 | スコア |
| 疼痛の程度 | なし | 痛みなし | 0 |
| 軽度 | 仕事(学業・家事)に若干の支障あり | 1 | |
| 中等度 | 横になって休憩したくなるほど仕事(学業・家事)への支障をきたす | 2 | |
| 重度 | 1日以上寝込み、仕事(学業・家事)ができない | 3 | |
| 鎮痛剤の使用状況 | なし | なし | 0 |
| 軽度 | 調査期間中の最も程度の重い疼痛の発現期間中に鎮痛剤を1日使用した | 1 | |
| 中等度 | 調査期間中の最も程度の重い疼痛の発現期間中に鎮痛剤を2日使用した | 2 | |
| 重度 | 調査期間中の最も程度の重い疼痛の発現期間中に鎮痛剤を3日以上使用した | 3 |
| プラセボ群(47例) | ジエノゲスト1mg/日群(47例) | |
| ベースラインa) | 4.6±1.1 | 4.3±1.0 |
| 投与12週時a) | 3.6±1.7 | 1.0±1.5 |
| 変化量a) | −1.0±1.8 | −3.3±1.6 |
| 変化量b,c) | −1.0[−1.4,−0.5] | −3.4[−3.8,−2.9] |
| 変化量のプラセボ群との差b,c) | −2.4[−3.1,−1.8] | |
| p値c) | <0.001 | |
18. 薬効薬理
18.1 作用機序
ジエノゲストはプロゲステロン受容体に対する選択的なアゴニスト作用を示し、卵巣機能抑制及び子宮内膜細胞の増殖抑制により月経困難症に対する有効性を示すと考えられる15)。
18.2 ステロイドホルモン受容体に対する作用
18.2.1 受容体アゴニスト活性
18.2.2 プロゲステロン作用
18.3 卵巣機能抑制作用
18.3.1 健康成人女性
健康成人女性にジエノゲスト1日2mgを2回に分け21日間経口投与注)したとき、通常の月経周期にみられる血清中エストラジオール及びプロゲステロン濃度の上昇の抑制、血清中LH及びFSH濃度の一過性の上昇の消失が認められた26)。
18.3.2 月経困難症患者
月経困難症患者にジエノゲスト1日0.5〜2mg又はプラセボを2回に分け12週間経口投与注)した。1mg/日群における投与3週時の血清中プロゲステロン濃度は、プラセボ群に比し有意に低下し(Wilcoxon 2標本検定、p<0.05)、1日1mg投与時の排卵抑制作用が示唆された27)。
18.4 子宮内膜細胞の増殖抑制作用
ヒト子宮内膜間質細胞を用いたin vitro試験で、細胞増殖の抑制が認められた28)。
注)本剤の承認された用法及び用量は「1日1mgを2回に分け経口投与」である。
19. 有効成分に関する理化学的知見
19.1. ジエノゲスト
20. 取扱い上の注意
PTPシートからの取り出し後は、遮光して保存すること。
22. 包装
PTP
140錠(14錠×10)
23. 主要文献
- Ebert,A.D.et al., J.Pediatr.Adolesc.Gynecol., 30 (5), 560-567, (2017) »PubMed
- 持田製薬販売社内資料:ジエノゲスト(MJR-35)の第I相試験−単回投与試験−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.7.6.3)
- 持田製薬販売社内資料:ジエノゲスト(MJR-35)の第I相試験−反復投与試験−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.7.6.3)
- 持田製薬販売社内資料:ジエノゲスト(MJR-35)の第I相試験−反復投与追加試験−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.7.6.3)
- 持田製薬販売社内資料:ジエノゲストの海外臨床薬物動態試験−健康成人男性における生物学的利用率の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.7.6.1)
- 持田製薬販売社内資料:ジエノゲストの薬物動態試験−ヒト血漿たん白結合(1)−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.4.4)
- 持田製薬販売社内資料:ジエノゲストの薬物動態試験−ヒト血漿たん白結合(2)−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.7.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬物動態試験−代謝に関与するCYP分子種の検討(1)−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.4.5)
- 持田製薬販売社内資料:ジエノゲストの薬物動態試験−代謝に関与するCYP分子種の検討(2)−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.4.5)
- 持田製薬販売社内資料:ジエノゲストの薬物動態試験−CYP分子種に対する阻害作用の検討(1)−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.4.7)
- 持田製薬販売社内資料:ジエノゲストの薬物動態試験−CYP分子種に対する阻害作用の検討(2)−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.4.7)
- 持田製薬販売社内資料:ジエノゲスト(MJR-35)の臨床薬物動態試験−クラリスロマイシン併用の薬物相互作用−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.7.6.4)
- Harada,T.et al., Fertil.Steril., 90 (5), 1583-1588, (2008) »PubMed
- 持田製薬販売社内資料:第III相試験−月経困難症患者における有効性および安全性を検討する試験−(ディナゲスト錠0.5mg:2020年1月23日承認、CTD 2.7.6.2)
- 起原又は発見の経緯(ディナゲスト錠1mg:2016年12月2日承認、CTD 1.5.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ヒトプロゲステロン・アンドロゲンおよびグルココルチコイド受容体に対するアゴニスト活性の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ヒトエストロゲン受容体に対するアゴニスト活性の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ヒトミネラルコルチコイド受容体に対するアゴニスト活性およびアンタゴニスト活性の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ヒトアンドロゲン・グルココルチコイド受容体に対するアンタゴニスト活性の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−エストロゲンを投与したラットの子宮重量増加に及ぼす影響−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−エストロゲンを投与したラットにおける子宮重量増加抑制作用の機序検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ウサギ子宮腺の発達に及ぼす影響(McPhail試験)−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ラットを用いたアンドロゲン作用の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.3)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ラットを用いたグルココルチコイド作用の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.3)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ラットを用いたミネラルコルチコイド作用の検討−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.3)
- 持田製薬販売社内資料:ジエノゲスト(MJR-35)の臨床薬理試験−健康成人女性におけるホルモン動態試験−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.7.6.5)
- 持田製薬販売社内資料:第II相試験−機能性月経困難症患者における有効性および安全性を検討する試験−(ディナゲスト錠0.5mg:2020年1月23日承認、CTD 2.7.6.1)
- 持田製薬販売社内資料:ジエノゲストの薬理試験−ヒト子宮内膜間質細胞の増殖に及ぼす影響−(ディナゲスト錠1mg:2007年10月19日承認、CTD 2.6.2.2)
24. 文献請求先及び問い合わせ先
文献請求先
持田製薬販売株式会社
くすり相談窓口
〒160-8515
東京都新宿区四谷1丁目7番地
電話:0120-189-566
製品情報問い合わせ先
持田製薬販売株式会社
くすり相談窓口
〒160-8515
東京都新宿区四谷1丁目7番地
電話:0120-189-566
26. 製造販売業者等
26.1 製造販売元
持田製薬販売株式会社
東京都新宿区四谷1丁目7番地
26.2 販売提携
持田製薬株式会社
東京都新宿区四谷1丁目7番地