医薬品情報
| 総称名 | テラムロ |
|---|---|
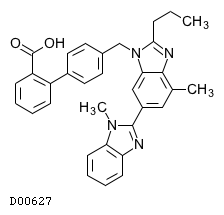
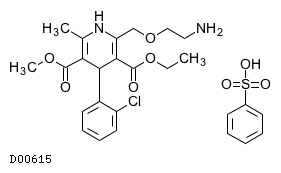
| 一般名 | テルミサルタン アムロジピンベシル酸塩 |
| 欧文一般名 | Telmisartan Amlodipine Besilate |
| 薬効分類名 | 胆汁排泄型持続性AT1受容体ブロッカー/持続性Ca拮抗薬合剤 |
| 薬効分類番号 | 2149 |
| ATCコード | C09DB04 |
| KEGG DRUG |
D09743
テルミサルタン・アムロジピンベシル酸塩
|
| KEGG DGROUP |
DG03231
血圧降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年2月 改訂(第4版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| テラムロ配合錠AP「NIG」 (後発品) | TERAMURO Combination Tablets | 日医工岐阜工場 | 2149117F1114 | 19.5円/錠 | 劇薬, 処方箋医薬品注) |
| テラムロ配合錠BP「NIG」 (後発品) | TERAMURO Combination Tablets | 日医工岐阜工場 | 2149117F2110 | 28.3円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
5. 効能または効果に関連する注意
5.1 過度な血圧低下のおそれ等があり、本剤を高血圧治療の第一選択薬としないこと。
5.2 原則として、テルミサルタン40mg及びアムロジピン5mgを併用している場合、あるいはいずれか一方を使用し血圧コントロールが不十分な場合に、テルミサルタン/アムロジピン40mg/5mgへの切り替えを検討すること。
5.3 原則として、テルミサルタン80mg及びアムロジピン5mgを併用している場合、あるいは以下のいずれかを使用し血圧コントロールが不十分な場合に、テルミサルタン/アムロジピン80mg/5mgへの切り替えを検討すること。
・テルミサルタン80mg
・テルミサルタン40mg及びアムロジピン5mgの併用
・テルミサルタン/アムロジピン40mg/5mg配合錠
6. 用法及び用量
テラムロ配合錠AP「NIG」
成人には1日1回1錠(テルミサルタン/アムロジピンとして40mg/5mg)を経口投与する。本剤は高血圧治療の第一選択薬として用いない。
テラムロ配合錠BP「NIG」
成人には1日1回1錠(テルミサルタン/アムロジピンとして80mg/5mg)を経口投与する。本剤は高血圧治療の第一選択薬として用いない。
7. 用法及び用量に関連する注意
7.1 以下のテルミサルタンとアムロジピンベシル酸塩の用法・用量を踏まえ、患者毎に本剤の適応を考慮すること。
<テルミサルタン>
通常、成人にはテルミサルタンとして40mgを1日1回経口投与する。ただし、1日20mgから投与を開始し漸次増量する。なお、年齢・症状により適宜増減するが、1日最大投与量は80mgまでとする。
<アムロジピンベシル酸塩>
高血圧症治療では、通常、成人にはアムロジピンとして2.5〜5mgを1日1回経口投与する。なお、症状に応じ適宜増減するが、効果不十分な場合には1日1回10mgまで増量することができる。
7.2 肝障害のある患者に投与する場合、テルミサルタン/アムロジピンとして40mg/5mgを超えて投与しないこと。[9.3.2参照]
8. 重要な基本的注意
8.1 本剤は、テルミサルタン40mg又は80mgとアムロジピン5mgとの配合剤であり、テルミサルタンとアムロジピン双方の副作用が発現するおそれがあるため、適切に本剤の使用を検討すること。
8.2 降圧作用に基づく失神、めまい、ふらつきがあらわれることがあるので、高所作業、自動車の運転等危険を伴う機械を操作する際には注意させること。
8.3 手術前24時間は投与しないことが望ましい。アンジオテンシンII受容体拮抗剤投与中の患者は、麻酔及び手術中にレニン-アンジオテンシン系の抑制作用による高度な血圧低下を起こす可能性がある。
8.4 本剤の成分であるテルミサルタンを含むアンジオテンシンII受容体拮抗剤投与中に肝炎等の重篤な肝障害があらわれたとの報告があるので、肝機能検査を実施するなど、観察を十分に行うこと。[11.1.5参照]
8.5 本剤の成分であるアムロジピンは血中濃度半減期が長く投与中止後も緩徐な降圧効果が認められるので、本剤投与中止後に他の降圧剤を使用するときは、用量並びに投与間隔に留意するなど慎重に投与すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 両側性腎動脈狭窄のある患者又は片腎で腎動脈狭窄のある患者
治療上やむを得ないと判断される場合を除き、使用は避けること。腎血流量の減少や糸球体ろ過圧の低下により急速に腎機能を悪化させるおそれがある。
9.1.2 高カリウム血症の患者
治療上やむを得ないと判断される場合を除き、使用は避けること。高カリウム血症を増悪させるおそれがある。
また、腎機能障害、コントロール不良の糖尿病等により血清カリウム値が高くなりやすい患者では、血清カリウム値に注意すること。
また、腎機能障害、コントロール不良の糖尿病等により血清カリウム値が高くなりやすい患者では、血清カリウム値に注意すること。
9.1.3 脳血管障害のある患者
過度の降圧が脳血流不全を引き起こし、病態を悪化させるおそれがある。
9.1.4 厳重な減塩療法中の患者
低用量から投与を開始し、増量する場合は徐々に行うこと。急激な血圧低下を起こすおそれがある。[11.1.4参照]
9.2 腎機能障害患者
9.2.1 重篤な腎障害(血清クレアチニン値3.0mg/dL以上の場合)のある患者
腎機能を悪化させるおそれがある。
9.2.2 血液透析中の患者
9.3 肝機能障害患者
9.3.1 胆汁の分泌が極めて悪い患者又は重篤な肝障害のある患者
9.3.2 肝機能障害患者
9.4 生殖能を有する者
9.4.1 妊娠する可能性のある女性
妊娠していることが把握されずアンジオテンシン変換酵素阻害剤又はアンジオテンシンII受容体拮抗剤を使用し、胎児・新生児への影響(腎不全、頭蓋・肺・腎の形成不全、死亡等)が認められた例が報告されている1)2)。
本剤の投与に先立ち、代替薬の有無等も考慮して本剤投与の必要性を慎重に検討し、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。また、投与が必要な場合には次の注意事項に留意すること。[9.5参照]
本剤の投与に先立ち、代替薬の有無等も考慮して本剤投与の必要性を慎重に検討し、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。また、投与が必要な場合には次の注意事項に留意すること。[9.5参照]
(1)本剤投与開始前に妊娠していないことを確認すること。本剤投与中も、妊娠していないことを定期的に確認すること。投与中に妊娠が判明した場合には、直ちに投与を中止すること。
(2)次の事項について、本剤投与開始時に患者に説明すること。また、投与中も必要に応じ説明すること。
・妊娠中に本剤を使用した場合、胎児・新生児に影響を及ぼすリスクがあること。
・妊娠が判明した又は疑われる場合は、速やかに担当医に相談すること。
・妊娠を計画する場合は、担当医に相談すること。
9.5 妊婦
9.6 授乳婦
授乳しないことが望ましい。テルミサルタンの動物実験(ラット)で、乳汁中へ移行することが報告されている。また、テルミサルタンの動物実験(ラット出生前、出生後の発生及び母動物の機能に関する試験)の15mg/kg/日以上の投与群で出生児の4日生存率の低下、50mg/kg/日投与群で出生児の低体重及び身体発達の遅延が報告されている。
アムロジピンはヒト母乳中へ移行することが報告されている3)。
アムロジピンはヒト母乳中へ移行することが報告されている3)。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に過度の降圧は好ましくないとされている。脳梗塞等が起こるおそれがある。
10. 相互作用
相互作用序文
テルミサルタンは、主としてUGT酵素(UDP-グルクロノシルトランスフェラーゼ)によるグルクロン酸抱合によって代謝される。[16.4参照]
アムロジピンの代謝には主として薬物代謝酵素CYP3A4が関与していると考えられている。
アムロジピンの代謝には主として薬物代謝酵素CYP3A4が関与していると考えられている。
薬物代謝酵素用語
UGT酵素(UDP-グルクロノシルトランスフェラーゼ)
薬物代謝酵素用語
CYP3A4
10.1 併用禁忌
| アリスキレンフマル酸塩 ラジレス (糖尿病患者に使用する場合。ただし、他の降圧治療を行ってもなお血圧のコントロールが著しく不良の患者を除く。)[2.4参照] | 非致死性脳卒中、腎機能障害、高カリウム血症及び低血圧のリスク増加が報告されている。 | テルミサルタン:レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
10.2 併用注意
| ジゴキシン | テルミサルタンとの併用により、血中ジゴキシン濃度が上昇したとの報告がある4)。 | テルミサルタン:機序不明 |
| カリウム保持性利尿剤 スピロノラクトン トリアムテレン等 カリウム補給剤 | 血清カリウム濃度が上昇するおそれがある。 | テルミサルタン:カリウム貯留作用が増強するおそれがある。 危険因子:特に腎機能障害のある患者 |
| リチウム製剤 炭酸リチウム | アンジオテンシン変換酵素阻害剤との併用により、リチウム中毒を起こすことが報告されている。 | テルミサルタン:明確な機序は不明であるが、ナトリウムイオン不足はリチウムイオンの貯留を促進するといわれているため、テルミサルタンがナトリウム排泄を促進することにより起こると考えられる。 |
| 利尿降圧剤 フロセミド、トリクロルメチアジド等 [11.1.4参照] | 急激な血圧低下を起こすおそれがあるので、低用量から投与を開始し、増量する場合は徐々に行うこと。 | テルミサルタン:利尿降圧剤で治療を受けている患者にはレニン活性が亢進している患者が多く、本剤が奏効しやすい。 |
| 非ステロイド性抗炎症薬(NSAIDs) | 糸球体ろ過量がより減少し、腎障害のある患者では急性腎障害を引き起こす可能性がある。 | テルミサルタン:プロスタグランジン合成阻害作用により、腎血流量が低下するためと考えられる。 |
| 非ステロイド性抗炎症薬(NSAIDs) | 降圧薬の効果を減弱させることが報告されている。 | テルミサルタン:血管拡張作用を有するプロスタグランジンの合成が阻害されるため、降圧薬の血圧低下作用を減弱させると考えられている。 |
| アンジオテンシン変換酵素阻害剤 | 急性腎障害を含む腎機能障害、高カリウム血症及び低血圧を起こすおそれがある5)。 | テルミサルタン:レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
| アリスキレンフマル酸塩 | 腎機能障害、高カリウム血症及び低血圧を起こすおそれがある。なお、eGFRが60mL/min/1.73m2未満の腎機能障害のある患者へのアリスキレンフマル酸塩との併用については、治療上やむを得ないと判断される場合を除き避けること。 | テルミサルタン:レニン-アンジオテンシン系阻害作用が増強される可能性がある。 |
| 降圧作用を有する薬剤 | 降圧作用が増強されるおそれがある。 | アムロジピン:相互に作用を増強するおそれがある。 |
| CYP3A4阻害剤 エリスロマイシン ジルチアゼム リトナビル イトラコナゾール等 | エリスロマイシン及びジルチアゼムとの併用により、アムロジピンの血中濃度が上昇したとの報告がある。 | アムロジピンの代謝が競合的に阻害される可能性が考えられる。 |
| CYP3A4誘導剤 リファンピシン等 | アムロジピンの血中濃度が低下するおそれがある。 | アムロジピンの代謝が促進される可能性が考えられる。 |
| グレープフルーツジュース | アムロジピンの降圧作用が増強されるおそれがある。 | グレープフルーツに含まれる成分がアムロジピンの代謝を阻害し、アムロジピンの血中濃度が上昇する可能性が考えられる。 |
| シンバスタチン | アムロジピンベシル酸塩とシンバスタチン80mg(国内未承認の高用量)との併用により、シンバスタチンのAUCが77%上昇したとの報告がある。 | 機序は不明である。 |
| タクロリムス | アムロジピンベシル酸塩との併用によりタクロリムスの血中濃度が上昇し、腎障害等のタクロリムスの副作用が発現するおそれがある。併用時にはタクロリムスの血中濃度をモニターし、必要に応じてタクロリムスの用量を調整すること。 | アムロジピンとタクロリムスは、主としてCYP3A4により代謝されるため、併用によりタクロリムスの代謝が阻害される可能性が考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 血管性浮腫(頻度不明)
顔面、口唇、咽頭・喉頭、舌等の腫脹を症状とする血管性浮腫があらわれ、喉頭浮腫等により呼吸困難を来した症例も報告されている。また、腹痛、嘔気、嘔吐、下痢等を伴う腸管血管性浮腫があらわれることがある。
11.1.2 高カリウム血症(頻度不明)
11.1.3 腎機能障害(頻度不明)
急性腎障害を呈した例が報告されている。
11.1.4 ショック、失神、意識消失(いずれも頻度不明)
11.1.5 劇症肝炎、肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、Al-P、LDH、γ-GTPの上昇等を伴う肝機能障害があらわれることがある。[8.4参照]
11.1.6 低血糖(頻度不明)
脱力感、空腹感、冷汗、手の震え、集中力低下、痙攣、意識障害等があらわれた場合には投与を中止し、適切な処置を行うこと。糖尿病治療中の患者であらわれやすい。
11.1.7 アナフィラキシー(頻度不明)
呼吸困難、血圧低下、喉頭浮腫等が症状としてあらわれることがある。
11.1.8 間質性肺炎(頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常等を伴う間質性肺炎があらわれることがあるので、このような場合には投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.9 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇を特徴とする横紋筋融解症があらわれることがあるので、このような場合には直ちに投与を中止し、適切な処置を行うこと。また、横紋筋融解症による急性腎障害の発症に注意すること。
11.1.10 無顆粒球症、白血球減少、血小板減少(いずれも頻度不明)
11.1.11 房室ブロック(頻度不明)
徐脈、めまい等の初期症状があらわれることがある。
11.2 その他の副作用
| 0.5〜5%未満 | 0.5%未満 | 頻度不明 | |
| 過敏症 | 湿疹、発疹 | そう痒、じん麻疹、紅斑、多形紅斑、光線過敏症、血管炎 | |
| 精神神経系 | 浮動性めまい | 体位性めまい、頭痛 | 片頭痛、眠気、不眠、頭のぼんやり感、頭重、不安感、抑うつ状態、気分動揺、振戦、末梢神経障害、錐体外路症状 |
| 血液 | 貧血、好酸球上昇 | 白血球増加、赤血球減少、ヘモグロビン減少、紫斑 | |
| 循環器 | 低血圧 | 心悸亢進、動悸、上室性頻脈、上室性期外収縮、期外収縮、心房細動、徐脈、洞房ブロック、洞停止、ほてり、ふらつき、起立性低血圧、頻脈 | |
| 消化器 | 口渇、口内炎、逆流性食道炎、腹部膨満、心窩部不快感、腹痛 | (連用により)歯肉肥厚、食欲不振、消化不良、心窩部痛、嘔気、嘔吐、胃炎、胃腸炎、鼓腸、排便回数増加、軟便、下痢、便秘、膵炎 | |
| 肝臓 | AST、ALT、Al-P、LDH、γ-GTP上昇等の肝機能異常 | 腹水 | |
| 呼吸器 | 喘息、咳 | 鼻出血、喀痰増加、咽頭炎、呼吸困難 | |
| 泌尿・生殖器 | 血清クレアチニン上昇、BUN上昇、血中尿酸値上昇、尿管結石、排尿障害、尿潜血陽性、尿中蛋白陽性、勃起障害、頻尿、女性化乳房 | ||
| 代謝異常 | 血清コレステロール上昇、糖尿病、高血糖、尿中ブドウ糖陽性 | ||
| 骨格筋 | 背部痛 | 関節痛、筋肉痛、下肢痛、腱炎、筋痙攣、下肢痙攣、筋緊張亢進 | |
| 電解質 | 血清カリウム上昇 | 血清カリウム減少、低ナトリウム血症 | |
| 一般的全身障害 | 疲労 | 倦怠感、脱力感、発熱、胸痛、疼痛、しびれ、体重増加、体重減少、浮腫 | |
| その他 | 耳鳴、眼痛、CK上昇 | 結膜炎、目のチカチカ感、羞明、視覚異常、視力異常、鼻炎、上気道感染、インフルエンザ様症状、尿路感染、膀胱炎、敗血症、多汗、脱毛、皮膚変色、味覚異常、異常感覚、CRP陽性 |
13. 過量投与
13.1 症状
テルミサルタンの過量服用(640mg)により、低血圧及び頻脈があらわれたとの報告がある。
アムロジピンでは、過度の末梢血管拡張により、ショックを含む著しい血圧低下と反射性頻脈を起こすことがある。
アムロジピンでは、過度の末梢血管拡張により、ショックを含む著しい血圧低下と反射性頻脈を起こすことがある。
13.2 処置
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.2 本剤を食後に服用している患者には、毎日食後に服用するよう注意を与えること。本剤の成分であるテルミサルタンの薬物動態は食事の影響を受け、空腹時投与した場合は、食後投与よりもテルミサルタンの血中濃度が高くなることが報告されており、副作用が発現するおそれがある。[16.2.1参照]
15. その他の注意
15.1 臨床使用に基づく情報
因果関係は明らかでないが、アムロジピンベシル酸塩による治療中に心筋梗塞や不整脈(心室性頻拍を含む)がみられたとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 反復投与
健康成人男子24例にテルミサルタン40mg錠とアムロジピン5mg錠、又はテルミサルタン80mg(テルミサルタン40mg錠×2錠)とアムロジピン5mg錠を1日1回10日間空腹時反復併用投与したときのテルミサルタン及びアムロジピンの血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。テルミサルタンの血漿中濃度は、両投与群ともに単回投与後に比べてやや高く、累積係数は1.3〜1.9であった。また、テルミサルタンのtmax及び半減期は、両投与群ともに初回投与後と反復投与後とで類似していた。テルミサルタンのCmaxは用量比以上に上昇した。一方、アムロジピンの血漿中濃度推移は、両投与群ともに初回投与後に比べて高く、累積係数は2.9〜3.5であった。また、アムロジピンのtmax及び半減期は、両投与群ともに単回投与後と反復投与後とで類似していた7)。
| 反復投与 | テルミサルタン | アムロジピン | |||
| 投与量 | T40mg+A5mg | T80mg+A5mg | T40mg+A5mg | T80mg+A5mg | |
| 1日目 | 例数 | 12 | 12 | 12 | 12 |
| Cmax(ng/mL) | 62.3(56.1) | 334(83.5) | 2.89(22.6) | 3.29(27.1) | |
| AUCτ(ng・hr/mL) | 460(44.0) | 1090(72.3) | 48.5(22.5) | 55.6(31.0) | |
| t1/2(hr) | 20.1(43.0) | 18.4(28.9) | 40.8(14.1) | 41.1(20.2) | |
| tmax(hr)a) | 1.50 (0.750-3.00) | 0.875 (0.500-1.00) | 4.00 (3.00-8.00) | 5.00 (3.00-8.00) | |
| 10日目 | 例数 | 12 | 11 | 12 | 11 |
| Cmax,ss(ng/mL) | 116(51.2) | 398(95.1) | 8.98(26.6) | 9.69(35.6) | |
| AUCτ,ss(ng・hr/mL) | 766(45.1) | 1370(72.1) | 168(26.9) | 190(35.5) | |
| t1/2,ss(hr) | 19.0(32.5) | 18.8(28.2) | 40.5(12.4) | 40.7(16.2) | |
| tmax,ss(hr)a) | 1.50 (0.500-3.00) | 0.750 (0.500-2.00) | 6.00 (3.00-8.00) | 6.00 (3.00-8.00) | |
16.1.2 テルミサルタンとアムロジピンの相互作用
健康成人男子12例にテルミサルタン120mg注1)とアムロジピン10mg注1)を併用投与したときとアムロジピン10mgを単独投与したときとの1日1回9日間反復投与後の薬物動態を比較した結果、アムロジピンの血漿中濃度推移は単独投与時と併用投与時とで類似しており、テルミサルタン併用投与によるアムロジピンの体内動態への影響は認められなかった8)(外国人データ)。
健康成人男女36名にテルミサルタン80mgとアムロジピン10mg注1)を併用投与したときとテルミサルタン80mgを単独投与したときとの1日1回9日間反復投与後の薬物動態を比較した結果、テルミサルタンの血漿中濃度推移は単独投与時と併用投与時とで類似しており、アムロジピン併用投与によるテルミサルタンの体内動態への影響は認められなかった9)(外国人データ)。
健康成人男女36名にテルミサルタン80mgとアムロジピン10mg注1)を併用投与したときとテルミサルタン80mgを単独投与したときとの1日1回9日間反復投与後の薬物動態を比較した結果、テルミサルタンの血漿中濃度推移は単独投与時と併用投与時とで類似しており、アムロジピン併用投与によるテルミサルタンの体内動態への影響は認められなかった9)(外国人データ)。
注1)本剤の承認用量はテルミサルタン/アムロジピンとして40mg/5mg又は80mg/5mgである。
16.1.3 生物学的同等性試験
<テラムロ配合錠AP「NIG」>
(1)テラムロ配合錠AP「NIG」とミカムロ配合錠APを、クロスオーバー法によりそれぞれ1錠[テルミサルタンとして40mg、アムロジピンベシル酸塩として6.93mg(アムロジピンとして5mg)]健康成人男子に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された10)。
・テルミサルタン
| 投与量 (mg) | AUC0-72 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
| テラムロ配合錠AP「NIG」 | 40 | 1115.54 ±449.20 | 120.91 ±59.22 | 2.09 ±1.12 | 22.90 ±9.27 |
| ミカムロ配合錠AP | 40 | 1032.44 ±359.51 | 105.92 ±45.44 | 2.20 ±1.21 | 25.85 ±19.76 |
・アムロジピン
| 投与量 (mg) | AUC0-120 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
| テラムロ配合錠AP「NIG」 | 5 | 141.3506 ±39.8673 | 3.4358 ±0.8782 | 6.66 ±1.45 | 39.93 ±8.29 |
| ミカムロ配合錠AP | 5 | 143.0350 ±36.3046 | 3.4921 ±0.9086 | 6.66 ±1.72 | 39.66 ±9.87 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
<テラムロ配合錠BP「NIG」>
(2)テラムロ配合錠BP「NIG」とミカムロ配合錠BPを、クロスオーバー法によりそれぞれ1錠[テルミサルタンとして80mg、アムロジピンベシル酸塩として6.93mg(アムロジピンとして5mg)]健康成人男子に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された10)。
・テルミサルタン
| 投与量 (mg) | AUC0-72 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
| テラムロ配合錠BP「NIG」 | 80 | 2927.42 ±1472.40 | 657.27 ±367.37 | 1.16 ±0.69 | 20.61 ±8.56 |
| ミカムロ配合錠BP | 80 | 2867.83 ±1458.64 | 719.74 ±465.64 | 1.12 ±0.46 | 21.41 ±11.71 |
・アムロジピン
| 投与量 (mg) | AUC0-120 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | |
| テラムロ配合錠BP「NIG」 | 5 | 126.9088 ±30.2255 | 3.0300 ±0.5395 | 6.53 ±1.37 | 38.95 ±7.27 |
| ミカムロ配合錠BP | 5 | 130.9679 ±34.0026 | 3.0528 ±0.7243 | 6.31 ±1.15 | 37.01 ±6.05 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.2.1 食事の影響
16.3 分布
16.4 代謝
16.5 排泄
テルミサルタンとして、以下の報告がある。
健康成人男子にテルミサルタン20、40、80mgを空腹時に単回経口投与(各群6例)したとき、未変化体はほとんど尿中に排出されず、投与後24時間までの平均累積尿中排泄率は、いずれの投与量においても0.02%以下であった15)。
健康成人男子5例に14C-テルミサルタン40mgを空腹時に単回経口投与したとき、投与後144時間までの放射能の尿中及び糞中総排泄率はそれぞれ約0.5%及び102%であり、吸収されたテルミサルタンの大部分が胆汁を介して糞中に排泄された16)(外国人データ)。
健康成人男子にテルミサルタン20、40、80mgを空腹時に単回経口投与(各群6例)したとき、未変化体はほとんど尿中に排出されず、投与後24時間までの平均累積尿中排泄率は、いずれの投与量においても0.02%以下であった15)。
健康成人男子5例に14C-テルミサルタン40mgを空腹時に単回経口投与したとき、投与後144時間までの放射能の尿中及び糞中総排泄率はそれぞれ約0.5%及び102%であり、吸収されたテルミサルタンの大部分が胆汁を介して糞中に排泄された16)(外国人データ)。
アムロジピンベシル酸塩として、以下の報告がある。
健康成人6例にアムロジピンとして2.5mg注2)又は5mgを単回経口投与した場合、尿中に未変化体として排泄される割合は小さく、いずれの投与量においても尿中未変化体排泄率は投与後24時間までに投与量の約3%、144時間までに約8%であった。また2.5mg注2)を1日1回14日間連続投与した場合の尿中排泄率は投与開始6日目でほぼ定常状態に達し、6日目以降の1日当たりの未変化体の尿中排泄率は6.3〜7.4%であった17)。
健康成人2例に14C-標識アムロジピン15mg注2)を単回経口投与した場合、投与12日目までに投与放射能の59.3%は尿中、23.4%は糞中に排泄され、投与後72時間までの尿中放射能の9%は未変化体であった。その他に9種の代謝物が認められた14)(外国人データ)。
なお、これら代謝物にはアムロジピンをしのぐ薬理作用は認められていない。
健康成人6例にアムロジピンとして2.5mg注2)又は5mgを単回経口投与した場合、尿中に未変化体として排泄される割合は小さく、いずれの投与量においても尿中未変化体排泄率は投与後24時間までに投与量の約3%、144時間までに約8%であった。また2.5mg注2)を1日1回14日間連続投与した場合の尿中排泄率は投与開始6日目でほぼ定常状態に達し、6日目以降の1日当たりの未変化体の尿中排泄率は6.3〜7.4%であった17)。
健康成人2例に14C-標識アムロジピン15mg注2)を単回経口投与した場合、投与12日目までに投与放射能の59.3%は尿中、23.4%は糞中に排泄され、投与後72時間までの尿中放射能の9%は未変化体であった。その他に9種の代謝物が認められた14)(外国人データ)。
なお、これら代謝物にはアムロジピンをしのぐ薬理作用は認められていない。
注2)本剤の承認用量はテルミサルタン/アムロジピンとして40mg/5mg又は80mg/5mgである。
16.6 特定の背景を有する患者
16.6.1 肝機能障害患者
テルミサルタンとして、以下の報告がある。
肝障害患者12例(Child-Pugh分類A(軽症):8例、B(中等症):4例)にテルミサルタン20mg及び120mg注3)を経口投与したとき、健康成人に比較しCmaxは4.5倍及び3倍高く、AUCは2.5倍及び2.7倍高かった18)(外国人データ)。[9.3.2参照]
肝障害患者12例(Child-Pugh分類A(軽症):8例、B(中等症):4例)にテルミサルタン20mg及び120mg注3)を経口投与したとき、健康成人に比較しCmaxは4.5倍及び3倍高く、AUCは2.5倍及び2.7倍高かった18)(外国人データ)。[9.3.2参照]
注3)肝障害のある患者に投与する場合の最大投与量は1日40mgである。
アムロジピンベシル酸塩として、以下の報告がある。
成人肝硬変患者(Child分類A,B)5例にアムロジピンとして2.5mgを単回投与した場合、健康成人に比し、投与72時間後の血中濃度が有意に上昇し、t1/2、AUCはやや高値を示したが有意差は認められなかった19)。
成人肝硬変患者(Child分類A,B)5例にアムロジピンとして2.5mgを単回投与した場合、健康成人に比し、投与72時間後の血中濃度が有意に上昇し、t1/2、AUCはやや高値を示したが有意差は認められなかった19)。
16.6.2 高齢者
アムロジピンベシル酸塩として、以下の報告がある。
老年高血圧患者6例(男2例、女4例、平均年齢79.7歳)にアムロジピンとして5mgを単回、及び8日間反復投与した場合、単回投与時に若年健康者(男6例、平均年齢22.3歳)に比べ、Cmax及びAUCは有意に高値を示したが、t1/2に有意差は認められなかった。反復投与時には老年者の血漿中アムロジピン濃度は若年者よりも高く推移したが、そのパターンは若年者に類似しており、老年者でその蓄積が増大する傾向は認められなかった20)。
老年高血圧患者6例(男2例、女4例、平均年齢79.7歳)にアムロジピンとして5mgを単回、及び8日間反復投与した場合、単回投与時に若年健康者(男6例、平均年齢22.3歳)に比べ、Cmax及びAUCは有意に高値を示したが、t1/2に有意差は認められなかった。反復投与時には老年者の血漿中アムロジピン濃度は若年者よりも高く推移したが、そのパターンは若年者に類似しており、老年者でその蓄積が増大する傾向は認められなかった20)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
アムロジピン5mg(A5mg)単剤で降圧効果不十分な本態性高血圧患者531例を対象とした無作為化二重盲検比較試験において、テルミサルタン/アムロジピン40mg/5mg(T40/A5mg)配合剤又はA5mgを1日1回、8週間経口投与した結果、T40/A5mg配合剤は、A5mg単剤継続投与に比べてトラフ時座位拡張期血圧下降度及び収縮期血圧下降度で有意な降圧効果を示した。結果は次表のとおりであった21)22)。
| 試験 | 投与群 | 拡張期血圧(mmHg) | 収縮期血圧(mmHg) | ||||
| 投与前値 平均値 (SD) | 下降度a) | 投与前値 平均値 (SD) | 下降度a) | ||||
| 調整 平均値 (SE) | 群間差b): 調整平均値 (SE) [両側95%CI] | 調整 平均値 (SE) | 群間差b): 調整平均値 (SE) [両側95%CI] | ||||
| A5で降圧効果不十分な患者を対象とした試験 | T40/A5 (263例) | 95.95 (5.02) | 9.56 (0.61) | 5.11 (0.57)b) [3.98,6.23] | 144.64 (11.75) | 13.04 (0.88) | 7.27 (0.85)b) [5.60,8.95] |
| A5 (257例) | 95.64 (4.88) | 4.45 (0.61) | 145.31 (10.36) | 5.77 (0.88) | |||
副作用発現割合はT40/A5mg配合剤で3.7%(10/269例)、A5mg単剤で1.9%(5/262例)であった。T40/A5mg配合剤投与群の主な副作用は浮動性めまい1.1%(3/269例)であった。
17.1.2 国内第III相試験
テルミサルタン40mg(T40mg)単剤で降圧効果不十分な本態性高血圧患者314例を対象とした無作為化二重盲検比較試験において、T40/A5mg配合剤又はT40mgを1日1回、8週間経口投与した結果、T40/A5mg配合剤はT40mg単剤継続投与に比べてトラフ時座位拡張期血圧下降度及び収縮期血圧下降度で有意な降圧効果を示した。結果は次表のとおりであった21)23)。
| 試験 | 投与群 | 拡張期血圧(mmHg) | 収縮期血圧(mmHg) | ||||
| 投与前値 平均値 (SD) | 下降度a) | 投与前値 平均値 (SD) | 下降度a) | ||||
| 調整 平均値 (SE) | 群間差b): 調整平均値 (SE) [両側95%CI] | 調整 平均値 (SE) | 群間差b): 調整平均値 (SE) [両側95%CI] | ||||
| T40で降圧効果不十分な患者を対象とした試験 | T40/A5 (153例) | 96.76 (5.30) | 13.49 (0.63) | 8.02 (0.82)b) [6.41,9.63] | 145.66 (12.18) | 17.86 (0.86) | 11.35 (1.12)b) [9.16,13.54] |
| T40 (158例) | 96.57 (6.05) | 5.47 (0.62) | 144.77 (13.38) | 6.51 (0.84) | |||
副作用発現割合はT40/A5mg配合剤で3.8%(6/156例)、T40mg単剤で1.3%(2/158例)であった。T40/A5mg配合剤投与群の副作用は、貧血、喘息、上腹部痛、発疹、血中カリウム増加、好酸球数増加でいずれも0.6%(1/156例)であった。
17.1.3 国内第III相試験
テルミサルタン80mg(T80mg)単剤で降圧効果不十分な本態性高血圧患者174例を対象とした無作為化二重盲検比較試験において、テルミサルタン/アムロジピン80mg/5mg(T80/A5mg)配合剤又はT80mgを1日1回、8週間経口投与した結果、T80/A5mg配合剤はT80mg単剤継続投与に比べてトラフ時座位拡張期血圧下降度及び収縮期血圧下降度で有意な降圧効果を示した。結果は次表のとおりであった24)。
| 試験 | 投与群 | 拡張期血圧(mmHg) | 収縮期血圧(mmHg) | ||||
| 投与前値 平均値 (SD) | 下降度a) | 投与前値 平均値 (SD) | 下降度a) | ||||
| 調整 平均値 | 群間差: 調整平均値 [両側95%CI] | 調整 平均値 | 群間差: 調整平均値 [両側95%CI] | ||||
| T80で降圧効果不十分な患者を対象とした試験 | T80/A5 (87例) | 98.03 (6.03) | 12.28 | 9.14 [7.09,11.18] | 143.70 (13.80) | 18.37 | 14.88 [11.82,17.94] |
| T80 (86例) | 98.46 (6.74) | 3.14 | 144.31 (14.52) | 3.49 | |||
17.1.4 国内第III相試験
本態性高血圧患者225例を対象とした無作為化二重盲検比較試験において、T80/A5mg配合剤又はT40/A5mg配合剤を1日1回、8週間経口投与した結果、T80/A5mg配合剤のトラフ時座位拡張期血圧下降度及び収縮期血圧下降度はT40/A5mg配合剤を上回った。結果は次表のとおりであった24)。
| 試験 | 投与群 | 拡張期血圧(mmHg) | 収縮期血圧(mmHg) | ||||
| 投与前値 平均値 (SD) | 下降度a) | 投与前値 平均値 (SD) | 下降度a) | ||||
| 調整 平均値 | 群間差: 調整平均値 [両側95%CI] | 調整 平均値 | 群間差: 調整平均値 [両側95%CI] | ||||
| T80/A5とT40/A5の降圧効果を比較した試験b) | T80/A5 (112例) | 90.11 (6.71) | 4.93 | 1.46 [-0.22,3.14] | 133.73 (10.59) | 5.55 | 2.14 [-0.36,4.64] |
| T40/A5 (112例) | 90.65 (7.96) | 3.47 | 134.49 (13.61) | 3.41 | |||
17.1.5 国内第III相試験(長期投与試験)
本態性高血圧患者259例に対し、テルミサルタン/アムロジピン配合剤を長期投与した。T40/A5mg配合剤の6週間投与で降圧効果が得られた高血圧患者はそのまま継続投与し、降圧効果不十分な高血圧患者にはT80/A5mg配合剤を増量投与した。その結果両剤ともに長期投与による降圧効果の減弱は認められなかった。T40/A5mg配合剤及びT80/A5mg配合剤を投与された患者全体(255例)の投与終了時(56週後)の血圧コントロール率は、拡張期87.8%(224/255例)、収縮期92.5%(236/255例)に達した。T40/A5mg配合剤では降圧効果不十分のためにT80/A5mg配合剤を増量投与した高血圧患者(48例)の投与終了時の血圧は、T80/A5mg配合剤へ増量した時点に比べ拡張期血圧で7.26mmHg、収縮期血圧で8.61mmHg(いずれも平均値)下降した。また、配合剤の安全性を検討した結果、忍容性に問題はなかった25)。
副作用発現割合は、T40/A5mg配合剤で1.9%(4/211例)、T80/A5mg配合剤で4.2%(2/48例)であった。T40/A5mg配合剤投与群の副作用は体位性めまい0.9%(2/211例)、血圧低下0.5%(1/211例)、湿疹0.5%(1/211例)で、T80/A5mg配合剤投与群の副作用は疲労2.1%(1/48例)、頭痛2.1%(1/48例)であった。
18. 薬効薬理
18.1 作用機序
18.1.1 テルミサルタン
テルミサルタンは主に血管平滑筋のアンジオテンシンII(A-II)タイプ1(AT1)受容体において、生理的昇圧物質であるA-IIと特異的に拮抗し、その血管収縮作用を抑制することにより降圧作用を発現する。テルミサルタンのAT1受容体親和性は高く(Ki=3.7nM)、AT1受容体から容易に解離しない。テルミサルタンは10〜1000nMの濃度範囲で、A-IIによる摘出ウサギ大動脈標本の血管収縮反応曲線を、濃度依存的に右方に移動させると共に最大収縮を40〜50%抑制する。また標本洗浄120分後においても有意な血管収縮抑制を示し、作用は持続的である。また、ブラジキニン分解酵素であるACE(キニナーゼII)に対しては直接影響を及ぼさない26)27)28)29)。
18.1.2 アムロジピンベシル酸塩
18.2 降圧作用
テルミサルタンあるいはアムロジピン単独あるいは併用による作用について、以下の報告がある。
覚醒下の雄性高血圧自然発症ラット(SHR)を用いて、1mg/kgテルミサルタン及び5mg/kgアムロジピンを1日1回経口投与し、5日間経時的に血圧を測定したところ、1mg/kgテルミサルタン及び5mg/kgアムロジピンは、それぞれ単独投与により平均血圧が約25mmHg低下し、ほぼ同様の血圧低下作用を示した。次に、1mg/kgテルミサルタン、5mg/kgアムロジピン併用で1日1回5日間経口投与を行い、経時的に血圧を測定した。テルミサルタンとアムロジピンの併用投与による血圧に対する作用は、単独投与による血圧低下作用(約25mmHgの低下)に比べ、有意な血圧低下作用(約50mmHgの低下)がみられた33)。
覚醒下の雄性高血圧自然発症ラット(SHR)を用いて、1mg/kgテルミサルタン及び5mg/kgアムロジピンを1日1回経口投与し、5日間経時的に血圧を測定したところ、1mg/kgテルミサルタン及び5mg/kgアムロジピンは、それぞれ単独投与により平均血圧が約25mmHg低下し、ほぼ同様の血圧低下作用を示した。次に、1mg/kgテルミサルタン、5mg/kgアムロジピン併用で1日1回5日間経口投与を行い、経時的に血圧を測定した。テルミサルタンとアムロジピンの併用投与による血圧に対する作用は、単独投与による血圧低下作用(約25mmHgの低下)に比べ、有意な血圧低下作用(約50mmHgの低下)がみられた33)。
19. 有効成分に関する理化学的知見
19.1. テルミサルタン
19.2. アムロジピンベシル酸塩
20. 取扱い上の注意
分包後は吸湿して軟化することがあるので、高温・多湿を避けて保存すること。
22. 包装
<テラムロ配合錠AP「NIG」>
100錠[10錠(PTP)×10]
<テラムロ配合錠BP「NIG」>
100錠[10錠(PTP)×10]
23. 主要文献
- 阿部真也ほか, 周産期医学, 47, 1353-1355, (2017)
- 齊藤大祐ほか, 鹿児島産科婦人科学会雑誌, 29, 49-54, (2021)
- Naito T et al., J Hum Lact., 31 (2), 301-306, (2015)
- Stangier J et al., J Clin Pharmacol., 40, 1373-1379, (2000)
- Makani H et al., BMJ., 346, f360, (2013)
- Laine K et al., Br J Clin Pharmacol., 43 (1), 29-33, (1997)
- 健康成人での薬物動態試験(ミカムロ配合錠;2010年7月23日承認、CTD 2.7.6.2、2.7.2)
- Stangier J et al., J Clin Pharmacol., 40, 1347-1354, (2000)
- 健康成人での薬物動態試験(ミカムロ配合錠;2010年7月23日承認、CTD 2.7.6.2.3、2.7.2)
- 社内資料:生物学的同等性試験
- 食事の影響試験(ミカムロ配合錠;2010年7月23日承認、CTD 2.7.6.1.3、2.7.1)
- 分布(ミカムロ配合錠;2010年7月23日承認、CTD 2.6.4.4)
- 第十八改正日本薬局方解説書, C-306-C-311, (2021), (廣川書店)
- Beresford A P et al., Xenobiotica., 18 (2), 245-254, (1988)
- 排泄(ミカルディスカプセル;2002年10月8日承認、申請資料概要 ヘ.3.2))
- Stangier J et al., J Clin Pharmacol., 40, 1312-1322, (2000)
- 中島光好ほか, 臨床医薬, 7 (7), 1407-1435, (1991)
- 肝機能障害患者における薬物動態試験(ミカルディスカプセル;2002年10月8日承認、申請資料概要 ヘ.3.(4))
- 足立幸彦ほか, 薬理と治療, 19 (7), 2923-2932, (1991)
- 桑島 巌ほか, Geriatric Medicine., 29 (6), 899-902, (1991)
- 有効性データの分析結果(ミカムロ配合錠;2010年7月23日承認、CTD 2.5.4.2.1)
- 検証試験(ミカムロ配合錠;2010年7月23日承認、CTD 2.7.6.3.1)
- 検証試験(ミカムロ配合錠;2010年7月23日承認、CTD 2.7.6.3.2)
- 審査報告書(ミカムロ配合錠;2012年12月21日)
- 長期投与試験(ミカムロ配合錠;2010年7月23日承認、CTD 2.7.6.3.3)
- Wienen W et al., Br J Pharmacol., 110 (1), 245-252, (1993)
- Wienen W et al., Cardiovascular Drug Reviews., 18 (2), 127-156, (2000)
- アンジオテンシンII受容体(AT1、AT2)に対する親和性(ミカルディスカプセル;2002年10月8日承認、申請資料概要 ホ.1.(2)2))
- アンジオテンシンII拮抗作用(in vitro試験)(ミカルディスカプセル;2002年10月8日承認、申請資料概要 ホ.1.(2)3))
- Yamada S et al., J Cardiovasc Pharmacol., 23 (3), 466-472, (1994)
- 山中教造ほか, 日本薬理学雑誌, 97 (3), 167-178, (1991) »PubMed
- Burges R A et al., J Cardiovasc Pharmacol., 9 (1), 110-119, (1987)
- 血圧の併用試験(ミカムロ配合錠;2010年7月23日承認、CTD 2.6.2.2.3)
24. 文献請求先及び問い合わせ先
文献請求先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
製品情報問い合わせ先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
26. 製造販売業者等
26.1 製造販売元
日医工岐阜工場株式会社
富山市総曲輪1丁目6番21
26.2 販売元
日医工株式会社
富山市総曲輪1丁目6番21