医薬品情報
| 総称名 | チモロール |
|---|---|
| 一般名 | チモロールマレイン酸塩 |
| 欧文一般名 | Timolol Maleate |
| 製剤名 | チモロールマレイン酸塩持続性点眼液 |
| 薬効分類名 | 持続性 緑内障・高眼圧症治療剤 |
| 薬効分類番号 | 1319 |
| ATCコード | C07AA06 S01ED01 |
| KEGG DRUG |
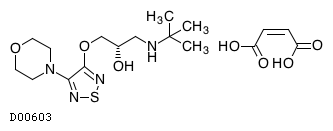
D00603
チモロールマレイン酸塩
|
| KEGG DGROUP |
DG03201
眼圧降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年3月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| チモロールXE点眼液0.25%「センジュ」 (後発品) | TIMOLOL XE OPHTHALMIC SOLUTION 0.25% | 千寿製薬 | 1319702Q3088 | 95.9円/mL | |
| チモロールXE点眼液0.5%「センジュ」 (後発品) | TIMOLOL XE OPHTHALMIC SOLUTION 0.5% | 千寿製薬 | 1319702Q4084 | 205.1円/mL |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
緑内障、高眼圧症
6. 用法及び用量
通常、0.25%製剤を1回1滴、1日1回点眼する。
なお、十分な効果が得られない場合は0.5%製剤を用いて1回1滴、1日1回点眼する。
なお、十分な効果が得られない場合は0.5%製剤を用いて1回1滴、1日1回点眼する。
8. 重要な基本的注意
8.1 全身的に吸収される可能性があり、β-遮断剤全身投与時と同様の副作用があらわれることがあるので、留意すること。
8.2 縮瞳剤から本剤投与に切り替える場合、縮瞳作用の消失に伴い、屈折調整を必要とすることがある。また、閉塞隅角緑内障に本剤を単独使用し眼圧上昇を来した例が報告されているので、閉塞隅角緑内障への使用に際しては縮瞳剤との併用が必要である1)。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 肺高血圧による右心不全のある患者
肺高血圧症による右心不全の症状を増悪させるおそれがある。[11.1.3参照]
9.1.2 うっ血性心不全のある患者
うっ血性心不全の症状を増悪させるおそれがある。[11.1.3参照]
9.1.3 糖尿病性ケトアシドーシス及び代謝性アシドーシスのある患者
アシドーシスによる心筋収縮力の抑制を増強するおそれがある。
9.1.4 コントロール不十分な糖尿病のある患者
血糖値に注意すること。低血糖症状をマスクすることがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。器官形成期のラットに500mg/kg/dayを経口投与した試験で骨化遅延が、マウスに1,000mg/kg/day、ウサギに200mg/kg/dayを経口投与した試験で死亡胎児数の増加が認められている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒト母乳中へ移行することがある。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に生理機能が低下している。
10. 相互作用
相互作用序文
本剤は、主としてCYP2D6によって代謝される。[16.4参照]
薬物代謝酵素用語
CYP2D6
10.2 併用注意
| オミデネパグ イソプロピル | 結膜充血等の眼炎症性副作用の発現頻度の上昇が認められている。 | 機序不明 |
| アドレナリン ジピベフリン塩酸塩 | 散瞳作用が助長されたとの報告がある。 | 機序不明 |
| カテコールアミン枯渇剤: レセルピン等 | 交感神経系に対し、過剰の抑制を来すことがあり、低血圧、徐脈を生じ、眩暈、失神、起立性低血圧を起こすことがある。 | カテコールアミンの枯渇を起こす薬剤は、β-遮断作用を相加的に増強する可能性がある。 |
| β-遮断剤(全身投与): アテノロール プロプラノロール塩酸塩 メトプロロール酒石酸塩 | 眼圧下降あるいはβ-遮断剤の全身的な作用が増強されることがある。 | 作用が相加的にあらわれることがある。 |
| カルシウム拮抗剤: ベラパミル塩酸塩 ジルチアゼム塩酸塩 | 房室伝導障害、左室不全、低血圧を起こすおそれがある。 | 相互に作用が増強される。 |
| ジギタリス製剤: ジゴキシン ジギトキシン | 心刺激伝導障害(徐脈、房室ブロック等)があらわれるおそれがある。 | 相加的に作用(心刺激伝導抑制作用)を増強させる。 |
| CYP2D6阻害作用を有する薬剤: キニジン硫酸塩水和物 選択的セロトニン再取り込み阻害剤 | β-遮断作用(例えば心拍数減少、徐脈)が増強するとの報告がある。 | これらの薬剤は本剤の代謝酵素であるP450(CYP2D6)を阻害し、本剤の血中濃度が上昇する可能性がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 眼類天疱瘡(頻度不明)
結膜充血、角膜上皮障害、乾性角結膜炎、結膜萎縮、睫毛内反、眼瞼眼球癒着等があらわれることがある。
11.1.2 気管支痙攣、呼吸困難、呼吸不全(いずれも頻度不明)
β-受容体遮断による気管支平滑筋収縮作用により、気管支痙攣、呼吸困難、呼吸不全があらわれることがある。[2.2参照]
11.1.3 心ブロック、うっ血性心不全、心停止(いずれも頻度不明)
11.1.4 脳虚血、脳血管障害(いずれも頻度不明)
11.1.5 全身性エリテマトーデス(頻度不明)
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 眼 | 灼熱感・かゆみ・異物感等の眼刺激症状 | 霧視・視力低下等の視力障害、角膜炎・角膜びらん・角膜上皮障害等の角膜障害、結膜充血、眼乾燥感 | 眼痛、眼瞼下垂、結膜浮腫、眼瞼炎、眼瞼浮腫、濾胞性結膜炎、眼脂、羞明 | 角膜知覚低下、複視、結膜炎、眼底黄斑部の浮腫・混濁注) |
| 循環器 | 動悸、徐脈等の不整脈、低血圧 | 失神、浮腫、レイノー現象、四肢冷感 | ||
| 精神神経系 | 頭痛、めまい、不眠 | 抑うつ、重症筋無力症の増悪、悪夢、感覚異常 | ||
| 消化器 | 悪心 | 下痢、消化不良、腹痛、口渇 | ||
| その他 | 不快、倦怠感 | 脱力感、耳鳴、筋肉痛、胸部圧迫感、発疹、咳 |
14. 適用上の注意
14.1 薬剤交付時の注意
患者に対し以下の点に注意するよう指導すること。
・点眼前にキャップをしたまま点眼容器を下に向け、1回振ること(何回も振る必要はない)。
・薬液汚染防止のため、点眼のとき、容器の先端が直接目に触れないように注意すること。
・患眼を開瞼して結膜のう内に点眼し、1〜5分間閉瞼して涙のう部を圧迫させた後、開瞼すること。
・他の点眼剤を併用する場合には、本剤を最後に点眼すること。その際、少なくとも10分以上間隔をあけること。やむを得ず本剤点眼後に他の点眼剤を使用する場合には、ゲル化した点眼液が他の点眼剤の吸収を妨げるおそれがあるので、十分な間隔をあけてから点眼すること。
・点眼直後、製剤の特徴として眼の表面で涙液と接触することにより点眼液がゲル化し、霧視又はべたつきが数分間持続することがあること。
・遮光して保存すること。
16. 薬物動態
16.1 血中濃度
・健康成人を対象としたクロスオーバー試験では、0.5%チモロールマレイン酸塩点眼液を両眼に1滴点眼投与した後、5分間の涙のう部圧迫処置(n=20)、又は5分間の閉瞼処置(n=16)を行い、1時間後の平均血漿中濃度を各々の無処置群(反対眼)と比較した。その結果、涙のう部圧迫処置群及び閉瞼処置群ではそれぞれ0.41ng/mL及び0.46ng/mLであったのに対し、各々の無処置群では1.28ng/mL及び1.34ng/mLであり、これらの処置による血漿中移行抑制が有意に認められた2)(外国人データ)。
・健康成人男性(6例)を対象としたクロスオーバー試験では、0.5%チモロール持続性点眼液(1日1回)又は0.5%チモロール点眼液(1日朝夕の2回)を8日間両眼に点眼投与した時の最高血漿中チモロール濃度の平均値を算出した。その結果、0.5%チモロール持続性点眼液では0.28ng/mL、0.5%チモロール点眼液では朝夕それぞれ0.46ng/mL及び0.35ng/mLであった3)(外国人データ)。
16.3 分布
・血漿タンパク結合率は約60%である4)。
・白色ウサギに1%の14C-チモロールマレイン酸塩点眼液を片眼に点眼投与したとき、角膜、虹彩、毛様体、前房水などに高濃度に分布するが、水晶体、視神経、血漿などへの分布は少なかった。一方、有色ウサギでは、メラニン色素を含まない組織での分布は白色ウサギと同等であるが、メラニン色素を含む虹彩、毛様体、網脈絡膜には白色ウサギより高濃度に分布し、メラニン親和性が見られた5)。
16.4 代謝
・14C-チモロールマレイン酸塩4mgを単回経口投与した後のヒト尿中には、ジメチルエチルアミノ基が脱離して生成されたカルボン酸代謝物、及びモルホリン環が開裂した代謝物が認められた7)(外国人データ)。
16.5 排泄
14C-チモロールマレイン酸塩4mgをヒトに単回経口投与したとき、尿中排泄の約20%が未変化体であった7)(外国人データ)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第II相試験
緑内障、高眼圧症患者102例(有効性解析対象89例)を対象に、全国29施設で0.25%又は0.5%チモロール持続性点眼液を1日1回、8週間点眼した結果、有効率は0.25%で71.1%(32/45例)、0.5%で79.5%(35/44例)であった8)。
副作用は101例中6例(5.9%)に認められ、主な副作用は角膜上皮欠損3例(3.0%)であった。
17.1.2 国内第III相試験
緑内障、高眼圧症患者390例(有効性解析対象350例)を対象に、全国89施設で0.5%チモロール持続性点眼液を1日1回又は0.5%チモロール点眼液を1日2回、8週間点眼した結果、両剤の有効性は同等であることが認められた9)。
副作用は0.5%チモロール持続性点眼液群の192例中19例(9.9%)に認められ、主な副作用は結膜充血6件であった。
18. 薬効薬理
18.1 作用機序
18.2 眼圧下降作用
ウサギにおけるα-キモトリプシン惹起高眼圧及び水負荷による眼圧上昇試験において、チモロールマレイン酸塩の点眼は有意に眼圧上昇を抑制することが認められている14)。
18.3 β-受容体遮断作用
18.4 生物学的同等性試験
<チモロールXE点眼液0.25%「センジュ」>
本剤(0.25%)とチモプトールXE点眼液0.25%を健康成人男子の両眼にそれぞれ1滴単回点眼し、眼圧値を測定した。各測定時点の眼圧値より得られたパラメータ(最大眼圧降下値、眼圧降下値−時間曲線下面積)注)について統計解析を行った結果、両剤の生物学的同等性が確認された17)。
| 判定パラメータ | ||
| 最大眼圧降下値 (mmHg) | 眼圧降下値-時間曲線下面積 (mmHg・hr) | |
| 本剤(0.25%) | 3.9±1.0 | 52.9±16.0 |
| チモプトールXE点眼液0.25% | 3.7±1.0 | 50.0±14.2 |
<チモロールXE点眼液0.5%「センジュ」>
本剤(0.5%)とチモプトールXE点眼液0.5%を健康成人男子の両眼にそれぞれ1滴単回点眼し、眼圧値を測定した。各測定時点の眼圧値より得られたパラメータ(最大眼圧降下値、眼圧降下値−時間曲線下面積)注)について統計解析を行った結果、両剤の生物学的同等性が確認された18)。
| 判定パラメータ | ||
| 最大眼圧降下値 (mmHg) | 眼圧降下値-時間曲線下面積 (mmHg・hr) | |
| 本剤(0.5%)※ | 3.6±1.0 | 46.4±20.8 |
| チモプトールXE点眼液0.5%※※ | 3.9±1.2 | 48.0±19.6 |
注)最大眼圧降下値並びに眼圧降下値-時間曲線下面積等のパラメータは、被験者の選択、眼圧の測定回数・時間等の試験条件によって異なる可能性がある。
19. 有効成分に関する理化学的知見
19.1. チモロールマレイン酸塩
20. 取扱い上の注意
・凍結を避けて保存すること。
・外箱開封後は、遮光して保存すること。
22. 包装
<チモロールXE点眼液0.25%「センジュ」>
プラスチック点眼容器 2.5mL×10
<チモロールXE点眼液0.5%「センジュ」>
プラスチック点眼容器 2.5mL×10
23. 主要文献
- 宇治幸隆 他, 眼科臨床医報, 74, 1036-1042, (1980)
- Zimmerman TJ, et al., Arch Ophthalmol, 102, 551-553, (1984) »PubMed
- Shedden AH, et al., Doc Ophthalmol, 103, 73-79, (2001) »PubMed
- 第十八改正日本薬局方解説書, C3266-C3270, (2021), (廣川書店)
- Araie M, et al., Jpn J Ophthalmol, 26, 248-263, (1982) »PubMed
- Volotinen M, et al., Drug Metab Dispos, 35, 1135-1141, (2007) »PubMed
- Tocco DJ, et al., Drug Metab Dispos, 3, 361-370, (1975) »PubMed
- 北澤克明 他, あたらしい眼科, 12, 1793-1804, (1995)
- 北澤克明 他, あたらしい眼科, 13, 143-154, (1996)
- Miichi H, et al., Invest Ophthalmol Vis Sci, 24, 1269-1275, (1983) »PubMed
- 新家 真 他, 日本眼科学会雑誌, 84, 1436-1446, (1980) »PubMed
- 藤永 豊 他, 眼科臨床医報, 74, 409-414, (1980)
- 玉田康房 他, 日本眼科紀要, 31, 1667-1673, (1980)
- Vareilles P, et al., Invest Ophthalmol Vis Sci, 16, 987-996, (1977) »PubMed
- Hall RA, et al., Arch Int Pharmacodyn Ther, 213, 251-263, (1975) »PubMed
- 田辺堅三郎 他, 応用薬理, 17, 455-467, (1979)
- 社内資料:生物学的同等性試験(0.25%)
- 社内資料:生物学的同等性試験(0.5%)
24. 文献請求先及び問い合わせ先
文献請求先
千寿製薬株式会社
カスタマーサポート室 受付時間 9:00〜17:30(土、日、祝日を除く)
〒541-0048
大阪市中央区瓦町三丁目1番9号
電話:0120-069-618
FAX:06-6201-0577
製品情報問い合わせ先
千寿製薬株式会社
カスタマーサポート室 受付時間 9:00〜17:30(土、日、祝日を除く)
〒541-0048
大阪市中央区瓦町三丁目1番9号
電話:0120-069-618
FAX:06-6201-0577
26. 製造販売業者等
26.1 製造販売元
千寿製薬株式会社
大阪市中央区瓦町三丁目1番9号
26.2 販売
武田薬品工業株式会社
大阪市中央区道修町四丁目1番1号