医薬品情報
| 総称名 | メキタジン |
|---|---|
| 一般名 | メキタジン |
| 欧文一般名 | Mequitazine |
| 薬効分類名 | 持続性抗ヒスタミン剤 |
| 薬効分類番号 | 4413 |
| ATCコード | R06AD07 |
| KEGG DRUG |
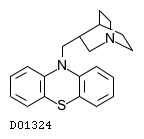
D01324
メキタジン
|
| KEGG DGROUP |
DG01482
ヒスタミンH1受容体拮抗薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年2月 改訂(第2版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| メキタジン錠3mg「NIG」 | 日医工岐阜工場 | 4413004F1332 | 10.8円/錠 |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分、フェノチアジン系化合物及びその類似化合物に対し過敏症の既往歴のある患者
2.2 閉塞隅角緑内障の患者[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
2.3 前立腺肥大等下部尿路に閉塞性疾患のある患者[抗コリン作用により排尿困難等を起こすことがある。]
4. 効能または効果
6. 用法及び用量
<気管支喘息>
通常成人1回メキタジンとして6mgを1日2回経口投与する。なお、年齢、症状に応じて適宜増減する。
<アレルギー性鼻炎、じん麻疹、皮膚疾患に伴うそう痒(湿疹・皮膚炎、皮膚そう痒症)>
通常成人1回メキタジンとして3mgを1日2回経口投与する。なお、年齢、症状に応じて適宜増減する。
8. 重要な基本的注意
眠気を催すことがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械操作には従事させないよう十分注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 開放隅角緑内障の患者
抗コリン作用により眼圧が上昇し、症状を悪化させることがある。
9.2 腎機能障害患者
長期投与例で臨床検査値異常としてBUN上昇がみられることがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないことが望ましい。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
臨床試験において口渇等の副作用の発現率が高い傾向が認められている。
10. 相互作用
10.2 併用注意
| 中枢神経抑制剤 (バルビツール酸誘導体、麻酔剤、麻薬性鎮痛剤、鎮静剤、精神安定剤等) フェノバルビタール等 | 眠気等があらわれることがあるので、減量するなど注意すること。 | 本剤の中枢神経抑制作用により、作用が増強されることがある。 |
| 抗コリン作用を有する薬剤(三環系抗うつ剤、MAO阻害剤等) イミプラミン塩酸塩、ブチルスコポラミン臭化物等 | 口渇、排尿困難等があらわれることがあるので、減量するなど注意すること。 | 本剤の抗コリン作用により、作用が増強されることがある。 |
| メトキサレン | 光線過敏症を起こすおそれがある。 | これらの薬剤は光線感受性を高める作用を有する。 |
| アルコール | 眠気等があらわれることがあるので、アルコール含有清涼飲料水等の摂取に注意すること。 | 本剤の中枢神経抑制作用により、作用が増強されることがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
血圧低下、呼吸困難、咽頭浮腫、蕁麻疹、嘔気等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.2 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、ALP等の上昇を伴う肝機能障害、黄疸があらわれることがある。また、劇症肝炎の報告がある。
11.1.3 血小板減少(頻度不明)
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 過敏症 | 発疹、光線過敏症 | ||
| 肝臓 | AST、ALTの上昇 | 黄疸 | |
| 血液 | 血小板減少 | ||
| 精神神経系 | 眠気、倦怠感、ふらふら感 | 頭痛、めまい | 興奮 |
| 消化器 | 口渇、胃部不快感 | 下痢、便秘、食欲不振、嘔吐、胃痛、腹痛 | |
| 循環器 | 胸部苦悶感、心悸亢進 | ||
| 泌尿器 | 排尿困難 | ||
| その他 | 咽頭痛、浮腫、顔面潮紅、視調節障害、月経異常、味覚異常、口内しびれ感 |
13. 過量投与
13.1 症状
眠気、悪心、嘔吐、軽度の抗コリン作用性障害がみられる。
13.2 処置
必要に応じ補助呼吸又は人工呼吸、抗痙攣剤を投与する。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.2 非臨床試験に基づく情報
動物実験(ラット)でメラニンに対する親和性が認められている。また、他のフェノチアジン系化合物の長期投与又は大量投与により角膜・水晶体の混濁、網膜・角膜の色素沈着が報告されているので注意すること。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
16.1.2 反復投与
健康成人に3mg(n=4)又は6mg(n=4)を食後反復経口投与した場合、血中濃度は投与7日目までに定常状態に達し、その血中濃度は単回投与の最高血中濃度の3〜4倍であり、生物学的半減期T1/2(β)は単回投与時とほぼ同程度であった2)。
16.1.3 生物学的同等性試験
メキタジン錠3mg「NIG」とゼスラン錠3mgを、クロスオーバー法によりそれぞれ2錠(メキタジンとして6mg)健康成人男子に絶食単回経口投与して血清中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について統計解析を行った結果、両剤の生物学的同等性が確認された3)。
| 投与量(mg) | AUC0-48(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | |
| メキタジン錠3mg「NIG」 | 6 | 97.5±19.1 | 5.7±0.8 | 3.5±0.5 | 12.5±1.0 |
| ゼスラン錠3mg | 6 | 97.7±5.2 | 5.9±0.5 | 3.6±0.5 | 12.9±1.4 |
血清中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.3 分布
16.4 代謝
健康成人に経口投与した場合、尿からは未変化体の他に3種類の代謝物(SO、NO、モノ水酸化体)とグルクロン酸抱合体が確認されている2)。
16.5 排泄
健康成人に経口投与した場合、48時間以内に約20%が尿中へ排泄される2)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<気管支喘息>
17.1.1 国内臨床試験(ケトチフェンを対照とした多施設二重盲検比較試験)
気管支喘息患者211例を対象にメキタジン6mg又はケトチフェン1mgを1日2回、10週間経口投与した結果、改善例数(中等度改善以上)は下表のとおりであった。メキタジン投与群の副作用は、眠気7.1%(7/98例)、口渇4.1%(4/98例)、フラフラ感、発疹、かゆみ、尿閉各1.0%(1/98例)であった6)。
| 投与群 | 有効性 | 安全性 | |||||||||
| 著明 改善 | 中等度 改善 | 軽度 改善 | 不変 | 軽度 悪化 | 中等度 悪化 | 著明 悪化 | 解析対象 例数 (179例) | 改善例数(%) (中等度 改善以上) | 解析対象 例数 195例 | 副作用 発現 例数(%) | |
| メキタ ジン | 9 | 34 | 30 | 14 | 2 | 2 | 0 | 91 | 43(47.3) | 98 | 11(11.2) |
| ケトチ フェン | 9 | 22 | 28 | 25 | 3 | 1 | 0 | 88 | 31(35.2) | 97 | 10(10.3) |
<アレルギー性鼻炎>
17.1.2 国内臨床試験(クレマスチンを対照とした二重盲検群間比較試験)
通年性鼻アレルギー患者185例を対象にメキタジン3mg又はクレマスチン1mgを1日2回、1週間経口投与した結果、改善例数(有効以上)は下表のとおりであった。メキタジン投与群の副作用は、眠気8.1%(7/86例)、倦怠感4.7%(4/86例)、口渇、発疹2.3%(2/86例)、ふらふら感、胃痛、嘔気各1.2%(1/86例)であった7)。
| 投与群 | 有効性 | 安全性 | |||||||
| 著効 | 有効 | やや有効 | 無効 | 悪化 | 解析対象例数 (157例) | 改善例数 (%) (有効以上) | 解析対象 例数 (174例) | 副作用 発現 例数(%) | |
| メキタ ジン | 7 | 38 | 15 | 17 | 2 | 79 | 45(57.0) | 86 | 12(14.0) |
| クレマ スチン | 5 | 35 | 24 | 14 | 0 | 78 | 40(51.3) | 88 | 19(21.6) |
<蕁麻疹、皮膚疾患に伴うそう痒(湿疹・皮膚炎、皮膚そう痒症)>
17.1.3 国内臨床試験(クレマスチンを対照とした二重盲検群間比較試験)
慢性蕁麻疹の患者297例を対象にメキタジン3mg又はクレマスチン1mgを1日2回、1週間経口投与した結果、改善例数(有効以上)は下表のとおりであった。メキタジン投与群の副作用は、眠気18.8%(27/144例)、倦怠感10.4%(15/144例)、便秘、口渇、吐気各0.7%(1/144例)であった8)。
| 投与群 | 有効性 | 安全性 | |||||||
| 著効 | 有効 | やや有効 | 不変 | 悪化 | 解析対象例数 (285例) | 改善例数 (%) (有効以上) | 解析対象 例数 (286例) | 副作用 発現 例数(%) | |
| メキタジン | 63 | 42 | 14 | 21 | 4 | 144 | 105(72.9) | 144 | 32(22.2) |
| クレマスチン | 53 | 37 | 29 | 11 | 11 | 141 | 90(63.8) | 142 | 48(33.6) |
18. 薬効薬理
18.1 作用機序
抗原抗体反応に伴って起こる肥満細胞からのヒスタミンやロイコトリエンC4・D4などのケミカルメディエーターの遊離を抑制すると共に、これらの作用に拮抗することにより、アレルギー症状を緩和する1)。
18.2 ケミカルメディエーター拮抗作用
18.2.1 ヒスタミン、ロイコトリエン、アセチルコリンによるモルモット摘出回腸・気管筋・肺実質収縮、ブラディキニン、セロトニンによるモルモット摘出回腸収縮、PAF(血小板活性化因子)によるモルモット摘出気管筋収縮、プロスタグランジンF2αによるモルモット摘出肺実質収縮を抑制する9)10)11)12)(in vitro)。
18.2.2 抗ヒスタミン作用
ヒスタミン致死を長時間防御する9)(マウス)。
18.3 ケミカルメディエーター遊離抑制作用
18.4 抗アレルギー作用
19. 有効成分に関する理化学的知見
19.1. メキタジン
20. 取扱い上の注意
アルミピロー包装開封後は遮光して保存すること。
22. 包装
100錠[10錠(PTP)×10]、1000錠[10錠(PTP)×100]
23. 主要文献
- 第十八改正日本薬局方解説書, C-5606-C-5609, (2021), (廣川書店)
- 第十八改正日本薬局方 医薬品情報 JPDI2021, 756-757, (2021), (じほう)
- 社内資料:生物学的同等性試験
- 宗田靖二他, 医薬品研究, 12 (2), 462-480, (1981)
- 横山信治他, 医薬品研究, 12 (2), 481-488, (1981)
- 長野準他, 臨床医薬, 4, 1013-1040, (1988)
- 武田一雄他, 耳鼻臨床, 74, 381-400, (1981) »DOI
- 久木田淳他, 西日本皮膚科, 43, 1346-1353, (1981) »DOI
- 藤村一他, 日薬理誌, 78, 279-289, (1981) »PubMed
- 藤村一他, 日薬理誌, 78, 291-303, (1981) »PubMed
- 河野茂勝他, 日薬理誌, 92, 145-157, (1988) »PubMed
- K.Tasaka et al., Arzneimittelforschung/Drug Res., 4010 (II), 1092-1097, (1990)
- 河野茂勝他, 日薬理誌, 92, 159-165, (1988) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
製品情報問い合わせ先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
26. 製造販売業者等
26.1 製造販売元
日医工岐阜工場株式会社
富山市総曲輪1丁目6番21
26.2 販売元
日医工株式会社
富山市総曲輪1丁目6番21