医薬品情報
| 総称名 | ノアルテン |
|---|---|
| 一般名 | ノルエチステロン |
| 欧文一般名 | Norethisterone |
| 製剤名 | ノルエチステロン錠 |
| 薬効分類名 | 経口黄体ホルモン剤 |
| 薬効分類番号 | 2479 |
| ATCコード | G03DC02 |
| KEGG DRUG |
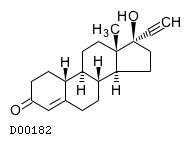
D00182
ノルエチステロン
|
| KEGG DGROUP |
DG02004
プロゲステロン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年4月 改訂(第2版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ノアルテン錠(5mg) | Norluten tablets | 富士製薬工業 | 2479002F1026 | 30.7円/錠 | 処方箋医薬品注) |
2. 禁忌
4. 効能または効果
無月経、月経周期異常(稀発月経、多発月経)又は生殖補助医療における調節卵巣刺激の開始時期の調整、月経量異常(過少月経、過多月経)、月経困難症、卵巣機能不全症、黄体機能不全による不妊症、機能性子宮出血、月経周期の変更(短縮及び延長)
5. 効能または効果に関連する注意
<生殖補助医療における調節卵巣刺激の開始時期の調整>
妊娠率や生産率の報告を踏まえると、本剤を含む黄体ホルモン剤と卵胞ホルモン剤の併用で調節卵巣刺激の開始時期の調整を行った場合は、開始時期の調整を行わない場合と比べて、妊娠率や生産率が低下する可能性があるので、このことを患者に説明した上で、本剤の投与の要否は、患者ごとに治療上の必要性を考慮して慎重に判断すること。[15.1.2参照]
6. 用法及び用量
<効能共通>
通常、成人にはノルエチステロンとして1日5〜10mgを1〜2回に分割経口投与する。
<月経周期の変更(延長)>
1日5mgを月経予定5日前から投与し始め、月経周期延長希望日まで連続投与する。
<月経周期の変更(短縮)>
1日5mgを卵胞期に投与し、数日間連続投与する。
8. 重要な基本的注意
<生殖補助医療における調節卵巣刺激の開始時期の調整、黄体機能不全による不妊症>
本剤は、不妊治療に十分な知識と経験のある医師のもとで使用すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心疾患のある患者又はその既往歴のある患者
ナトリウム又は体液の貯留があらわれることがある。
9.2 腎機能障害患者
9.2.1 腎疾患のある患者又はその既往歴のある患者
ナトリウム又は体液の貯留があらわれることがある。
9.3 肝機能障害患者
9.3.1 重篤な肝障害・肝疾患のある患者
投与しないこと。肝障害・肝疾患を悪化させることがある。[2.1参照]
9.5 妊婦
9.5.1 妊婦又は妊娠している可能性のある女性には投与しないこと。妊娠初期・中期に投与した場合には、まれに新生女児の外性器の男性化が起こることがある。[2.2参照]
9.5.2 黄体ホルモン剤の使用と先天異常児出産との因果関係は、いまだ確立されたものではないが、心臓・四肢等の先天異常児を出産した母親では、対照群と妊娠初期に黄体又は黄体・卵胞ホルモン剤を使用していた群との間に、有意差があったとの疫学的調査結果が報告されている1)。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 アナフィラキシー(頻度不明)
アナフィラキシー(呼吸困難、蕁麻疹、血管性浮腫、そう痒感等)があらわれることがあるので、このような症状があらわれた場合には投与を中止し、適切な処置を行うこと。
11.2 その他の副作用
| 5%以上又は頻度不明 | 0.1〜5%未満 | 0.1%未満 | |
| 過敏症 | 発疹等 | ||
| 肝臓 | 肝機能異常 | ||
| 電解質代謝 | 浮腫、体重増加等 | ||
| 消化器 | 食欲不振、悪心・嘔吐、下痢、腹痛等 | ||
| 子宮 | 不正出血、破綻出血、点状出血、経血量の変化、下腹部痛等 | ||
| 乳房 | 乳房緊満感、乳房痛等 | ||
| 精神神経系 | 頭痛 | 眠気等 | |
| その他 | ざ瘡、熱感、腰痛 | 倦怠感 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
16. 薬物動態
16.1 血中濃度
女性にノルエチステロン10mgを単回経口投与したとき、投与2時間後に最高血中濃度に達し、消失半減期は約5時間であった4)。
[測定法:competitive protein binding(CPB)]
16.4 代謝
子宮癌術後の女性に、ノルエチステロン100mg注)を単回経口投与し、フェノール性代謝物の定性試験を行ったとき、ノルエチステロンは主に肝臓で17α-エチニルエストラジオールに一部代謝されることが証明された5)。
16.5 排泄
子宮癌末期患者に3H-標識ノルエチステロン5.0mgを単回経口投与したとき、尿中から投与量の約30%が5日間で排泄され、6日目以降は尿中から放射活性は認められなかった6)。
注)本剤の承認用量は、「1日5〜10mgを1〜2回に分割経口投与する。」である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<無月経、月経周期異常(稀発月経、多発月経)、月経量異常(過少月経、過多月経)、月経困難症、卵巣機能不全症、機能性子宮出血、月経周期の変更(短縮及び延長)>
18. 薬効薬理
18.1 作用機序
18.2 黄体ホルモン作用
ウサギにおけるノルエチステロンの黄体ホルモン作用は、Miyake-Pincus法(経口投与)でノルエチノドレルの約3倍である30)。
18.3 卵胞ホルモン作用
マウスにおいて卵胞ホルモン作用をわずかながら有する31)。
18.4 ゴナドトロピン抑制作用
ラットにおいてゴナドトロピン抑制作用を有する32)。
19. 有効成分に関する理化学的知見
19.1. ノルエチステロン
22. 包装
100錠[10錠(PTP)×10]
23. 主要文献
- Nora JJ,et al., Lancet., 1 (7809), 941-942, (1973) »PubMed
- Kalra PA,et al., Br Med J., 294 (6575), 808, (1987)
- Cochrane Database Syst Rev, 5, (2017), (CD006109)
- 宮越洋二ほか, 日本内分泌学会雑誌, 47 (12), 1077, (1972)
- 石原貞尚, 日本内分泌学会雑誌, 42 (1), 55-65, (1966) »DOI
- 村田修吾, 日本内分泌学会雑誌, 43 (11), 1083-1096, (1968) »DOI
- 楠田雅彦, 産婦人科の世界, 10, 1003-1011, (1958)
- 赤須文男ほか, 最新医学, 12, 1789-1793, (1957)
- 赤須文男ほか, ホルモンと臨床, 11, 1135-1143, (1963)
- 奥村健次ほか, 産科と婦人科, 33, 1045-1048, (1956)
- 御国生雄三ほか, 産婦人科の世界, 11, 937-940, (1959)
- 村上旭ほか, 日本不妊学会雑誌, 3, 41-43, (1958)
- 足高義雄ほか, 最新医学, 13, 2681-2686, (1958)
- 唐澤陽介ほか, 産科と婦人科, 33, 362-366, (1956)
- 宮崎英智ほか, 産婦人科治療, 15, 107-110, (1967)
- 小坂清吉ほか, モダンテラピー, 13, 30-34, (1960)
- 的埜中, 産婦人科治療, 1, 271-281, (1960)
- 島津志行ほか, 新薬と臨牀, 9, 721-724, (1960)
- 山本孝也, 東京医科大学雑誌, 26, 385-403, (1968)
- 有光桂子, 新薬と臨牀, 9, 593-600, (1960)
- 的埜中ほか, 産婦人科の実際, 7, 456-464, (1958)
- 植田安雄ほか, 日本医事新報, 21-25, (1958)
- 山田広道, 新薬と臨牀, 7, 875-878, (1958)
- 飯塚理八ほか, 臨床婦人科産科, 13, 699-706, (1959)
- 石塚直隆ほか, モダンテラピー, 12, 4-12, (1959)
- 上田博雄ほか, 産婦人科の進歩, 18, 203-205, (1966) »DOI
- 足立春雄, モダンテラピー, 13, 2-12, (1960)
- 岡田弘二編著, 産婦人科における薬物療法, 27-31, (1991)
- たか折修二ほか監訳, グッドマン・ギルマン薬理書 第11版, 1978-1980, (2007), (廣川書店)
- Miyake T,et al., Endocrinol., 63 (12), 816-824, (1958)
- Miyake T,et al., Endocrinol., 69 (3), 534-546, (1961)
- 徳田源市ほか, 日本不妊学会雑誌, 13 (3), 256-263, (1968)
24. 文献請求先及び問い合わせ先
文献請求先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
製品情報問い合わせ先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
26. 製造販売業者等
26.1 製造販売元
富士製薬工業株式会社
富山県富山市水橋辻ヶ堂1515番地
26.2 提携先
Searle
米国